Автоматизированное измерение доплеровской скорости с использованием дешевого преобразователя
Иллюстрации
Показать всеГруппа изобретений относится к медицинской технике, а именно к ультразвуковому исследованию кровеносных сосудов тела. Ультразвуковое устройство для анализа потока текучей среды тела для осуществления способа ультразвукового анализа содержит ультразвуковой зонд для исследования объема и схему управления, сконфигурированную с возможностью осуществления этапов, на которых если при исследовании внутри объема находят один или более сосудов, то выбирают для анализа потока текучей среды сосуд из числа сосудов, найденных внутри объема, формируют информацию, конкретно относящуюся к выбранному сосуду, далее определяют, совпадает ли выбранный сосуд с целевым сосудом, в случае если совпадает, то тогда предоставляют индикацию в отношении нормального состояния потока текучей среды в выбранном сосуде, в противном случае повторяют выбор, формирование и определение для следующего сосуда из числа найденных сосудов до тех пор, пока внутри объема не будет найден никакой другой следующий сосуд, причем упомянутые действия не зависят от отображения изображений ультразвукового сканирования и выполняются автоматически и без необходимости вмешательства пользователя. Считываемый компьютером носитель данных содержит компьютерную программу, причем инструкции компьютерной программы исполняются посредством процессора для осуществления действий способа. Данная группа изобретений позволяет расширить арсенал технических средств. 3 н. и 8 з.п. ф-лы, 3 ил.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к исследованию сосуда тела в интересующем объеме и, более конкретно, к использованию ультразвука для проведения исследования.
Уровень техники изобретения
Оценка состояния плода является очень важной клинической практикой при сопровождении беременности. В настоящее время наиболее распространенными способами для оценки врачами эмбрионального состояния являются анализ частоты сердечных сокращений плода, используя кардиотокограф (CTG), и оценка кровотока через кровеносную систему матери и плода, используя ультразвуковой доплеровский эффект. Анализ сигнала при ультразвуковой доплерографии для определенных кровотоков плода и матери является частью установившейся медицинской практики и стандартной рекомендацией в различных клинических руководствах по диагностике и оценке беременностей с высокой степенью риска (диабет 2 типа, гипертония или преэклампсия у матери и IUGR - внутриматочное ограничение роста плода). Одна из основных целей обычного дородового ухода состоит в идентификации "подверженного риску" плода, чтобы клинически вмешаться, уменьшая, таким образом, перинатальную заболеваемость и смертность. Некоторыми из сосудов, полезных при оценке состояния плода, являются пупочная артерия, средняя артерия головного мозга, венозный проток и (левая и правая) маточные артерии и аллантоисные вены.
Ультразвуковые сканеры стали необходимым инструментом при контроле беременности во всем мире. В настоящее время они обеспечивают наилучший вариант контроля роста и развития плода. Дуплексные ультразвуковые сканеры обеспечивают ультразвуковое импульсно-волновое доплеровское исследование в дополнение к обычному сканированию. Цветовые и энергетические доплеровские сканеры являются новыми дополнениями к ряду сканеров, которые обеспечивают получение изображений сосудов. В частности, как правило, обеспечиваются цветовые доплеровские исследования, приводя к тому, что часто называют "триплексным" сканером.
Доплеровские исследования для получения клинически полезного результата измерения обычно требуют высокой степени мастерства. Например, правильная ориентация зонда относительно сосуда важна, чтобы гарантировать, что угол между потоком и лучом составляет меньше 60 градусов. Ошибки в измерениях увеличиваются, когда при определении скоростей используются углы больше 60 градусов. Стандартная последовательность выполнения операций на клиническом ультразвуковом сканере позволяет специалисту по ультразвуковой эхографии определить ориентацию зонда относительно сосуда, используя стандартный B-режим и дисплей цветового потока Color Flow. Затем получают спектральные доплеровские результаты измерений, гарантируя, таким образом, что измеренные скорости правильны.
Использование ультразвука в применениях для сосудов, чтобы выполнять измерение доплеровских скоростей, требует наличия квалифицированного персонала.
Раскрытие изобретения
В странах развивающегося рынка, таких как Индия, дефицит специалистов ограничивает наличие и доступ к ультразвуковой технологии. Следовательно, автоматизированный способ сбора данных и доплеровской оценки для клинической диагностики (не требующий от пользователя интерпретации сканированного ультразвукового изображения) был бы полезен для нерадиологов, таких как акушеры/гинекологи или кардиологи, оказывающих первичную помощь.
Кроме того, дешевая система важна для обеспечения привлекательного решения в среде развивающихся рынков. Устройства, доступные в настоящий момент на рынке для дородовых проверок и родов, являются ультразвуковыми и CTG-устройствами. Однако оба эти устройств относительно дороги.
На этих рынках существует потребность в дешевом, удобном в работе решении по предоставлению результата доплеровского измерения скорости для ведения скрининга и контроля беременностей с высоким риском.
Настоящее изобретение направлено на решение одной или более из описанных выше проблем.
В соответствии с настоящим изобретением, ультразвуковое устройство предназначено для выполнения последовательности этапов автоматически и без необходимости вмешательства пользователя. Эти этапы содержат исследование с использованием ультразвука на наличие в объеме сосудов тела; и если при исследовании обнаружены один или более сосудов, выбор сосуда для анализа потока текучей среды из числа одного или более сосудов. Это устройство может быть спроектировано так, чтобы иметь низкую цену, как подробно описывается здесь далее.
В варианте изобретения этапы дополнительно содержат формирование необходимой для анализа информации, относящейся к конкретно выбранному сосуду.
В другом варианте сформированная информация содержит количественную характеристику формы сигнала. Форма сигнала представляется определяемой во времени величиной скорости текучей среды в выбранном сосуде.
В дополнительном варианте этапы содержат исследование, выбор и формирование и дополнительно содержат выполнение анализа сформированной информации. Дополнительно вводимым этапом является, в зависимости от результата, основанного на анализе, предоставление на основе собранной информации индикации нормальности потока текучей среды в выбранном сосуде.
В еще одном дополнительном варианте этапы содержат исследование и выбор и дополнительно содержат, по меньшей мере, пока не выполнено предоставление результата, повторение последовательности этапов для каждого следующего выбранного сосуда из числа найденных сосудов, служащего в качестве текущего сосуда. Этапы последовательности являются следующими: выбор, формирование, выполнение анализа и предоставление результата.
В еще одном другом варианте этапы содержат классификацию выбранного сосуда, основываясь на сформированной информации, с предоставлением результата, подвергающегося классификации.
В дополнительном варианте, перед исследованием задается целевой сосуд в пределах категории сосудов, причем категория основана на физиологии. На основе сформированной информации определяется, совпадает ли выбранный сосуд с целевым сосудом.
В сопутствующем варианте исследование и выбор сопровождаются использованием ультразвука для формирования информации, конкретной для выбранного сосуда, и предоставлением на основе сформированной информации индикации нормальности потока текучей среды в выбранном сосуде.
В другом варианте устройство реализуется как карманное автономное устройство.
В еще одном другом варианте устройство реализуется как одна или более интегральных схем.
В альтернативном варианте устройство содержит двумерный преобразователь, содержащий элементы для исследования с использованием ультразвука представленных в объеме сосудов. Элементы расположены с интервалом по меньшей мере на одну длину волны ультразвука, излучаемого элементами при исследовании.
В сопутствующем варианте устройство выполнено с возможностью автоматической выписки заключения, основанного на результате исследования.
В подварианте выписка заключения содержит принятие основанного на исследовании решения в отношении нормальности потока текучей среды в сосуде, найденном при исследовании.
В еще одном подварианте устройство выполнено с возможностью выбора для анализа потока текучей среды из числа одного или более сосудов, найденных при исследовании, причем выписка основывается на результате анализа.
В еще одном дополнительном варианте устройство выполнено с возможностью выбора артерии и выбора вены.
В еще одном варианте выполнено без электронной фокусировки ультразвука и без необходимости отображения на дисплее изображения любого из сосудов.
В другом альтернативном варианте элементы имеют соответствующие плоскости приема ультразвука, каждая с площадью поверхности, по меньшей мере, 10 квадратных миллиметров.
В дополнительном варианте каждая из плоскостей имеет площадь поверхности, по меньшей мере, 25 квадратных миллиметров.
В еще одном дополнительном варианте интервал является интервалом длиной, по меньшей мере, две длины волны ультразвука.
В одном дополнительном альтернативном варианте ультразвуковое устройство выполнено с возможностью проведения последовательности действий, причем такая последовательность содержит исследование объема для нахождения сосуда тела и извлечение из сосуда тела, найденного при исследовании, клинического доплеровского параметра, причем упомянутая последовательность выполняется автоматически и без необходимости вмешательства пользователя.
Подробности устройства ультразвукового исследования изложены ниже с помощью следующих чертежей.
Краткое описание чертежей
Фиг.1 - пример ультразвукового зонда, временные диаграммы передачи/приема, интересующий объем, содержащий кровеносные сосуды, и форма сигнала кровотока и соответствующие клинические доплеровские показатели в соответствии с настоящим изобретением;
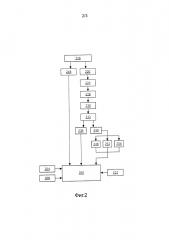
Фиг.2 - концептуальная блок-схема примерной обработки сигнала в соответствии с настоящим изобретением; и
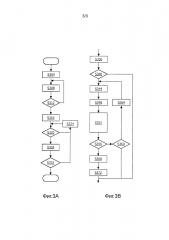
Фиг.3A и 3B - блок-схемы последовательности операций примера работы зонда в соответствии с настоящим изобретением.
Осуществление изобретения
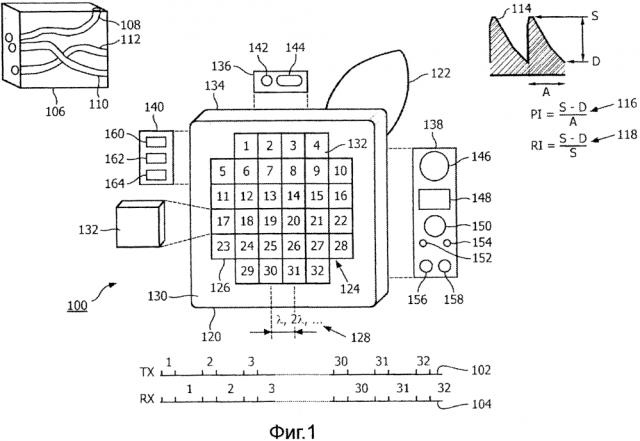
На фиг.1 в качестве иллюстративного и не создающего ограничений примера показан ультразвуковой зонд 100, временные диаграммы 102, 104 передачи/приема и объем или "интересующий объем" 106, содержащий кровеносные сосуды 108, 110, 112. Дополнительно изображены кровоток или форма 114 сигнала "спектрального доплеровского ультразвука" и соответствующие клинические доплеровские показатели 116, 118.
Зонд 100 может быть реализован как автоматическое, карманное, автономное, независимое ультразвуковое исследовательское устройство. Он имеет корпус 120 преобразователя и ручку 122.
Внутри корпуса 120 преобразователя содержится нефазированный, двумерный преобразователь 124, состоящий из элементов 126 преобразователя, причем количество элементов определяется объемом и анатомией сканирования.
Как видно на фиг.1, например, количество элементов 126 равно 32. Таким образом, при размере элемента 10 мм охватывается объем приблизительно 6 см × 6 см. Заподлицо с передней поверхностью 130 корпуса 120 находятся принимающие ультразвук поверхности 132 элементов 126 преобразователя, причем те же самые поверхности также передают, то есть излучают ультразвук.
Установлено всего только 32 элемента 126, что составляет разительный контраст по сравнению с гораздо большим количеством элементов, которое должно потребоваться при стандартном получении медицинских изображений, чтобы охватить тот же самый объем 6 см × 6 см.
В этом отношении, электронная фокусировка для получения медицинских изображений, как в преобразователе с фазированной матрицей, требует межэлементного интервала, составляющего 1/2 длины волны, то есть 1/2λ или меньше. Доплеровский ультразвук для получения изображения обычно может иметь частоту между 2×106 и 4×106 периодов в секунду (2-4 МГц). Ультразвук проходит через мягкую ткань тела со скоростью приблизительно 1540 метров/с. Длина волны, то есть λ, равна скорости, деленной на частоту. Здесь, это 1540 м/с, деленные приблизительно на 2×106 периодов/с = 0,8 мм. Получение медицинского ультразвукового изображения для отображения может поэтому потребовать межэлементного интервала меньше 0,4 мм и площади поверхности элемента меньше (0,4 мм)2, что меньше чем 0,2 мм2. Поэтому при малом размере элемента порядка 1/2λ могли бы потребоваться тысячи элементов 126 для построения двумерной матрицы, которая, подобно показанной на фиг.1, охватывает объем 6 см × 6 см.
Интервал (размер) элементов на фиг.1 составляет 10 мм, что, как обсуждалось выше, обычно должно быть больше 12λ ультразвука, используемого при исследовании интересующего объема 106 для присутствующих кровеносных сосудов 108, 110, 112.
В более общем плане, элементы 126, в соответствии с тем, что предложено здесь, располагают с интервалами более 1/2λ, хотя межэлементный интервал 128 может быть равен λ, 2λ или больше, как обсуждалось выше. Площадь поверхности 132, соответственно, составляет, по меньшей мере, 0,6 квадратных миллиметра (мм2) и может быть больше, такой как 10 мм2, 25 мм2 или 100 мм2, как на фиг.1.
Предпочтительно, чтобы прийти к диагнозу, автоматическое ультразвуковое устройство 100 не полагается на отображаемое на экране медицинское изображение; вместо этого оно характеризуется матрицей, состоящей из меньшего количества элементов преобразователя и, следовательно, меньшего количества каналов. Таким образом, стоимость производства является низкой, тогда как за счет автоматической работы надежность сохраняется. Надежность может даже быть увеличена, как для случая, когда медицинские исследования должны выполняться в более быстром темпе. Автоматическая работа также имеет тенденцию сокращать время исследования, уменьшая, таким образом, нагрузку на работников и делая исследование более удобным.
Во время сбора доплеровских данных элементы 126 запускаются либо последовательно, как показано на временных диаграммах 102, 104, либо группами, заботясь, чтобы акустический сигнал от одного элемента не влиял на другие, которые возбуждаются в то же самое время. Как видно на фиг.1, период приема для каждого элемента запаздывает относительно периода передачи для заданного элемента, обозначенного номером от 1 до 32. Доплеровское окно приема располагается, соответственно, в периоде приема, чтобы позволить выборку из соответствующей глубины внутри интересующего объема 106.
На обратной поверхности 134 корпуса 120, которая обращена к пользователю, находится множество панелей интерфейса пользователя для ввода-вывода, к которым относятся верхняя панель 136, левая панель 138 и правая панель 140. Выключатель 142 и поверхность 144 громкоговорителя расположены на верхней панели 136. Левая панель 138 обрамляет функциональную кнопку 146 навигации/приведения в действие, дисплей 148, доплеровский индикатор 150 обнаружения мощности, индикатор 152 сбора данных о сердцебиении плода, индикатор 154 сбора данных о сердцебиении матери, индикатор 156 нормального кровотока и индикатор 158 аномального кровотока. Правая панель 140 содержит три окна 160, 162, 164 обратной связи ввода параметров инициализации.
Клиническими доплеровскими показателями, такими как показатель 116 пульсации (PI) и показатель 118 сопротивляемости (RI), являются доплеровские результаты измерения пульсации крови, независимые от угла. Символы S, D и A представляют, соответственно, пиковый систолический частотный сдвиг, конечный диастолический частотный сдвиг и один сердечный цикл. Это видно на форме 114 сигнала кровотока, которая является графиком доплеровской частоты и, таким образом, скоростью кровотока в зависимости от времени.
Зонд 100 может использовать оба показателя, PI и RI, для идентификации кровеносных сосудов и оценки нормальности кровотока. Внутри зонда 100 схема управления (не показана), служащая в качестве устройства по п.1 формулы изобретения, может быть выполнена в виде одной или более интегральных схем (IC). Одна или более IC в соответствии с п.1 формулы изобретения могут альтернативно быть выполнены с возможностью установки в существующее оборудование, такое как ультразвуковые дуплексные сканеры.
Обработка сигналов, содержащаяся в классификации кровеносного сосуда 108-112, найденного зондом 100 внутри интересующего объема 106, показана, например, на фиг.2.
Классификатор 200 кровеносных сосудов может быть реализован как k-й ближайший соседний (K-) классификатор, где, например, K=3.
Классификатор используется, в первую очередь, чтобы предсказать, является ли сосуд 108-112 веной или артерией. Используют различные вводы признаков в классификатор 200, такие как PI, причем каждый из М-типов ввода соответствует размерности в М-мерном пространстве признаков. Другим типом ввода в классификатор являются, например, тестовые примеры. Каждый тестовый пример соответствует реальному клиническому случаю и содержит вводы М-признаков для случая, определяющего пример как конкретную точку, то есть "точку примера", в М-мерном пространстве. С каждой точкой примера связан соответствующий результат в виде "вена" или "артерия", в зависимости от того, относится ли данный тестовый пример фактически к вене или артерии. Классификатор 200 инициализируется с помощью тестовых примеров, и точка в М-мерном пространстве формируется, используя вводы признаков, полученных для кровеносного сосуда 108-112, классифицируемого в настоящий момент. Для K=3 идентифицируются 3 ближайших соседних точки (примера). Каждый сосед будет иметь в качестве своего результата значение "артерия" или "вена". Решение принимается по большинству. Никаких других связей нет, так как 3 - нечетное число.
Если сосуд классифицирован как артерия, классификатор 200 затем определяет, принадлежит ли она матери или плоду, посредством того же самого алгоритма ближайшего соседа. Если кровеносный сосуд является материнской артерией, производится определение, является ли он утробной артерией. Если, с другой стороны, сосуд является артерией плода, делается определение в отношении того, является ли эта артерия пупочной. Последние два определения используют один и тот же алгоритм ближайшего соседа.
Классификаторы ближайших соседей обладают преимуществом простоты, хотя вместо них могут использоваться другие альтернативные способы, такие как нейронные сети или векторные машины поддержки (SVM).
Вводы в классификатор от пользователя содержат внутриутробный возраст 204 плода и грубое, приблизительное расположение 208 зонда на животе матери. Также обеспечивается сосудистая модель 212 в форме подготовительных примеров для классификатора 200.
Другие вводы поступают прямо или косвенно из эховой информации, получаемой из принятого ультразвука 216.
Непосредственно из ультразвука 216, для ткани вокруг зонда 100 делается средняя оценка 218 показателя отражения. Этот показатель сравнивается с заданным показателем отражения, чтобы определить положение зонда 100 на теле матери.
Чтобы сформировать косвенные вводы, принятый ультразвук демодулируется в демодуляторе 220 для извлечения из несущей частоты ультразвукового доплеровского сигнала 224. Быстрое преобразование Фурье (FFT) 228 выполняется для доплеровского сигнала 224, чтобы сформировать спектрограмму 230 или "сонограмму на FFT-основе". Из спектрограмм 230 извлекаются один или более соответствующих спектральных профилей 232. Термин "спектральный профиль" означает часть сонограммы 230, которая соответствует кровотоку через артерию или вену. Спектральный профиль 232 может аппроксимироваться как область между кривыми, соответствующими максимальной и минимальной спектральным скоростям (или спектральным частотам). Спектральная ширина 236 извлеченного спектрального профиля 232 оценивается и подается на классификатор 200. Из спектрального профиля(-ей) 232 извлекается кривая 240, соответствующая пику (или, альтернативно, среднему значению) спектральной скорости. Конкретные временные признаки 248 также извлекаются из спектрального профиля(-ей) 232. Эти признаки содержат, например, присутствие метки, непосредственно предшествующей импульсу на форме 114 сигнала кровотока утробной артерии. PI и RI для сосуда, который должен быть подвергнут классификации 252, также извлекаются. В процедуре инициализации, которая предшествует исследованию текущего интересующего объема 106, оценка 256 времени пульсового цикла выполняется на основе спектрального профиля(-ей) 232 и затем извлекается.
В процессе работы и как показано на фиг.3A и 3B, пользователь, который может быть клиницистом, акушеркой, терапевтом, акушеркой/гинекологом или эмбриональным радиологом, вводит, как часть процедуры инициализации, целевой кровеносный сосуд для исследования, например левая утробная артерия (попадающая в физиологическую категорию кровеносных сосудов как "утробная артерия"), внутриутробный возраст плода и грубое описание расположения зонда, которое он будет иметь, когда инициализация закончится, и исследование начинается. Конкретно, после приведения в действие выключателя 142 пользователь дважды быстро нажимает функциональную кнопку 146 навигации/приведения в действие. В ответ на дисплее 148 появляется первый кровеносный сосуд для выбора. Если появившийся сосуд не является целью исследования, кнопка 146 нажимается один раз, чтобы на дисплее 148 предложить новый вариант для выбора. Это делается многократно, пока на экране не появится вариант, являющийся нужным вариантом для выбора. Затем кнопка 148 удерживается, и выбранный вариант отображается в окнах 160 обратной связи ввода параметров инициализации. На дисплее 148 появляется вариант для выбора внутриутробного возраста плода в месяцах или неделях. Подобным образом пользователь перемещается к правильному возрасту и удерживает кнопку 146, чтобы вернуть сделанный выбор в окно 162. Чтобы завершить ввод параметров инициализации, та же самая процедура выполняется для расположения зонда и выбранное местоположение отображается в окне 164 (этап S304).
Затем пользователь продолжает инициализацию, помещая зонд на живот матери для оценки 256 времени пульсового цикла. Пользователь нажимает функциональную кнопку 146 навигации/приведения в действие, чтобы запустить ультразвуковую доплеровскую операцию. Преобразователь будет сканировать глубины в месте расположения каждого элемента, чтобы обнаружить движение крови, то есть доплеровскую мощность. Если доплеровский индикатор 150 обнаружения мощности светится, доплеровская мощность в полосе частот 300-1000 Гц, представляющая кровоток, обнаружена, то есть имеет достаточную величину, чтобы прийти к заключению, что сердцебиение плода или матери может быть измерено по артериальному кровотоку. Частота сердечных сокращений матери обычно ниже, чем частота сердечных сокращений плода эмбриона. В дополнение к индикатору 150 динамик 144 может излучать короткий звуковой сигнал, чтобы предупредить пользователя о начале обнаружения доплеровской мощности. Альтернативно или в дополнение, через громкоговоритель 144 может осуществляться звуковая обратная связь по доплеровскому сигналу. Зонд 100 удерживается на месте в течение нескольких секунд; в противном случае доплеровская мощность падает и следует снова добиться загорания индикаторной лампочки 150. Если в конце периода продолжительностью несколько секунд не обнаружено сердцебиение ни матери, ни плода, пользователь может переместить зонд в другое место на животе матери и делать это многократно, пока не обнаружит сердцебиение. Если посредством последовательности обработки сигналов 220-232, 240, 256 сердцебиение плода или матери обнаружено, то есть найден сосуд тела и, в частности, артерия, загорается соответствующий индикатор 152 получения данных о частоте сердечных сокращений плода или индикатор 154 получения данных о частоте сердечных сокращений матери (этап S308). Пользователь повторно перемещает зонд 100 в следующее местоположение на животе матери, пока не загорятся оба индикатора 152, 154 (этап S312), указывая, что время пульсового цикла, клинический доплеровский параметр, было получено и извлечено как для матери, так и для плода.
Пользователь теперь помещает зонд так, чтобы проверить нормальность/аномальность кровотока в соответствующем сосуде матери или плода, который является целевым сосудом (этап S316). Если доплеровский индикатор 150 обнаружения мощности не светится (этап S320), доплеровская мощность в полосе частот 300-1000 Гц, представляющая кровоток, не обнаружена или ее величина недостаточна, чтобы найти один или более кровеносных сосудов. В этом случае, пользователь перемещает или наклоняет зонд 100 (этап S324), пока не загорится индикатор 150.
Когда индикатор загорелся, зонд 100 удерживается на месте несколько секунд, чтобы обработать интересующий объем 106 (этап S328).
Предпочтительно, этот процесс происходит автоматически и без необходимости вмешательства пользователя. Так как отображение кровеносного сосуда не требуется, то не требуется и никакая электронная фокусировка ультразвука. Устройство, таким образом, упрощается и становится дешевым.
Результатом обработки может быть зеленое свечение индикатора 156 нормального кровотока, красное свечение индикатора 158 аномального кровотока или отсутствие любого свечения, если кровеносный сосуд, исследуемый в настоящий момент, не совпадает с целевым сосудом. Если никакой из индикаторов 156, 158 не светится (этап S332), обработка возвращается к этапу S324.
Пример обработки на этапе S328 представлен на фиг.3B. Интересующий объем 106, который может изменяться каждый раз, когда зонд 100 перемещается или наклоняется, но который зафиксирован, когда пользователь удерживает зонд неподвижным, подвергается исследованию на наличие в нем кровеносных сосудов. В частности, вычисляется доплеровская мощность в полосе частот 300-1000 Гц. Это формирует трехмерное (3D) представление сосудов 108-112 в объеме сканирования. Общее количество сосудов в объеме сканирования идентифицируется, используя критерии непрерывности. Например, для 8 непосредственно соседствующих пикселей, то есть 4 боковых и 4 диагональных пикселей, предполагается, что смежные пиксели, для которых обнаружен кровоток, представляют один и тот же кровеносный сосуд. При этом кровеносные сосуды могут отображаться в режиме 3D, так как логические элементы приемника преобразователя могут быть установлены на различные глубины. В режиме 3D используется алгоритм линейной подгонки на основе наименьших квадратов, чтобы найти прямую линию, соединяющую точки, идентифицированные, используя критерий непрерывности. Затем вычисляется угол прямой линии от поверхностей 132 приема ультразвука элементов 126 преобразователя. Это приводит к трехмерной карте, по которой могут быть идентифицированы индивидуальные сосуды и их индивидуальные ориентации. Имея идентифицированные ориентации, по карте можно определить пространственные признаки. Например, при сканировании утробной артерии объем доплеровской выборки обычно помещается в место псевдопересечения утробной и подвздошной артерий. Пересечение определяется как местоположение минимальной суммы квадратов расстояний между пикселями на сосудах (этап S336).
Если карта сосудов не содержит сосуды 108-112 (этап S340), обработка текущего интересующего объема 106 заканчивается, никакой диагноз не предоставляется и управление переходит к этапу S332.
В противном случае, если сосуд 108-112 обнаружен, сосуд из числа тех, которые найдены в интересующем объеме 106, выбирается для анализа потока текучей среды и как кандидат на соответствие целевому сосуду (этап S344). Для выбора может использоваться любой критерий, поскольку выбор кандидатов не заканчивается до тех пор, пока не найден целевой сосуд или пока все сосуды 108-112 в интересующем объеме 106 не будут обработаны.
Информация, относящаяся к выбранному сосуду, формируется, как показано на фиг.2 (этап S348). Информация содержит, например, спектральные характеристики доплеровского сигнала (оценку средней частоты, времени цикла - промежутка времени между 2 последовательными пиками, спектральной ширины - ширины между максимумом и минимумом огибающей частоты на пиках и провалах), время до пика, дефект держателя и клинические доплеровские показатели (такие как, S/D, PI и RI).
На основе собранной информации и ее анализа классификатор 200 кровеносных сосудов классифицирует выбранный сосуд (этап S352).
Если классификация не соответствует целевому сосуду (этап S356) и никакой следующий сосуд из числа найденных в интересующем объеме 106 не существует (этап S360), управление переходит к этапу S332.
В противном случае, если классификация не соответствует целевому сосуду, но существует следующий сосуд, управление возвращается обратно к этапу S344, причем этот следующий сосуд служит в качестве выбранного сосуда (этап S364).
Если, с другой стороны, классификация совпадает с целевым сосудом, зонд 100 делает заключение относительно нормальности кровотока в целевом, то есть, выбранном сосуде. В частности, и для примера, доплеровские параметры сравниваются с номограммами, то есть таблицами, представляющими диапазон ожидаемых доплеровских показателей как функцию внутриутробного возраста плода, чтобы определить, является ли профиль потока нормальным или аномальным (этап S368).
Основываясь на заключении, индикация в отношении нормальности кровотока в выбранном сосуде обеспечивается зеленым свечением индикатора 156 нормального кровотока или красным свечением индикатора 158 аномального кровотока (этап S372).
Хотя методология настоящего изобретения может предпочтительно применяться при предоставлении медицинского диагноза для исследуемого человека или животного, объем применения настоящего изобретения этим не ограничивается. В более широком плане, способы настоящего изобретения направлены на нахождение и проведение анализа потока текучей среды, сосудов в ткани тела в живом организме, в лаборатории или вне живого организма.
То, что здесь предлагается, относится к автоматизированному доплеровскому устройству для предоставления клинического диагноза, основываясь на результате анализа характеристик спектральных доплеровских сигналов. Применениями являются скрининг сонной и почечных артерий, измерения ABI для обнаружения заболевания периферических артерий (PAD), обнаружение трансчерепного кровотечения при травме или других кровоизлияниях в дополнение к оценке состояния плода.
Автоматическое автономное, карманное ультразвуковое устройство для исследования кровеносных сосудов требует меньшего количества элементов преобразователя и представляет упрощенный пользовательский интерфейс без необходимости отображения на экране изображения любого из сосудов. Зонд в одном из вариантов осуществления собирает данные и исследует интересующий объем, ищет целевой сосуд, тестирует сосуд на нормальность кровотока и сообщает диагноз, причем все это делается автоматически и без необходимости вмешательства пользователя. В другом варианте осуществления зонд находит сосуд тела в объеме и извлекает клинический доплеровский параметр, причем все это делается автоматически и без необходимости вмешательства пользователя.
Хотя изобретение было представлено и подробно описано на чертежах и в предшествующем описании, такое представление и описание должны считаться иллюстративными или примерными и не создающими ограничений и изобретение не ограничивается раскрытыми вариантами осуществления.
Например, во время инициализации может назначаться более одного целевого кровеносного сосуда. Они могут обрабатываться в том порядке, в котором были найдены, или во время инициализации может быть указан определенный порядок.
Другие изменения в раскрытых вариантах осуществления могут стать понятны и осуществляться специалистами в данной области техники при практической реализации заявленного изобретения, основываясь на изучении чертежей, раскрытия и приложенной формулы изобретения. В формуле изобретения слово "содержащий" не исключает другие элементы или этапы и единственное число не исключает множественное число. Любые ссылочные позиции в формуле изобретения не должны истолковываться как ограничение объема изобретения.
Компьютерная программа может храниться на мгновение, временно или в течение более длительного промежутка времени на соответствующем считываемом компьютером носителе, таком как оптический носитель или твердотельный носитель. Такой носитель является непередаваемым только в том смысле, что он не является передаваемым, распространяющимся сигналом и, таким образом, может быть реализован, например, как память на регистрах, процессорный кэш или RAM.
Единый процессор или другой блок могут выполнять функции нескольких позиций, упомянутых в формуле изобретения. Простой факт, что определенные критерии повторяются во взаимно различных зависимых пунктах формулы изобретения, не указывает, что объединение этих критериев не может быть использовано с целью достижения преимуществ.
1. Ультразвуковое устройство (100) для ультразвукового анализа потока текучей среды тела, содержащее:
a) ультразвуковой зонд для исследования объема, чтобы найти сосуды тела, присутствующие (S336) внутри объема; и
b) схему управления, сконфигурированную с возможностью осуществления следующих действий: если при упомянутом исследовании (S340) внутри объема находят один или более сосудов, то b1) выбирают для анализа потока текучей среды сосуд из числа упомянутых сосудов, найденных внутри объема (S344), b2) формируют для упомянутого анализа потока текучей среды информацию, конкретно относящуюся к выбранному сосуду (S348), b3) определяют на основе сформированной информации, совпадает ли упомянутый выбранный сосуд с целевым сосудом (S352, S356), при этом действия дополнительно содержат назначение (S304) перед упомянутым исследованием целевого сосуда внутри категории сосудов, причем упомянутая категория основывается на физиологии, и b4) если выбранный сосуд совпадает с целевым сосудом, то тогда b4) (i) предоставляют на основе сформированной информации индикацию в отношении нормального состояния потока текучей среды в выбранном сосуде (S368, S372), в противном случае b4)(ii) повторяют выбор, формирование и определение для следующего сосуда из числа найденных сосудов (S360, S364) до тех пор, пока внутри объема не будет найден никакой другой следующий сосуд из числа сосудов,
причем упомянутые действия по исследованию, выбору, формированию, предоставлению и повтору (i) не зависят от отображения изображений ультразвукового сканирования и (ii) выполняются автоматически и без необходимости вмешательства пользователя для интерпретации изображения ультразвукового сканирования.
2. Ультразвуковое устройство по п. 1, в котором сформированная информация содержит количественную характеристику (232) формы сигнала (114), в которой упомянутая форма сигнала представляется величиной во времени скорости текучей среды в упомянутом выбранном сосуде.
3. Ультразвуковое устройство по п. 2, в котором упомянутые действия дополнительно содержат выполнение упомянутого анализа потока текучей среды на основе сформированной информации и в соответствии с результатом, основанным на упомянутом анализе (248, 252) потока текучей среды, предоставление на основе упомянутой сформированной информации индикации в отношении нормального состояния потока текучей среды в упомянутом выбранном сосуде.
4. Ультразвуковое устройство по п. 3, в котором упомянутые действия дополнительно содержат этапы а) и b); и
с) по меньшей мере до тех пор, пока не выполнено упомянутое предоставление результата, повторяют для упомянутого выбранного сосуда, служащего текущим сосудом (S364), этап b) для каждого следующего сосуда из числа упомянутых найденных сосудов.
5. Ультразвуковое устройство по п. 4, в котором упомянутые действия дополнительно содержат классификацию упомянутого выбранного сосуда, основываясь на упомянутой сформированной информации (S352), причем упомянутое предоставление результата подчиняется упомянутой классификации.
6. Ультразвуковое устройство по п. 1, в котором исследование дополнительно содержит использование ультразвука (216) для получения объемных данных для исследования.
7. Ультразвуковое устройство по п. 1, в котором упомянутые действия дополнительно содержат использование ультразвука для формирования информации, конкретной для выбранного сосуда; и предоставление на основе сформированной информации индикации в отношении нормального состояния потока текучей среды в упомянутом выбранном сосуде (S372).
8. Ультразвуковое устройство по п. 1, в котором ультразвуковое устройство осуществляется как карманное (122) автономное устройство, причем схема управления включает в себя интегральную схему.
9. Ультразвуковое устройство по п. 1, в котором схема управления включает в себя одну или более интегральных схем.
10. Способ для ультразвукового анализа потока текучей жидкости тела, причем упомянутый способ содержит этапы, на которых:
конфигурируют ультразвуковое устройство для выполнения, автоматически и без необходимости вмешательства пользователя для интерпретац