Способ лечения остеохондропатии головки бедренной кости
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к ортопедии. Выполняют ребенку длительную эпидуральную анальгезию с применением катетера, установленного в поясничном отделе позвоночника. При этом лечение проводят без ограничения физической активности. По катетеру дозированно, по 12 часов в сутки вводят лекарственную смесь 0,2% раствора наропина с адреналином 0,2 мкг/мл на протяжении не менее 120-180 часов, при этом индивидуально измеряют скорость введения препарата от 2 до 8 мл в час, добиваясь появления двигательной активности нижних конечностей и выполнения ребенком физических упражнений. Способ позволяет прервать патологический процесс на ранних стадиях остеохондропатии головки бедренной кости, до коллапса хрящевого края, укрепить мышцы бедра, увеличить объем движений в тазобедренном суставе. 4 ил., 1 пр.
Реферат
Изобретение относится к медицине, а именно к ортопедии, и может быть использовано в лечении болезни Легга-Кальве-Пертеса (асептический некроз головки бедренной кости, остеохондропатия головки бедренной кости у детей). Способ применим не только на ранних стадиях в качестве монотерапии, на поздних - в качестве дополнительного лечения к оперативному вмешательству или симптоматическому лечению, но и в нестандартных, сложных случаях, когда стандартное консервативное лечение в виде физиотерапии невозможно, или оперативное лечение заведомо не даст положительного результата.
Патогенез остеохондропатии головки бедренной кости у детей состоит в нарушении гемодинамики за счет спазма венозных и артериальных сосудов области тазобедренного сустава. При недостаточном поступлении артериальной крови и венозном застое наступает ишемия субхондрального слоя головки бедренной кости. Это приводит к некрозу подхрящевого слоя и поэтапному развитию заболевания. Характерным для остеохондропатии головки бедренной кости у детей является конечная стадия восстановления, которая может закончиться полным выздоровлением ребенка в случае отсутствия деформаций головки бедренной кости. Подобная деформация может наступить вследствие ненадлежащего лечения и компрессии со стороны края вертлужной впадины после импрессионного перелома головки бедра. Прерывание патологического процесса в этой стадии возможно путем улучшения кровоснабжения тазобедренного сустава. Одним из вариантов может быть купирование спазма сосудов области тазобедренного сустава путем длительной симпатической блокады и укрепление мышц области тазобедренного сустава. При достижении этого эффекта улучшается кровоснабжение головки бедра, что в совокупности приводит к восстановлению структуры кости и излечиванию заболевания.
Идея использования блокады симпатического отдела нервной системы для улучшения нейротрофической функции принадлежит А.В. Вишневскому (1944) [1]. Также исследования И.А. Ибатуллина (2003) и Н.В. Самойловой показали, что применение регионарных блокад разрешает спазм при ишемиях, восстанавливает нарушенные условия микроциркуляции, осуществляет ликвидацию гипоксии [2, 3].
В исследовании Dr. Brech (2006) группы детей с болезнью Пертеса, как монотерапия, применялась лечебная гимнастика [4]. Лечебные упражнения, заключающиеся в пассивном растяжении мышц пораженного бедра, упражнения на баланс с применением изометрических приемов, проводились ежедневно в течение 2 недель. По сравнению с контрольной группой, где не проводилось лечение, им получены достоверные положительные результаты. Недостатком этого метода является высокий риск прогрессирования заболевания, поскольку отсутствует дополнительное стимулирование кровоснабжения костной ткани, которое позволяет прекратить патологический процесс.
Применение эпидуральной анальгезии имеет ряд преимуществ по сравнению с другими методами. Отличительной особенностью ее, например, от внутритазовой и паравертебральной блокады является быстрота и продолжительность действия при минимальном использовании анестетика. От спинномозговой анестезии отличие состоит в меньшем развитии осложнений, таких как головная боль, повреждение корешков спинного мозга [5].
Известно использование у детей пролонгированной эпидуральной анальгезии в качестве дополняющего метода лечения врожденного вывиха бедра [6]. Лечение заключается во введении каждые 5 ч в эпидуральное пространство через катетер 0,5% Маркаина в дозе 2-2,5 мг/кг массы до момента достижения вправления вывиха бедра, в течение 7 суток. Недостатком данного метода является недостаточно длительное введение препарата и отсутствие полной мышечной функции (развитие миоплегии) ввиду жесткой фиксации в ортезе.
При всем этом известно использование пролонгированной эпидуральной инфузии смеси 0,2%-ного раствора ропивакаина с фентанилом 2 мкг/мл с адреналином 2 мкг/мл со скоростью 5-10 мл/ч, при операциях на позвоночнике, а после операции - проведение постоянной инфузии смеси со скоростью 4-8 мл/ч [7]. Недостатком данного метода является отсутствие у больного полной двигательной функции, так как он предусматривает передвижение больных только при помощи ходунков.
В качестве прототипа предлагаемого изобретения принят способ стойкого купирования болевого синдрома при дегенеративно-дистрофических заболеваниях тазобедренного сустава, включающий введение Наропина 0,2% в эпидуральное пространство, что позволяет обеспечить стабилизацию патологического процесса за счет симпатической блокады [8]. Недостатком этого способа является постоянное введение Наропина 0,2% (240 часов), как следствие - больший расход препарата, и отсутствие специфических методик для закрепления результата.
Сущность изобретения заключается в совокупности существенных признаков, обеспечивающих достижение искомого технического результата, состоящего в прерывании патологического процесса на ранних стадиях остеохондропатии головки бедренной кости, до коллапса хрящевого слоя, что обеспечивает улучшение результатов лечения заболевания, заключающегося в укреплении мышц бедра и увеличении объема движений в тазобедренном суставе.
Сущность способа лечения остеохондропатии головки бедренной кости у детей включает длительную эпидуральную анальгезию с применением катетера, установленного в поясничном отделе позвоночника. Лечение проводят без ограничения физической активности, при этом по катетеру дозированно, по 12 часов в сутки, вводят лекарственную смесь 0,2% раствора наропина с адреналином 0,2 мкг/мл на протяжении не менее 120-180 часов, при этом
индивидуально измеряют скорость введения препарата от 2 до 8 мл в час, добиваясь появления двигательной активности нижних конечностей и выполнения ребенком физических упражнений.
Способ основан на прерывании патологической импульсации симпатической нервной системы области пораженных тазобедренных суставов. Так как симпатический ствол связан с торакоабдоминальным отделом спинного мозга, иннервирующим гладкие мышцы артерий и вен, при медикаментозной симпатэктомии с помощью местного анестетика происходит снижение тонуса сосудистой стенки, и возникает вазодилатационный эффект, что, в свою очередь, способствует улучшению процесса микроциркуляции в области тазобедренного сустава. В отличие от методики эпидуральной анальгезии у взрослых установка катетера при эпидуральной анальгезии у детей проводится под общим наркозом. Минимальный срок введения снижен до 120-180 часов в связи с высокой чувствительностью детского организма к действию местных анестетиков. Суточная доза корригируется путем уменьшения времени введения смеси в течение суток или снижением скорости введения до 2 мл в час, при этом основными критериями служат отсутствие ограничений двигательной функции пациента и купирование болевого синдрома. Применение смеси с адреналином позволило уменьшить расход раствора Наропина 0,2% при неизменных сроках лечения и продлить требуемый эффект с 6 до 12 часов. Соотношение местного анестетика и адреналина, общепринятое в анестезиологической практике, составляет разведение 1 капли 0,01% адреналина на 10 мл раствора анестетика, что соответствует 0,2 мкг/мл [7]. Комплекс упражнений позволяет сохранить полученный результат даже после удаления катетера.
Предлагаемый метод не ограничивает физическую активность и не создает неудобств пациенту, а применение специальных упражнений на укрепление мышц бедра и увеличение объема движений закрепляет и улучшает результат. Принципиальным является продленное, дозированное, периодическое поступление анестетика в эпидуральное пространство, в сочетании с двигательными процедурами во время действия смеси с анестетиком. В низких концентрациях местный анестетик действует селективно, блокируя чувствительные волокна задних корешков и избирательно-вегетативные волокна передних корешков. Адреналин усиливает и продлевает действие местного анестетика, чем достигается требуемый лечебный результат при уменьшении расхода препарата по сравнению с постоянным введением, без двигательных ограничений.
Способ поясняют чертежи, где:
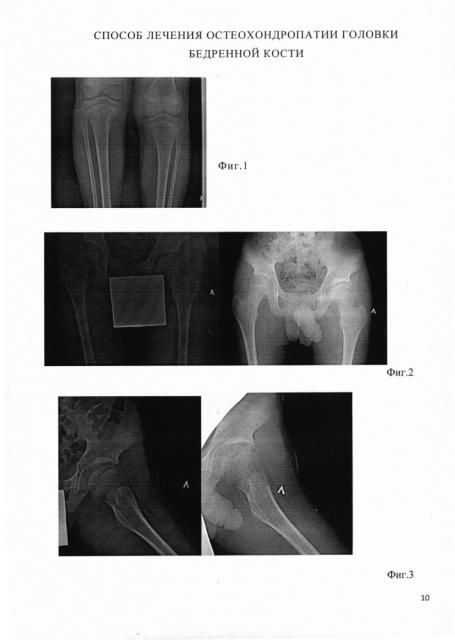
На фиг. 1 - рентгенография голеней в прямой проекции, фиброзная дисплазия верхней трети правой большеберцовой кости.
На фиг. 2 - рентгенограммы тазобедренного сустава в двух проекциях за месяц до начала лечения;
На фиг. 3 - рентгенограммы тазобедренного сустава в двух проекциях через 7 месяцев после курса лечения эпидуральной анальгезии;
На фиг. 4 - функциональные возможности во время проведения эпидуральной анальгезии.
Способ осуществляют следующим образом.
В асептических условиях, под общим обезболиванием, в положении пациента лежа на боку нижние конечности максимально согнуты в тазобедренных суставах, колени приведены к животу, производят пункцию и катетеризацию эпидурального пространства на уровне L2-L3. Катетер по разметке проводят краниально на глубину 3,5-4,0 см. После проведения тест-дозы S. Lidocaini 2% - 4,0 и подтверждения правильного расположения катетера к нему подсоединяют систему дозированной подачи растворов, позволяющую дозаправку.
Ежедневно, периодически, по 12 часов в сутки, в эпидуральное пространство по катетеру вводят смесь раствора местного анестетика Наропин 0,2% с адреналином 0,2 мкг/мл. При необходимости индивидуально изменяют скорость введения от 2 до 8 мл в час, добиваясь появления двигательной активности нижних конечностей. Препараты разрешены в педиатрии, обладают длительным обратимым действием на симпатические волокна, аллергические реакции отмечаются значительно реже, чем при использовании других местных анестетиков [9, 10, 11]. Длительность консервативного лечения - 10-15 суток, что не противоречит общим правилам продленной анестезии [12]. Важным элементом является применение лечебных упражнений при достижении обезболивающего эффекта процедуры при сохранении двигательных возможностей со стороны нижних конечностей. В этой связи суточную дозировку препарата подбирают индивидуально для каждого пациента. Причем в первый и последующие дни она, как правило, отличалась в сторону уменьшения.
Клинический пример.
Пациент Р., 12 лет, жалобы на боль в левом тазобедренном суставе, хромоту в течение четырех месяцев, в апреле 2013 года поставлен диагноз: Болезнь Пертеса слева 1 ст., фиброзная дисплазия верхней трети правой большеберцовой кости. Болевой синдром до лечения составил 5 баллов по визуально аналоговой шкале (ВАШ). Данные микроциркуляции ЛАКК-2 в пораженном тазобедренном суставе составили: снижение М на 78%, дельта σ 0%, коэффициент Kv больше нормы на 342%.
Стандартное консервативное лечение в виде физиотерапии и парафина в данном случае из-за наличия фиброзной дисплазии было противопоказано. От оперативного лечения родители пациента отказались. В асептических условиях, под общей анестезией установлен катетер в эпидуральное пространство на уровне L2-L3. Подача 0,2% Наропина с адреналином 0,2 мкг/мл осуществлялась при помощи инфузионной помпы со скоростью 6 мл в час. Было отмечено снижение силы мышц нижних конечностей. Скорость скорректирована поэтапно до 2 мл в час до восстановления полноценной двигательной функции и наличия симпатического блока. Продолжительность ежедневного введения анестетика составила 12 часов в сутки на протяжении 12 дней. Лечебные упражнения на укрепление и стабилизацию мышц бедра проводились с инструктором ежедневно. После первого курса лечения отмечено улучшение состояния: увеличение сгибания и ротационных движений в тазобедренном суставе, купирование болевого синдрома, улучшение походки.
Через 7 месяцев после проведенного лечения болевой синдром составил 0-1 баллов по ВАШ, микроциркуляция ЛАКК-2 в пораженном тазобедренном суставе увеличина: средний поток крови в интервалах времени (М) увеличился до 4,8 баллов, что на 152% больше по сравнению с нормой, среднее колебание перфузии (σ) увеличилось до 50%, разность коэффициента состояния микроциркуляции (Kv) уменьшилась на 40% по сравнению со здоровым суставом. Такое изменение значений соответствует улучшению микроциркуляции по гиперемическому типу, при котором происходит снижение симпатического влияния.
Функциональные возможности оценены как отличные, улучшилась походка и увеличился объем движений в тазобедренном суставе.
По данным рентгенографии - частичное восстановление высоты головки левой бедренной кости в переднезадней проекции, склерозирование очага некроза в прямой и боковой проекции.
Таким образом, в течение 7 месяцев после проведенного лечения произошел регресс заболевания: улучшилась микроциркуляция области пораженного сустава с купированием болевого синдрома.
По предложенному способу в детском отделении травматологии и ортопедии ГАУЗ "Республиканская клиническая больница" Министерства Здравоохранения Республики Татарстан проведено лечение 13 пациентам, во всех случаях отмечалось выраженное улучшение рентгенологических, лабораторных и клинических показателей.
Источники информации
1. Вишневский А.В. О вагосимпатическом блоке / Хирургия. - 1944. - №4. - С. 16-18.
2. Ибатуллин И.А., Тараско А.Д., Фаизов Т.Т. и др. Регионарные блокады в хирургии: Руководство для врачей. - Казань: Медицина, 2003. - С. 336, - с. 13-14.
3. Самойлова Н.В. и др. Лечение хронического болевого синдрома у пациентов с заболеваниями позвоночника и суставов» Российская научно-практическая конференция с международным участием «Хронические болевые синдромы», тезисы докладов, 23-25 мая, 2007. - С. 116.
4. Brech GC, Guarnieiro R. Evaluation of physiotherapy in the treatment of disease. Clinics (Sao Paulo). 2006 Dec; 61 (6): 521-8.
5. Кузин M.И., Харнас С.Ш. / Местное обезболивание / - М.: Медицина, 1991. – С. 84-119.
6. Патент РФ №2417080, А61K 31/435, A61F 5/00, А61Р 19/02, БИ №12, 2011.
7. Заявка на изобретение №2008117721, А61М 5/142, БИ №31, 2009.
8. Патент РФ №2465926, А61М 19/00, А61Н 31/02, А61K 31/165, А61K 31/02, БИ №31, 2012.
9. Инструкция по применению Наропина. РЛС.
10. Мартов В.Ю. Лекарственные средства в анестезиологии. М.: «Медицинская литература», 2003, стр. 100.
11. Лукьянов Д.С. и др. Эпидуральная анестезия как компонент анестезиологической защиты при операциях на поясничном отделе позвоночника» // Хирургия позвоночника, №3, 2004, - с. 61.
12. Дж. Эдвард Морган-мл. Клиническая анестезиология. Кн. I. - М.: Бином, 1998, - с. 397-398.
Способ лечения остеохондропатии головки бедренной кости у детей, включающий длительную эпидуральную анальгезию с применением катетера, установленного в поясничном отделе позвоночника, отличающийся тем, что лечение проводят без ограничения физической активности, при этом по катетеру дозированно, по 12 часов в сутки вводят лекарственную смесь 0,2% раствора наропина с адреналином 0,2 мкг/мл на протяжении не менее 120-180 часов, при этом индивидуально измеряют скорость введения препарата от 2 до 8 мл в час, добиваясь появления двигательной активности нижних конечностей и выполнения ребенком физических упражнений.