Агент для связывания жиров, полученный из биомассы, образующейся в процессе пивоварения
Иллюстрации
Показать всеИзобретение относится к богатой полисахаридами композиции, содержащей бета-глюкан, хитин и хитозан, извлеченные из клеточной стенки Saccharomyces cerevisiae из биомассы, представляющей собой побочный продукт процесса пивоварения. Способ получения композиции включает следующие стадии: подготовку реактора с помощью раствора NaOH с концентрацией от 0,25 до 3 М при перемешивании и температуре от 50 до 95°С, добавление к указанному раствору биомассы, полученной в процессе пивоварения, поддержание указанных условий в течение по меньшей мере 1 часа. Далее проводят охлаждение указанного раствора до комнатной температуры, нейтрализацию раствора путем по меньшей мере однократного добавления кислого раствора или воды до достижения рН 7. Причем в случае проведения более чем однократного добавления между добавлениями осуществляют стадию отделения твердого продукта от указанного раствора. Затем осуществляют передачу твердого продукта на по меньшей мере однократную промывку водой и отделение полученного твердого продукта, сушку твердого продукта до постоянной массы и тонкое измельчение. Полученную композицию можно приготовить в виде съедобного, фармацевтического или ветеринарного продукта. Изобретение позволяет получить композицию, которая обладает способностью селективного связывания жиров, и поэтому ее можно применять для предотвращения и/или лечения заболеваний, таких как избыточный вес, ожирение, гиперхолестеринемия, гипертриглицеридемия, гипертония и сердечно-сосудистые расстройства. 5 н. и 8 з.п. ф-лы, 5 ил., 18 табл., 9 пр.
Реферат
Настоящее изобретение относится к области медицины и питания, в частности к пищевым добавкам для применения для контроля за массой тела и снижения уровня жиров, негативно влияющих на сердечно-сосудистую систему.
УРОВЕНЬ ТЕХНИКИ
Нездоровые пищевые привычки и образ жизни нашего общества привели к все возрастающей проблеме, связанной со здоровьем населения. Согласно существующей градации в рамках рекомендуемой пирамиды ежедневного приема пищи, наиболее критическими моментами, как было обнаружено, является избыточное потребление насыщенных жирных кислот и холестерина. Рекомендуется 7% насыщенных жирных кислот с точки зрения потребляемой энергии и <250 мг/день холестерина, хотя в реальности указанные значения достигают 15% и 350 мг/день, соответственно. Избыток потребляемой энергии обусловлен, главным образом, избыточным потреблением насыщенных жиров, тогда как избыточное потребление холестерина вызвано избыточным потреблением животных продуктов.
Все эпидемиологические исследования свидетельствуют, что чрезмерное потребление богатой жиром пищи, сопровождающееся уменьшением расхода энергии за счет физической активности, приводит к появлению ряда широко распространенных расстройств здоровья, избыточному весу/ожирению и гиперхолестеринемии, причисляемым к наиболее серьезным расстройствам. Наряду с ухудшением качества жизни, избыточный вес и ожирение связывают в качестве причинных факторов с серьезными неблагоприятными состояниями здоровья, включающими сердечно-сосудистые заболевания, сахарный диабет 2 типа, проблемы с мышечно-скелетной системой и рак. С другой стороны, полагают, что гиперхолестеринемия, поскольку она приводит к атеросклерозу, является основным фактором риска развития коронарных заболеваний сердца - основной причины смерти в развитых странах.
В связи с вышеизложенным, отпускаемые без рецепта гиполипидемические средства, которые могли бы способствовать уменьшению массы тела и понижению уровня холестерина, становятся все более популярными. В результате, независимо от их варьирующей и не всегда в полной мере обоснованной эффективности, на рынке продается множество безрецептурных гиполипидемических пищевых добавок. Среди указанных добавок хитозан, доступный в форме капсул и таблеток, рекламируется как препарат, способный как понизить холестерин, так и вызвать быструю потерю веса.
Хитозан представляет собой полиаминосахарид, полученный из хитина. Хитин, один из наиболее обильно возобновляемых органических ресурсов в природе, обнаруживаемый, главным образом, в наружном скелете ракообразных, с химической точки зрения представляет собой линейный полимер, состоящий из N-ацетил-D-глюкозаминовых звеньев и D-глюкозаминовых звеньев, связанных β-(1-4)-гликозидной связью, причем N-ацетил-D-глюкозаминовые звенья в такой полимерной цепи преобладают. Деацетилированную форму хитина называют хитозаном. Хитин обычно относят к сополимеру со степенью ацетилирования более 40% [т.е. количеством N-ацетил-D-глюкозамина более 40% и количеством D-глюкозамина менее 60%], при этом хитин нерастворим в разбавленных кислотах. Название хитозан применяют для сополимера с степенью ацетилирования (DA) менее 40% [т.е. СД (степень деацетилирования) более 60%, количество N-ацетил-D-глюкозамина менее 40% и количество D-глюкозамина более 60%], который в большинстве случаях будет растворим в разбавленной кислоте. Хитин и хитозан с химической точки зрения можно рассматривать как аналоги целлюлозы, в которой гидроксилы при углероде-2 были заменены на ацетамидо- и аминогруппы, соответственно. Хитозан обладает ярко выраженными химическими и биологическими свойствами, связанными с присутствием нескольких аминогрупп в его молекулах. Его можно использовать в различных процессах, включая медицинское лечение, что возможно благодаря отличной биосовместимости и физиологической инертности хитозана.
Хитин и хитозан обнаружены в качестве придающих жесткость материалов у многих водных организмов (в раковинах креветок и крабов и в костяных пластинах кальмаров и каракатиц), у многих насекомых, у наземных ракообразных (Armadillidium vulgare, Porcellio scaber), у нематод, в грибах, и в некоторых микроорганизмах (дрожжах, грибках и водорослях). Раковины водных животных содержат приблизительно 30-40% белка, 30-50% карбоната кальция и 20-30% хитина в пересчете на сухое вещество. Указанные пропорции меняются в зависимости от вида ракообразного и сезона. Традиционно хитин производят путем декальцинации и депротеинизации раковин крабов или креветок, что включает растворение карбоната кальция в растворе кислоты и удаление белков в щелочной среде или с помощью ферментов, соответственно. Хитозан также можно получить путем деацетилирования хитина с помощью горячего щелочного раствора и на стадии изменения окраски. Такой способ получения хитозана характеризуется рядом неблагоприятных особенностей. Например, указанный способ требует применения дорогостоящей тепловой энергии и едкой щелочи, которая представляет собой потенциальную опасность для здоровья. Указанный способ также приводит к образованию больших количеств отходов, что, тем самым, требует значительных расходов на их удаление. Кроме того, поставка раковин креветок или крабов сильно зависит от сезонных и экологических факторов, что приводит к непредсказуемым ограничениям производственной мощности и нестабильным физико-химическим характеристикам конечных продуктов, предназначенных для использования в медицине и сельском хозяйстве. Кроме того, хитозан, полученный из раковин креветок, может передавать в конечный продукт антигены, что может вызвать аллергии у потребителя. Таким образом, хотя хитозан клинически хорошо переносится, его нельзя рекомендовать людям, имеющим аллергию на ракообразных. Указанные проблемы можно обойти путем выделения хитозана из других источников.
Настоящее исследование направлено на извлечение чистого хитозана из компонентов клеточных стенок грибков. С этой целью N. Nwe с соавторами исследовал связь между хитозаном и глюканом в грибковой клеточной стенке для разработки ферментативного способа получения очень чистого хитозана из грибка Gongroella butleri с высоким выходом (N. Nwe et al. 2010, «Production of fungal chitosan by enzymatic method and applications in plant tissue culture and tissue engineering: eleven years of our progress, present situation and future prospects» Biopolymers, edited by Magdy Elnashar, published: September 28, 2010, chapter 7, pp. 135-162).
В ЕР 1483299 описан способ, позволяющий отделить хитин от β-глюканов контролируемым путем без разрушения или превращения хитиновых цепей. Указанный способ основан на приведении в контакт грибковых клеток Aspergillus niger с щелочным раствором, приведении в контакт нерастворимой в щелочи фракции с кислым раствором, и, тем самым, получение суспензии подкисленной нерастворимой в щелочи фракции, содержащей указанные производные клеточной стенки, и в конце приведение в контакт указанной суспензии с β-глюканазными ферментами с получение продукта, представляющего собой хитин, или с хитиндезацетилазой с получение продукта, представляющего собой хитозан.
Одним из применений хитозана является применение в качестве пищевой антилипидемической добавки, при котором вследствие ограниченного гидролиза под действием пищеварительных ферментов человека хитозан проходит по пищеварительной системе до толстой кишки практически интактным, эффективно действуя подобно пищевому волокну. Как полагают, хитозан уменьшает всасывание жиров из желудочно-кишечного тракта путем связывания с анионными карбоксильными группами жирных и желчных кислот и препятствует эмульгированию нейтральных липидов (т.е. холестерина, других стеринов) путем их связывания с помощью гидрофобных связей. Антигиперлипидемический потенциал хитозана был изучен как in vivo, так и in vitro. Исследования in vivo включают испытания, проводимые как на животных, так на людях, и состоят из определения различных параметров, главным образом, массы тела, уровней липидов в сыворотке и концентраций липидов в экскрементах. Удивительно, но приведенные данные являются противоречивыми. Хотя испытания на животных в основном показали уменьшение влияния хитозана на массу тела и уровни холестерина (Н. Yao et al., «Effect of chitosan on plasma lipids, hepatic lipids, and fecal bile acid in hamsters human trials failed to show these effects» J. Food Drug Anal. 2006, vol. 14, pp. 183-189), испытания на людях не показали такие эффекты (M.D. Gades et al., «Chitosan supplementation and fat absorption in men and women» J. Am. Diet. Assoc. 2005, vol. 105, pp. 72-77, C.N. Mhurchu et al., «Effect of chitosan on weight loss in overweight and obese individuals: a systematic review of randomized controlled trials» Obes. Rev. 2005, vol. 6, pp. 35-42).
Составы пищевых добавок на основе хитозана похожи, но не идентичны. Сам хитозан представляет собой продукт химического деацетилирования сырьевого материала - хитина, при этом степень деацетилирования продукта меняется в зависимости от условий реакции. Некоторые факторы при обработке, такие как степень деацетилирования и молекулярная масса молекул, соотношение хитин/хитозан, растворимость, ионная сила, рН, размер частиц, и температура, влияют на получение хитозана и его свойства. Можно ожидать, что эффективность хитозана будет зависеть от его физико-химических свойств. Однако не было установлено корреляции между связывающей способностью и измеренными физико-химическими свойствами хитозана. Наряду с прочим, это указано в исследовании, в котором описана способность связывать желчные кислоты, способность связывать жиры, способность к набуханию, степень деацетилирования и вязкость 11 выбранных препаратов хитозана в растворе (K. Zhou et al., «In vitro binding of bile acids and triglycerides by selected chitosan preparations and their physico-chemical properties» Food Science and Technology 2006, vol. 39, pp. 1087-1092).
Пищевые добавки на основе хитозана продают в качестве «ловушек жира» и «жировых магнитов». Рекламные утверждения в отношении некоторых из указанных добавок могут дать потребителю несбыточные ожидания. Хотя согласно рекламным объявлениям такие добавки способны как понизить холестерин, так и привести к быстрой потере массы тела, они одновременно могут вызвать антипитательные эффекты вследствие их способности также улавливать молекулы на основе липидов, которые являются полезными для здоровья человека, такие как растворимые в жирах витамины А, D, Е, K, холестерин липопротеинов высокой плотности, растительные стерины и полиненасыщенные жирные кислоты, такие как омега жирные кислоты 3 и 6.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложена богатая полисахаридами композиция, содержащая бета-глюкан, хитин и хитозан, извлеченные из клеточной стенки Saccharomyces cerevisiae из биомассы, представляющей собой побочный продукт процесса пивоварения, способ получения указанной композиции и ее применение. Так как композиция согласно изобретению богата полисахаридами (хитином, хитозаном и бета-глюканом), в настоящем описании ее называют «богатой полисахаридами композицией». «Композиция», «продукт» и «композиция согласно изобретению» также используют взаимозаменяемо и относятся к композиции согласно настоящему изобретению.
Соответственно, первый аспект настоящего изобретения относится к способу получения богатой полисахаридами композиции, содержащей бета-глюкан, хитин и хитозан, извлеченные из клеточной стенки Saccharomyces cerevisiae из биомассы, представляющей собой побочный продукт процесса пивоварения, включающему следующие стадии:
i) подготовку реактора с помощью раствора NaOH при концентрации от 0,25 до 3 М при перемешивании и температуре от 50 до 95°С;
ii) добавление к указанному раствору биомассы, полученной в процессе пивоварения;
iii) поддержание указанных условий в течение по меньшей мере 1 ч;
iv) охлаждение указанного раствора до комнатной температуры;
v) нейтрализация раствора путем по меньшей мере однократного добавления кислого раствора или воды до достижения рН 7, причем в случае проведения более чем однократного добавления между добавлениями осуществляют стадию отделения твердого продукта от указанного раствора;
vi) отделение твердого продукта, полученного на стадии (v), от указанного раствора;
vii) после проведения нейтрализации на стадии (v) путем добавления кислого раствора передачу твердого продукта на по меньшей мере однократную промывку водой и отделение полученного твердого продукта; и
viii) сушку твердого продукта до постоянной массы и тонкое измельчение.
Другой аспект настоящего изобретения состоит в обеспечении композиции, получаемой по способу, описанному выше.
С учетом оказания на человека нескольких положительных эффектов, композицию согласно изобретению можно применять в качестве терапевтического или профилактического средства. Таким образом, другой аспект настоящего изобретения относится к композиции согласно изобретению для применения в качестве профилактического и/или терапевтического средства. В частности, композиция применима для предотвращения и/или лечения у животного, в том числе, у человека, расстройства, выбранного из группы, состоящей из избыточного веса, ожирения, гиперхолестеринемии, гипертриглицеридемии, гипертонии и сердечно-сосудистых расстройств. В настоящем изобретении описано применение композиции для производства лекарственного средства для предотвращения и/или лечения упомянутых выше расстройств. Этот аспект можно альтернативно сформулировать как способ предотвращения и/или лечения у животного, в том числе, у человека, расстройства, выбранного из группы, состоящей из избыточного веса, ожирения, гиперхолестеринемии, гипертриглицеридемии, гипертонии и сердечно-сосудистых расстройств, включающий введение указанному животному, нуждающемуся в этом, эффективного количества композиции согласно изобретению.
Еще один аспект настоящего изобретения относится к композиции согласно изобретению для применения в качестве средства для связывания жиров в пищеварительном тракте.
В другом аспекте композицию согласно изобретению можно применять в качестве детоксицирующего средства.
В другом аспекте композицию согласно изобретению можно применять в качестве иммуностимулирующего средства.
Другой аспект настоящего изобретения относится к фармацевтическому и/или ветеринарному средству, содержащему эффективное количество композиции, описанной выше, совместно с подходящими количествами фармацевтически или ветеринарно приемлемых вспомогательных веществ. В настоящей заявке термин «эффективное количество» означает количество активного вещества, достаточно высокое для обеспечения требуемого благоприятного воздействия, но достаточно низкое для избежания побочных эффектов в рамках медицинских представлений.
Дополнительный аспект настоящего изобретения относится к съедобному продукту, содержащему эффективное количество композиции согласно изобретению совместно с подходящими количествами других съедобных ингредиентов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Клеточные стенки Saccharomyces cerevisiae могут содержать от 20 до 30% сухой клеточной массы. Указанная масса главным образом состоит из маннопротеинов и бета-глюканов и меньших количеств хитина и липидов. Соотношение указанных компонентов может варьировать в зависимости от штаммов и условий культивирования. Как было описано выше, в данной области техники существуют способы выделения хитозана из компонентов грибковых клеточных стенок. С другой стороны, в данной области техники также описаны способы получения бета-глюканов из дрожжей и, в частности, из Saccharomyces cerevisiae. В WO 91/03495 описаны способы получения растворимых глюканов для стимулирования выработки тромбоцитов. Один из способов начинается с обработки целых глюкановых частиц, предварительно полученных из высушенных пекарских дрожжей согласно процедуре, описанной Jamas с соавторами в US 4810646, и включает дополнительные стадии растворения нерастворимых глюкановых частиц. Другой способ, описанный в примере 2 указанной патентной заявки, относится к последовательности стадий обработки для получения растворимых глюканов из выбранного штамма S.cerevisiae.
Таким образом, несмотря на то, что в данной области техники описаны способы получения с одной стороны хитина/хитозана и с другой стороны бета-глюканов из дрожжей, качество и количество конечного продукта, извлеченного из грибного мицелия, зависят от происхождения гриба, условий его роста (состава сбраживаемой среды: источника и концентрации углерода, источника и концентрации азота, а также ионов металлов и их концентрации; и условий брожения: размера инокулята, времени сбора, температуры сбраживания); и от стадий процесса извлечения.
В настоящем изобретении описан промышленный способ получения богатой полисахаридами композиции. Указанный способ включает стадии, описанные в предыдущем разделе. Реактор получают с применением раствора NaOH при концентрации от 0,25 до 3 М при перемешивании и температуре от 50 до 95°С. Согласно конкретным вариантам реализации настоящего изобретения концентрацию NaOH выбирают из 0,25, 0,50, 0,75, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9 и 3 М. В частности, концентрация NaOH составляет от 0,25 до 1,5 М. Более конкретно, концентрация NaOH составляет 0,25 М. Согласно другому конкретному варианту реализации изобретения концентрация NaOH составляет 1 М.
Согласно другому варианту реализации настоящего изобретения обработку раствором NaOH в реакторе выполняют при температуре, выбранной из 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94 и 95°С. В частности, температура составляет от 65 до 85°С, и более конкретно 80°С.
Согласно одному из вариантов реализации настоящего изобретения после охлаждения раствора (стадия (iv)), раствор нейтрализуют путем добавления кислого раствора для достижения рН 7 и твердую фазу отделяют от раствора. В частности, кислый раствор представляет собой раствор фосфорной кислоты, раствор HCl или раствор уксусной кислоты. Далее, твердый продукт передают на по меньшей мере одну промывку водой. Между промываниями твердый продукт отделяют от раствора.
Согласно другому варианту реализации настоящего изобретения стадию нейтрализации осуществляют путем по меньшей мере однократного добавления воды, в частности дистиллированной воды. Если осуществляют более чем однократное добавление, стадию отделения твердого продукта от раствора осуществляют в промежутке между добавлениями. При осуществлении нейтрализации путем добавления воды нет необходимости промывать твердую фазу после нейтрализации, но такую промывку можно выполнить при необходимости получения более чистого твердого продукта.
Согласно конкретному варианту реализации настоящего изобретения до проведения нейтрализации указанный способ включает стадию, которая состоит в отделении твердого продукта от раствора после охлаждения. Отделение осуществляют, например, путем центрифугирования. При промышленном масштабе партия 2, например, была сделана при добавлении такой стадии.
Согласно конкретному варианту реализации настоящего изобретения биомассу, полученную в процессе пивоварения, добавляют в реактор в количестве от 1:2 до 1:5. В частности, это количество составляет 1:3. Указанное количество выражено как влажная биомасса: раствор NaOH. Как видно из примеров, таким способом были приготовлены партии 2-4 при добавлении биомассы в количествах 1:3 (партия 2 и 3) и 1:2 (партия 4). Если указанные количества выразить в пересчете на высушенный продукт, количества, применяемые в указанном примере, будут составлять 1:39 и 1:23, соответственно.
Таким образом, биомассу, представляющую собой побочный продукт процесса пивоварения, можно добавить в реактор вместе с раствором NaOH, направляя непосредственно из процесса пивоварения. Соответственно, такая биомасса является влажной (в настоящей заявке ее называют «влажной биомассой»), поскольку содержит примеси процесса пивоварения.
Биомассу, представляющую собой побочный продукт процесса пивоварения, можно также ввести в реактор в высушенном виде. Следовательно, согласно другому варианту реализации изобретения способ дополнительно включает предварительную обработку биомассы, полученной в процессе пивоварения, перед добавлением биомассы к раствору NaOH. Предварительная обработка включает следующие стадии: (а) просеивание биомассы для отделения биомассы Saccharomyces cerevisiae от примесей процесса пивоварения; (b) сушку биомассы S.cerevisiae, полученной на стадии (а); и (с) измельчение продукта S.cerevisiae, полученного на стадии (b). В этом случае высушенный продукт S.cerevisiae добавляют в реактор в количестве от 1:20 до 1:40 мас./об. В частности, указанное количество составляет 1:30 мас./об. Как видно из примеров, таким способом была приготовлена партия 1 при добавлении биомассы в количестве 1:30.
Указанные условия в реакторе поддерживают в течение по меньшей мере 1 часа. В частности, условия поддерживают от 5 до 20 ч и, предпочтительно в течение 16 ч. Согласно другому варианту реализации изобретения реакция заняла 10 ч (см., например, партию 4).
Конечный продукт сушат и в конце подвергают тонкому измельчению. Продукт предпочтительно помещают в стеклянные лотки и сушат в вакуумной печи при 60°С до постоянной массы и затем подвергают тонкому измельчению. Сушку можно выполнить под вакуумом для уменьшения длительности процесса. Согласно конкретному варианту реализации изобретения сушку осуществляют путем распылительной сушки продукта до содержания растворителя ниже 5% по массе.
Настоящее изобретение охватывает все возможные комбинации конкретных условий, описанных в настоящей заявке. Приведенные ниже примеры (партии 1-4) показывают, что определенные условия реакции и стадии процесса могут варьировать без значительного изменения характеристик продукта (как можно видеть в разделе 9.4 при описании примеров).
В результате указанного процесса получают композицию, содержащую бета-глюкан, хитин и хитозан, полученные из клеточной стенки S.cerevisiae. Согласно одному из вариантов реализации настоящего изобретения соотношение хитозана, хитина и бета-глюкана в композиции составляет от 1:10:80 до 1:20:150. Согласно другому варианту реализации настоящего изобретения растворимость композиции при рН 3,5 в дистиллированной воде составляет от 650 до 800 мг/л. Согласно другому варианту реализации настоящего изобретения процентное содержание на основе атомной массы углерода, водорода и азота в композиции составляет, соответственно, от 36 до 44% для углерода, от 5,5 до 7% для водорода и от 0,2 до 0,8% для азота.
Согласно конкретному варианту реализации настоящего изобретения процесс получения композиции осуществляют при концентрации NaOH 0,25 М при 80°C с применением в реакторе высушенного продукта S.cerevisiae в количестве 1:30 мас./об. при времени реакции 16 ч. Химические свойства композиции, полученной при указанных условиях, описаны ниже в разделе 2 ПРИМЕРЫ. В частности, соотношение хитозана, хитина и бета-глюкана в композиции составляет 1:14:116; растворимость композиции при рН 3,5 в дистиллированной воде составляет 710 мг/л; и процентное содержание на основе атомной массы углерода, водорода и азота в композиции составляет 40,32, 6,35 и 0,24%, соответственно.
Согласно конкретному варианту реализации настоящего изобретения процесс получения композиции проводят при концентрации NaOH 0,25 М, при 80°C с применением в реакторе влажной биомассы S.cerevisiae в количестве 1:3, при времени реакции 16 ч. Перед стадией нейтрализации продукт отделяют от раствора после охлаждения. Согласно конкретному варианту реализации изобретения полученный продукт имеет свойства, описанные в разделе 9.4 Партия 2.
Согласно конкретному варианту реализации настоящего изобретения процесс получения композиции проводят при концентрации NaOH 0,25 М, при 80°C с применением в реакторе влажной биомассы S.cerevisiae в количестве 1:3 при времени реакции 16 ч. После гидролиза смесь сразу же нейтрализуют путем добавления кислого раствора (без первого центрифугирования реакционной смеси). После нейтрализации смесь центрифугируют и затем промывают. Согласно конкретному варианту реализации изобретения полученный продукт имеет свойства, описанные в разделе 9.4 Партия 3.
Согласно конкретному варианту реализации настоящего изобретения процесс получения композиции проводят при концентрации NaOH 0,32 М при 80°C с применением в реакторе влажной биомассы S.cerevisiae в количестве 1:2 при времени реакции 10 ч. После гидролиза смесь сразу же нейтрализуют путем добавления кислого раствора (без первого центрифугирования реакционной смеси). После нейтрализации смесь центрифугируют и затем промывают. Согласно конкретному варианту реализации изобретения полученный продукт имеет свойства, описанные в разделе 9.4 Партия 4.
β-Глюканы известны как модификаторы биологического отклика благодаря их способности активировать иммунную систему. Кроме того, Европейское агентство по безопасности продуктов питания (EFSA) согласно недавнему научно-обоснованному мнению пришло к выводу, что между потреблением бета-глюканов и снижением концентраций холестерина в крови можно установить причинно-следственную связь. Пищевым компонентом, который подвергался исследованию, были бета-глюканы, которые представляли собой растворимые злаковые волокна. Что касается контроля за массой тела, ни одна из ссылок, предоставленных EFSA, не касается влияния потребления бета-глюкана на массу тела, поэтому экспертная группа пришла к выводу, что между потреблением бета-глюканов и поддержанием или достижением нормального веса причинно-следственную связь не была установлена (Scientific Opinion on the substantiation of health claims related to beta glucans and maintenance of normal blood cholesterol concentrations (ID 754, 755, 757, 801, 1465, 2934) and maintenance or achievement of a normal body weight (ID 820, 823) pursuant to Article 13(1) of Regulation (EC) №1924/2006 EFSA Journal 2009; vol. 7(9) pp. 1254 [18 pp.]).
Неожиданно оказалось, что в клинических испытаниях на людях композиция согласно изобретению на основе смеси бета-глюканов и хитина/хитозана, выделенных из биомассы Saccharomyces cerevisiae, полученной в процессе пивоварения, проявляла липид-специфический снижающий эффект, а также эффект понижения массы тела и уменьшение окружности талии.
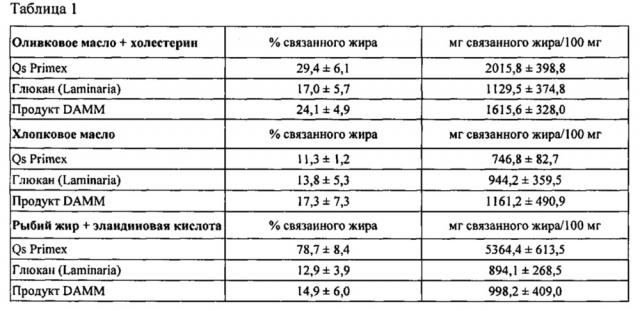
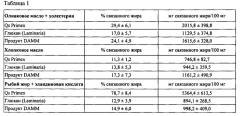
Демонстрационные примеры, приведенные ниже, показали, что композиция согласно изобретению приводила к значительному усилению способности улучшать липидный профиль потребления. Согласно конкретному варианту реализации настоящего изобретения композиция имеет жиросвязывающую способность, по меньшей мере в 10 раз большую ее массы, как определено согласно анализу, включающему: i) приведение хлопкового масла в контакт с композицией в кислом растворе в течение двух часов при 37°С и при постоянном перемешивании; ii) центрифугирование раствора для отделения хлопкового масла, связанного с композицией, от несвязанного хлопкового масла, присутствующего в надосадочной жидкости; iii) смешивание надосадочной жидкости с гексаном и центрифугирование смеси; и iv) извлечение верхней фазы центрифугированной смеси, что позволяет гексану испаряться, и взвешивание несвязанного хлопкового масла. Указанный анализ также подробно описан в разделе 3 ПРИМЕРЫ.
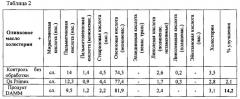
Кроме того, описанные ниже демонстрационные примеры показали, что животные, которых кормили продуктом согласно настоящему изобретению, проявляли меньшее увеличение массы тела по сравнению с похожими коммерческими связывателями жиров, используемыми в качестве контрольных групп. Эффективность потребления энергии (г прибавленного веса на ккал съеденного корма) представляет собой величину, которая четко показывает эффективность продукта с точки зрения уменьшения всасывания. В этом случае продукт согласно настоящему изобретению понижал общее всасывание жиров, измеряемое как общая эффективность питания, по сравнению с контрольными группами. Потребление продукта согласно настоящему изобретению не приводило к значительному увеличению фекальной экскреции у животных. Такой же вывод нельзя сделать для группы, принимавшей коммерческий продукт (хитозан S). Продукт хитозан S приводил к чрезвычайно высоким значениям экскреции и сухого вещества. Этот факт, в отличие от того, что происходит с продуктом согласно настоящему изобретению, означает, что имеется неселективный эффект в случае продукта хитозан S, который не будет специфически связывать жир, но связывает многие другие питательные вещества. Таким образом, продукт согласно настоящему изобретению имеет преимущество, состоящее в отсутствии антипитательных эффектов, оказываемых другими коммерческими связывателями жиров, как показано в приведенных примерах. Селективное связывание жиров представляет большой интерес, поскольку экскреция насыщенных жирных кислот значительно возрастала после потребления продукта DAMM. Далее и по всему тексту настоящего документа продукт, получаемый в результате процесса, описанного в разделе ПРИМЕР 1, также называют «продуктом DAMM» или «партией 1». Экскреция мононенасыщенных жирных кислот возрастала, хотя результаты не были статистически значимыми, тогда как экскреция полиненасыщенных жирных кислот не увеличивается.
Жиросвязывающее действие продукта согласно настоящему изобретению было также продемонстрировано in vivo на людях. Результаты функциональных клинических испытаний на людях показали снижение массы тела на 0,7 кг и уменьшение окружности талии на 2 см, в то время, как группа, принимавшая плацебо, в целом демонстрировала увеличение на 1,4 кг после лечения в течение 3 месяцев. После приема продукта наблюдали уменьшение общего содержания жира в организме на 0,82%. Наблюдали перераспределение жира, в результате которого происходило уменьшение ее накопления в брюшной области. Такое перераспределение связано с потенциальным положительным воздействием, направленным на уменьшение факторов риска сердечно-сосудистых заболеваний, гипертензии и диабета. На основании указанных результатов можно сделать вывод, что предложенный продукт способствует потере массы тела, при этом общее уменьшение массы составляет 2,1 кг и уменьшение окружности талии составляет 2 см после 3 месяцев лечения. Указанные результаты являются клинически значимыми, поскольку результаты уменьшения массы и окружности талии были получены в отсутствии специальной ограничительной диеты и в течение короткого времени лечения (3 месяцев).
Помимо действия в виде селективного уменьшения всасывания входящих в рацион жиров, композиция согласно изобретению также проявляла биофункциональные возможности при метаболизме глюкозы. В пероральных тестах толерантности к глюкозе на животной модели максимальная концентрация глюкозы в крови, в частности, в момент непосредственно после приема пищи, продемонстрировала снижение по сравнению с отрицательным контролем и одинаковый порядок при положительном контроле с применением коммерческого препарата.
Продукт согласно настоящему изобретению также продемонстрировал, что его можно использовать в качестве детоксицирующего агента, поскольку он захватывает различные соответствующие токсичные вещества: микотоксин афлатоксин В1, ртуть, полихлорированные бифенилы (ПХБ 209) и фуран.
Другие воспроизведения способа получения композиции позволили получить гомогенный продукт, который сохранял такие же описанные биологические функциональные свойства. Таким образом, преимущество способа и продукта согласно изобретению состоит в том, что свойства и полезность конечного продукта не зависят от сырьевого материала, как это имеет место в случае хитина/хитозана, извлеченного из ракообразных. Дополнительным и важным преимуществом является то, что с помощью способа согласно настоящему изобретению можно получать идентичный материал в течение всего года; и извлеченная композиция не содержит тяжелые металлы, такие как никель, медь, которые присутствуют в композициях, выделенных из ракообразных.
Согласно другому варианту реализации изобретения способ получения богатой полисахаридами композиции включает вторую термощелочную обработку для изменения степени деацетилирования хитина. Таким образом, после нейтрализации и отделения твердого продукта, полученного в результате первой реакции, продукт направляют на вторую обработку с применением NaOH при концентрации от 25 до 50% при температуре от 40 до 80°С и при времени реакции от 30 до 240 минут. В частности, концентрацию NaOH выбирают из 25, 37,5 и 50%. Температуру реакции выбирают между 40, 60 и 80°С; и время выбирают между 30, 120, 135 и 240 минутами. Как показано ниже в демонстрационных примерах (раздел 7), продукты, полученные в результате такой обработки, применимы в качестве детоксицирующих агентов, поскольку они способны захватывать различные важные токсичные вещества: микотоксин афлатоксин В1, ртуть, полихлорированные бифенилы (ПХБ 209) и фуран.
Согласно другому варианту реализации изобретения фракции, полученные в результате такой второй термощелочной обработки, можно применять в качестве иммуностимулирующих средств, как показано ниже в демонстрационном примере (раздел 7). В частности, в исследовании in vivo, принимающие добавки животные проявляли улучшенные защитные свойства против бактериальных инфекций вследствие увеличения процентного содержания активированных клеток с окислительной активностью. Конкретная композиция, применимая в качестве иммуностимулирующего средства, представляет собой композицию, полученную путем гидролиза исходного продукта в течение 30 минут с применением 25% NaOH при 40°С, полученную способом, описанным в разделе 1 ПРИМЕРЫ.
В настоящем изобретении также предложены фармацевтические и/или ветеринарные продукты, которые содержат эффективное количество композиции согласно изобретению совместно с соответствующими количествами фармацевтически или ветеринарно приемлемых вспомогательных веществ. В этом отношении фармацевтический продукт можно получить для перорального введения в форме таблеток, пилюль, капсул, микрокапсул, гранул, суспензий, сиропов, сухих порошков, жидких препаратов и т.п. Выбор вспомогательных веществ и наиболее подходящих способов приготовления с учетом конкретной цели композиции находится в рамках компетенции обычных специалистов в области технологии фармацевтического производства. Пероральное введение является предпочтительным.
В настоящей заявке термин «фармацевтически приемлемый» относится к соединениям, материалам, композициям и/или лекарственным формам, которые в рамках разумных медицинских представлений подходят для применения при контакте с тканями субъекта (например, человека), не вызывая избыточной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, в соответствии с разумным соотношением польза/риск. Каждый носитель, вспомогательное вещество и т.п. также должен быть "приемлемым» в смысле совместимости с другими ингредиентами состава. Подходящие носители, вспомогательные вещества и т.п. можно обнаружить в стандартных фармацевтических текстах. Подобным образом, термин "ветеринарно приемлемый" означает подходящий для применения при контакте с тканями животных, не относящихся к человеку.
Кроме того, композиция согласно изобретению может включать различные съедобные продукты, такие как молочный продукт, йогурт, творог, сыр (например, кварк, творожный сыр, обработанный, мягкий и твердый), кисломолочный продукт, сухое молоко, сброженный продукт на основе молока, мороженое, сброженный продукт на основе зерновых, порошок на основе молока, напиток, заправка и корм для животных. В настоящей заявке термин "съедобный продукт" применяют в самом широком смысле, включающем любой вид продукта, изготовленный в любой форме, которую животное может принять вовнутрь, но за исключением фармацевтических и ветеринарных средств. Примерами других съедобных продуктов являются мясные продукты (например, печеночный паштет, сосиска и колбасы типа салями или мясные пасты), шоколадные пасты, начинки (например, трюфельные, сливочные) и глазури, шоколад, кондитерские изделия (например, карамель, помадки или тоффи), хлебобулочные изделия (кексы, кондитерская выпечка), соусы и супы, фруктовые соки и забеливатели кофе. Особенно интересными съедобными продуктами являются пищевые добавки и детские смеси. С точки зрения настоящего изобретения, пищевые добавки также включают нутрицевтики, которые, как известно, представляют собой экстракты из пищевых продуктов, оказывающие лечебный эффект на здоровье человека. В объем настоящего изобретения также включены фуражные растения для корма для животных. Композиции