Литий-ионный аккумулятор
Иллюстрации
Показать всеИзобретение относится к электротехнической промышленности и может быть использовано при производстве литий-ионных аккумуляторов (ЛИА) и батарей на их основе, предназначенных для использования в качестве накопителей энергии для электротранспорта, альтернативной энергетики, источников бесперебойного питания, систем рекуперации электроэнергии и выравнивания сетевых нагрузок. В конструкции предлагаемого литий-ионного аккумулятора сочетается активный материал отрицательного электрода на основе Li4Ti5O12 и активный материал положительного электрода на Li3V2(PO4)3. Активный материал отрицательного электрода на основе Li4Ti5O12 может быть допирован хромом по позициям титана и представляет собой соединение состава Li4Ti5-xCrxO12, где 0<x≤0,2. Активный материал положительного электрода может быть допирован натрием по позициям лития, одним или несколькими металлами из группы, содержащей магний, алюминий, иттрий и лантан по позициям ванадия, фтором или хлором по позициям фосфата, и представляет собой соединение состава Li3-xNaxV2-yMy(PO4)3-zHalz/C, где М - один или несколько металлов из группы, содержащей Mg, Al, Y, La; Г=F, Cl; 0<x≤0,1; 0<y≤0,2; 0<z≤0,16. Кристаллы активных материалов отрицательного и положительного электродов могут быть покрыты поверхностным слоем углерода, который получен за счет введения в смесь исходных реагентов углеродсодержащего прекурсора - крахмала. Изобретение позволяет создать конструкции высокоэнергоемких ЛИА с повышенными мощностью, безопасностью и стабильностью при циклировании. 4 з.п. ф-лы, 4 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к электротехнической промышленности и может быть использовано при производстве литий-ионных аккумуляторов (ЛИА) и батарей на их основе, предназначенных для использования в качестве накопителей энергии для электротранспорта, альтернативной энергетики, источников бесперебойного питания, систем рекуперации электроэнергии и выравнивания сетевых нагрузок.
УРОВЕНЬ ТЕХНИКИ
Значительный прогресс в технологии литий-ионных аккумуляторов (ЛИА) сделал автономные источники электропитания этого типа наиболее энергоемкими среди перезаряжаемых электрохимических систем. Традиционным материалом отрицательного электрода (анода) в таких аккумуляторах является углерод, способный обратимо внедрять литий [1], а материалом положительного электрода (катода) - литированный оксид кобальта (кобальтат лития, оксид лития-кобальта) LiCoO2 [2]. Несмотря на то, что ЛИА системы «углерод - оксид лития-кобальта» в настоящее время занимают значительную часть рынка источников питания для портативной электроники, их применение для питания транспорта и энергетики невозможно из-за ряда присущих им недостатков. Недостатками литированного углерода как анодного материала ЛИА являются [3-5]:
- вероятность теплового разгона и воспламенения при повышении температуры;
- резкая деградация емкости при повышенной скорости заряда/разряда;
- очень малая остаточная емкость и невозможность заряда аккумуляторов при отрицательных температурах.
Недостатками кобальтата лития при использовании в качестве катодного материала ЛИА являются [5-7]:
- пожароопасность при высоких температурах;
- деградация емкости при высоких потенциалах, температурах и скоростях циклирования;
- малый срок службы (не более 800 циклов).
Аккумуляторы для электротранспорта и энергетики должны сочетать в себе такие характеристики, как энергоемкость, мощность (т.е. способность к быстрому заряду и стойкость к воздействию высоких нагрузочных токов), широкий интервал рабочих температур, длительный срок службы и безопасность эксплуатации, поэтому их создание требует разработки и применения принципиально новых активных электродных материалов.
Известны анодные материалы на базе сплавов лития с кремнием [8]. Теоретическая емкость наиболее богатого литием соединения кремния (Li22Si5) достигает 4200 мА⋅ч/г в расчете на чистый кремний или 2011 мА⋅ч/г в расчете на соединение Li22Si5. Главным препятствием стабильной работы литий-кремниевого интеркаляционного электрода являются большие объемные изменения, происходящие в ходе циклов внедрения/экстракции лития. Эти изменения достигают 310% исходного объема кремния и являются причиной механической нестойкости материала [9].
Известны анодные материалы на основе сплавов лития с оловом [10]. Находясь в одной подгруппе периодической системы с кремнием, олово образует схожие кристаллические структуры и аналогичные по стехиометрии соединения. Оно также сплавляется с литием с образованием Li22Sn5. Однако олово имеет и больший по сравнению с кремнием объем элементарной ячейки, в связи с чем оно меньше страдает от объемных изменений [11]. Недостатком предлагаемого решения является то, что олово вчетверо тяжелее кремния, и удельная интеркалируемая емкость Li22Sn5 во столько же раз ниже - 990 мА⋅ч/г против 4200 мА⋅ч/г у Li22Si5 [11].
Возможности повышения удельной емкости углеграфитовых материалов в настоящее время исчерпаны и соответствуют наиболее богатому литием соединению LiC6 (372 мА⋅ч/г). Перспективным решением проблемы ограниченной емкости литированного углерода является использование литерованных композитов Si-C, Sn-C или Si-Sn-C [12]. Недостатком данного решения является высокая активность лития в вышеперечисленных материалах, обусловливающая их недостаточную безопасность [13].
Перспективными анодными материалами для применения в конструкции ЛИА является группа соединений с умеренными значениями емкости, у которых активность лития и, соответственно, электродный потенциал имеют промежуточное значение между традиционными анодными и катодными материалами. Типичным примером является литий-титановая шпинель, или титанат лития, Li4Ti5O12 [14]. Данный материал имеет теоретическую емкость 175 мА⋅ч/г и потенциал плато зарядно-разрядной кривой ~1,55 В. Этот потенциал намного выше потенциалов восстановления большинства органических растворителей, поэтому на поверхности материала не образуется твердоэлектролитных пленок с высоким сопротивлением, а выделение металлического лития на аноде практически исключается. Другим преимуществом Li4Ti5O12 по сравнению с соединениями кремния и олова являются малые объемные изменения (менее 0,2%) при литировании и делитировании, что гарантирует стабильность при длительном циклировании. Кроме всего перечисленного, материал обладает высокими проводящими свойствами по ионам лития: значение удельной проводимости составляет 5,8⋅10-8 Ом-1⋅см-1 уже при комнатной температуре [15].
Для создания работоспособной конструкции ЛИА с оптимальным сочетанием энергии, мощности, срока службы и безопасности, необходим подбор активного материала положительного электрода, имеющего достаточно высокий электродный потенциал, но в то же время лишенного всех недостатков кобальтата лития. В определенной мере этим требованиям соответствуют слоистые смешанные литерованные оксиды никеля, кобальта и марганца состава LiNi1-x-yCoxMnyO2 по патенту [16]. Этот материал обладает сопоставимой с LiCoO2 энергоемкостью, превосходя его по мощности, безопасности и стабильности при циклировании. Недостатком данного материала является резкое падение емкости при циклировании из-за роста сопротивления реакции переноса заряда на поверхности материала вследствие его деградации [6]. Кроме того, данные реакционной калориметрии [5] свидетельствуют о хотя и значительно сниженной, но достаточно определенной вероятности возникновения теплового разгона в ЛИА на основе данного активного материала.
Известен материал положительного электрода ЛИА на основе литий-марганцевой шпинели LiMn2O4 [17], нетоксичный, более дешевый, мощный и безопасный в эксплуатации по сравнению с кобальтатом лития. Недостатками литий-марганцевой шпинели являются невысокое значение удельной емкости и ее необратимое падение вследствие растворения марганца в процессе циклирования, особенно при повышенной температуре [6, 7], что делает данный материал неподходящим при разработке ЛИА для транспорта и энергетики.
Известен материал положительного электрода ЛИА на основе феррофосфата лития LiFePO4 [18], обладающий такими преимуществами, как нетоксичность, высокая емкость, стабильность и безопасность при циклировании благодаря тому, что в структуре фосфата кислород химически связан сильнее, чем в структуре оксида. С другой стороны, строение молекул феррофосфата лития обусловливает ряд присущих ему недостатков. Из-за особенностей кристаллической структуры ионы лития при заряде и разряде аккумулятора могут передвигаться только в одном измерении [19], а не в трех, как в традиционных катодных материалах на основе оксидов переходных металлов. Это является причиной низкой проводимости катодного материала, как ионной, так и электронной, что, в свою очередь, обусловливает пониженное значение удельной энергии (380 Вт⋅ч/кг). Кроме того, из-за низкой проводимости феррофосфата лития наблюдается значительное снижение емкости и мощности ЛИА в процессе эксплуатации при низких температурах [20, 21]. Кроме того, в паре с титанатом лития Li4Ti5O12 феррофосфат лития LiFePO4 дает низкую разность потенциалов (1,9 В и ниже) [22], что отрицательно сказывается на удельных энергетических характеристиках ЛИА. Это, в свою очередь, увеличивает массу и габариты аккумуляторных батарей, что особенно критично для электротранспорта, а также повышает стоимость 1 КВт⋅ч запасаемой батареями энергии вследствие необходимости установки большего количества аккумуляторов для достижения приемлемых уровней напряжения и энергии.
Наиболее близким к заявляемому аккумулятору является решение по заявке [23], согласно которому для создания аккумулятора с высокой энергоемкостью и мощностью предлагается использовать сочетание титаната лития Li4Ti5O12 в качестве материала отрицательного электрода и фосфата лития-кобальта LiCoPO4 в роли материала положительного электрода. Недостатком данного решения является невозможность создания стабильно работающего аккумулятора данной электрохимической системы на настоящем этапе развития техники вследствие низких значений разрядной емкости, необратимых потерь лития и ускоренного падения емкости в процессе циклирования и связанного с этим неприемлемо малого ресурса LiCoO4-электрода (10 циклов) [24].
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачей заявляемого изобретения являлась разработка ЛИА, сочетающего в своей конструкции активный материал отрицательного электрода на основе титаната лития Li4Ti5O12 и активный материал положительного электрода, обладающий высокими значениями электрохимического потенциала и удельной емкости, и в то же время способный к длительному обратимому циклированию в широком интервале зарядно-разрядных токов и температур. Применение подобного сочетания электродных материалов позволяет сконструировать накопители энергии на основе ЛИА, пригодные для использования в электротранспорте, системах выравнивания сетевых нагрузок, аварийного энергоснабжения и бесперебойного питания.
Техническим результатом является создание конструкции высокоэнергоемких ЛИА с повышенными мощностью, безопасностью и стабильностью при циклировании.
Указанный технический результат достигается тем, что в конструкции аккумулятора применяется сочетание активного материала отрицательного электрода на основе титаната лития Li4Ti5O12 и активного материала положительного электрода на основе фосфата лития-ванадия (фосфованадата лития) Li3V2(PO4)3. По уровню удельной энергии Li3V2(PO4)3 сопоставим с оксидными активными материалами, а по уровню безопасности, благодаря фосфатной структуре, он близок к LiFePO4, однако имеет ряд отличительных особенностей, обусловливающих его преимущества, к числу которых относятся:
- высокое теоретическое значение удельной емкости - 198 мА⋅ч/г и возможность достижения практических значений удельной емкости, близких к теоретическому;
- более высокое среднее напряжение на разряде - 4,8 В отн. лития для моноклинной структурной модификации и 4,3 В для ромбоэдрического (насиконоподобного) структурного типа. Таким образом, в сочетании с титанатом лития насиконоподобный Li3V2(PO4)3 дает разность потенциалов порядка 2,8 В, а моноклинный Li3V2(PO4)3 - порядка 3,3 В;
- повышенный циклический ресурс - до 2500 циклов заряда-разряда;
- высокая удельная мощность - 2000 Вт/кг;
- высокие значения разрядных токов - более 40 C.
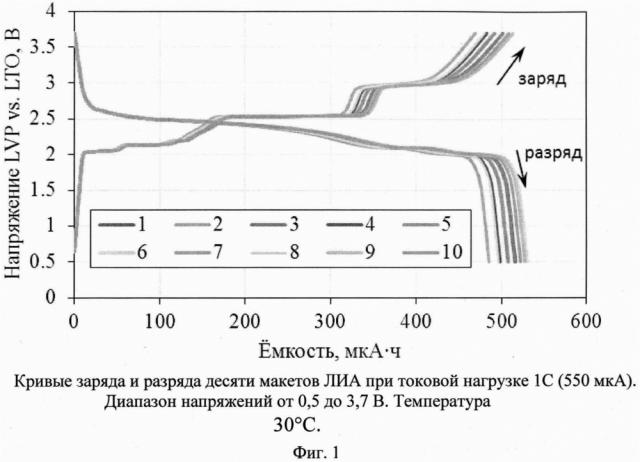
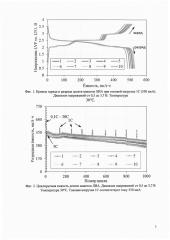
Результаты испытаний макетов ЛИА системы Li4Ti5O12-Li3V2(PO4)3 показывают их приемлемую работоспособность и циклируемость (фиг. 1 и 2).
Поставленная задача решается также тем, что активный материал отрицательного электрода на основе Li4Ti5O12 допирован хромом по позициям титана и представляет собой соединение состава Li4Ti5-xCrxO12, где 0<x≤0,2. Частичное замещение титана хромом в указанных количествах вызывает изменение структуры кристаллической решетки активного материала, приводящее к увеличению коэффициента использования, в результате сохранность емкости в ходе циклирования возрастает на 1,3%.
Обозначенная задача также решается за счет того, что активный материал положительного электрода допирован натрием по позициям лития, одним или несколькими металлами из группы, содержащей магний, алюминий, иттрий и лантан по позициям ванадия, фтором или хлором по позициям фосфата, и представляет собой соединение состава Li3-xNaxV2-yMy(PO4)3-zHalz/C, где М - один или несколько металлов из группы, содержащей Mg, Al, Y, La; Hal=F, Cl; 0<x≤0,1; 0<y≤0,2; 0<z≤0,16. Модификация структуры фосфованадата лития указанным путем приводит к улучшению электропроводности активного материала, в результате чего возрастают его разрядная емкость и структурная стабильность, что ведет к увеличению удельной энергии, мощности и ресурса ЛИА. В качестве примера положительного воздействия допирования фосфата лития-ванадия магнием на фиг. 3 показано увеличение его разрядной емкости при циклировании током 10 °C.
Обозначенный технический результат достигается также за счет модифицирования применяемых в конструкции ЛИА активных материалов путем нанесения на поверхность их частиц проводящего углеродного покрытия. В результате уменьшается электрическое сопротивление на границе кристаллов активного вещества, что ведет к увеличению поверхностной электропроводности активного материала, что, в свою очередь, способствует улучшению таких его характеристик, как удельная емкость, коэффициент использования активного материала, мощность и циклируемость. Результат также достигается за счет использования крахмала в качестве углеродного прекурсора, который при синтезе активного материала образует вязкую среду, способствующую образованию частиц особо малого размера. В качестве иллюстрации положительного воздействия обозначенного технического решения на свойства активного материала на фиг. 4 приведены экспериментальные данные, показывающие способность композита фосфата лития-ванадия с углеродом (Li3V2(PO4)3/С) к циклированию экстремально высокими токами (до 320 °C).
Источники информации
1. Патент США №4,668,595 от 26 мая 1987 г. Вторичный химический источник тока.
2. Патент США №4,302,518 от 24 ноября 1981 г. Электрохимический элемент с новыми быстрыми ионными проводниками.
3. J. Vetter et al. Ageing Mechanisms in Lithium-Ion Batteries // Journal of Power Sources. - Vol. 147, 2005. - P. 269-281.
4. C. Mikolajczak et al. Lithium-Ion Batteries Hazard and Use Assessment: Final Report // Fire Protection Research Foundation: Quincy, MA, 2011. - 126 p.
5. D. Doughty, E.P. Roth. A General Discussion of Li ion Battery Safety // The Electrochemical Society Interface. - Summer 2012. - P. 37-44.
6. В.А. Тарнопольский. Некоторые тенденции усовершенствования катодных материалов для литий-ионных аккумуляторов // Электрохимическая энергетика. - №1, Т. 8, 2008. - С. 3-11.
7. P. Ramadass et al. Performance Study of Commercial LiCoO2 and Spinel-based Li-ion Cells // Journal of Power Sources. - Vol. 111, 2002. - P. 210-220.
8. Патент США №3,969,139 от 13 июля 1976 г. Литиевый электрод и накопитель электрической энергии на его основе.
9. L.Y. Beaulieu et al. Colossal Reversible Volume Changes in Lithium Alloys // Electrochemical and Solid-State Letters. - Vol. 4, 2001. - P A137-A140.
10. Патент США №3,506,490 от 14 апреля 1970 г. Источник тока с твердым электролитом и анодом из лития или литиевого сплава.
11. S.-C. Chao et al. Study on Microstructural Deformation of Working Sn and SnSb Anode Particles for Li-Ion Batteries by in Situ Transmission X-ray Microscopy // Journal of Physical Chemistry C: Nanomaterials and Interfaces. - Vol. 115, 2011. - P. 22040-22047.
12. Патент США №5,587,256 от 24 декабря 1996 г. Углеродистые соединения внедрения и их применение в качестве анодов в перезаряжаемых химических источниках тока.
13. J. Hassoun et al. A Nanostructured Sn-C Composite Lithium Battery Electrode with Unique Stability and High Electrochemical Performance // Advanced materials. - Vol. 20, 2008. - P. 3169-3175.
14. Патент США №5,545,468 от 13 августа 1996 г. Перезаряжаемый литиевый источник тока и технология изготовления анода для него.
15. Поротников, Н.В. Синтез и исследование электропроводности сложных оксидов в системе Li2O-ZnO-TiO2 / Н.В. Поротников, Н.Г. Чабан, К.И. Петров // Известия АН СССР. Неорг. материалы. - 1982. - Т. 18, №6. - С. 1066-1067.
16. Патент США №6,677,082 B2 от 13 января 2004 г. Литий-металл-оксидные электроды для литиевых аккумуляторов и батарей.
17. Патент США №4,507,371 от 26 марта 1985 г. Твердотельный элемент, в котором анод, твердый электролит и катод имеют структуру, представляющую собой плотную кубическую упаковку.
18. Патент США №5,910,382 от 8 июня 1999 г. Катодные материалы для вторичных (перезаряжаемых) литиевых источников тока.
19. Y. Wang et al. Olivine LiFePO4: Development and Future // Energy & Environmental Science. - No. 4, 2011. - P. 805-817.
20. B. Wu et al. LiFePO4 Cathode Material // Electric Vehicles - The Benefits and Barriers, In-Tech, 2011. - P. 199-216.
21. Y. Zhang et al. Cycling Degradation of an Automotive LiFePO4 Lithium-Ion Battery // Journal of Power Sources. - Vol. 196, 2011. - P. 1513-1520.
22. С.P. Sandhya et al. Litihum Titanate as Anode Material for Lithium-ion Cells: A Review // Ionics. - Vol. 20, 2014. - P. 601-620.
23. Заявка США №20080014503 A1 от 17 января 2008 г. Литий-ионный аккумулятор с высокими мощностью и напряжением.
24. N.N. Bramnik et al. Electrochemical and Structural Study of LiCoPO4-based Electrodes // Journal of Solid State Electrochemistry. - Vol. 8, 2004. - P. 558-564.
1. Литий-ионный аккумулятор, отличающийся тем, что в качестве активного материала отрицательного электрода используется соединение, представляющее собой продукт модифицирования литированного оксида титана Li4Ti5O12, а в роли активного материала положительного электрода выступает соединение, представляющее собой продукт модифицирования фосфата лития-ванадия Li3V2(PO4)3.
2. Литий-ионный аккумулятор по п. 1, отличающийся тем, что активный материал отрицательного электрода допирован хромом по позициям титана и представляет собой соединение состава Li4Ti5-xCrxO12, где 0<х≤0,2.
3. Литий-ионный аккумулятор по п. 1, отличающийся тем, что активный материал положительного электрода допирован натрием по позициям лития, одним или несколькими металлами из группы, содержащей магний, алюминий, иттрий и лантан по позициям ванадия, фтором или хлором по позициям фосфата, и представляет собой соединение состава Li3-xNaxV2-уМу(PO4)3-zГz/С, где М - один или несколько металлов из группы, содержащей Mg, Al, Y, La; Г=F, Cl; 0<х≤0,1; 0<у≤0,2; 0<z≤0,16.
4. Литий-ионный аккумулятор по любому из пп. 1, 2, 3, отличающийся тем, что кристаллы активных материалов отрицательного и положительного электродов покрыты поверхностным слоем углерода.
5. Литий-ионный аккумулятор по п. 4, отличающийся тем, что поверхностный слой углерода на кристаллах активных материалов получают за счет введения в смесь исходных реагентов углеродсодержащего прекурсора - крахмала.