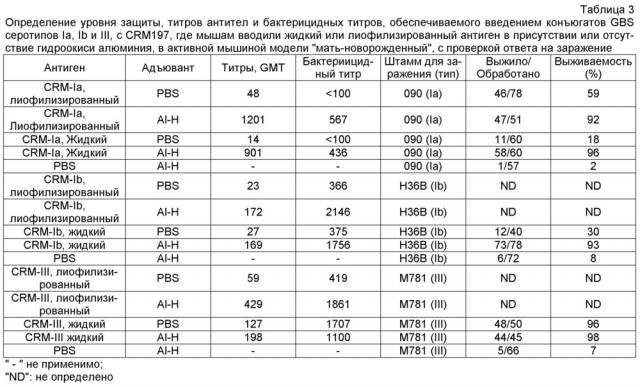
Иммуногенные композиции
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к иммунологии, и может быть использовано для получения иммуногенной композиции. Иммуногенная композиция содержит а) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем; b) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем; и с) конъюгат, который представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем, где (i) где каждый капсулярный сахарид GBS присутствует в количестве 5 мкг, 10 мкг или 20 мкг на единицу дозы, (ii) белок-носитель в а), b) и с) представляет собой токсоид дифтерии или CRM197, и iii) иммуногенная композиция не содержит адъювант на основе соли алюминия. Использование данного состава иммуногенной композиции, имеющей эффективные количества полисахаридов GBS типа Ia, Ib и III, конъюгированных с CRM197, позволяет использовать ее в качестве вакцины для профилактики инфекции GBS в организме человека. 13 з.п. ф-лы, 4 ил., 21 табл.
Реферат
Настоящая заявка испрашивает приоритет предварительной заявки США № 61/383668, поданной 16 сентября 2010 г., и заявки на патент Великобритании № 1101665.6, поданной 31 января 2011 г., при этом полное содержание обоих документов включено сюда ссылкой.
ОБЛАСТЬ ТЕХНИКИ
Это изобретение относится к области иммуногенных композиций, включающих конъюгаты капсулярных сахаридов Streptococcus agalactiae с белками-носителями. Композиции являются полезными для иммунизации.
УРОВЕНЬ ТЕХНИКИ
Капсулярные сахариды бактерий использовались много лет в вакцинах против капсулированных бактерий. Поскольку сахариды представляют собой Т-независимые антигены, то они являются слабоиммуногенными. Конъюгирование с носителем может преобразовать Т-независимые антигены в Т-зависимые антигены, увеличивая таким образом ответы памяти, и обеспечивая развитие защитного иммунитета. Поэтому самые эффективные сахаридные вакцины основаны на гликоконъюгатах, и был создан прототип конъюгатной вакцины против Haemophilus influenzae типа b ("Hib") [например, см. главу 14 ссылки 84].
Другая бактерия, для которой были описаны конъюгатные вакцины, является Streptococcus agalactiae, также известная как "стрептококк группы B" или обозначаемая как "GBS". Большая часть этой работы была выполнена Dennis Kasper с коллегами, и описана в документах, таких как ссылки 1-9. Как было показано, конъюгатные вакцины для каждого из GBS серотипов Ia, Ib, II, III и V были безопасны и иммуногенны для людей [10]. Однако все еще остается потребность в улучшенных конъюгатных вакцинах следующего поколения против GBS.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
В первом варианте выполнения изобретения используется один или несколько конъюгатов, которые представляют собой капсулярные сахариды GBS серотипов Ia, Ib, III или V, конъюгированные с белком-носителем. В частности, изобретение предоставляет иммуногенные композиции, включающие один или несколько таких конъюгатов. Композиции могут использоваться в качестве вакцин для предотвращения инфекции этим(и) серотипом(ами) GBS.
Во втором варианте выполнения изобретения предоставляется способ иммунизирования пациента против инфекции GBS, включающий стадию введения пациенту конъюгата, который представляет собой капсулярный сахарид GBS, конъюгированный с токсоидом дифтерии или его производным, где пациент был предварительно иммунизирован токсоидом дифтерии или его производным. Как правило, конъюгат является одним из конъюгатов GBS иммуногенной композиции по первому варианту выполнения изобретения.
Иммуногенные композиции
В одном варианте выполнения изобретения предоставляется иммуногенная композиция, включающая конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем. Во втором варианте выполнения изобретения предоставляется иммуногенная композиция, включающая конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем. В третьем варианте выполнения изобретения предоставляется иммуногенная композиция, включающая конъюгат, который представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. В четвертом варианте выполнения изобретения предоставляется иммуногенная композиция, включающая конъюгат, который представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем.
Иммуногенные композиции могут включать более одного конъюгата. Варианты выполнения изобретения, включающие два, три или четыре конъюгата, описаны ниже. Авторы изобретения нашли, что среди этих композиций композиции, включающие конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, могут предоставить защиту против GBS серотипа Ia, в дополнение к GBS серотипа Ib. Это наблюдение отличается от раскрытия ссылки 11, где предполагается, что конъюгаты типа Ib не способны к стимулированию антител, которые могут уничтожить бактерии типа Ia. Соответственно, варианты выполнения изобретения, описанные ниже, включающие конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, могут быть полезны тем, что они обеспечивают увеличенную защиту против серотипа Ia (когда композиция также включает конъюгат, который представляет собой капсулярный сахарид GBS серотипа, конъюгированный с белком-носителем), и даже могут обеспечить защиту, когда композиция не содержит конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем.
Как указано выше, иммуногенные композиции могут включать два конъюгата. В одном варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем. Во втором варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид от GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. В третьем варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем. В четвертом варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. В пятом варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем. В шестом варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем.
Таким же образом, иммуногенные композиции могут включать три конъюгата. В одном варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, и третий конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. Авторы изобретения нашли, что такие композиции (например, такие, как показанные ниже) являются, в частности, подходящими для использования в качестве вакцины для предотвращения инфекции GBS. В этой связи этот вариант представляет собой предпочтительный вариант выполнения изобретения. Во втором варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, и третий конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем. В третьем варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем, и третий конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем. В четвертом варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем, и третий конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем.
Аналогично, иммуногенные композиции могут включать четыре конъюгата. В одном варианте выполнения изобретения первый конъюгат представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем, в то время как второй конъюгат представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем, третий конъюгат представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем, и четвертый конъюгат представляет собой капсулярный сахарид GBS серотипа V, конъюгированный с белком-носителем.
Как правило, иммуногенные композиции, описанные выше, не будут включать иных конъюгатов, кроме точно указанных, в частности, не будут включать конъюгатов, включающих капсулярные сахариды иных серотипов GBS, кроме точно указанных. Однако, в некоторых в вариантах выполнения изобретения композиции могут включать и другие конъюгаты, включая конъюгаты, включающие капсулярные сахариды других серотипов GBS. Например, композиции могут включать конъюгат, который представляет собой капсулярный сахарид GBS серотипа II, конъюгированный с белком-носителем. Также композиции могут включать конъюгат, который представляет собой капсулярный сахарид GBS серотипа VI, конъюгированный с белком-носителем. В другом варианте выполнения изобретения, композиции могут включить конъюгат, который представляет собой капсулярный сахарид GBS серотипа VIII, конъюгированный с белком-носителем.
Иммуногенные композиции, описанные выше, могут включать любое подходящее количество капсулярного сахарида(ов) на единицу дозы. Подходящее количество капсулярного сахарида(ов) может составлять от 0,1 до 50 мкг на единицу дозы. Как правило, каждый капсулярный сахарид GBS присутствует в количестве от 1 до 30 мкг, например от 2 до 25 мкг, и в частности - от 5 до 20 мкг. Подходящее количество капсулярного сахарида(ов) может включать 5, 10 и 20 мкг на единицу дозы. Авторы изобретения нашли, что это количество является приемлемым, в частности, когда иммуногенная композиция включает капсулярные сахариды GBS серотипов Ia, Ib и/или III. Поэтому приемлемое количество на единицу дозы каждого капсулярного сахарида в вариантах выполнения изобретения, описанных выше, может быть выбрано из различных вариантов в последующих далее таблицах, где соответствующие варианты выполнения композиций по изобретению обозначены ссылкой на серотип(ы), из которого(ых) получен(ы) капсулярный(ые) сахарид(ы).
| Таблица AИммуногенные композиции, включающие один конъюгат | ||||
| Вариант дозирования | Вариант выполнения изобретения | |||
| Ia | Ib | III | V | |
| 1 | Ia: 5 мкг | Ib: 5 мкг | III: 5 мкг | V: 5 мкг |
| 2 | Ia: 10 мкг | Ib: 10 мкг | III: 10 мкг | V: 10 мкг |
| 3 | Ia: 20 мкг | Ib: 20 мкг | III: 20 мкг | V: 20 мкг |
| Таблица BИммуногенные композиции, включающие два конъюгата | ||||||
| Вариант дозирования | Вариант выполнения изобретения | |||||
| Ia+Ib | Ia+III | Ia+V | Ib+III | Ib+V | III+V | |
| 1 | Ia: 5 мкгIb: 5 мкг | Ia: 5 мкгIII: 5 мкг | Ia: 5 мкгV: 5 мкг | Ib: 5 мкгIII: 5 мкг | Ib: 5 мкгV: 5 мкг | III: 5 мкгV: 5 мкг |
| 2 | Ia: 5 мкгIb: 10 мкг | Ia: 5 мкгIII: 10 мкг | Ia: 5 мкгV: 10 мкг | Ib: 5 мкгIII: 10 мкг | Ib: 5 мкгV: 10 мкг | III: 5 мкгV: 10 мкг |
| 3 | Ia: 5 мкгIb: 20 мкг | Ia: 5 мкгIII: 20 мкг | Ia: 5 мкгV: 20 мкг | Ib: 5 мкгIII: 20 мкг | Ib: 5 мкгV: 20 мкг | III: 5 мкгV: 20 мкг |
| 4 | Ia: 10 мкгIb: 5 мкг | Ia: 10 мкгIII: 5 мкг | Ia: 10 мкгIb: 5 мкг | Ib: 10 мкгIII: 5 мкг | Ib: 10 мкгV: 5 мкг | III: 10 мкгV: 5 мкг |
| 5 | Ia: 10 мкгIb: 10 мкг | Ia: 10 мкгIII: 10 мкг | Ia: 10 мкгV: 10 мкг | Ib: 10 мкгIII: 10 мкг | Ib: 10 мкгV: 10 мкг | III: 10 мкгV: 10 мкг |
| 6 | Ia: 10 мкгIb: 20 мкг | Ia: 10 мкгIII: 20 мкг | Ia: 10 мкгV: 20 мкг | Ib: 10 мкгIII: 20 мкг | Ib: 10 мкгV: 20 мкг | III: 10 мкгV: 20 мкг |
| 7 | Ia: 20 мкгIb: 5 мкг | Ia: 20 мкгIII: 5 мкг | Ia: 20 мкгV: 5 мкг | Ib: 20 мкгIII: 5 мкг | Ib: 20 мкгV: 5 мкг | III: 20 мкгV: 5 мкг |
| 8 | Ia: 20 мкгIb: 10 мкг | Ia: 20 мкгIII: 10 мкг | Ia: 20 мкгV: 10 мкг | Ib: 20 мкгIII: 10 мкг | Ib: 20 мкгV: 10 мкг | III: 20 мкгV: 10 мкг |
| 9 | Ia: 20 мкгIb: 20 мкг | Ia: 20 мкгIII: 20 мкг | Ia: 20 мкгV: 20 мкг | Ib: 20 мкгIII: 20 мкг | Ib: 20 мкгV: 20 мкг | III:20 мкгV: 20 мкг |
| Таблица CИммуногенные композиции, включающие три конъюгата | ||||
| Вариант дозирования | Вариант выполнения изобретения | |||
| Ia, Ib+III | Ia, Ib+V | Ia, III+V | Ib, III+V | |
| 1 | Ia: 5 мкгIb: 5 мкгIII: 5 мкг | Ia: 5 мкгIb: 5 мкгV: 5 мкг | Ia: 5 мкгIII: 5 мкгV: 5 мкг | Ib: 5 мкгIII: 5 мкгV: 5 мкг |
| 2 | Ia: 5 мкгIb: 5 мкгIII: 10 мкг | Ia: 5 мкгIb: 5 мкгV: 10 мкг | Ia: 5 мкгIII: 5 мкгV: 10 мкг | Ib: 5 мкгIII: 5 мкгV: 10 мкг |
| 3 | Ia: 5 мкгIb: 5 мкгIII: 20 мкг | Ia: 5 мкгIb: 5 мкгV: 20 мкг | Ia: 5 мкгIII: 5 мкгV: 20 мкг | Ib: 5 мкгIII: 5 мкгV: 20 мкг |
| 4 | Ia: 5 мкгIb: 10 мкгIII: 5 мкг | Ia: 5 мкгIb: 10 мкгV: 5мкг | Ia: 5 мкгIII: 10 мкгV: 5мкг | Ib: 5 мкгIII: 10 мкгV: 5мкг |
| 5 | Ia: 5 мкгIb: 10 мкгIII: 10 мкг | Ia: 5 мкгIb: 10 мкгV: 10 мкг | Ia: 5 мкгIII: 10 мкгV: 10 мкг | Ib: 5 мкгIII: 10 мкгV: 10 мкг |
| 6 | Ia: 5 мкгIb: 10 мкгIII: 20 мкг | Ia: 5 мкгIb: 10 мкгV: 20 мкг | Ia: 5 мкгIII: 10 мкгV: 20 мкг | Ib: 5 мкгIII: 10 мкгV: 20 мкг |
| 7 | Ia: 5 мкгIb: 20 мкгIII: 5 мкг | Ia: 5 мкгIb: 20 мкгV: 5 мкг | Ia: 5 мкгIII: 20 мкгV: 5 мкг | Ib: 5 мкгIII: 20 мкгV: 5 мкг |
| 8 | Ia: 5 мкгIb: 20 мкгIII: 10 мкг | Ia: 5 мкгIb: 20 мкгV: 10 мкг | Ia: 5 мкгIII: 20 мкгV: 10 мкг | Ib: 5 мкгIII: 20 мкгV: 10 мкг |
| 9 | Ia: 5 мкгIb: 20 мкгIII: 20 мкг | Ia: 5 мкгIb: 20 мкгV: 20 мкг | Ia: 5 мкгIII: 20 мкгV: 20 мкг | Ib: 5 мкгIII: 20 мкгV: 20 мкг |
| 10 | Ia: 10 мкгIb: 5 мкгIII: 5 мкг | Ia: 10 мкгIb: 5 мкгV: 5 мкг | Ia: 10 мкгIII: 5 мкгV: 5 мкг | Ib: 10 мкгIII: 5 мкгV: 5 мкг |
| 11 | Ia: 10 мкгIb: 5 мкгIII: 10 мкг | Ia: 10 мкгIb: 5 мкгV: 10 мкг | Ia: 10 мкгIII: 5 мкгV: 10 мкг | Ib: 10 мкгIII: 5 мкгV: 10 мкг |
| 12 | Ia: 10 мкгIb: 5 мкгIII: 20 мкг | Ia: 10 мкгIb: 5 мкгV: 20 мкг | Ia: 10 мкгIII: 5 мкгV: 20 мкг | Ib: 10 мкгIII: 5 мкгV: 20 мкг |
| 13 | Ia: 10 мкгIb: 10 мкгIII: 5 мкг | Ia: 10 мкгIb: 10 мкгV: 5 мкг | Ia: 10 мкгIII: 10 мкгV: 5 мкг | Ib: 10 мкгIII: 10 мкгV: 5 мкг |
| 14 | Ia: 10 мкгIb: 10 мкгIII: 10 мкг | Ia: 10 мкгIb: 10 мкгV: 10 мкг | Ia: 10 мкгIII: 10 мкгV: 10 мкг | Ib: 10 мкгIII: 10 мкгV: 10 мкг |
| 15 | Ia: 10 мкгIb: 10 мкгIII: 20 мкг | Ia: 10 мкгIb: 10 мкгV: 20 мкг | Ia: 10 мкгIII: 10 мкгV: 20 мкг | Ib: 10 мкгIII: 10 мкгV: 20 мкг |
| 16 | Ia: 10 мкгIb: 20 мкгIII: 5 мкг | Ia: 10 мкгIb: 20 мкгV: 5 мкг | Ia: 10 мкгIII: 20 мкгV: 5 мкг | Ib: 10 мкгIII: 20 мкгV: 5 мкг |
| 17 | Ia: 10 мкгIb: 20 мкгIII: 10 мкг | Ia: 10 мкгIb: 20 мкгV: 10 мкг | Ia: 10 мкгIII: 20 мкгV: 10 мкг | Ib: 10 мкгIII: 20 мкгV: 10 мкг |
| 18 | Ia: 10 мкгIb: 20 мкгIII: 20 мкг | Ia: 10 мкгIb: 20 мкгV: 20 мкг | Ia: 10 мкгIII: 20 мкгV: 20 мкг | Ib: 10 мкгIII: 20 мкгV: 20 мкг |
| 19 | Ia: 20 мкгIb: 5 мкгIII: 5 мкг | Ia: 20 мкгIb: 5 мкгV: 5 мкг | Ia: 20 мкгIII: 5 мкгV: 5 мкг | Ib: 20 мкгIII: 5 мкгV: 5 мкг |
| 20 | Ia: 20 мкгIb: 5 мкгIII: 10 мкг | Ia: 20 мкгIb: 5 мкгV: 10 мкг | Ia: 20 мкгIII: 5 мкгV: 10 мкг | Ib: 20 мкгIII: 5 мкгV: 10 мкг |
| 21 | Ia: 20 мкгIb: 5 мкгIII: 20 мкг | Ia: 20 мкгIb: 5 мкгV: 20 мкг | Ia: 20 мкгIII: 5 мкгV: 20 мкг | Ib: 20 мкгIII: 5 мкгV: 20 мкг |
| 22 | Ia: 20 мкгIb: 10 мкгIII: 5 мкг | Ia: 20 мкгIb: 10 мкгV: 5 мкг | Ia: 20 мкгIII: 10 мкгV: 5 мкг | Ib: 20 мкгIII: 10 мкгV: 5 мкг |
| 23 | Ia: 20 мкгIb: 10 мкгIII: 10 мкг | Ia: 20 мкгIb: 10 мкгV: 10 мкг | Ia: 20 мкгIII: 10 мкгV: 10 мкг | Ib: 20 мкгIII: 10 мкгV: 10 мкг |
| 24 | Ia: 20 мкгIb: 10 мкгIII: 20 мкг | Ia: 20 мкгIb: 10 мкгV: 20 мкг | Ia: 20 мкгIII: 10 мкгV: 20 мкг | Ib: 20 мкгIII: 10 мкгV: 20 мкг |
| 25 | Ia: 20 мкгIb: 20 мкгIII: 5 мкг | Ia: 20 мкгIb: 20 мкгV: 5 мкг | Ia: 20 мкгIII: 20 мкгV: 5 мкг | Ib: 20 мкгIII: 20 мкгV: 5 мкг |
| 26 | Ia: 20 мкгIb: 20 мкгIII: 10 мкг | Ia: 20 мкгIb: 20 мкгV: 10 мкг | Ia: 20 мкгIII: 20 мкгV: 10 мкг | Ib: 20 мкгIII: 20 мкгV: 10 мкг |
| 27 | Ia: 20 мкгIb: 20 мкгIII: 20 мкг | Ia: 20 мкгIb: 20 мкгV: 20 мкг | Ia: 20 мкгIII: 20 мкгV: 20 мкг | Ib: 20 мкгIII: 20 мкгV: 20 мкг |
Из всех вариантов дозирования, описанных в таблице C, авторы изобретения нашли, что эффективными являются варианты 1, 14 и 27, в частности, когда иммуногенная композиция включает: a) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем; b) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем; и c) конъюгат, который представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. В этой связи эти варианты дозирования предпочтительны для использования в изобретении, в частности, для такого варианта выполнения изобретения. Может быть выгодным минимизировать общее количество капсулярного сахарида(ов) на единицу дозы для того, чтобы уменьшить потенциальную токсичность. Соответственно, вариант дозирования 1 является, в частности, предпочтительным.
Вполне возможно дополнительно минимизировать количество капсулярного сахарида(ов) на единицу дозы. В частности подходящее количество капсулярного сахарида(ов) может составлять от 0,1 до 5 мкг на единицу дозы. Как правило, каждый капсулярный сахарид GBS может присутствовать в количестве от 0,1 до 5 мкг, например, в количестве 0,5, 2,5 или 5 мкг на единицу дозы. Например, каждый капсулярный сахарид GBS может присутствовать в количестве от 0,5 до 5 мкг, от 1 до 4 мкг, от 2 до 3 мкг, или присутствовать в количестве приблизительно 2,5 мкг на единицу дозы. Авторы изобретения считают, что это количество будет подходящим, когда иммуногенная композиция, в частности, включает a) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ia, конъюгированный с белком-носителем; b) конъюгат, который представляет собой капсулярный сахарид GBS серотипа Ib, конъюгированный с белком-носителем; и c) конъюгат, который представляет собой капсулярный сахарид GBS серотипа III, конъюгированный с белком-носителем. В этой связи, в таком варианте выполнения изобретения подходящее количество каждого капсулярного сахарида на единицу дозы может быть выбрано из перечисленных вариантов в нижеследующей таблице.
| Таблица C'Иммуногенные композиции, включающие капсулярные сахариды серотипов GBS Ia, Ib и III | |||
| Вариант дозирования | Количество капсулярного сахарида на единицу дозы (мкг) | ||
| Ia | Ib | III | |
| 1 | 0,5 | 0,5 | 0,5 |
| 2 | 0,5 | 0,5 | 2,5 |
| 3 | 0,5 | 0,5 | 5 |
| 4 | 0,5 | 2,5 | 0,5 |
| 5 | 0,5 | 2,5 | 2,5 |
| 6 | 0,5 | 2,5 | 5 |
| 7 | 0,5 | 5 | 0,5 |
| 8 | 0,5 | 5 | 2,5 |
| 9 | 0,5 | 5 | 5 |
| 10 | 2,5 | 0,5 | 0,5 |
| 11 | 2,5 | 0,5 | 2,5 |
| 12 | 2,5 | 0,5 | 5 |
| 13 | 2,5 | 2,5 | 0,5 |
| 14 | 2,5 | 2,5 | 2,5 |
| 15 | 2,5 | 2,5 | 5 |
| 16 | 2,5 | 5 | 0,5 |
| 17 | 2,5 | 5 | 2,5 |
| 18 | 2,5 | 5 | 5 |
| 19 | 5 | 0,5 | 0,5 |
| 20 | 5 | 0,5 | 2,5 |
| 21 | 5 | 0,5 | 5 |
| 22 | 5 | 2,5 | 0,5 |
| 23 | 5 | 2,5 | 2,5 |
| 24 | 5 | 2,5 | 5 |
| 25 | 5 | 5 | 0,5 |
| 26 | 5 | 5 | 2,5 |
| 27 | 5 | 5 | 5 |
Из вариантов дозирования, описанных в таблице C', авторы изобретения выделяют, в частности, варианты 1, 14 и 27. В этих вариантах капсулярные сахариды GBS представлены в равных долях (например, как в композициях с более высокими дозами, показанных ниже).
| Таблица DИммуногенные композиции, включающие четыре конъюгата | |||||
| Вариант дозирования | Вариант выполнения - Ia, Ib, III и V | ||||
| Вариант дозирования | Вариант дозирования | ||||
| 1 | Ia: 5 мкгIb: 5 мкгIII: 5 мкгV: 5 мкг | 28 | Ia: 10 мкгIb: 5 мкгIII: 5 мкгV: 5 мкг | 55 | Ia: 20 мкгIb: 5 мкгIII: 5 мкгV: 5 мкг |
| 2 | Ia: 5 мкгIb: 5 мкгIII: 5 мкгV: 10 мкг | 29 | Ia: 10 мкгIb: 5 мкгIII: 5 мкгV: 10 мкг | 56 | Ia: 20 мкгIb: 5 мкгIII: 5 мкгV: 10 мкг |
| 3 | Ia: 5 мкгIb: 5 мкгIII: 5 мкгV: 20 мкг | 30 | Ia: 10 мкгIb: 5 мкгIII: 5 мкгV: 20 мкг | 57 | Ia: 20 мкгIb: 5 мкгIII: 5 мкгV: 20 мкг |
| 4 | Ia: 5 мкгIb: 5 мкгIII: 10 мкгV: 5 мкг | 31 | Ia: 10 мкгIb: 5 мкгIII: 10 мкгV: 5 мкг | 58 | Ia: 20 мкгIb: 5 мкгIII: 10 мкгV: 5 мкг |
| 5 | Ia: 5 мкгIb: 5 мкгIII: 10 мкгV: 10 мкг | 32 | Ia: 10 мкгIb: 5 мкгIII: 10 мкгV: 10 мкг | 59 | Ia: 20 мкгIb: 5 мкгIII: 10 мкгV: 10 мкг |
| 6 | Ia: 5 мкгIb: 5 мкгIII: 10 мкгV: 20 мкг | 33 | Ia: 10 мкгIb: 5 мкгIII: 10 мкгV: 20 мкг | 60 | Ia: 20 мкгIb: 5 мкгIII: 10 мкгV: 20 мкг |
| 7 | Ia: 5 мкгIb: 5 мкгIII: 20 мкгV: 5 мкг | 34 | Ia: 10 мкгIb: 5 мкгIII: 20 мкгV: 5 мкг | 61 | Ia: 20 мкгIb: 5 мкгIII: 20 мкгV: 5 мкг |
| 8 | Ia: 5 мкгIb: 5 мкгIII: 20 мкгV: 10 мкг | 35 | Ia: 10 мкгIb: 5 мкгIII: 20 мкгV: 10 мкг | 62 | Ia: 20 мкгIb: 5 мкгIII: 20 мкгV: 10 мкг |
| 9 | Ia: 5 мкгIb: 5 мкгIII: 20 мкгV: 20 мкг | 36 | Ia: 10 мкгIb: 5 мкгIII: 20 мкгV: 20 мкг | 63 | Ia: 20 мкгIb: 5 мкгIII: 20 мкгV: 20 мкг |
| 10 | Ia: 5 мкгIb: 10 мкгIII: 5 мкгV: 5 мкг | 37 | Ia: 10 мкгIb: 10 мкгIII: 5 мкгV: 5 мкг | 64 | Ia: 20 мкгIb: 10 мкгIII: 5 мкгV: 5 мкг |
| 11 | Ia: 5 мкгIb: 10 мкгIII: 5 мкгV: 10 мкг | 38 | Ia: 10 мкгIb: 10 мкгIII: 5 мкгV: 10 мкг | 65 | Ia: 20 мкгIb: 10 мкгIII: 5 мкгV: 10 мкг |
| 12 | Ia: 5 мкгIb: 10 мкгIII: 5 мкгV: 20 мкг | 39 | Ia: 10 мкгIb: 10 мкгIII: 5 мкгV: 20 мкг | 66 | Ia: 20 мкгIb: 10 мкгIII: 5 мкгV: 20 мкг |
| 13 | Ia: 5 мкгIb: 10 мкгIII: 10 мкгV: 5 мкг | 40 | Ia: 10 мкгIb: 10 мкгIII: 10 мкгV: 5 мкг | 67 | Ia: 20 мкгIb: 10 мкгIII: 10 мкгV: 5 мкг |
| 14 | Ia: 5 мкгIb: 10 мкгIII: 10 мкгV: 10 мкг | 41 | Ia: 10 мкгIb: 10 мкгIII: 10 мкгV: 10 мкг | 68 | Ia: 20 мкгIb: 10 мкгIII: 10 мкгV: 10 мкг |
| 15 | Ia: 5 мкгIb: 10 мкгIII: 10 мкгV: 20 мкг | 42 | Ia: 10 мкгIb: 10 мкгIII: 10 мкгV: 20 мкг | 69 | Ia: 20 мкгIb: 10 мкгIII: 10 мкгV: 20 мкг |
| 16 | Ia: 5 мкгIb: 10 мкгIII: 20 мкгV: 5 мкг | 43 | Ia: 10 мкгIb: 10 мкгIII: 20 мкгV: 5 мкг | 70 | Ia: 20 мкгIb: 10 мкгIII: 20 мкгV: 5 мкг |
| 17 | Ia: 5 мкгIb: 10 мкгIII: 20 мкгV: 10 мкг | 44 | Ia: 10 мкгIb: 10 мкгIII: 20 мкгV: 10 мкг | 71 | Ia: 20 мкгIb: 10 мкгIII: 20 мкгV: 10 мкг |
| 18 | Ia: 5 мкгIb: 10 мкгIII: 20 мкгV: 20 мкг | 45 | Ia: 10 мкгIb: 10 мкгIII: 20 мкгV: 20 мкг | 72 | Ia: 20 мкгIb: 10 мкгIII: 20 мкгV: 20 мкг |
| 19 | Ia: 5 мкгIb: 20 мкгIII: 5 мкгV: 5 мкг | 46 | Ia: 10 мкгIb: 20 мкгIII: 5 мкгV: 5 мкг | 73 | Ia: 20 мкгIb: 20 мкгIII: 5 мкгV: 5 мкг |
| 20 | Ia: 5 мкгIb: 20 мкгIII: 5 мкгV: 10 мкг | 47 | Ia: 10 мкгIb: 20 мкгIII: 5 мкгV: 10 мкг | 74 | Ia: 20 мкгIb: 20 мкгIII: 5 мкгV: 10 мкг |
| 21 | Ia: 5 мкгIb: 20 мкгIII: 5 мкгV: 20 мкг | 48 | Ia: 10 мкгIb: 20 мкгIII: 5 мкгV: 20 мкг |