Липосомальная композиция для использования в перитонеальном диализе
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к липосомальной композиции для использования в перитонеальном диализе у пациентов, страдающих эндогенной или экзогенной интоксикацией, где значение рН внутри липосом отличается от значения рН в перитонеальной полости и составляет предпочтительно 1,5-4,0 или 9,0-10,0, и где значение рН внутри липосомы приводит к образованию заряженного токсина, включенного в липосому. Изобретение обеспечивает детоксикацию субъекта за счет захвата заряженного токсина в пределах липосомы. 7 з.п. ф-лы, 5 пр., 5 ил.
Реферат
Настоящее изобретение относится к липосомальной композиции для перитонеального диализа у пациентов, страдающих эндогенной и экзогенной интоксикацией, где значение pH внутри липосом отличается от значения pH в брюшной полости, и где значение pH внутри липосомы приводит к образованию заряженного токсина, включенного в липосомы. Изобретение также относится к разработке фармацевтической композиции, в состав которой входят эти липосомы. Изобретение также относится к разработке методики лечения пациентов, страдающих интоксикацией эндогенного и экзогенного типа. Прежде всего это виды интоксикации, вызванные приемом лекарственных препаратов, метаболитами, пестицидами, инсектицидами, токсинами и применением химического оружия, а также страдающих гипераммониемией, включая стадию введения в терапевтической дозировке в перитонеальное пространство пациента, нуждающегося в лечении. Полезность изобретения не ограничивается заболеваниями человека. Настоящее изобретение также подходит и для ветеринарии.
Предпосылки создания изобретения
Для изменения фармакокинетики и биораспределения лекарственных препаратов разработан и охарактеризован ряд частиц на основе липидов и полимеров, в состав которых входят липосомы. Это небольшие частицы с липидными бислоями и диаметром, определяемым в нанометрах и микрометрах. При этом липидный бислой окружает водную среду внутри. В настоящее время липосомы уже нашли применение в медицине как средство доставки лекарственных препаратов к месту назначения, а также в исследованиях возможности их применения при снятии интоксикации лекарственными препаратами.
Лекарственные препараты могут быть включены в липосомы разными методами, например пассивными методами и методикой использования градиента pH. Более подробно - см. Фенске и Кулис «Включение лекарственных препаратов внутри липосома pH-градиентными методами». Липосомальные технологии, том II, под ред. Грегори Грегориадиса, Informa Healthcare, сентябрь 2006 года, 27-50. Преимущество pH-градиента применительно к липидному бислою в том, что, как только в него попадает лекарственный препарат, он получает заряд за счет присоединения нового или утраты собственного протона (в зависимости от самого препарата и от значения pH). Таким образом, создается препятствие для его обратного переноса вовне, через липофильную мембрану. См., например: Майер и др. Труды по биохимии и биофизике, 857: 123-126, 1986, и Мэдден и др. «Химия и физика липидов», 53: 37-46, 1990. Системы переноски липосом могут служить серьезным буфером для токсического воздействия лекарственных препаратов, захватывая их в пространстве собственного просвета в своеобразную ловушку. Липосомальные препараты обычно вводят внутривенно или в предполагаемом месте действия препарата - например, интраперитонеально. Более подробно об интраперитонеальной доставке липосомальных препаратов - см. Фершреген и др. Журнал исследований рака, клиническая онкология, 129: 549-555, 2003; и Паркер и др. Исследования рака, 41: 1311-1317, 1981. Перитонеальная ретенция лекарств, введенных интраперитонеально и включенных в липосомы, зависит от формы и рецептуры композиции (например, жидкая форма липидного бислоя), содержания в нем холестерина, размера липосомы, заряда липосомы и/или ее оболочки - например, ПЭГ (полиэтиленгликоль). Интраперитонеально вводимые липосомальные лекарственные препараты переносятся кровью и через лимфатическую систему (Их содержание можно выявить в крови, лимфатических узлах и ряде других органов). На перитонеальную ретенцию, в частности, влияет размер липосом. При внутривенных инъекциях липосом диаметром, оптимальным для длительного обращения в крови, часто считается около 100 нм. Повышение размера липосом усиливает перитонеальную ретенцию, если липосомы вводить в виде интраперитонеальных инъекций. Липосомы с размером около 1000 нм и выше дают максимальную ретенцию в брюшной полости. Более подробно о факторах, влияющих на перитонеальную ретенцию интраперитонеально вводимых липосом - см. Садзука и др. «Токсикологические записки» 116: 51-59, 2000; Дадашзаде и др. Журнал контролируемого высвобождения, 148: 177-186, 2010; Мирамахди и др. Международный журнал фармацевтики, 383: 7-13, 2010; Хирано и Хант, Журнал фармацевтических наук, 74 (9), 915-921, 1985.
Более того липосомы, также как и липиды в эмульсии, применяют при снятии интоксикации лекарственными препаратами.
У Джамати и др. Клиническая токсикология 48: 1-27, 2010, приведен обзор специальной литературы по применению внутривенных жировых эмульсий (ВЖЭ). Это липидные эмульсии, применяемые при острых лекарственных отравлениях. Intralipid® - название торговой марки клинически значимой, коммерческой жировой эмульсии, 10, 20 или 30% веса которой приходится на очищенное соевое масло, а также очищенные яичные фосфолипиды, глицерин и воду для внутривенного или парентерального ввода лечебного питания пациентам, страдающим от плохого или недостаточного питания. Он также служит средством доставки анестетиков (пропофола и этомидата) и лечения тяжелых проявлений кардиотоксичности, вызванных передозировкой анестетиков местного действия (таких как бупивакаин), спасающих жизнь пациентов, не реагирующих на обычные методы реанимации. Как средство питания и противоядия, Intralipid® принимают внутривенно. Кейв и Гарви (Академическая медицина скорой помощи, 16: 151-156, 2009) провели обзор специальной литературы по применению ВЖЭ в качестве противоядия. Исследования на животных показали, что у кроликов, которым вводили инфузию кломипрамина, а также Intralipid® (внутривенно и перитонеально одновременно), кломипрамин экстрагировался активнее, чем только при внутривенном приеме Intralipid® (см. Гарви и др. Академическая медицина скорой помощи, 16: 815-824, 2009). Механизм действия ВЖЭ как противоядия состоит в том, что липидная композиция поглощает и тем самым «маскирует» токсичный препарат путем липидного экстрагирования. Правда, этот механизм работает только у препаратов, обладающих достаточной липофильностью, и зависит от коэффициента экстрагирования препарата в липидной композиции.
Как и ВЖЭ, липосомы, вводимые внутривенно, исследуются как потенциальные средства снятия интоксикации сердечно-сосудистыми препаратами. Ж.-К. Леру, Биотехнология природы, 2: 679-864, 2007, проводит обзор практики инъекций наноносителей (в частности, липосом) при снятии лекарственных интоксикаций. Бертран и др., ACS Nano, 4 (12), 7552-7558, 2010, демонстрируют случай детоксикации при помощи внутривенно введенных, трансмембранных и pH-градиентных липосом у крыс, которым внутривенно вводили болюс или перфузию сердечно-сосудистого препарата «дилтиазем». В отличие от липидного экстрагирования при помощи ВЖЭ механизм действия липосом состоит в поглощении и заряжении препарата на градиент pH так, чтобы поглощение стало необратимым. По сравнению с ВЖЭ липосомы намного эффективнее поглощают и удаляют введенные препараты (такие как блокаторы кальциевых каналов). Об этом есть сведения у: Форстер и др. Биоматериалы 33, 3578-3585, 2012.
Гипераммониемия - это клиническое состояние, связанное с повышением уровня аммиака в плазме крови больного. Оно проявляется по-разному, в том числе как аномалии в центральной нервной системе (ЦНС). Высокая концентрация аммиака в организме токсична. Эндогенная интоксикация аммиаком может наступить при нарушении способности организма к выводу азотистых шлаков (например, при врожденной ферментной недостаточности). К интоксикации аммиаком могут приводить экологические факторы и прием лекарственных средств. Обзор данных по аммониемии можно найти у Аурон и Брофи. Детская нефрология, 27: 207-222, 2012; и Клей и Хейнлайн. ГРУДНАЯ КЛЕТКА, Официальный журнал Американской коллегии врачей - специалистов по заболеваниям грудной клетки, (132), 1368-1378, 2007. Обычно гипераммониемия сопровождается отеком головного мозга, снижением мозгового метаболизма и усилением мозгового кровотока. Помимо лечения, устраняющего внутричерепную гипертонию, питания, препятствующего развитию белкового катаболизма и прекращению поступления белков с пищей, пациенту может потребоваться снижение уровня аммиака в организме путем его активного удаления. Его можно удалять, во-первых, за счет фармакологического вывода азота (например, путем приема натрия фенилацетата и натрия бензоата). Во-вторых, можно использовать «альтернативные» пути метаболизма, перитонеальный диализ, гемодиализ, непрерывная веновенозная гемофильтрация, непрерывная веновенозная гемодиафильтрация и непрерывная артериовенозная гемодиафильтрация. Это эффективные методы удаления аммиака, снимающие состояние гипераммониемии, связанное с нарушениями мочевинного цикла у детей и взрослых. У детей с врожденными нарушениями метаболизма веновенозный гемодиализ и непрерывный перитонеальный диализ - предпочтительный вид неотложной помощи при лечении гипераммониемии; см. Арбайтер и др. Нефролиз, диализ, трансплантация, 25: 1257-1265, 2010; Пела и др.; Детская нефрология, 23: 163-168, 2008.
Цели, лежащие в основе настоящего изобретения, - создание новых направлений применения липосомальных композиций в медицине. Еще одна цель - создание новых направлений лечения эндогенной и экзогенной интоксикации (в частности лечения интоксикаций лекарственными препаратами) метаболитами, пестицидами, инсектицидами, токсинами и химическим оружием. Еще одна цель настоящего изобретения заключается в обеспечении нового лечения гипераммониемии.
Все эти задачи можно успешно решать при помощи липосомальных композиций для использования в перитонеальном диализе у пациентов, страдающих интоксикацией эндогенного и экзогенного характера. При этом значение pH внутри липосом отличается от значения pH в брюшной полости, а pH внутри липосомы приводит к образованию заряженного токсина, включенного в липосому.
Далее по тексту, термин «липосомальная композиция для использования в перитонеальном диализе» означает композицию липосом: (i) пригодную для интраперитонеального приема, т.е. смесь физиологически приемлемых липидов и других компонентов; (ii) стабильную в физиологической среде (особенно в брюшной полости и крови) в течение времени, достаточного для поглощения и длительного удержания лекарств и метаболитов; и (iii) переносимую через мембрану.
Для введения изобретения в медицинскую практику необходима разница между значением pH внутри липосом и значением pH в брюшной полости, и то, чтобы значение pH внутри липосом вело к образованию заряженного токсина, включенного в липосому.
Липосомальная композиция настоящего изобретения является физиологически приемлемой, стабильной, трансмембранной и pH-градиентной. Она предназначена для перитонеального приема с адаптацией значения pH к конкретному токсину, который должен приобрести заряд внутри липосомы.
Термин «перитонеальный диализ» имеет (далее по тексту) общепринятое значение, понятное любому специалисту с опытом проведения перитонеального диализа. Для осуществления данного изобретения на практике в брюшную полость вводится терапевтическая дозировка композиции, например, путем инъекции одного болюса или непрерывной инфузии или перфузии. Липосомы внутри полости и прилегающих тканей и органов будут поглощать токсин, который необходимо вывести из организма. Значение pH внутри липосомы адаптируется так, чтобы при переносе через мембрану токсин получал заряд (т.е. получал дополнительный протон или терял один из своих протонов). В результате токсин, ставший положительно или отрицательно заряженным, не может быть перенесен обратно, через гидрофобный липосомальный бислой.
Липосома, поглощающая лекарство, надолго секвестрирует токсин и снижает токсичную концентрацию свободного соединения. Липосому вполне можно оставить в брюшной полости или тканях организма, если токсичная концентрация, возникающая в ходе последующего биологического разложения липосомы и высвобождения токсина, не приводит к образованию патологий у пациента. С другой стороны, предпочтительно, чтобы состав и/или размер липосом был адаптирован к длительному местонахождению в брюшной полости. В этом случае предпочтительно, чтобы поглотившие токсин липосомы в абдоминальной полости экстрагировались путем всасывания из перитонеальной полости. Интраперитонеальный ввод и экстрагирование можно проводить последовательно и/или одновременно.
Приготовление физиологически приемлемых, трансмембранных, pH-градиентных липосомальных композиций, пригодных для медицинской практики в соответствии с настоящим изобретением, подробно описано в предыдущем разделе - например, в документах, на которые сделана ссылка выше. Липосомальная композиция может включать в себя везикулы разного характера (однослойные, многослойные), состава, размера и характеристик, окружая водную среду разных композиций, значения pH и осмотической силы. В предпочтительных вариантах осуществления изобретения, основные компоненты мембраны липосомально-липидного слоя отбирают из группы натуральных или синтетических фосфолипидов, таких как:
- 1,2-дилауроил-sn-глицеро-3-фосфохолин (ДЛФХ)
- 1,2-димиристоил-sn-глицеро-3-фосфохолин (ДМФХ)
- 1,2-дипальмитоил-sn-глицеро-3-фосфохолин (ДПФХ)
- 1,2-дистеароил-sn-глицеро-3-фосфохолин (ДСФХ)
- 1,2-диолеоил-sn-глицеро-3-фосфохолин (ДОФХ)
- 1,2-димиристоил-sn-глицеро-3-фосфоэльханоламин (ДМФЭ)
- 1,2-дипальмитоил-sn-глицеро-3-фосфоэльханоламин (ДПФЭ)
- 1,2-дистеароил-sn-глицеро-3-фосфоэльханоламин (ДСФЭ)
- 1,2-диолеоил-sn-глицеро-3-фосфоэльханоламин (ДОФЭ)
- 1-миристоил-2-пальмитоил-sn-глицеро-3-фосфохолин (МПФХ)
- 1-пальмитоил-2-миристоил-sn-глицеро-3-фосфохолин (ПМФХ)
- 1-стеароил-2-пальмитоил-sn-глицеро-3-фосфохолин (СПФХ)
- 1-пальмитоил-2-стеароил-sn-глицеро-3-фосфохолин (ПСФХ)
- 1,2-димиристоил-sn-глицеро-3-[фосфо-rac-(1-глицерол)] (ДМФГ)
- 1,2-дипальмитоил-sn-глицеро-3-[фосфо-rac-(1-глицерол)] (ДПФГ)
- 1,2-дистеароил-sn-глицеро-3-[фосфо-rac-(1-глицерол)] (ДСФГ)
- 1,2-диолеоил-sn-глицеро-3-[фосфо-rac-(1-глицерол)] (ДОФГ)
- 1,2-димиристоил-sn-глицеро-3-фосфат (ДМФА)
- 1,2-дипальмитоил-sn-глицеро-3-фосфат (ДПФА)
- 1,2-дипальмитоил-sn-глицеро-3-[фосфо-L-серин] (ДПФС)
- Натуральный L-α-фосфатидилхолин (из куриных яиц, ЯФХ, или сои, СФХ)
Из фосфолипидов предпочтительнее всего - насыщенные и обладающие длинными цепочками, т.е. фосфолипиды с алкиловыми цепочками, в которых более 12, предпочтительнее - более 14, еще предпочтительнее - более 16 и предпочтительнее всего - более 18 атомов углерода.
Предпочтительное содержание липосом в композиции в соответствии с изобретением: одно- и/или многослойные липосомы, которые содержат
(i) 1-100, предпочтительнее 40-70 мол. % физиологически приемлемых фосфолипидов, предпочтительнее всего их выбирать в группе веществ, включающей в себя ДЛФХ, ДМФХ, ДПФХ, ДСФХ, ДОФХ, ДМФЭ, ДПФЭ, ДСФЭ, ДОФЭ, МПФХ, ПМФХ, СПФХ, ПСФХ, ДМФГ, ДПФГ, ДСФГ, ДОФГ, ДМФА, ДПФА, ДПФС, ЯФХ и/или СФХ.
(ii) 1-100, предпочтительнее 40-70 мол. % сфинголипидов, предпочтительно сфингомиелина;
(iii) 1-100, предпочтительно 40-70 мол. % сюрфактантов; прежде всего это гидрофобные простые эфиры алкилов, например, эфиры полиоксиэтилена («Бридж»)), сложные эфиры алкилов, полисорбаты, сложные эфиры сорбитана и/или амиды алкилов;
(iv) 5-100, предпочтительно 50-100 мол. % амфифильных полимеров и/или сополимеров, предпочтительно блок-сополимеров, состоящих из не менее чем одного блока гидрофильного полимера или сополимера, например полиэтиленгликоля и не менее, чем одного блока гидрофобного полимера или сополимера, например, поли(лактида), поли(капролактона), поли(бутилена оксида), поли(стирола оксида), поли(стирола), поли(этилэтилена) или полидиметилсилоксанов),
(v) 0-60 мол. %, предпочтительно 20-50 мол. % составов, усиливающих удержание токсинов, предпочтительно производные стерина - особенно холестерин,
(vi) 0-30 мол. %, предпочтительнее всего 1-5 мол. % стерических стабилизаторов, лучше пегилированных композиций, еще лучше - пегилированных липидов, предпочтительнее всего - ДСФЭ-ПЭГ.
В предпочтительных вариантах осуществления изобретения липосомоподобные везикулы состоят из полимеров и не содержат липидов. Поэтому они формально не считаются липосомами и называются полимерсомами. Однако в соответствии с настоящим изобретением на полимерсомы должен распространяться термин «липосома», так как он используется при определении цели изобретения и пунктов формулы изобретения.
Аналогичным образом липосомоподобные везикулы, состоящие из синтетических сюрфактантов и не содержащие липидов, называются ниосомами. Однако в соответствии с настоящим изобретением на ниосомы должен распространяться термин «липосома», так как он использован при определении цели изобретения и пунктов формулы изобретения.
В одном из предпочтительных вариантов осуществления изобретения липосомы, применяемые в соответствии с изобретением, включают в себя 10-100, предпочтительно 30-80, предпочтительнее - 40-70 и наиболее предпочтительно - 50-60 мол. % физиологически приемлемых фосфолипидов.
В одном из предпочтительных вариантов осуществления изобретения липосомы, применяемые в соответствии с изобретением, включают в себя 10-100, предпочтительно 25-75, предпочтительнее - 40-70 и наиболее предпочтительно - 50-60 мол. % сфинголипидов, предпочтительно сфингомиелина.
В одном из предпочтительных вариантов осуществления изобретения липосомы, применяемые в соответствии с изобретением, включают в себя 30-100, предпочтительно 40-95 и предпочтительнее - 45-60 мол. % сюрфактантов.
В одном из предпочтительных вариантов осуществления изобретения липосомы, применяемые в соответствии с изобретением, включают в себя 5-100, предпочтительно 30-100, предпочтительнее - 60-100 и предпочтительное всего - 95-100 мол. % амфифильных полимеров и/или сополимеров.
В предпочтительных вариантах осуществления изобретения концентрация стеринов в липосомальной композиции равна 0-60, предпочтительно 20-50 и предпочтительнее - 30-45 мол. % для усиления ретенции метаболита или лекарственного препарата.
Еще в одном предпочтительном варианте осуществления изобретения, концентрация стерического стабилизатора, предпочтительно пегилированных липидов в липосомальной композиции составляет 0-30, предпочтительно 0,5-20 и предпочтительное - 1-5 мол. %.
Еще в одном предпочтительном варианте изобретения диаметр липосом превышает 600, предпочтительно, если он более 700 и предпочтительное всего более 800 нм. Это означает: диаметр 600 нм - 10 мкм, предпочтительно 700 нм - 10 мкм, наиболее предпочтительно - 800 нм - 5 мкм. Это препятствует слишком быстрому дренированию перитонеального пространства.
Водный раствор внутри липидного бислоя липосомы имеет по преимуществу изотонический характер. Предпочтительно, если у него высокая буферная емкость при низком значении pH (цитратный, сульфатный, ацетатный, бензоатный, формиатный, гликолятный и малатный буфер и т.д.). Это обеспечивает высокую ретенцию основных соединений и высокую буферную емкость с высоким значением pH (буфер: кальция ацетат, бис-трис-пропан, сульфонаты (CAPS, CABS, TABS, CHES), бицин, трицин, этаноламин). Все это обеспечивает высокую степень удержания кислотных соединений. Уровень значения pH и буферные соединения необходимо адаптировать к выводимому токсину. Так, аммония сульфат (слабое основание) к поглощению аммиака с сильным основанием (т.е. лечением гипераммониемии) не пригоден. Напротив, он будет лишь вводить аммиак в организм, хотя это вещество должно выводиться из организма. При секвестрации слабых кислот основным буфером должен служить внутренний водный раствор (кальция ацетат и т.п.).
Предпочтительно, чтобы липосомальная композиция изобретения имела значение pH 1-6.5, предпочтительнее - 1.5-5, предпочтительнее всего - 1.5-4.
Также предпочтительно, чтобы значение pH липосомальной композиции было равно 8.5-12, предпочтительнее - 9-11, предпочтительнее всего - 9-10.
В одном из наиболее предпочтительных вариантов изобретения липосомальная композиция, применяемая в соответствии с изобретением, имеет липосомальный бислой, который включает в себя:
(i) 50-60, предпочтительно около 54 мол. % ДПФХ,
(ii) 40-50, предпочтительно 45 мол. % холестерина (ХОЛ)
и 0.5-2, предпочтительно 1 мол. % 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-N-[метокси(полиэтиленгликоль)-2000] (ДСФЭ-ПЭГ); и водный раствор внутри липосом (включает в себя 250 мкм цитратного раствора, буферированного при pH 1.5-3, предпочтительно 2, при этом диаметр липосом равен 800 нм и выше, предпочтительнее - 900 нм и выше и предпочтительнее всего - 1000 нм и выше.
Такая липосомальная композиция оптимальна при лечении гипераммониемии. Дополнительные примеры липосом, которые можно применять в соответствии с изобретением (в молярных соотношениях): ДМФХ/ХОЛ, 2:1; ДПФХ/ХОЛ, 2:1; ДСФХ:ХОЛ, 2:1; ДСФХ/ХОЛ/ПЭГ2000-ДСФЭ, 2:1:0,2; ДСФХ/ДСФГ/ХОЛ, 60:10:30; ДСФХ/ДСФГ/ХОЛ/ПЭГ2000-ДСФЭ, 55.83:10:27.92:6.25, ЯФХ/ХОЛ/DESP-ПЭГ, 50:45:5, сфингомиелин/ДПФХ/ХОЛ/ДСФЭ-ПЭГ, 25:25:45:5, куда входит внутренний цитратный буфер (110 ммоль pH 4, 200 ммоль pH 3, 250 ммоль pH 3, 250 ммоль pH 2 или 300 ммоль pH 2).
Термины «экзогенная интоксикация» и «эндогенная интоксикация» указывают на присутствие токсина, вырабатываемого самим организмом (т.е. эндогенный токсин) и токсина, поступающего в организм извне (т.е. экзогенный токсин) соответственно.
Предпочтительно применять липосомальную композицию изобретения для лечения экзогенной интоксикации, вызываемой метаболитами, лекарственными препаратами, пестицидами, инсектицидами, токсинами и применением химического оружия. Гербицидные интоксикации, от которых предпочтительно применять липосомальную композицию, - интоксикации ауксинами и атразином, а пестицидная интоксикация - интоксикация неоникотиноидом.
Один из предпочтительных вариантов осуществления изобретения направлен на лечение метаболитной интоксикации. Термин «метаболитная интоксикация», используемый настоящим, означает токсичную концентрацию эндогенных соединений, ведущую к развитию патологических состояний (аммиак, аргининосукцинат, мочевая кислота, изовалериановая кислота и пропионовая кислота и т.п.). Этот термин не распространяется на патологии, вызываемые экзогенными (например, лекарственными) метаболитами.
Метаболитные виды интоксикации, которые предпочтительно устранять в соответствии с изобретением: гипераммониемия, повышенное содержания в крови аргининосукциновой кислоты, мочевой кислоты, изовалериановой кислоты и пропионовой кислоты.
В соответствии с еще одним предпочтительным вариантом изобретения лечение можно проводить для устранения лекарственной интоксикации - предпочтительно от интоксикации, вызываемой кислотными и основными лекарственными препаратами.
Лекарственные препараты, которые липосома может поглощать интраперитонеально в соответствии с изобретением:
(1) средства против опухолей (прежде всего митоксантрон, эпирубицин, даунорубицин, доксорубицин, ципрофлоксацин, винкристин, винорелбин и винбластин);
(2) анестетики местного действия (прежде всего прокаин, лидокаин, бупивакаин, хлорпромазин, мидазолам и дибукаин);
(3) антагонисты адренергиков (прежде всего пропранолол, фенилэфрин, альпренолол, атенолол, кленбутерол, сальбутамол и тимолол);
(4) средства от аритмии (прежде всего хинидин);
(5) холинергики (прежде всего пилокарпин и физостигмин);
(6) антидепрессанты (прежде всего имипрамин, нортриптилин, амитриптилин, бупропион, доксепин и венлафаксин);
(7) антигистаминовые средства (прежде всего дифенилгидрамин и хлорфенамин);
(8) средства от малярии (прежде всего примахин, хинин, хлорохин, амодиахин и пириметамин);
(9) антипротозойные средства (прежде всего хинакрин);
(10) анальгетики (прежде всего кодеин, ацетаминофен, аспирин, фентанил, метадон и петидин);
(11) сердечно-сосудистые препараты (прежде всего дилтиазем, верапамил и дипиридамол);
(12) средства от конвульсий (прежде всего вальпроевая кислота и фенобарбитал);
(13) средства от психоза (прежде всего кветиапин, хлорпромазин и галоперидол);
(14) анксиолитики (прежде всего альпразолам и диазепам);
(15) противовоспалительные средства (прежде всего диклофенак и ибупрофен);
(16) средства от эректильной дисфункции (прежде всего сильденафил и тадалафил);
(17) средства от туберкулеза (прежде всего этамбутол, изониазид и пиразинамид);
(18) нейромедиаторы (прежде всего эпинефрин и норэпинефрин);
(19) психостимуляторы (прежде всего амфетамин, МДМА, метилфенидат, кокаин и героин).
Лекарственные препараты, интоксикацию которыми предпочтительнее всего лечить при помощи липосомальных композиций, используемых при перитонеальном диализе в соответствии с изобретением:
Ацетилсалициловая кислота, альпразолам, амитриптилин, амлодипин, амфетамин, атенолол, атропин, бупивакаин, бупропион, каптоприл, хлорохин, хлорфенирамин, хлорпромазин, хлорпропамид, кленбутерол, кокаин, кодеин, диазепам, дилтиазем, дифенгидрамин, дипиридамол, дизопирамид, доксепин, этамбутол, фентанил, фентанил, галоперидол, героин, ибупрофен, имипрамин, изониазид, кетопрофен, лидокаин, лоразепам, МДМА, метформин, метадон, метадон, метилфенидат, нифедипин, нортриптилин, петидин, фенобарбитал, фенпрокоумон, прокаинамид, пропранолол, пириметамин, кветиапин, хинакрин, хинидин, хинин, ропивакаин, сильденафил, вальпроевая кислота, венлафаксин, верапамил и варфарин.
Липосомальные композиции, входящие в предмет изобретения, предпочтительно применять для лечения эндогенных и экзогенных видов интоксикации у человека. Эти композиции также применимы при лечении эндогенных и экзогенных интоксикаций у млекопитающих, таких как свинья, крупный рогатый скот, собаки, кошки, овцы, козы и лошадь, и птиц.
Есть еще один аспект настоящего изобретения. Речь идет о фармацевтических композициях, включающих в себя не менее одной липосомальной композиции, входящей в изобретение, и (по выбору) один или несколько фармацевтически приемлемых инертных наполнителей (эксципиентов). Обычно в эти композиции входит терапевтическая дозировка липосомальной композиции, а также (по выбору) вспомогательные вещества (фармацевтически приемлемый эксципиент (эксципиенты) и т.п.). Производство упомянутых фармацевтических композиций проводится по технологиям, широко известным в фармацевтике. Носителем или эксципиентом может быть жидкий материал, служащий основой или средой для активного компонента. Такие носители (эксципиенты) хорошо известны специалистам-фармакологам. В их число входят стабилизаторы, суспендирующие средства, осмотически активные вещества (такие как растворы глюкозы, желатин, ксилитол, сорбитол, маннитол, полимер глюкозы (например, икодекстрин) и аминокислоты), противомикробные консерванты, антиоксиданты, pH-регулирующие вещества (натрия и калия лактат и т.п.), контрастные вещества и т.д. В соответствии с изобретением фармацевтическая композиция должна быть пригодной для интраперитонеального ввода (предпочтительно человеку) в форме растворов, суспензий и тому подобного.
Еще один аспект настоящего изобретения - методика лечения, т.е. способ лечения пациента, страдающего эндогенной или экзогенной интоксикацией. При этом предполагается прием липосомальной композиции в терапевтической дозировке путем ввода в перитонеальное пространство пациента.
Какие виды интоксикации экзогенного характера поддаются лечению в соответствии с изобретением? Это интоксикация, вызываемая лекарственными препаратами, пестицидами, инсектицидами, токсинами и применением химического оружия. Из видов интоксикации метаболитного характера, это - гипераммониемия, повышенное содержание в крови аргининосукциновой кислоты, мочевой кислоты, изовалериановой кислоты и пропионовой кислоты.
Лечение в соответствии с данным вариантом изобретения предпочтительно проводить при интоксикации у человека.
Еще в одном варианте изобретения лечение применимо к эндогенным и экзогенным видам интоксикации у птиц и млекопитающих (прежде всего свиней, крупного рогатого скота, собак, кошек, овец, коз, лошадей и т.д.).
При лечении видов эндогенной и экзогенной интоксикации, описанных выше, липосомальную композицию изобретения можно вводить в любой форме и любым методом, обеспечивающим биодоступность липосом и липосомоподобных везикул (полимерсом, ниосом и т.д.) в брюшной полости в терапевтической дозировке. Предпочтительно интраперитонеальный ввод липосом проводить в форме болюсных инъекций, инфузии и/или перфузии. Любой специалист с опытом приготовления интраперитонеальных композиций может легко выбрать правильную форму и правильный метод ввода композиции в зависимости от характеристик токсина, подлежащего секвестрации и/или выводу из организма.
В одном из предпочтительных вариантов изобретения методика оказания медицинской помощи включает в себя экстрагирование липосом из абдоминальной полости - последовательно и/или одновременно.
Ниже приведены примеры осуществления изобретения (с указаниями экспериментальных вариантов осуществления изобретения и рисунков), ни один из которых не ограничивает предмет изобретения прилагаемыми пунктами формулы изобретения.
Чертежи
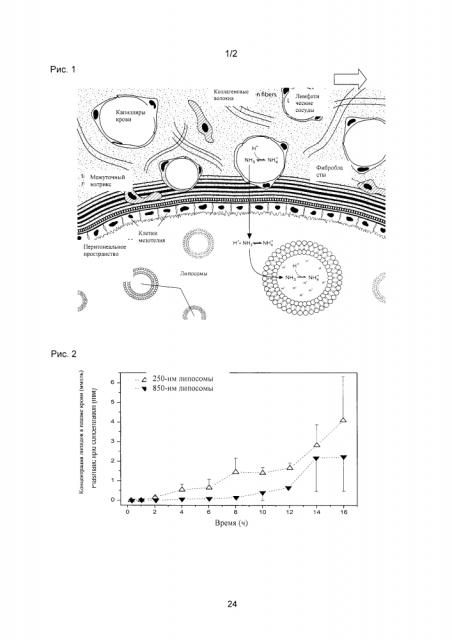
Фиг. 1: секвестрация токсичных веществ (например, лекарственных препаратов и аммиака, NH3) в перитонеальном пространстве при помощи трансмембранных pH-градиентных липосом (слабое основание). Происходит диффузия неионизированного соединения из капилляров крови в перитонеальное пространство, где он (уже в ионизированной форме ()) попадает в везикулы. Диффузия продолжается, пока не исчерпывается внутренняя буферная емкость липосом.
Фиг. 2: дренирование липосом из перитонеального пространства в кровь после интраперитонеального ввода. Контрастное вещество необменного стерина (холестерил BODIPY® FL-C12, компания Invitrogen) включен (0.05 мол. %) в липосомальную мембрану (в процессе образования липидной пленки). После интраперитонеального ввода липосом флюоресценция контрастного вещества (λex=470 нм, λem=520 нм) определялась в аликвотах плазмы крови и подвергалась сравнению с показателями кривой калибрации. Это позволяло получить показатель концентрации липосомальных липидов. Более крупные липосомы оставались в перитонеальном пространстве дольше (8 ч). Липосомы же небольшого размера выявлялись в крови в серьезных концентрациях через 4 ч. Средний показатель ± среднее отклонение (CO) (n=3).
Фиг. 3: поглощение аммиака (в лабораторных условиях) pH-градиентными липосомами в 50% сыворотке крови эмбрионов крупного рогатого скота при температуре 37°C. Липосомы поглощали аммиак быстро и эффективно. Первоначальная концентрации аммиака и липосом установлена на уровне 1.7 и 3.8 ммоль. Потенциально это обеспечивало максимальную захватоемкость на уровне 0.45 мкмоль аммиака/мкмоль липида. Интересно отметить, что везикулы секвестрировали аммиак в объеме, превышающем его общий объем, поступивший в данную систему (пунктирная линия). Излишек поступал за счет нативного аммиака, содержащегося в сыворотке крови. Диаметр липосом составлял 840 нм. Средний показатель ± CO (n=6).
Фиг. 4: концентрация аммиака (NH3) в перитонеальном диализате в отсутствие (замкнутые треугольники) и при наличии (открытые треугольники) липосом. Диализная жидкость вводилась здоровым крысам путем инъекции, интраперитонеально, t=0 ч. Дозировка инъекций липосом составила 180 мг/мг, а концентрация липидов в диализной жидкости - 15 ммоль. Диаметр липосом составлял 850 нм.
Фиг. 5: концентрация верапамила (ВП) в перитонеальном диализате в отсутствие (замкнутые треугольники) и при наличии (открытые треугольники) липосом. Прием ВП проводился пероральным путем, через зонд, t=0 ч (50 мг/кг,), после чего вводилась интраперитонеальная инъекция диализной жидкости, t=1 ч (). Дозировка инъекций липосом составила 180 мг/кг, а концентрация липидов в диализной жидкости - 15 ммоль. Диаметр липосом составлял 850 нм.
Примеры
В примерах ниже показано, что возможна длительная ретенция липосомальной композиции (Пример 1) в перитонеальном пространстве после интраперитонеального ввода в зависимости от размера липосом (Пример 2). Эти липосомы быстро и эффективно поглощали аммиак в 50% сыворотке крови эмбрионов крупного рогатого скота (Пример 3). Они также проявляли способность к захвату и концентрации аммиака (Пример 4) и перорально принятого препарата «верапамил» (Пример 5) в перитонеальном пространстве. Тем самым наглядно продемонстрирована способность липосом к детоксикации метаболитов и лекарственных препаратов путем их интраперитонеального ввода.
Пример 1 - Липосомальная композиция и ее приготовление
Композиция, проходившая испытания в ходе описанных ниже экспериментальных исследований в лабораторных условиях, состояла из ДПФХ с 45 мол. % ХОЛ и 5 мол. % ДСФЭ-ПЭГ. Водный раствор внутри липосом представлял собой раствор натрия цитрата (250 ммоль), буферированный при pH 2. Требуемые вещества получены методом гидратации/экструзии липидной пленки. (См.: Хоуп М., Бэлли М., Уэбб Г., Каллис П.Р. «Образование крупных однослойных везикул в ходе быстрой экструзии. Характеристика распределения по размерам, захваченного объема и способности к сохранению мембранного потенциала». Труды по биохимии и биофизике, 1985, 55-65). Липиды, ХОЛ и, в конечном итоге, контрастное вещество холестерила BODIPY® FL-C12, от компании Invitrogen (0.05 мол. %) сначала растворили в хлороформе, который затем удалили в условиях непрерывного азотного потока и высокого вакуума в течение >12 ч. Липидная пленка гидратировалась цитратным буфером (250 ммоль, pH 2). Крупные везикулы образовались путем экструзии через 2 пакетированные мембраны размером 5 мкм. Трансмембранный pH-градиент установлен путем диализа в физиологическом растворе в течение >12 ч (мембранное отсечение: 1000 кДа).
Пример 2 - Дренирование липосом из перитонеального пространства в кровь после интраперитонеального ввода
Группе крыс Спрейга-Доули (самцы, 300 г) ввели легкую анестезию путем ингаляции изофлурана (2%) и 20 мл раствора икодекстрина (7.5%), содержавшего липосомы (диаметром 250 либо 850 нм) с контрастным веществом необменного стерина (холестерил BODIPY® FL-C12, компания Invitrogen, 0.05 мол. %) в своей мембране. Через специально сделанный стерильный прокол их медленно ввели путем инъекции в перитонеальное пространство. Затем через хвостовые вены взяли пробы аликвот крови (250 мкл) - через 15 минут и через 1, 2, 4, 6, 8, 10, 12, 14 и 16 ч после интраперитонеальной инъекции. Сепарацию плазмы от аликвот крови провели путем центрифугирования (6000 г за 10 мин), а флюоресценцию контрастного вещества в плазме крови определили на уровне λem=520 нм (λex=470 нм).
Пример 3 - Поглощение аммиака pH-градиентными липосомами в 50% сыворотке крови эмбрионов крупного рогатого скота (в лабораторных условиях)
Кинетика поглощения аммиака (NH3) находилась под мониторингом в 50% сыворотке крови эмбрионов крупного рогатого скота (СКЭРС), в прилегающих диффузионных ячейках (компания PermGear, город Хеллертаун, штат Пенсильвания) при температуре 37°C. Липосомы, используемые в эксперименте, имели диаметр 850 нм и содержали 54 мол. % ДПФХ, 45 мол. % холестерина, 1 мол. % ДСФЭ-ПЭГ и внутренний цитратный раствор, (250 ммоль) буферированный при pH 2. Ячейка-донор (без липосом) отделялась от ячейки-реципиента (с липосомами) поликарботантной мембраной с 100-нм порами. Молярное соотношение между NH3 и липидами установлено на уровне 0.45, а первоначальная концентрация NH3 - на уровне 1.7 ммоль в обеих ячейках, чтобы достичь равновесия. Поглощение NH3 везикулами в ячейке-реципиенте имело прямую причинно-следственную связь со снижением концентрации токсина в ячейке-доноре. Аликвоты (100 мкл) взяли на исследование из ячейки-донора через 3, 30 минут, а также через 1, 2, 4, 8 и 24 ч после инъекции pH-градиентных липосом в ячейку-реципиент. После этого путем колориметрического анализа исследователи определили количественные показатели NH3 (Бертло М.П.Э. Анилиновый фиолетовый, Repert Chim Appl 1859, 1: 284).
Пример 4 - Концентрация аммиака в перитонеальном диализате в отсутствие и с наличием липосом
Группе крыс Спрейга-Доули (300 г) ввели легкую анестезию изофлураном (2.5%, 0.6 л/мин O2), хранившимся под подогреваемым защитным покрытием/слоем. Затем им в перитонеальное пространство через стерильный абдоминальный прокол медленно ввели 20 мл раствора икодекстрина (7.5%) с наличием липосом (3 мг/мл)