Ионные жидкости как антимикробные препараты
Иллюстрации
Показать всеИзобретение относится к области медицины и предназначено для лечения инфекционных процессов, вызванных чувствительными микроорганизмами. Изобретение раскрывает применение тетрахлорферрата N-децилпиридиния в качестве противомикробного средства. Использование данного соединения, обладающего противомикробным действием, обеспечивает лечение инфекционных процессов, вызванных чувствительными микроорганизмами. 1 ил., 1 табл.
Реферат
Изобретение относится к области медицины и может быть использовано в медицинской практике в качестве средства, обладающего противомикробным действием, для лечения инфекционных процессов, вызванных чувствительными микроорганизмами.
Четвертичные аммониевые соединения, содержащие в молекуле один или два высших радикала, уже много лет применяют в медицинской практике в качестве противомикробных средств. Установлен ряд важных закономерностей связи, между химической структурой этих веществ и их противомикробным действием, позволивший создать ряд эффективных препаратов [А.Г. Голиков, П.В. Решетов, А.П. Кривенько и др., Хим.-фарм. журн., 39(9), 23-25 (2005).; А.А. Фефелов, Автореф. дис. канд. хим. наук, УФА (2006).; О.В. Гудзь, Провизор, 6, 1-10 (1998)]. Потребность в подобных препаратах определяется, прежде всего, выраженной изменчивостью микроорганизмов, формированием и широким распространением их резистентных вариантов, общим нарушением экологических связей и интенсивным загрязнением внешней среды [Н.В. Климова, H.М. Зайцева, Н. И. Авдюнина и др., Хим.-фарм. журн., 24(1), 26-29 (1990)].
Известно, что производные четвертичного аммония и гетероциклических аминов сравнительно легко могут быть синтезированы. Существенный интерес представляет изучение механизма противомикробного действия этих соединений на клеточном, субклеточном и молекулярном уровнях, который позволит предсказать спектр биологических свойств и осуществить направленный синтез новых соединений.
Несомненно, что на биологическую активность четвертичных солей аминов оказывает влияние как природа катиона, так и аниона, поэтому замена традиционных галогенид анионов в структуре соли на объемные типа [PF6]-, [BF4]-, [FeCl4]- и другие анионы должна сказаться на изменении их биологической активности. Подобные соединения - четвертичные соли аммония, пиридиния, имидазолия, содержащие объемные гидрофобные или гидрофильные анионы и находящиеся в жидком состоянии в широком интервале температур, называемые ионными жидкостями (ИЖ), в последнее время привлекают внимание исследователей в виду уникальности их свойств. Негорючесть, пренебрежимо малое давление паров и гидрофобность ИЖ практически исключает их попадание в окружающую среду; нетоксичность обусловливает принадлежность ИЖ к классу растворителей, отвечающих современным экологическим требованиям [P. Wasserscheid, T. Welton (eds.), Ionic Liquids in Synthesis, Wiley - VCH Verlag GmbH & Co. KgaA, Weinheim (2002), p. 355., H.В. Шведене, Д.В. Чернышев, И.В. Плетнев, Журн. Рос. хим. об-ва им. Д.И. Менделеева, 42(2), 80-91 (2008)].
Поскольку проблема поиска новых антисептических препаратов остается актуальной, представлялось интересным проследить, сохраняется ли антимикробная активность и для соответствующих ионных жидкостей, полученных на основе классических четвертичных солей аммония, пиридиния и морфолиния.
В качестве аналогов могут выступать следующие несколько работ. Известно использование в качестве антимикробных препаратов широкого круга соединений, относящихся к классу ионных жидкостей (US 20110144079 antimicrobial system). Недостатком является то, что из всего огромного перечня предложенных соединений антимикробная активность (зоны задержки роста микроорганизмов) исследована только лишь для нескольких отдельных соединений с катионом 1,3-диалкилимидазолия и хлорид анионом.
Также известно использование в качестве антимикробного препарата терпенсульфида 2-(1'-гидрокси-4'-изопропенил-1'-метилциклогексил-2-тио)-метилэтаноата, обладающего противомикробной активностью (RU 2556509). Недостатком этого соединения является достаточно сложная методика его синтеза и в конечном счете высокая стоимость.
Известно использование ионных жидкостей с катионом хинолиния и изохинолиния с различными анионами как соединения, обладающие антимикробной активностью (RU 2010146005). Недостатком является использование дополнительно соединений, поддерживающих вязкость, а также присутствие ионов металлов: серебра, меди и др.
В качестве прототипа может выступать патент (WO 2009125222 Antimicrobial system). Авторами предложено использовать широкий ряд ионных жидкостей с алифатическими и гетероциклическими азотсодержащими катионами и различными органическими и неорганическими анионами в качестве антимикробных препаратов. Недостатком может служить отсутствие данных по исследованию антимикробной активности соединений, в состав которых входят катион пиридиния с длинноцепочечным радикалом и неорганическими анионами.
Противомикробные свойства заявляемых соединений: тетрафторбората, сульфата, нитрита, нитрата и тетрахлорферрата N-децилпиридиния в литературе не описаны.
Целью изобретения является поиск эффективных соединений, обладающих повышенной противомикробной активностью.
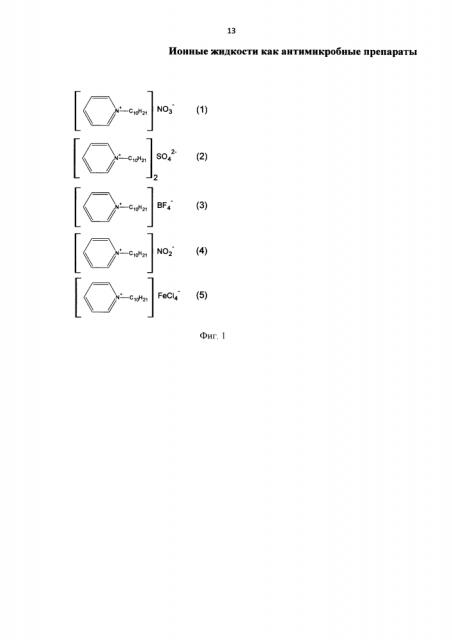
Данная задача решается за счет использования в качестве противомикробных препаратов следующих соединений: тетрафторбората, сульфата, нитрита, нитрата и тетрахлорферрата N-децилпиридиния, обладающего противомикробной активностью (Фиг. 1).
Техническое решение заключается в повышении эффективности воздействия на жизнеспособность различных микроорганизмов.
Сущность изобретения поясняется чертежом и таблицей, на которых изображено следующее.
На фиг. 1. представлены соединения, обладающие противомикробной активностью, где 1 - нитрат N-децилпиридиния, 2 - сульфат N-децилпиридиния, 3 - терафторборат N-децилпиридиния, 4 - нитрит N-децилпиридиния, 5 - тетрахлорферрат N-децилпиридиния.
В таблице 1 представлена антимикробная активность исследуемых соединений по отношению к тест-культурам патогенных и условно-патогенных микроорганизмов.
Антимикробная активность соединений исследовалась дискодиффузионным методом (ДДМ) в агар на газоне тест-культур: грамположительные Bacillus subtilis 6633, Staphylococcus aureus P209 АТСС 25923, Streptococcus pyogenes NCTC/2696/ATCC/96/5; грамотрицательные E.coli АТСС 25922, Shigella sonnei III №1908, Salmonella typhimurium 5715, Pseudomonas aeruginosa ATCC 27853 и дрожжевые грибы Candida albicans АТСС 885-653. Антибактериальную активность материала выражали в мм диаметра задержки роста. Высокая активность - диаметр зоны задержки роста более 25 мм; активное - диаметр зоны задержки роста 16-25 мм; малоактивное - диаметр зоны задержки роста 10-15 мм.
Для определения чувствительности ДДМ использовали Агар Мюллера-Хинтона (для стрептококков с добавлением бараньей крови), приготовленный в соответствии с инструкцией изготовителя. Толщина слоя агара в чашке составляла 4,0±0,5 мм, что достигалось при внесении в чашку Петри диаметром 90 мм строго 20 мл агара, диаметром 100 мм - 25 мл агара. Перед заполнением расплавленной средой чашки Петри устанавливали на строго горизонтальную поверхность (выверенную по уровню, без впадин и выпуклостей). После заполнения чашки оставляли при комнатной температуре для застывания. Использовали свежеприготовленные чашки, которые перед инокуляцией подсушивали инкубацией при 37°С с приоткрытой крышкой в течение 10-20 мин. Перед инокуляцией контролировали отсутствие конденсата жидкости на внутренней поверхности крышек.
Для определения чувствительности ДДМ использовали стандартизированные диски НД-ПМП-1 из картона технического фильтровального ГОСТ 6722-75 (ФГУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Л. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека).
Хранение дисков НД-ПМП-1 из картона технического фильтровального осуществляли в герметичной упаковке предприятия-изготовителя в сухом темном месте при температуре 2-8°С в течение всего срока годности набора. Небольшие партии дисков, используемые при повседневной работе, хранили при температуре до 25°С не более 15 дней плотно укупоренными так, чтобы гарантировать невозможность попадания во флакон влаги, кроме того, для дополнительной защиты от влаги во флаконах (картриджах) с дисками содержится специальный влагопоглотитель (силикагель). Перед использованием флаконы с дисками выдерживали при комнатной температуре 18-25°С в течение 1 ч для предотвращения образования конденсата на внутренней стенке флакона. Вскрытый флакон с дисками хранили при температуре 2-8°С в течение всего срока годности набора, при условии сохранения цвета индикаторного силикагеля от светло-голубого до синего. Непосредственно перед применением диски пропитывали исследуемым соединением. В качестве контроля использовали диски, пропитанные дистиллированной водой.
Для определения чувствительности ДДМ использовали стандартный инокулюм, соответствующий по плотности 0,5 по стандарту Мак-Фарланда и содержащий примерно 1,5×108 КОЕ/мл. Инокулюм использовали в течение 15 мин после приготовления. Для инокуляции приготовленных чашек с агаром использовали стерильные ватные тампоны промышленного производства (палочка-тампон (пластик-хлопок) CITOSWAB стерильный в индивидуальной упаковке). Тампон погружали в стандартную суспензию микроорганизма, затем избыток инокулюма удаляли, отжав тампон о стенки пробирки. Инокуляцию проводили штриховыми движениями в трех направлениях, поворачивая чашку Петри на 60°.
Не позднее чем через 15 мин после инокуляции на поверхность питательной среды наносили диски, пропитанные исследуемыми соединениями и дистиллированной водой. Аппликацию дисков проводили с помощью стерильного пинцета. Расстояние от диска до края чашки и между дисками составляло 15-20 мм. Для равномерного контакта с поверхностью агара диски аккуратно прижимали пинцетом.
Непосредственно после аппликации дисков на поверхность питательной среды чашки Петри помещали в термостат кверху дном и инкубировали при температуре 37°С в течение 18-24 ч (в зависимости от вида тестируемого микроорганизма).
После окончания инкубации чашки помещали кверху дном на темную матовую поверхность так, чтобы свет падал на них под углом в 45° (учет в отраженном свете). Диаметр зон задержки роста измеряли с точностью до 1 мм с помощью линейки лекало (Hi Antibiotic Zone Scale (PW 2097) (Hi Media Laboratories Pvt. Limited, India)).
В качестве препарата сравнения использовался противомикробный препарат диоксидин (производное ди-N-оксихиноксалина), широко применяемый в лечебной практике. Этот препарат обладает высокой химиотерапевтической активностью in vitvo на модельных инфекциях, близких по патогенезу к патологическим процессам у человека (гнойные менингиты, пиелонефриты, септикопиемии) и вызванных штаммами анаэробных бактерий, устойчивых (в том числе полирезистентных) к препаратам других классов, включая штаммы синегнойной. Диоксидин характеризуется широким антибактериальным спектром с бактерицидным действием, активен также в отношении грамположительных и грамотрицательных аэробных условно-патогенных бактерий. Показана активность диоксидина в отношении микобактерий туберкулеза (Падейская Е.Н. Антибактериальный препарат диоксидин: особенности биологического действия и значение в терапии различных форм гнойной инфекции / Е.Н. Падейская // Инфекции и антимикробная терапия. - 2011. - Т. 3 - №5. - С. 105-155).
Антимикробную активность соединений выражали в мм диаметра задержки роста. Результаты определения представлены в Таблице 1.
Все соединения проявили среднюю и высокую антимикробную активность в отношении всех тест-культур микроорганизмов.
Наиболее выраженной активностью образцы обладали в отношении гноеродного стрептококка (Streptococcus pyogenes), зоны задержки роста составляли от 20 до 31 мм в диаметре, и спорообразующей сенной палочки (Bacillus subtilis), диаметр зоны задержки роста - 20-26 мм. В отношении другого грампозитивного микроорганизма золотистого стафилококка (Staphylococcus aureus) высокой бактериостатической активностью (20-22 мм) обладали образцы №2-5 и средней (15-18 мм) соединение №1.
Грамотрицательные микроорганизмы (кишечная палочка, шигеллы, сальмонеллы, псевдомонады) проявили промежуточную чувствительность к исследуемым соединениям. Диаметр зоны задержки роста составил 10-19 мм. Наибольшую антимикробную активность по отношению к подавляющему большинству микроорганизмов показал тетрахлорферрат N-децилпиридиния, причем его активность к штаммам микроорганизмов E.coli, Shigella sonnei, Candida albicans, Bacillus subtilis выше, чем у препарата сравнения - диоксидина. Все исследованные соединения показали антимикробную активность на уровне диоксидина или выше в отношении большинства грамположительных и грамотрицательных микроорганизмов.
Дрожжевые грибы Candida albicans проявили промежуточную чувствительность к исследуемым соединениям с одинаковой зоной задержки роста 15 мм в диаметре, кроме соединения №4, которое проявило высокую активность.
Таким образом, все исследованные соединения обладают широким спектром антибактериальной активности. Причем в большей степени данные образцы действуют на грамположительные бактерии стрептококки и стафилококки, которые вызывают в основном гноеродные инфекции, а также пневмонии, ревматизм, скарлатину, рожистые воспаления, колиты и др. заболевания кожи, слизистой оболочки, кишечника и др. органов, включая кариес зубов, и могут быть предложены в качестве противомикробных препаратов.
Среднюю антимикробную активность соединения оказывали на грамотрицательные микроорганизмы кишечной группы бактерий (эшеришии, шигеллы, сальмонеллы, псевдомонады), возбудителей эшерихиозов, бактериальной дизентерии, сальмонеллеза и на дрожжевые грибы рода Candida.
Применение тетрахлорферрата N-децилпиридиния в качестве противомикробного средства.