Фармацевтическая композиция для лечения, профилактики или облегчения двигательных расстройств и ее применение
Иллюстрации
Показать всеГруппа изобретений относится к лечению двигательных расстройств. Предложено применение композиции, содержащей золмитриптан или его фармацевтически приемлемую соль и агонист 5-HT-рецепторов буспирон или его фармацевтически приемлемую соль, для лечения, профилактики или облегчения двигательных расстройств и применение набора, содержащего фармацевтическую композицию золмитриптана или его соли и фармацевтическую композицию агониста 5-HT-рецепторов буспирона или его соли, по тому же назначению. Технический результат – повышение эффективности комбинированного лечения в части проявлений поздней дискинезии и снижения симптомов болезни Паркинсона на ее модели у крыс. 2 н. и 11 з.п. ф-лы, 4 ил., 9 пр.
Реферат
Область техники
Данное изобретение относится к применению агонистов 5-HT1-рецепторов в качестве соединений в составе фармацевтических композиций и к способам лечения двигательных расстройств, связанных с нарушениями неврологических функций. В частности, настоящее изобретение относится к способу лечения пациентов, страдающих от двигательных расстройств, связанных с пониженным уровнем дофамина в нейронном синапсе, таких как поздняя дискинезия, болезнь Паркинсона и связанные с ней нарушения. Данное изобретение предусматривает также наборы элементов, в которых содержатся соединения или фармацевтические композиции по изобретению, а также способы их получения.
Уровень техники
Двигательные расстройства представляют собой группу заболеваний, которые влияют на способность совершать и контролировать различные движения тела и часто связаны с неврологическими расстройствами или состояниями, связанными с неврологической дисфункцией. Двигательные расстройства могут проявляться в аномальных подвижности и скорости движения, в гипертрофированных или непроизвольных движениях или в замедлении или отсутствии сознательных движений. Например, акатизия представляет собой двигательное расстройство, характеризующееся неприятными ощущениями "внутреннего" беспокойства, смутного недовольства или дисфорией, что приводит к неспособности пациента сидеть спокойно или оставаться неподвижным. Пациенты обычно находятся в возбужденном состоянии, непрерывно двигаются, в том числе, раскачиваются, переступая с ноги на ногу, или же двигаются, стоя на месте, волочат ноги и притоптывают, раскачиваются взад и вперед или же поворачиваются, а, сидя, постоянно перекладывают одну ногу на другую. В случаях серьезного заболевания пациенты постоянно расхаживают взад и вперед, пытаясь заглушить чувство беспокойства, так как возбужденное состояние длится от момента пробуждения до момента засыпания поздно вечером. Некоторые пациенты описывают это чувство как ощущение внутреннего напряжения и пытку или как муки при действии химических веществ.
Другим примером двигательного расстройства является дискинезия, которая характеризуется непроизвольными движениями, которые могут затрагивать отдельные части тела или все туловище и приводят к потере дееспособности. Поздняя дискинезия представляет собой один из примеров дискинезии, который характеризуется повторяющимися непроизвольными и бесцельными движениями, такими как гримасничанье, высовывание языка, чмоканье губами, сморщивание и поджимание губ и быстрое моргание глазами. Могут появляться непроизвольные движения пальцев, как если бы пациент играл на невидимой гитаре или невидимом пианино.
Часто неврологическое расстройство или состояние, которое вызывает двигательное расстройство, связано с дисфункцией базальных ганглиев. Такая дисфункция может быть идиопатической, вызванной некоторыми лекарственными препаратами или инъекциями или же вызванной генетическими дефектами.
Болезнь Паркинсона (PD) является примером неврологического расстройства, связанного с дисфункцией базальных ганглиев. PD приводит к двигательным расстройствам и характеризуется окостенением мышечной ткани, тремором, постуральной аномалией, аномальной походкой и замедлением выполнения физических движений (брадикинезией), а в экстремальных случаях потерей двигательной способности (акинезией). Это заболевание вызвано прогрессивной гибелью и дегенерацией дофаминовых (DA) нейронов в компактной части черной субстанции мозга и аномальным регулированием дисфункциональной дофаминергической нейротрансмиссии. Для того, чтобы возместить потерю дофамина, PD лечат в настоящее время леводопой (леводофой) (L-DOPA), являющейся предшественником дофамина, в сочетании с агонистами дофамина или другими агентами, которые приводят к увеличению концентрации дофамина в синаптической щели. PD является распространенной болезнью, которая поражает 1% людей старше 60 лет.
К сожалению, лечение PD с помощью L-DOPA часто приводит к возникновению дискинезии (уменьшению сознательных движений и наличию непроизвольных движений) у пациентов с прогрессирующей PD при ограниченном регулировании количества дофамина. Этот особый вид дискинезии называют дискинезией, вызванной применением L-DOPA (LID), она вызвана чрезмерным количеством дофамина в синапсах (Jenner: Nat. Rev. Neurosci. 2008; 9 (9): 665-677; Del Sorbo and Albanese: J. Neurol. 2008; 244, Suppl. 4: 32-41). Около 50% пациентов, которых лечат при помощи L-DOPA, страдают от LID, которая сильно ограничивает оптимальное лечение и ухудшает качество жизни.
Двигательные расстройства, вызываемые лекарствами, могут также быть связаны с лечением других неврологических и психиатрических заболеваний. Примеры таких заболеваний включают позднюю дискинезию и акатизию, которые обычно развиваются в качестве побочного эффекта длительного лечения нейролептиками, например, у пациентов, которые страдают от шизофрении.
Поздняя дискинезия может возникнуть в течение месяцев, лет, прошедших после прекращения приема лекарств, и даже стать постоянной. Предотвращение возникновения поздней дискинезии прежде всего достигается за счет применения самых маленьких эффективных доз нейролептика в течение короткого времени. Если поздняя дискинезия диагностирована, терапия с помощью лекарства, являющегося причиной ее возникновения, прекращается.
Вскоре после появления антипсихотических средств в 1950-е годы акатизия была признана как один из наиболее распространенных и быстро возникающих побочных эффектов. Оценка случаев появления акатизии у людей, принимающих нейролептики, показала, что она возникает у 20-75% пациентов, наиболее часто в течение первых трех месяцев приема лекарств. Акатизия связана не только с постоянным приемом нейролептика, но также и с быстрым увеличением его дозы. К сожалению, акатизию трудно отличить от психического возбуждения или беспокойства, особенно, если человек описывает субъективные ощущения при акатизии в терминах, которые появляются при внешних обстоятельствах. Следовательно, доза лекарства, которая вызывает двигательное расстройство, может быть еще более увеличена после появления симптомов акатизии.
Двигательные расстройства часто возникают из-за ухудшенного регулирования нейротрансмиссии дофамина. Дофамин связывает синаптические дофаминовые рецепторы D1, D2, D4 и D5, и это связывание контролируется путем регулируемого высвобождения и обратного захвата дофамина. Ухудшенное регулирование высвобождения и обратного захвата дофамина может привести к избытку дофамина в синапсах, которое вызывает развитие двигательных расстройств.
Как уже упоминалось выше, PD является примером двигательного расстройства, связанного с дисфункциональным регулированием нейротрансмиссии дофамина, которое вызывается прогрессивной дегенерацией дофаминовых нейронов. Поздняя дискинезия является другим примером двигательного расстройства, связанного с дисфункциональным регулированием нейротрансмиссии дофамина. Нейролептики действуют в основном на дофаминовую систему и представляют собой лекарства, которые блокируют рецепторы D2 дофамина для предотвращения развития состояний, связанных с повышенным уровнем дофамина. Предполагают, что поздняя дискинезия в основном возникает из-за сверхчувствительности дофамина в пути черной субстанции мозга, вызванной приемом нейролептика, при этом наиболее повреждается рецептор D2 дофамина. Более старые нейролептики, которые характеризуются большим сродством к сайгу связывания D2, связаны с большими рисками развития поздней дискинезии.
Высвобождение и обратный захват дофамина регулируются рядом нейротрансмиттеров, включая серотонин (5HT). Другие нейротрансмиттеры, непосредственно или косвенно регулирующие нейротрансмиссию дофамина, представляют собой ингибирующую нейротрансмиттерную гамма-аминомасляную кислоту (GABA), возбуждающую аминокислоту глутамат.
Серотонин действует путем связывания различных серотонинергических рецепторов. Они включают 5-HT 1A, 5-HT 1B, 5-HT 1D, 5-HT 1E, 5-HT 1F, 5-HT 2A, 5-HT 2B, 5-HT 2C, 5-HT 3, 5-HT 4, 5-HT 5, 5-HT 6 и 5-HT 7, для которых были найдены агонисты и антагонисты. Рецепторы серотонина 5-HT 1A, 5-HT 1B, 5-HT 1D, 5-HT 1E, 5-HT 1F расположены и пресинаптически, и постсинаптическии и на клетках тела. Нейротрансмиссия серотонина регулируется этими рецепторами и механизмами обратного захвата (Filip et al., Pharmacol. Reports, 2009, 61, 761-777; Ohio, Central Nervous System Agents in Medicinal Chemistry, 2010, 10, 148-157).
Агонисты и антагонисты некоторых серотонинергических рецепторов были изучены с целью применения при лечении некоторых двигательных расстройств. Некоторые агонисты 5-HT 1A серотонина, как было показано, ослабляют экстрапирамидальные побочные эффекты (EPS), связанные с лечением нейролептиками, и улучшают познавательные способности пациентов, страдающих от шизофрении. (Newman-Tancredi: Current Opinion in Investigational Drugs, 2010, 11 (7): 802-812).
Было показано, что регуляторы нейротрансмиссии серотонина (5-HT) улучшают протекание LID или предотвращают возникновение LID. Одним таким примером является саризотан, который представляет собой агонист 5-HT 1A и антагонист дофаминового рецептора (Gregoire et al., Parkinsonism Relat. Disord., 2009, 15(6), 445-52). На стадии 2A открытого исследования и при изучении меченого саризотана последний уменьшал развитие LID. Однако на стадии 2b при проведении нескольких исследований не было обнаружено значительного влияния саризотана по сравнению с плацебо, и полагают, что отсутствие эффекта обусловлено отсутствием эффективности лекарства или усилением симптомов болезни Паркинсона, вызванным антагонистическим действием дофаминовых рецепторов.
Влияние буспирона на течение болезни Паркинсона было изучено при проведении небольшого открытого исследования (Ludwig et al., Clin. Neuropharmacol., 1986, 9(4), 373-378). Было установлено, что дозы (10-60 мг/день), которые обычно применяли для лечения пациентов, страдающих от беспокойства, не оказывали никакого влияния на развитие болезни Паркинсона или дискинезии. При более высоких дозах (100 мг/день) наблюдалось, что буспирон уменьшал развитие дискинезии, но с увеличением показателей потери трудоспособности. Это свидетельствовало о том, что высокие дозы буспирона могли отрицательно влиять на развитие акинезии, связанной с болезнью Паркинсона.
Способы лечения LID при помощи других агонистов 5-HT 1A были также предложены в заявке США на патент №2007/0249621. Кроме того, при проведении исследования было показано, что переспирон, который является агонистом 5-HT 1A, может уменьшать количество непроизвольных движений у пациентов, которые страдают от болезни Хантингтона (Roppongi et al., Prog. Neuropsychopharmacol. Biol. Psychiatry, 2007, 31(1), 308-310).
Недавно было установлено, что комбинация агонистов 5-HT 1A и 5-HT 1B, повышающая эффективность уменьшения развития дискинезии, вызванной применением L-DOPA, может быть получена на животных моделях (см., например, Muňos et al., Brain, 2008, 131 (Pt.12), 3380-94; Muňos et al., Experimental Neurology, 219 (2009), 298-307). Агонисты 5-HT 1B способны тормозить LID по нескольким механизмам. Однако, как было установлено, рецепторы 5-HT 1B находятся в сердце, и было предположено, что модуляторы этих рецепторов могут участвовать в развитии порока сердца и других сердечных болезней, связанных с применением модуляторов серотониновых рецепторов и обратным захватом серотонина (Elangbam et al., J. Histochem. Cytochem., 53, 671-677, 2005).
Комбинированный агонист 5-HT 1A и 5-HT 1B, принимаемый в больших дозах, может привести к развитию серотонинового синдрома или серотониновой токсичности, формы отравления. Синдром или токсичность вызваны увеличенной активацией 5-HT 1A и 5-HT 1B-рецепторов. Серотониновый синдром по определению характеризуется группой симптомов, свидетельствующих о ментальных изменениях, дисфункции автономной нервной системы и нервно-мышечных недомоганиях. Пациенты могут испытывать замешательство, возбуждение, диарею, потливость, дрожь, повышение давления, лихорадочное состояние, могут иметь повышенное содержание белых кровяных телец, испытывать нескоординированность, заметное увеличение рефлексов, мышечные конвульсии, тремор, чрезмерную скованность, судороги и даже могут впасть в кому. Степень таких изменений меняется от умеренной до фатальной. Следовательно, из-за серьезности развития серотонинового синдрома важно поддерживать низкие концентрации агониста 5-HT 1A.
Раскрытие изобретения
Настоящее изобретение относится к применению агонистов 5-HT 1 при лечении двигательных расстройств. Комбинированная активация различных серотонинергических рецепторов может привести к синергическому эффекту, который более эффективно влияет на уровень дофамина в синапсе и ведет к эффективному лечению двигательных расстройств, описанных в данной заявке. Кроме того, поскольку комбинация различных агонистов 5-HT 1, предусмотренная данным изобретением, может обеспечить снижение дозы агониста 5-HT 1A по сравнению с известными способами лечения, данное изобретение может предотвратить или снизить риск развития серотонинового синдрома и неблагоприятных эффектов лечения при помощи агонистов 5-HT 1.
Фармацевтические композиции согласно данному изобретению содержат соединение, которое является или агонистом двух или более рецепторов серотонина, выбранных из группы рецепторов:
- 5-HT 1B,
- 5-HT 1D и
-5-HT 1F,
или селективным агонистом рецептора 5-HT 1D, или селективным агонистом рецептора 5-HT 1F, или фармацевтически приемлемыми их производными, и применяется для лечения, профилактики или облегчения двигательных расстройств.
Фармацевтические композиции согласно данному изобретению могут содержать комбинацию двух или более соединений, при этом по меньшей мере одно из них является а) агонистом рецептора 5-HT 1A и по меньшей мере одно другое соединение б) выбрано из: агониста двух или более рецепторов из группы 5-HT 1B, 5-HT 1D и 5-HT 1F, или селективного агониста рецептора 5-HT 1D, или селективного агониста рецептора 5-HT 1F.
Таким образом, данное изобретение может относиться к эффективному лечению двигательных расстройств при использовании лекарств, которые представляют собой агонисты серотонинового рецептора 5-HT 1A, и лекарств, которые представляют собой или агонисты нескольких серотониновых рецепторов, включая рецепторы 5-HT 1B, 5-HT 1D и 5-HT 1F, или селективные агонисты рецептора 5-HT 1D, или селективные агонисты рецептора 5-HT 1F.
В соответствии с данным изобретением указанное соединение может быть комбинированным агонистом рецептора 5-HT 1B и рецептора 5-HT 1D, или селективным агонистом рецептора 5-HT 1F, или комбинированным агонистом рецептора 5-HT 1B, рецептора 5-HT 1D и рецептора 5-HT 1F, или фармацевтически приемлемым производным всех упомянутых выше агонистов.
Согласно другому варианту данного изобретения указанное соединение представляет собой или комбинированный агонист рецептора 5-HT 1B, рецептора 5-HT 1D и рецептора 5-HT 1F, имеющий более высокую степень сродства и/или эффективность активации рецепторов для рецептора 5-HT 1D, чем для рецептора 5-HT 1B или имеющий более высокую степень сродства и/или эффективность активации рецепторов для рецептора 5-HT 1D, чем для рецепторов 5-HT 1B и 5-HT 1F.
Согласно предпочтительному варианту данного изобретения фармацевтическая композиция содержит соединение, выбранное из группы суматриптана, золмитриптана, ризатриптана, наратриптана, алмотриптана, фроватриптана и элетриптана или их производного.
Согласно другому варианту данного изобретения фармацевтическая композиция содержит соединение, выбранное из группы COL-144 (LY573144), LY334370, LY344864 или их производного.
Согласно одному варианту данного изобретения фармацевтическая композиция содержит агонист 5-HT 1A, выбранный из группы алнемпирона, биноспирона, буспирона, гепирона, ипсапирона, пероспирона, тандоспирона, бефирадола, репинотана, пиклозотана, осемозотана, флесиноксана, флибансерина и саризотана или их производных, при этом особенно предпочтительными являются агонисты 5-HT 1A буспирон и тандоспирон.
Согласно одному из вариантов соединение представляет собой агонист двух или более рецепторов 5-HT 1B, 5-HT 1D и 5-HT 1F или селективный агонист 5-HT 1D, или селективный агонист 5-HT 1F, и это соединение вводится в дозах составляющих 0,05-200 мг/день, предпочтительно в пределах от 0,5 до 60 мг/день и, даже более предпочтительно, в пределах от 0,5 до 10 мг/день.
Согласно предпочтительному варианту данного изобретения агонист 5-HT 1A вводится в дозах от 0,5 мг/день до 100 мг/день, и это соединение представляет собой комбинированный агонист двух или более рецепторов 5-HT 1B, 5-HT 1D и 5-HT 1F или селективный агонист 5-HT 1D, или селективный агонист 5-HT 1F и оно вводится в дозах от 0,1 мг/день до 60 мг/день, еще более предпочтительно, когда агонист 5-HT 1A вводится в дозах от 0,5 мг/день до 30 мг/день и соединение представляет собой комбинированный агонист двух или более рецепторов из 5-HT 1B, 5-HT 1D и 5-HT 1F, или селективный агонист 5-HT 1D, или селективный агонист 5-HT 1F и оно вводится в дозах от 0,5 мг/день до 10 мг/день.
Фармацевтическая композиция согласно данному изобретению может также включать один или более вторых активных агентов.
Фармацевтическая композиция согласно данному изобретению может также включать один или более агентов, выбранных из группы агентов, которые повышают концентрацию дофамина в синаптической щели, дофамина, L-DOPA или агонистов рецепторов дофамина или их производных.
Двигательные расстройства в соответствии с данным изобретением связаны с измененным содержанием синаптического дофамина, например, такие расстройства, которые выбраны из группы акатезии, поздней дискинезии и дискинезии, связанной с болезнью Паркинсона и, в частности, дискинезии, вызванной приемом L-DOPA.
Фармацевтические композиции согласно данному изобретению могут быть получены для парентерального введения или для энтерального введения, такого как оральное введение. Они могут быть также получены для того, чтобы они пересекали гематоэнцефалический барьер.
Данное изобретение предусматривает также соединения, которые представляют собой комбинированный агонист 5-HT 1B, 5-HT 1D и 5-HT 1F, для лечения, профилактики или облегчения проявления двигательных расстройств.
Аспектами настоящего изобретения являются также способы лечения, профилактики или облегчения двигательных расстройств, включающие одну или более стадий введения эффективного количества фармацевтической композиции или соединения, определение которых дано в настоящей заявке.
Согласно предпочтительному варианту такие способы могут также включать стадию одновременного, последовательного или раздельного введения эффективного количества одного или более вторых активных ингредиентов, таких как агонист 5-HT 1A.
Агонисты 5-HT 1A, применяемые при осуществлении способов по изобретению, могут быть выбраны из группы алнеспирона, биноспирона, буспирона, гепирона, ипсапирона, пероспирона, тандоспирона, бефирадола, репинотана, пиклозотана, осемозотана, флесиноксана, флибансерина и саризотана или их производных, при этом предпочтительными являются буспирон и тандоспирон.
Согласно одному из вариантов способа лечения по данному изобретению агонист 5-HT 1A вводится в дозе от 0,05 мг/день до 500 мг/день, при этом предпочтительными являются дозы от 0,5 мг/день до 100 мг/день и еще более предпочтительны дозы от 0,5 мг/день до 30 мг/день.
Способы согласно данному изобретению могут также включать стадии введения одного или более агентов, выбранных из группы агентов, которые повышают концентрацию дофамина в синаптической щели, дофамина, L-DOPA или агонистов рецепторов дофамина или их производных.
Данное изобретение предусматривает также наборы частей, содержащих фармацевтическую композицию или соединение, описанные в данной заявке, которые предназначены для лечения профилактики или ослабления двигательных расстройств путем их одновременного, последовательного или раздельного введения. Такие наборы могут также содержать один или более вторых активных ингредиентов, таких как агонист 5-HT 1A, например, выбранный из группы алнеспирона, биноспирона, буспирона, гепирона, ипсапирона, пероспирона, тандоспирона, бефирадола, репинотана, пиклозотана, осемозотана, флесиноксана, флибансерина и саризотана или их производных (при этом предпочтительными являются буспирон и тандоспирон и их производные) или агент, повышающий концентрацию дофамина в синаптической щели, дофамин, L-DOPA или агонист рецепторов дофамина или их производные.
Данное изобретение предусматривает также способы получения фармацевтической композиции, описанной в данной заявке.
Определения
Термин "ауторецептор", применяемый в данной заявке, представляет собой рецептор, расположенный в пресинаптической нервной клетке, который служит как часть обратной связи в сигнальной трансдукции. Он обладает чувствительностью к тем нейротрансмиттерам или гормонам, которые высвобождаются нейроном, в мембране которого находится ауторецептор, и понижающее регулирует высвобождение нейротрансмиттеров в синапсе.
Термин "гематоэнцефалический барьер" относится к селективным непроницаемым эндотелиальным клеткам в капиллярах ЦНС, которые ограничивают прохождение растворенных веществ в спинномозговую жидкость (CSF).
Термин "агонист", применяемый в данной заявке, относится к веществу, способному к связыванию и активации рецептора. Так, агонист 5-HT 1A-рецептора (агонист 5-HT 1A) способен связывать и активировать рецептор 5-HT 1A. Агонист 5-HT 1B-рецептора (агонист 5-HT 1B) способен связывать и активировать рецептор 5-HT 1B. Агонист 5-HT 1D рецептора (агонист 5-HT 1D) способен связывать и активировать рецептор 5-HT 1D. Агонист 5-HT 1F-рецептора (агонист 5-HT 1F) способен связывать и активировать рецептор 5-HT 1F. Такой агонист может быть агонистом нескольких различных типов рецепторов и, следовательно, он может быть способен связывать и активировать несколько различных типов рецепторов.
Указанный агонист может также быть селективным агонистом, который связывает и активирует только один тип рецептора.
Термин "антагонист", применяемый в данной заявке, относится к веществу, способному ингибировать действие агониста рецептора.
Термины "дофамин", "DA" и "4-(2-аминоэтил)бензил-1,2-диол", применяемые в данной заявке, относятся к нейротрансмиттеру катехоламина и гормона. Дофамин представляет собой предшественник адреналина (эпинефрина) и норадреналина (норэпинефрина) и активирует пять типов рецепторов дофамина - D1, D2, D3, D4 и D5 - и их варианты.
Термин "гетерорецептор", применяемый в данной заявке, представляет собой рецептор, регулирующий синтез и/или высвобождение медиаторов, отличных от его лиганда. Гетерорецепторы являются пресинаптическими рецепторами, которые отвечают на действие нейротрансмиттеров, нейромодуляторов или нейрогормонов, высвободившихся из соседних нейронов или клеток.
Термин "индивидуум", применяемый в данной заявке, относится к человеку, который может получить выгоду от введения соединения или фармацевтической композиции в соответствии с данным изобретением. Такой индивидуум может страдать от двигательного расстройства или же быть в группе риска заболеть этим двигательным расстройством. Индивидуум может представлять собой любого человека, мужчину или женщину, ребенка, человека средних лет или пожилого человека. Двигательное расстройство у индивидуума, которое подвергается лечению или профилактике, может быть связано с возрастом индивидуума независимо от того, страдал он раньше от таких расстройств или болезней, которые могли вызвать двигательные расстройства у этого индивидуума, или нет.
"L-DOPA" или "3,4-дигидроксифенилаланин" является предшественниеком нейротрансмиттеров дофамина, норэпинефрина (норадреналина) и эпинефрина (адреналина). L-DOPA способна проходить через гематоэнцефалический барьер и превращается в дофамин под действием фермента декарбоксилазы ароматических L-аминокислот (AADC), известной также как DOPA-декарбоксилаза (DDC). L-DOPA применяется для лечения болезни Паркинсона.
Термин "нейротрансмиттер", применяемый в данной заявке, обозначает вещество, которое передает сигналы от нейрона к целевой клетке через нейронный синапс.
Термины "болезнь Паркинсона", "паркинсонизм" и "PD", применяемые в данной заявке, относятся к неврологическому синдрому, который характеризуется дефицитом дофамина, возникшим вследствие дегенеративных, сосудистых или воспалительных изменений в базальных ганглиях черного вещества мозга. Этот термин относится также к синдрому, который напоминает болезнь Паркинсона, но который может быть и может не быть вызванным болезнью Паркинсона, например, подобные паркинсонизму побочные эффекты, вызванные приемом некоторых антипсихотических лекарств. Болезнь Паркинсона называется также дрожательным параличом и парезом.
Термин "частичные агонисты", применяемый в данной заявке, обозначает соединения, способные связывать и активировать данный рецептор, но обладающие только частичной эффективностью в отношении рецептора по сравнению с полными агонистами. Частичные агонисты могут действовать как антагонисты при конкурировании с полным агонистом для связывания рецепторов и получения уменьшения сетчатой структуры при активации рецептора по сравнению с действием или активацией, наблюдаемыми в случае одного полного агониста.
Термин "селективные агонисты" в контексте данной заявки относится к соединениям, которые являются селективными и поэтому связывают и активируют только один тип рецептора. Так, селективный агонист 5-HT 1D-рецептора является селективным в отношении только 5-HT 1D-рецептора, а селективный агонист 5-HT 1F-рецептора является селективным в отношении только 5-HT 1F-рецептора.
Термин "синапс" относится к области нейрона, которая позволяет этому нейрону передавать электрический или химический сигнал другой клетке. В синапсе плазматическая мембрана нейрона, передающего сигнал, (пресинаптического нейрона) приходит в тесное соприкосновение с мембраной целевой (постсинаптической) клетки.
Термин "фармацевтически приемлемое производное" в контексте данной заявки относится к фармацевтически приемлемым солям, которые не являются вредными для пациента. Такие соли включают фармацевтически приемлемые соли присоединения оснований или кислот, а также фармацевтически приемлемые соли металлов, соли аммония и соли алкиламмония. Фармацевтически приемлемое производное включает также сложные эфиры и пролекарства или другие предшественники соединения, которые могут биологически метаболизироваться с образованием активного соединения или кристаллических форм соединения.
Термины "серотонин", "5-гидрокситриптамин" и "5-HT", применяемые в данной заявке, относятся к феноламинному трансмиттеру, полученному из триптофана путем гидроксилирования и декарбоксилирования в серотонинергических нейронах центральной нервной системы и энтерохромаффиновых клетках желудочно-кишечного тракта. Серотонин является предшественником мелатонина.
Термин "терминал", применяемый в данной заявке, относится к терминалу нейрона.
Термин "терапевтически эффективное количество" соединения, применяемый в данной заявке, относится к количеству, являющемуся достаточным для лечения, профилактики, уменьшения риска или частичной остановки клинических проявлений данного заболевания или расстройства и осложнений после них. Количество, адекватное для выполнения этой задачи называется "терапевтически эффективным количеством".
Термины "лечение", "терапия", применяемые в данной заявке, относятся к медицинской помощи и лечению пациента при борьбе с патологическим состоянием, болезнью или расстройством. Эти термины включают полный спектр медицинских мер для данного состояния, от которого страдает пациент, например, введение активного соединения с целью: облегчения или ослабления симптомов или осложнений; задержки развития патологического состояния, болезни или расстройства; излечения или исчезновения патологического состояния, болезни или расстройства; и/или профилактики патологического состояния, болезни или расстройства; при этом термины "профилактика" или "предотвращение" относятся к медицинской помощи и лечению пациента с целью препятствия развития патологического состояния, болезни или расстройства и они включают введение активного соединения для предотвращения или уменьшения риска начала появления симптомов или осложнений. Пациент, который подвергается лечению, предпочтительно является млекопитающим, в частности, человеком. Однако лечение животных, таких как мыши, крысы, собаки, кошки, коровы, овцы и свиньи, также входит в объем данного изобретения. Пациенты, которые подвергаются лечению согласно данному изобретению, могут быть разного возраста.
Термин "триптан" в контексте данной заявки обозначает соединение, являющееся членом семейства лекарств на основе триптаминов, используемых как абортивные средства при лечении мигреней и сильных приступообразных головных болей. Триптаны представляют собой агонисты серотониновых рецепторов 5-HT 1B, 5-HT 1D, 5-HT 1E и/или 5-HT 1F и могут быть или не быть селективными агонистами одного или более серотониновых рецепторов 5-HT 1B, 5-HT 1D, 5-HT 1E и/или 5-HT 1F.
Описание фигур
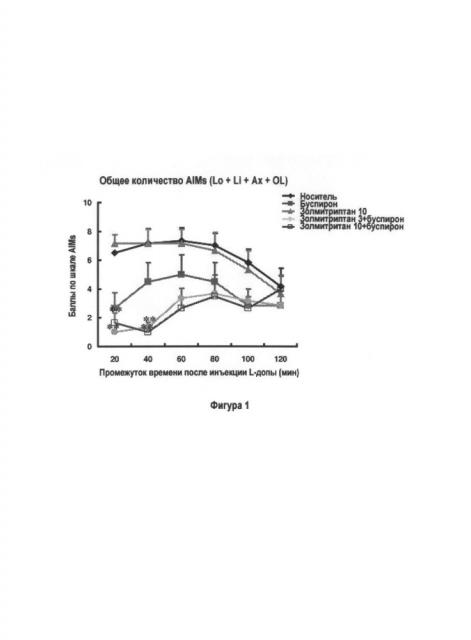
Фигура 1: Действие комбинации буспирона и золмитриптана на развитие аномальных непроизвольных движений, вызванных приемом L-DOPA (AIMs) у крыс. (Общее количество AIMs = сумме локомотивных движений (LO) или осевых (AX) перемещений, движений конечностей (LI) и оральных (OL) движений по шкале AIMs). Звездочки (**) обозначают результаты при показателе P (достоверности различий между показателями контрольных крыс (носитель) и опытных крыс) <0,01 по данным метода однофакторного дисперсионного анализа (ANOVA) и теста Тьюки по полученным результатам в каждый момент времени. Ромбики обозначают крыс, которым вводили только носитель, зачерненные квадратики обозначают крыс, которым вводили 1 мг/кг/день буспирона, треугольники - крыс, которым вводили 10 мг/кг/день золмитриптана, зачерненные кружочки - крыс, которым вводили 3 мг/кг/день золмитриптана в комбинации с 1 мг/кг/день буспирона и белые квадратики - крыс, которым вводили 10 мг/кг/день золмитриптана в комбинации с 1 мг/кг/день буспирона. Результаты показывают, что комбинированное применение буспирона (агонист 5-HT 1A) и золмитриптана (комбинированный агонист 5-HT 1B/5-HT 1D рецепторов, который имеет большую степень сродства и/или эффективности активации рецепторов 5-HT 1D по сравнению с рецепторами 5-HT 1B) может снижать AIM более значительно по сравнению с применением буспирона или золмитриптана в отдельности.
Фигура 2: Влияние золмитриптана (3 мг/кг) и буспирона (1 мг/кг) на координацию крыс Sprague-Dawley (SD) во время проведения теста на вращающемся стержне. Звездочки (**) обозначают результаты при показателе P<0,01 по данным метода однофакторного дисперсионного анализа (ANOVA) и теста Тьюки по полученным результатам в каждый момент времени. Первая колонка слева показывает результаты для крыс, которым вводили только носитель, средняя колонка - для крыс, которым вводили пентобарбитал и последняя колонка слева - для крыс, которым вводили комбинацию золмитриптана (3 мг/кг) и буспирона (1 мг/кг). Результаты показывают, что комбинация золмитриптана (3 мг/кг) и буспирона (1 мг/кг) не вызывает значительного седативного эффекта.
Фигура 3: Влияние золмитриптана (3 мг/кг) и буспирона (1 мг/кг) на общую длину перемещения крыс, не подвергнутых воздействию, при проведении теста "открытое поле". Звездочки (**) обозначают результаты при показателе P<0,01 по данным метода однофакторного дисперсионного анализа (ANOVA) и теста Тьюки по полученным результатам в каждый момент времени. Первая колонка слева показывает результаты для крыс, которым вводили только носитель, средняя колонка - для крыс, которым вводили пентобарбитал и последняя колонка слева - для крыс, которым вводили комбинацию золмитриптана (3 мг/кг) и буспирона (1 мг/кг). Результаты показывают, что комбинация золмитриптана (3 мг/кг) и буспирона (1 мг/кг) не вызывает значительного седативного эффекта.
Фигура 4: Действие комбинации буспирона и золмитриптана на развитие аномальных непроизвольных движений, вызванных приемом L-DOPA (AIMs) у крыс.(Общее количество AIMs = сумме локомотивных движений (LO) или осевых (AX) перемещений, движений конечностей (LI) и оральных (OL) движений по шкале AIMs). Звездочки (**) обозначают результаты при показателе P<0,01 по данным метода однофакторного дисперсионного анализа (ANOVA) и теста Тьюки по полученным результатам в каждый момент времени. Золмитриптан вводили за 35 мин до L-DOPA, а буспирон давали за 30 мин до L-DOPA. Ромбики обозначают крыс, которым вводили только носитель, зачерненные квадратики обозначают крыс, которым вводили 0,5 мг/кг буспирона, треугольники - крыс, которым вводили 3 мг/кг золмитриптана в комбинации с 0,5 мг/кг буспирона, зачерненные кружочки - крыс, которым вводили 10 мг/кг золмитриптана в комбинации с 0,5 мг/кг буспирона и белые квадратики - крыс, которым вводили 10 мг/кг/день золмитриптана в комбинации с 1 мг/кг/день буспирона. Кривые показывают разные результаты лечения: буспирон (0,5 мг/кг); буспирон (0,5 мг/кг) + золмитриптан (3 мг/кг); буспирон (0,5 мг/кг) + золмитриптан (10 мг/кг) и буспирон (1 мг/кг) + золмитриптан (10 мг/кг).
Подробное описание изобретения
Данное изобретение относится к применению комбинаций соединений, которые способны модулировать нейротрансмиссию дофамина при помощи активации серотониновых рецепторов. Более конкретно, данное изобретение относится к комбинациям соединений, которые действуют как агонисты серотонинового 5-HT 1A-рецептора и соединений, которые являются агонистами нескольких серотониновых рецепторов, включая рецепторы 5-HT 1B, 5-HT 1D и 5-HT 1F.
5-HT 1-рецепторы
Серотонин или 5-гидрокситриптамин (5-HT) представляет собой нейротрансмиттер, который выполняет важные функции в центральной нервной системе людей и животных. Было установлено, что серотонин регулирует настроение, аппетит, мышечные сокращения и некоторые познавательные функции, включая память и обучаемость. Серотонин действует путем связывания с различными серотонинергическими рецепторами, известными также как 5-HT-рецепторы. Они представляют собой группу рецепторов, сопряженных с G-белком (GPCRs) лигандзависимых ионных каналов (LGICs), обнаруженных в центральной и периферической нервных системах. 5-HT-рецепторы включают рецепторы 5-HT 1A, 5-HT-1B, 5-HT 1D, 5-HT 1E и 5-HT 1F, 5-HT 2A, 5-HT 2B, 5-HT 2C, 5-HT 3, 5-HT 4, 5-HT 5, 5-HT 6, 5-HT 7, для которых были найдены как агонисты, так и антагонисты.
5-HT 1-рецепторы составляют подсемейство 5-HT-рецепторов, включая 5-HT 1A, 5-HT-1B, 5-HT 1D, 5-HT 1E и 5-HT 1F, которые являются рецепторами, сопряженными с G-белком (GPCRs), которые осуществляют опосредование ингибиторной нейротрансмиссии. Они расположены на постсинаптической мембране, пресинаптической мембране или на клетках нейронов в кортексе, гиппокампе, перегородке, в миндалине, в ядре шва, базальных ганглиях и в таламусе. Благодаря их ингибиторной роли в нейротрансмиссии 5-HT 1-рецепторы играют важную роль в регулировании высвобождения дофамина.
5-HT 1A-рецепторы широко распределены в ЦНС. В основном они расположены в гиппокампе, в извитом конце энторинального кортекса, в боковой перегородке и в ядрах швов мезэнцефальной области. 5-HT 1A-рецепторы принимают участие в двигательном поведении, в действиях, завершающихся половой деятельностью, в эмоциональном поведении и в познавательных процессах. 5-HT 1A-рецепторы являются ауторецепторами в ядрах шва, где они расположены в клеточных телах или дендритах 5-HT нейронов или они являются постсинаптическими рецепторами. В общем, активация 5-HT 1A-рецепторов снижает высвобождение нейротрансмиттеров, таких как 5-HT, и возбуждающей аминокислоты глутамата, что далее приводит к изменениям в высвобождении дофамина.
Рецептор 5-HT 1B высокоэкспрессирован в базальных ганглиях и во фронтальном кортексе. Они функционируют как ауторецепторы на терминалах 5-HT нейронов, ингибируя высвобождение 5-HT, или как терминальные гетерорецепторы к гамма-аминомасляной кислоте, ацетилхолину (Ach) и глутамату на нейронах, где они регулируют высвобождение этих нейротрансмиттеров.
Рецептор 5-HT 1D присутствует в центральной нервной системе как пресинаптический, так и постсинаптический. Самая высокая экспрессия 5-HT 1D-рецептора в мозге крыс была обнаружена в базальных ганглиях (особенно в черной субстанции мозга, в бледном шаре и в дорсальном стриатуме), в гиппокампе и кортексе, в то время как в мозге человека она наблюдалась в базальных ганглиях (в черной субстанции мозга, в бледном шаре), в