Способ прогнозирования развития аллергического ринита
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к иммунологии, и может быть использовано для прогнозирования развития аллергического ринита. Для этого проводят оценку экспрессии генов дифференцировочных факторов субпопуляций Т-хелперов: Tbet, GATA3, RORC. Рассчитывают величину 2-ΔΔCt по формуле: , где 2-ΔΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой фракции мононуклеаров, Ctк - номер порогового цикла в контроле, Cto - номер порогового цикла в опыте, В2М - ген β2-микроглобулина, Х - исследуемый ген, при значениях для Tbet, равных 2,56 и ниже, для GATA3, равных 8,92 и более, для RORC, равных 3,72 и более, прогнозируют развитие аллергического ринита. Использование данного способа позволяет прогнозировать развитие аллергического ринита под влияниям компонентов вредных производственных факторов и природных пыльцевых аллергенов. 1 ил., 4 табл., 5 пр.
Реферат
На сегодняшний день аллергическими заболеваниями в той или иной степени страдают до 20% населения планеты. Общее число пациентов с аллергическими заболеваниями по РФ составляет примерно 20 млн человек, в том числе с пыльцевой аллергией - 8 млн человек [1]. В промышленно-развитых странах все более важным фактором, влияющим на развитие аллергий, становится загрязнение окружающей среды. Но речь идет не об аллергических реакциях на загрязнение как таковое, а о том, что загрязнение усиливает аллергическую реакцию, вызываемую пыльцой растений [2]. О биохимических механизмах этой взаимосвязи мы практически ничего не знаем. Решение именно этой проблемы представляется нам одной из самых важных задач, поскольку оно позволит в будущем выработать более эффективные меры профилактики.
Отмечено, что в крупных городах поллинозы встречаются в 6 раз чаще, чем в сельской местности [2, 3]. Это напрямую коррелирует с уровнем загрязнения атмосферного воздуха. Под влиянием вредных факторов химической природы происходит своеобразная перестройка слизистой оболочки бронхов (замещение клеток реснитчатого эпителия бокаловидными клетками, гипертрофия слизистых желез). Продукция слизи увеличивается, а ее свойства (вязкость, эластичность, антимикробная активность) нарушаются. Длительная гиперфункция приводит к истощению мукоцилиарного аппарата бронхов, дистрофии и атрофии эпителия. Нарушение дренажной функции бронхов приводит к задержке секрета, что способствует развитию вторичной, периодически обостряющейся инфекции, основными возбудителями которой являются пневмококк и гемофильная палочка [4, 5, 6, 7].
На слизистые оболочки соли тяжелых металлов оказывают выраженное местное действие. В зависимости от ряда условий местное действие этих веществ может быть вяжущим, раздражающим или прижигающим [7, 8, 9, 10].
Механизм местного действия солей тяжелых металлов обусловлен их способностью взаимодействовать с белками тканей. В результате такого взаимодействия белки свертываются и образуют с ионами металлов альбуминаты (соединения типа белковых солей металлов). При этом, если происходит частичное свертывание белков, только в самых поверхностных слоях тканей, наблюдается вяжущий или раздражающий эффект, имеющий обратимый характер. В случае свертывания белков, охватывающего значительную массу тканевых клеток и вызывающего их гибель, возникает прижигающий эффект, при котором происходят необратимые изменения тканей в виде некроза. По силе местного действия тяжелые металлы могут быть расположены в следующем порядке: Hg, Ag, Fe, Cu, Zn, Bi, Pb, где наиболее активными являются ионы ртути, а наименее активными - ионы свинца.
Ведущим патогенетическим механизмом при поражении слизистых оболочек полости рта солями тяжелых металлов является отложение их в слизистой, но не исключаются и другие механизмы (аллергизация, биотропизм).
Оксиды серы SO2, SO3, азота NO, NO2, монооксид углерода СО - «кислые» газы со специфическим, относительно однотипным характером влияния на органы дыхания. Вследствие образования слабых кислот при соприкосновении со слизистыми оболочками дыхательных путей они раздражают и прижигают слизистые, вызывая тем самым начальные морфологические повреждения эпителия и угнетение местного иммунитета [7, 8, 9, 10].
Оксиды, прежде всего диоксид серы, адсорбируются на твердых взвешенных частицах, глубина проникновения которых в организм зависит от их размеров: чем мельче частицы, тем больше их поступает в бронхи и альвеолы. Раздражение сопровождается выбросом гистаминов, что может приводить к бронхоспазмам, а в дальнейшем - к формированию астмоидного бронхита и бронхиальной астмы [11, 12].
Ближайшим аналогом изобретения является определение изменения экспрессии генов транскрипционных факторов под влиянием аллергенов у здоровых доноров и больных риноконъюктивитом (Никонова М.Ф. и др. Влияние препаратов аллергенов из пыльцы растений на экспрессию генов транскрипционных факторов, контролирующих дифференцировку Т-хелперов, в культуре лимфоцитов здоровых доноров и больных аллергическим риноконъюктивитом // Иммунология, 2012, №1, стр. 45-48).
Однако в данной работе отсутствуют критерии диагностики аллергического ринита при оценке сочетанного влияния компонентов вредных производственных факторов и природных пыльцевых аллергенов.
Поэтому задачей изобретения была разработка способа оценки сочетанного влияния компонентов вредных производственных факторов и природных пыльцевых аллергенов для возможного прогнозирования развития аллергического ринита у жителей регионов с неблагоприятной экологической обстановкой.
Для прогнозирования развития аллергического ринита оценивали экспрессию генов дифференцировочных факторов субпопуляций Т-хелперов: Tbet, GATA3, RORC, включающий расчет величины 2-ΔΔCt по формуле:
,
где 2-ΔΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой фракции
мононуклеаров, Ctк - номер порогового цикла в контроле, Cto - номер порогового цикла в опыте, В2М - ген β2-микроглобулина, X - исследуемый ген,
и при значениях для Tbet, равных 2,56 и ниже, для GATA3, равных 8,92 и более, для RORC, равных 3,72 и более, прогнозируют развитие аллергического ринита.
Техническим результатом предлагаемого способа является выявление группы пациентов с предрасположенностью к развитию аллергического ринита под сочетанным влиянием компонентов вредных производственных факторов и природных пыльцевых аллергенов путем оценки экспрессии генов дифференцировочных факторов субпопуляций Т-хелперов: Tbet, GATA3, RORC, рассчитывая величину 2-ΔΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой клеточной популяции, отражая не только уровень экспрессии гена каждой клеткой, но долю клеток, экспрессирующих ген, чтобы интегрально оценить преимущественное направление дифференцировки CD4+ Т-клеток и «ориентацию» иммунных процессов.
Краткое описание чертежей.
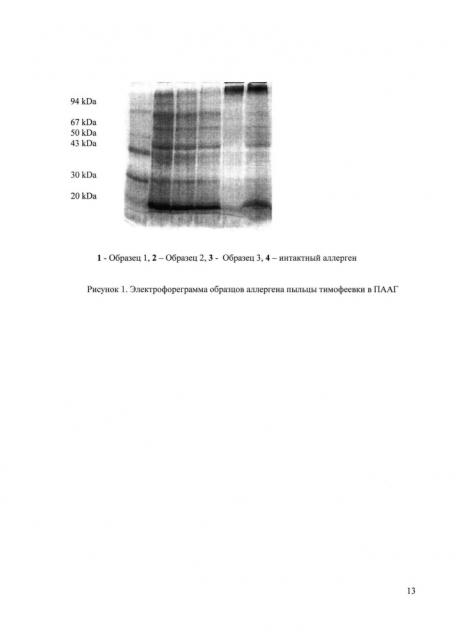
Рисунок 1. Электрофореграмма образцов аллергена пыльцы тимофеевки в ПААГ
ИЗОБРЕТЕНИЕ ИЛЛЮСТРИРУЮТ ПРИМЕРЫ.
Пример 1. Получение модельных аллергенов из пыльцы тимофеевки, содержащих тяжелые металлы.
Из пыльцы тимофеевки выделяли аллергены, методом водно-солевой экстракции бикарбонатом аммония. Количество белка в выделенном препарате составило 35,5% на 1 мг общей массы. Готовили аликвоты по 100 мг и добавляли водный раствор нитрата свинца. Затем образцы подвергали лиофильному высушиванию. Итоговые концентрации свинца в образцах аллергена составили 10,0 (образец 1), 25,0 (образец 2) и 50,0 (образец 3) мг/кг, что соответствует высокой степени загрязнения пыльцы выхлопными газами.
Вертикальный электрофорез проводили в градиентном полиакриламидном геле (3-15%). Мажорные аллергены тимофеевки Phl1 (связывает 80% специфического IgE) и Phl4 (связывает 70% специфического IgE) определяются в диапазоне 30-35 и 56-58 кДа соответственно. При проведении вертикального электрофореза в ПААГ во всех трех препаратах, выделенных из пыльцы тимофеевки, определили 15 белковых фракций в диапазоне молекулярных масс от 14 до 60 кДа. Различий по белковому составу аллергенов не прослеживалось, полосы на геле были идентичны (рисунок 1).
Для проведения иммуноблоттинга использовали пулированные положительные сыворотки, протестированные на содержание соответствующего специфического IgE в системе ImmunoCAP (Pharmacia). Аллергены из пыльцы тимофеевки разделяли в вертикальном электрофорезе в ПААГ, переносили на нитроцеллюлозную мембрану и разделяли на стрипы, совпадающие с дорожками пробега белков. Далее стрипы помещали в емкости с соответствующими контрольными сыворотками и инкубировали. Следующую инкубацию проводили с МАТ и затем проявляли реакцию ДАБ. На стрипах каждого из трех препаратов аллергенов, инкубированных с сывороткой, содержащей специфический IgE против аллергенов тимофеевки, проявилось выраженное окрашивание в виде широкой полосы в зоне молекулярных масс 56-60 кДа.
В иммуноблоттинге не наблюдалось достоверных различий между тремя исследуемыми образцами. Полосы окрашивания на нитроцеллюлозной мембране были идентичны. Даже 50-кратное превышение нормы по содержанию свинца не изменило иммунохимические свойства аллергена пыльцы тимофеевки. Это согласуется с полученными ранее результатами для пыльцы березы повислой.
Главными критериями качества любых иммунобиологических препаратов является их подлинность и специфическая активность.
Подлинность препарата определяется по способности взаимодействовать со специфическим к нему IgG из сывороток крови больных аллергическими заболеваниями, вызванными пыльцой тимофеевки. В качестве положительных контролей использовали пулированные сыворотки с высоким содержанием специфических IgG антител. Сыворотки для них, содержащие не менее 10 mgA/l, были отобраны, с использованием коммерческих флюороиммуноферментных наборов, на приборе ImmunoCAP (Pharmacia biotech). Результаты определения подлинности для образцов модельных аллергена представлены в таблице 1.
Видно, что оптические плотности интактного и модельных аллергенов очень близки, различие недостоверно (р>0,05). Таким образом, показана подлинность полученных нами модельных аллергенов пыльцы тимофеевки. Добавление свинца не повлияло на IgG-связывание образцов.
Определение специфической активности модельных аллергенов из пыльцы тимофеевки оценивали по способности связывать специфический IgE контрольного образца. Контроль неспецифического связывания в реакции - нулевая сыворотка, не содержащая IgE-антител. В качестве положительного контроля использовали пулированную сыворотку с высоким содержанием специфических IgE антител. Сыворотки для нее, содержащие не менее 85 kUA/l, были отобраны с использованием коммерческих флюороиммуноферметных наборов, на приборе ImmunoCAP (Pharmacia biotech). Результаты определения специфической активности представлены в таблице 2.
Из таблицы видно, что образцы полученных модельных аллергенов обладают специфической активностью, различие с контролем недостоверно (р>0,05).
Присутствие свинца в составе аллергена не изменило его иммунохимические свойства.
Полученные образцы могут быть использованы для изучения влияния модельных аллергенов на факторы пролиферации лимфоидных клеток здоровых доноров и больных аллергией.
Пример 2. Получение мононуклеаров из периферической крови.
Методика основана на определении спектра генов транскрипционных факторов Т-клеток (ТВХ21, GATA3, RORC и FOXP3), экспрессируемых покоящимися и активированными Т-клетками (в составе фракции мононуклеаров) in vitro, с помощью полимеразной цепной реакции в реальном времени с предварительной обратной транскрипцией (ОТ-ПЦР).
Забор периферической крови в количестве 0,5 мл проводят в стерильные пробирки для крови BD Vacutainer с объемом вакуума 2-4 мл, содержащие антикоагулянт (K3EDTA в концентрации 2 мг/мл).
Разделение клеточных элементов крови проводят путем центрифугирования в одноступенчатом градиенте плотности фиколла-верографина (плотность 1,077 г/мл) по методу Boyum А. Принцип метода основан на различии в плавучей плотности форменных элементов крови. Кровь, разведенную физиологическим раствором в соотношении 1:1, наслаивают на 0,5 мл фиколла-верографина. После центрифугирования при 18°C в течение 20 мин при 400g интерфазное кольцо мононуклеаров собирают в пробирки «Эппендорф» и дважды отмывают физиологическим раствором. Количество клеток подсчитывают в камере Горяева. Жизнеспособность клеток после выделения должна быть выше 95% (методом исключения 0,1% трипанового синего).
Для активации выделенные мононуклеары ресуспендируют в полной питательной среде RPMI 1640, содержащей 25 мМ HEPES (Sigma), 2 мМ L-глутамина (Sigma) и 10% эмбриональной телячьей сыворотки (Sigma), в концентрации 2 млн/мл. Клетки культивируют в полной питательной среде в количестве 5⋅105/лунку в 24-луночных планшетах (Nunc) в присутствии аллергена в течение 4 часов. Аллерген добавляют к клеткам для получения концентраций 100 нг/мл и 10 нг/мл в пересчете на содержание белка в выделенном препарате.
Затем клетки из лунок переносят в пробирки «Эппендорф» и дважды отмывают физиологическим раствором. Осадок клеток в 50 мкл физиологического раствора используют для выделения РНК.
Пример 3. Выделение РНК из МНПК.
Для выделения нуклеиновых кислот используют наборы «Проба НК» («ДНК-Технология»). Метод основан на лизисе образцов в 4М растворе гуанидинтиоцианата, осаждении нуклеиновых кислот изопропанолом с последующими отмывками этанолом и ацетоном.
Клетки (5⋅105) в 50 мкл физиологического раствора встряхивают на вортексе в течение 3-5 сек. В пробирки «Эппендорф» с клетками добавляют 150 мкл лизирующего раствора, не касаясь края пробирки. Пробирки «Эппендорф» закрывают крышками и снова встряхивают на вортексе в течение 3-5 сек с дальнейшей инкубацией в течение 15 мин при 65°C. После инкубирования необходимо осадить конденсат центрифугированием при 13000 об/мин в течение 30 сек.
В пробирки «Эппендорф» с клетками и лизирующим раствором добавляют 200 мкл реагента для преципитации. Полученную смесь встряхивают на вортексе в течение 3-5 сек и центрифугируют при 13000 об/мин в течение 15 мин. Из каждой пробирки удаляют надосадок с помощью индивидуального наконечника.
К осадку клеток добавляют 250 мкл промывочного раствора. Пробирку с клетками в промывочном растворе следует 3-5 раз аккуратно перевернуть и затем центрифугировать при 13000 об/мин в течение 5 мин. Надосадок удаляют индивидуальным наконечником. К полученному осадку добавляют 150 мкл промывочного раствора. Пробирку с клетками в промывочном растворе аккуратно переворачивают 3-5 раз и центрифугируют при 13000 об/мин в течение 5 мин. Надосадок также удаляют индивидуальным наконечником. Крышки пробирок «Эппендорф» следует открыть и высушить осадок в течение 5 мин при 65°C.
К осадку добавляют 25 мкл буфера для растворения, в котором его встряхивают на вортексе в течение 3-5 сек с последующим осаждением конденсата центрифугированием в течение 3-5 сек. Пробирки прогревают при 65°C в течение 15 мин с дальнейшим осаждением конденсата центрифугированием при 13000 об/мин в течение 30 сек.
Полученный препарат РНК рекомендуют сразу использовать для постановки реакции обратной транскрипции.
Пример 4. Постановка ПЦР «в реальном времени» с предварительной обратной транскрипцией
С помощью полимеразной цепной реакции «в реальном времени» с обратной транскрипцией определяют экспрессию мРНК GATA3, ТВХ21, RORC и FOXP3. Результаты оценивают относительно уровня экспрессии гена «домашнего хозяйства» β2-микроглобулина (В2М).
Для проведения реакции обратной транскрипции и ПЦР используют TaqMan One-Step RT-PCR Master Mix Reagents Kit («Applied Biosystems»).
Для каждого транскрипционного фактора готовят ПЦР-смесь (без добавления РНК) в отдельной пробирке «Эппендорф», (5 пробирок для определения экспрессии генов: 1) GATA3, 2) ТВХ21, 3) RORC, 4) FOXP3, 5) В2М), ПЦР-смесь готовят с учетом внутреннего контрольного (ВК - смесь нуклеиновых кислот, выделенной из клеток 20 доноров) и отрицательного контрольного образца (проба без добавления РНК).
ПЦР-смесь в объеме 24 мкл вносят в пробирки для ПЦР (стрипы на 0,2 мл). В каждую пробу добавляют по 1 мкл РНК. Стрипы закрывают крышками и помещают в детектирующий амплификатор "7300 Real-Time PCR System" («Applied Biosystems»).
Для расчета относительных количеств исследуемых нуклеиновых кислот использовали сравнительный метод (метод «ΔCt»). Уровень экспрессии мРНК исследуемых генов определяли относительно экспрессии мРНК гена «домашнего хозяйства» β2-микроглобулина (В2М, «Applied Biosystems») по формуле:
,
где 2-ΔΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой фракции мононуклеаров, Ctк - номер порогового цикла в контроле, Cto - номер порогового цикла в опыте, В2М - ген β2-микроглобулина, X - исследуемый ген.
Статистическую обработку результатов исследования проводили с использованием методов непараметрического анализа. Исследованные количественные показатели представляли в виде Me (L-H), где Me - медиана, L - нижний квартиль, Н - верхний квартиль. Для сопоставления двух групп по количественным признакам использован U-критерий Манна-Уитни. Для выявления взаимосвязи переменных проводили расчет коэффициента ранговой корреляции по Спирмену. Различие групп полагали статистически значимым при Р<0,05.
Обработку проводили в программном пакете StatSoft Statistica.
Пример 5. Изучение влияния модельных аллергенов на факторы пролиферации лимфоидных клеток здоровых доноров и больных аллергией.
Периферическую кровь от здоровых и больных аллергическим ринитом людей (10 человек) обоего пола в возрасте 25-55 лет забирали в стерильные пробирки для крови, содержащие К3ЭДТА в качестве антикоагулянта. Разделение клеточных элементов крови проводили путем центрифугирования в одноступенчатом градиенте плотности фиколла-верографина (плотность 1,077 г/мл) по методу Boyum А.
Было изучено влияние модельных аллергенов пыльцы тимофеевки, содержащих свинец, на синтез транскрипционых факторов, ответственных за дифференцировку соответствующих форм Т-лимфоцитов. В настоящее время установлены транскрипционные факторы, специфически контролирующие развитие четырех вариантов (субпопуляций) CD4+ Т-клеток: развитие Th1 - клеток обеспечивается фактором T-bet, Th2-клеток - фактором GATA-3, Th17-клеток - фактором RORc, Трег - фактором FOXP3. Синтез клеткой названных факторов обусловливается экспрессией генов, которые их кодируют - соответственно ТВХ21, GATA3, RORC и FOXP3. Избирательная экспрессия этих генов зависит от внутриклеточных факторов, индуцируемых микроокружением клеток, прежде всего цитокинами. В конечном счете можно утверждать, что экспрессия гена того или иного фактора и его синтез клеткой предопределяет направление дифференцировки CD4+ Т-клетки, а преобладающее направление дифференцировки этих клеток обусловливает развитие той или иной формы иммунного ответа, т.е. состояние готовности к определенным формам иммунного ответа.
Поскольку в условиях дисбаланса субпопуляций CD4+ Т-клеток возникает риск развития различных форм иммунопатологии, спектр экспрессируемых транскрипционных факторов данной группы предопределяет склонность данного организма к развитию различных видов иммунологических нарушений. Так известно, что несбалансированное преобладание дифференцировки Th2-клеток под влиянием преимущественной экспрессии фактора GATA-3 обусловливает предрасположенность к аллергии, преобладание экспрессии факторов, способствующих дифференцировке Th17 и Th1-клеток, повышает риск развития различных форм аутоиммунных процессов, а чрезмерная экспрессия FOXP3 способствует развитию иммунодефицитных состояний.
Присутствие свинца в составе аллергена несколько изменяет ее способность влиять на экспрессию генов транскрипционных факторов CD4+ Т-клеток. Существенно влияние свинца проявляется при введении в культуру аллергена в концентрации 100 нг/мл. Исследования проведены на клетках, выделенных от 10 здоровых доноров. Основных эффектов было два:
- ослабление усиливающего действия аллергена на экспрессию гена ТВХ21, кодирующего фактор T-bet, который отвечает за дифференцировку Th1-клеток;
- усиление экспрессии гена RORC, кодирующего фактор RORc, который отвечает за дифференцировку Th17-клеток.
Результаты исследования представлены в Таблице 3.
У больных аллергическим ринитом показатели экспрессии транскрипционных факторов изменяются при воздействии модельных аллергенов аналогично (Таблица 4).
Основной эффект свинца сводился к влиянию на соотношение факторов, определяющих дифференцировку Т-хелперов Th1 (снижаются) и Th17 (возрастают). Преобладание дифференцировки Th17-клеток, как известно, чревато развитием аутоиммунных процессов, ослабление дифференцировки Th1-клеток - ослаблением защиты против внутриклеточных патогенов, и возможным запуском по принципу обратной связи, Т-хелперов Th2, что может привести к запуску аллергопатологии. Следует отметить, что у лиц с аллергопатологией усилена экспрессия проаллергического гена GATA3.
У больных аллергическим ринитом показатели экспрессии транскрипционных факторов изменяются при воздействии модельных аллергенов: при значениях для Tbet, равных 2,56 и ниже, для GATA3, равных 8,92 и более, для RORC, равных 3,72, что является критерием прогноза развития аллергического риноконъюктивита.
Таким образом, способ позволяет выявить группу пациентов с предрасположенностью к развитию аллергического ринита под сочетанным влиянием компонентов вредных производственных факторов путем оценки экспрессии генов дифференцировочных факторов субпопуляций Т-хелперов: Tbet, GATA3, RORC, рассчитывая величину 2-ΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой клеточной популяции, отражая не только уровень экспрессии гена каждой клеткой, но долю клеток, экспрессирующих ген, чтобы интегрально оценить преимущественное направление дифференцировки CD4+ Т-клеток и «ориентацию» иммунных процессов и, как результат, позволяет определить схему коррекции нарушений.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Ильина Н.И. Статистические сведения об аллергических заболеваниях и заболеваниях иммунной системы в России. Аллергология и иммунология: национальное руководство. Под ред. P.M. Хаитова, Н.И. Ильиной, М., «ГЭОТАР-Медиа», 2009, С. 656.
2. Бессонова В.П. Состояние пыльцы как показатель загрязнения среды тяжелыми металлами. // Экология. 1992. №4. С. 45-50.
3. Тарасова Н.Е., Башкиров А.А. Распространенность аллергических заболеваний и зависимость их динамики от социально-экономических факторов. Вестн. Росс. Ун-та дружбы народов. Сер. Экол. и безопас. жизнед., 2003, №9, С. 139-143.
4. Федоскова Т.Г., Ильина Н.И. Роль аллергических заболеваний в общеклинической практике, Рус. мед. ж., 2004, т. 12, №14, С. 876-885.
5. Лютина Е.И., Манеров Ф.К. К вопросу об эпидемиологии аллергических заболеваний, Аллергология, 2004, №4, С. 55-57.
6. Хаитов P.M., Ильина Н.И., Курбачева О.М., Павлова К.С. Традиции, достижения и инновации в современной аллергологии, Физиология и патология иммунной системы, 2010, т. 14, №1, С. 3-14.
7. Дуева Л.А., Коган В.Ю., Суворов С.В., Штеренгарц Р.Я.. Промышленные аллергены. М. Госкомприрода СССР. 1989, 203 с.
8. Хаитов P.M., Ильина Н.И., Лусс Л.В. // Значение научно-исследовательских работ в области иммунологии и аллергологии в общей оценке состояния здоровья персонала предприятий, обслуживаемых ФМБА России, и в проведении лечебно-профилактических мероприятий. // Медицина экстремальных ситуаций. 2007, №1 (19), с. 82-91.
9. Орадовская И.В., Лейко И.А., Феоктистов В.В. и соавторы // Мониторинг иммунного статуса лиц, занятых на производстве с техногенно-агрессивной средой, и населения. Российский алллергологический журнал, 2009, №55, с. 18-28.
10. Рембовский В.Р., Филатов Б.Н. // Научное медико-гигиеническое сопровождение работ по уничтожению химического оружия в России. Медицина экстремальных ситуаций. №3 (21), 2007, с. 92-103.
11. Клиническая иммунология. Руководство для врачей. Под. ред. Е.И. Соколова. М., Медицина. 1998, 270 с.
12. Маркова Т.П., Чувиров Т.Н. // Классификация вторичных иммунодефицитов. Практическое пособие по клинической иммунологии и аллергологии под ред. Р.М. Хаитова. М., Торус Пресс.2005, с. 11-30.
Способ прогнозирования развития аллергического ринита методом оценки экспрессии генов дифференцировочных факторов субпопуляций Т-хелперов: Tbet, GATA3, RORC, включающий расчет величины 2-ΔΔCt по формуле:
,
где 2-ΔΔCt - суммарный уровень экспрессии соответствующих генов в изучаемой фракции мононуклеаров, Ctк - номер порогового цикла в контроле, Cto - номер порогового цикла в опыте, В2М - ген β2-микроглобулина, Х - исследуемый ген,
и при значениях для Tbet, равных 2,56 и ниже, для GATA3, равных 8,92 и более, для RORC, равных 3,72 и более, прогнозируют развитие аллергического ринита.