Устройство для назальной доставки лекарственных средств
Иллюстрации
Показать всеГруппа изобретений относится к медицине и медицинской технике и может быть использована для доставки композиции в обонятельную область назальной полости. Предложено устройство, содержащее контейнер, диффузор, камеру для композиции и сопло. При этом контейнер вмещает пропеллент. Диффузор сообщается и с контейнером, и с камерой для композиции. Сопло сообщается с камерой для композиции. Предложен способ с использованием этого устройства для доставки композиции в обонятельную область назальной полости. Изобретения обеспечивают эффективное введение композиции в обонятельную область и соответственно её доставку через гематоэнцефалический барьер за счёт усовершенствования механизма доставки большей части распылённого лекарственного препарата в верхнюю часть назальной полости для увеличения экспозиции в обонятельном эпителии. 2 н. и 31 з.п. ф-лы, 25 ил., 4 табл., 5 пр.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка претендует на приоритет документа США № 61/449008, поданного 3 марта 2011 г., документа США № 61/451935, поданного 11 марта 2011 г., документа США № 61/484025, поданного 9 мая 2011 г., и документа США № 61/498974, поданного 20 июня 2011 г., которые настоящим целиком включены сюда в качестве ссылок.
ЗАЯВЛЕНИЕ О ПРАВИТЕЛЬСТВЕННОМ ИНТЕРЕСЕ
Настоящее изобретение было выполнено при поддержке правительства США согласно гранту армии США по программе SBIR (новаторские разработки малых предприятий) W81XWH-10-C-0238. Правительство может обладать определенными правами на данную заявку.
ИЗВЕСТНЫЙ УРОВЕНЬ ТЕХНИКИ
Центральная нервная система (ЦНС) включает мозг, ствол головного мозга и спинной мозг. ЦНС изолирована от внешнего мира несколькими оболочками, которые амортизируют и защищают мозг, ствол головного мозга и спинной мозг. Например, оболочки, образующие гематоэнцефалический барьер (ГЭБ), защищают мозг от определенных компонентов крови. Гематоликворный барьер (ГЛБ) защищает другие части ЦНС от многих химических композиций и микроорганизмов.
Традиционные способы доставки композиций в ЦНС типично являются инвазивными. Например, имплантированный в череп насос, такой как интрацеребровентрикулярный насос, может доставлять в мозг различные композиции. Однако имплантация такого насоса требует хирургии мозга, которая может повлечь различные серьезные осложнения. Определенные композиции, например эпидуральные болеутоляющие средства, могут быть введены прямыми инъекциями через защитную оболочку в ЦНС. Однако такая инъекция для большинства композиций является непрактичной.
Интраназальное введение традиционно было сфокусировано на распределении растворов лекарственных средств в виде аэрозолей для местной доставки к назальному эпителию. Вследствие легкой доступности сосудистого ложа назальной полости, назальное введение лекарственных препаратов было сфокусировано на доставке лекарственных препаратов локально в назальную полость или непосредственно в кровоток.
Значительная часть современных исследований мозга сосредоточена на усилении доставки лекарственных средств в мозг с помощью различных композиций. Традиционные подходы к улучшению поглощения композиций мозгом за счет рецептуры композиции включают (1) мукоадгезивные композиции; 2) усилители пенетрации; 3) липосомы; 4) вазоконстрикторы; и 5) наночастицы. Примеры различных композиций с улучшенными композициями включают различные цитокины, например факторы некроза опухоли, интерлейкины и интерфероны, описанные в патенте США 6991785, и фактор роста и дифференцировки-5 (GDF-5) и родственные белки, описанные в публикации США № 20100074959.
Направленная доставка лекарственных средств в центральную нервную систему (ЦНС) является сложной задачей. Большое количество лекарственных средств, включая биотехнологические продукты, является кандидатами для лечения заболеваний ЦНС, но направленная доставка лекарственных средств в мозг проблематична. Лечение опухолей мозга ограничено тем, что менее 1% большинства терапевтических агентов при системном введении способны проходить через ГЭБ. Транспорт малых молекул через ГЭБ является исключением, а не правилом, и 98% всех малых молекул не проходят через ГЭБ (Pardride, NeuroRx. 2005 January; 2(1): 1-2. 2005); приблизительно 100% лекарственных средств с большими молекулами или генами не проходят через ГЭБ (Pardride, NeuroRx. 2005 January; 2(1): 1-2. 2005). ГЭБ позволяет малым (менее примерно 500 Да) липофильным молекулам из кровотока проникать в ЦНС (Pardridge, Arch Neurol. 2002; 59:35-40). Многие более крупные терапевтические агенты не достигают мозга для лечения расстройств ЦНС, таких как, без ограничений, болезнь Паркинсона, болезнь Альцгеймера, депрессия, инсульт и эпилепсия (Pardridge, NeuroRx. 2005 January; 2(1): 3-14). Расстройства, включая аутизм, лизосомальную болезнь накопления, синдром ломкой X-хромосомы, атаксию и слепоту, являются серьезными расстройствами, для которых практически не существует эффективных способов лечения. Во многих из этих случаев ген, лежащий в основе заболевания, известен, но доставка через ГЭБ является лимитирующей проблемой при генной терапии или заместительной терапии ферментами, и никаких терапевтических средств разработано не было. Доставка лекарственных средств терапевтических композиций, например белков, сталкивается с несколькими серьезными проблемами вследствие их нестабильности, высокого ферментативного метаболизма, низкого желудочно-кишечного всасывания, быстрого почечного элиминирования и потенциальной иммуногенности.
Существует потребность в устройствах, которые могут доставлять композиции в верхнюю часть назальной полости для прямой доставки из носа-в-мозг. Некоторые существующие устройства для назальной доставки лекарственных средств в недостаточной степени выталкивают лекарственное средство из устройства. Недостаточное выталкивание лекарственного средства вследствие ненадлежащего приведения в действие пользователем является далеким от оптимального. Кроме того, факел выброса, создаваемый такими существующими устройствами, слишком широк. В дополнение к этому, некоторые лекарственные продукты плохо смешиваются и/или остаются суспендированными в пропеллентах в устройствах типа MDI (ингаляторы с мерными дозами). Некоторые из существующих устройств для назальных лекарственных средств используют тангенциальный разгон для выталкивания лекарственных препаратов на обонятельный эпителий. Традиционные тангенциальные устройства приводят к тому, что на обонятельном эпителии откладывается небольшая часть композиции. Тангенциальный компонент в аэрозольном факеле имеет склонность приводить к более широкому факелу, причем часть аэрозольных частиц попадает на боковые стенки назальной полости в нижней ее части.
Требуются усовершенствованные механизмы для введения желательных агентов в мозг, ствол головного мозга и/или спинной мозг.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Описано устройство для доставки композиции в обонятельную область назальной полости, включающее контейнер, пригодный для содержания в нем пропеллента, диффузор, сообщающийся с контейнером, камеру композиции, сообщающуюся с диффузором, и сопло, сообщающееся с камерой композиции, где устройство способно доставлять композицию в обонятельную область назальной полости.
В одном аспекте, устройство включает контейнер, находящийся под давлением.
В другом аспекте, пропеллент включает ГФА (гидрофторалкан (HFA)), азот или ХФУ (хлорфторуглерод).
В другом аспекте, устройство включает камеру композиции, содержащую лекарственное средство или агент визуализации.
В еще одном аспекте, лекарственное средство представляет собой оксим.
В еще одном аспекте, диффузор представляет собой фритту (frit).
В еще одном аспекте, агентом визуализации является FDG (фтордезоксиглюкоза, ФДГ) или FLT (3-дезокси-3-[18F]фтортимидин).
В еще одном аспекте, устройство содержит пропеллент, где пропеллент представляет собой жидкость под давлением.
В еще одном аспекте, жидкость под давлением представляет собой ГФА (гидрофторалкан).
В другом аспекте, находящийся под давлением жидкий ГФА высвобождается из контейнера и входит в контакт с диффузором, причем диффузор превращает находящийся под давлением жидкий ГФА в газообразный ГФА.
В другом аспекте, диффузор превращает меньшую часть находящегося под давлением жидкого ГФА в газообразный ГФА.
В дополнительном аспекте, диффузор превращает большую часть находящегося под давлением жидкого ГФА в газообразный ГФА.
В еще одном аспекте, устройство доставляет по меньшей мере 62,6% композиции в обонятельную область.
В еще одном аспекте, устройство доставляет более 64,2% композиции в обонятельную область.
В другом аспекте, устройство доставляет по меньшей мере 64,3% композиции в обонятельную область.
В еще одном аспекте, устройство включает контейнер, где контейнер представляет собой шприц, сиретту или баллон.
В еще одном аспекте, композиция не является агентом визуализации.
В дополнительном аспекте, композиция не является ФДГ.
В одном аспекте, лекарственное средство имеет форму жидкой суспензии, жидкой дисперсии, порошка или водного раствора.
В еще одном аспекте, устройство дополнительно включает направляющий элемент.
В еще одном аспекте, направляющий элемент помогает наведению сопла устройства на обонятельную область пользователя.
В еще одном аспекте, устройства дополнительно включают отверстие для введения, сообщающееся с камерой композиции.
В еще одном аспекте, устройство дополнительно включает индикатор, предназначенный для информирования пользователя о глубине или степени введения капсулы в назальную полость пользователя.
В одном аспекте, диффузор является пористым.
В другом аспекте, диффузор является неоднородно пористым.
В другом аспекте, диффузор является однородно пористым.
В другом аспекте, диффузор является удлиненным.
В еще одном аспекте, диффузор представляет собой дискообразный элемент, включающий элементы конической формы, имеющие дистальные отверстия.
В еще одном аспекте, контейнер представляет собой ингалятор с мерными дозами.
В другом варианте исполнения описано устройство для доставки композиции, включающее контейнер, пригодный для размещения пропеллента, диффузор, сообщающийся с контейнером, камеру композиции, сообщающуюся с диффузором, и сопло, сообщающееся с камерой композиции, где устройство способно доставлять композицию в ухо, на кожу, в щечный карман или в глаза.
В другом варианте исполнения описан способ доставки лекарственного средства в обонятельную область назальной полости, включающий обеспечение контейнера, пригодного для размещения пропеллента, диффузора, сообщающегося с контейнером, камеры композиции, сообщающейся с диффузором, и сопла, сообщающегося с камерой композиции, где при приведении в действие устройство способно доставлять композицию в обонятельную область назальной полости.
В одном аспекте, способ включает доставку лекарственного средства для лечения инфекционной болезни, онкологии или иммунологической болезни.
В одном аспекте, способ включает приведение в действие устройства для подачи пропеллента из контейнера, причем диффузор рассеивает жидкий пропеллент из контейнера в газообразный пропеллент, газообразный пропеллент контактирует с композицией в камере композиции, и композиция и газообразный пропеллент выходят через сопло устройства.
В другом аспекте способа, диффузор превращает меньшую часть находящегося под давлением жидкого ГФА в газообразный ГФА.
В другом аспекте способа, диффузор превращает большую часть находящегося под давлением жидкого ГФА в газообразный ГФА.
В еще одном аспекте способа, по меньшей мере 64,2% композиции доставляется в обонятельную область.
В еще одном аспекте способа, более 64,2% композиции доставляется в обонятельную область.
В другом аспекте способа, композиция представляет собой лекарственное средство или диагностический агент.
В другом аспекте способа, композиция представляет собой лекарственное средство.
В еще одном аспекте способа, диагностический агент является агентом визуализации.
В еще одном аспекте способа, лекарственное средство представляет собой оксим.
В еще одном аспекте способа, агентом визуализации является фтордезоксиглюкоза или фтортимидин.
В еще одном аспекте способа, композиция не является фтордезоксиглюкозой.
В еще одном аспекте способа, композиция не является агентом визуализации.
В еще одном аспекте способа, лекарственное средство имеет форму жидкой суспензии, жидкой дисперсии, порошка, липосом или водного раствора и их комбинаций.
В еще одном аспекте способа, устройство включает один или несколько направляющих элементов.
В еще одном аспекте способа, направляющий элемент помогает наведению сопла устройства на обонятельную область пользователя.
В другом аспекте способа, устройство включает отверстие для введения, сообщающееся с камерой композиции.
В аспекте способа, устройство включает индикатор, предназначенный для информирования пользователя о глубине введения устройства в назальную полость пользователя.
В другом аспекте способа, диффузор является пористым.
В другом аспекте способа, диффузор является неоднородно пористым.
В другом аспекте способа, диффузор является однородно пористым.
В аспекте способа, диффузор является удлиненным.
В другом аспекте способа, диффузор представляет собой дискообразный элемент, включающий элементы конической формы, имеющие дистальные отверстия.
В аспекте способа, контейнер представляет собой ингалятор с мерными дозами.
В другом варианте исполнения описана интраназальная композиция оксима для использования при лечении воздействия органофосфата.
В еще одном варианте исполнения описан способ доставки оксима через гематоэнцефалический барьер нуждающемуся в этом субъекту, включающий введение субъекту терапевтически эффективной дозы оксима, где доза доставляется в верхнюю обонятельную область назальной полости.
В одном аспекте способа, терапевтически эффективное количество оксима, которое вводится пользователю, находится в диапазоне значений от примерно 0,001 мг/кг до примерно 100 мг/кг.
В другом аспекте способа, терапевтически эффективное количество оксима, которое вводится пользователю, находится в диапазоне значений от примерно 0,01 мг/кг до примерно 10 мг/кг.
В еще одном аспекте способа, терапевтически эффективное количество оксима, которое вводится пользователю, находится в диапазоне значений от примерно 0,1 мг/кг до примерно 1 мг/кг.
В еще одном аспекте, описанный способ доставки оксима предназначен для лечения воздействия органофосфата.
В другом варианте исполнения описан способ доставки оксима интраназально пользователю, включающий обеспечение назальной лекарственной формы оксима, выталкивание назальной лекарственной формы с помощью пропеллента и доставку назальной лекарственной формы в назальную полость пользователя, так чтобы оксим доставлялся в назальную полость и затем в центральную нервную систему и/или мозг пользователя.
В одном аспекте, доставляемый оксим включает 2-PAM, MMB4, HI6, TMB4 или Hlo7 и их комбинации.
В другом аспекте, назальная лекарственной формы оксима представляет собой порошок, водный раствор, суспензию или липидсодержащий продукт и их комбинации.
В другом аспекте, пользователь был подвергнут воздействию органофосфатного средства, включая зарин, табун, зоман, Ви-Экс (Russian VX) или диизопропилфторфосфат и их комбинации.
В другом аспекте, большая часть оксима в назальной лекарственной форме откладывается в назальной полости.
В другом аспекте, интраназально доставляется назальная лекарственная форма агониста мускаринового рецептора или антагониста мускаринового рецептора.
В еще одном аспекте, интраназально доставляется назальная лекарственная форма атропина или скополамина или их комбинации.
В еще одном аспекте, интраназально доставляется назальная лекарственная форма антагониста бензодиазепина.
В еще одном аспекте, антагонист бензодиазепина включает диазепам, мидалозам или лоразепам или их комбинации.
В еще одном аспекте, назальная лекарственная форма представляет собой антагонист бензодиазепина, агонист мускаринового рецептора или антагонист мускаринового рецептора или их комбинации.
В еще одном аспекте, интраназальная лекарственная форма включает диазепам, мидалозам, лоразепам, атропин или скополамин или их комбинации.
В еще одном аспекте, назальная лекарственная форма доставляется в назальную полость пользователя, подвергшегося воздействию органофосфата.
В другом аспекте, назальная лекарственная форма доставляется в назальную полость пользователя до воздействия органофосфата.
В еще одном аспекте, назальная лекарственная форма доставляется в назальную полость пользователя после воздействия органофосфата.
В еще одном аспекте, воздействие оксима увеличивает экспозицию оксима в ЦНС. В дополнительных аспектах, по меньшей мере 53% оксима транспортируется непосредственно (directly transported, DTP) в мозг.
Изобретение будет лучше понятно из приведенного далее детального описания различных вариантов исполнения, рассматриваемого в сочетании с сопровождающими чертежами. Приведенное ниже описание является наглядным, иллюстративным и описательным и не должно рассматриваться как ограничивающее объем, определяемый любыми пунктами прилагаемой формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
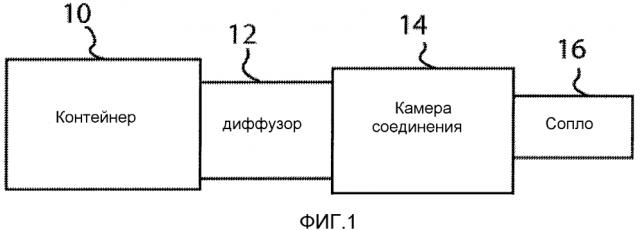
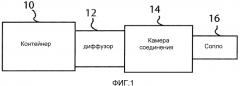
Фиг.1 представляет собой схематический чертеж одного варианта исполнения изобретения.
Фиг.2 изображает вариант исполнения изобретения.
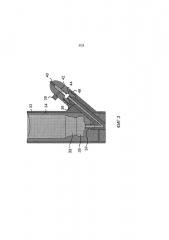
Фиг.3 изображает вариант исполнения изобретения.
Фиг.4 изображает другой вариант исполнения изобретения.
Фиг.5 изображает другой вариант исполнения изобретения.
Фиг.6 изображает другой вариант исполнения изобретения.
Фиг.7 изображает другой вариант исполнения изобретения.
Фиг.8 изображает другой вариант исполнения изобретения с присоединенным назальным направляющим элементом.
Фиг.9 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим и однородно пористым.
Фиг.10 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим и однородно пористым, с непористым открытым кончиком конусной формы, выступающим в готовую лекарственную форму.
Фиг.11 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим, с открытым кончиком конусной формы, выступающим в готовую лекарственную форму, и является однородно пористым.
Фиг.12 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим со множеством конических выступов, с открытым кончиком, позволяющим газообразному пропелленту заходить в камеру композиции.
Фиг.13 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим со множеством конических выступов, позволяющих газообразному пропелленту заходить в камеру лекарственного средства. Он также включает трубку, позволяющую пропелленту заходить в камеру композиции до лекарственного средства для улучшения распыления.
Фиг.14 изображает вариант исполнения диффузора и камеры композиции, причем диффузор является цилиндрическим и однородно пористым. Он также включает трубку, позволяющую пропелленту заходить в камеру композиции до лекарственного средства для улучшения распыления.
Фиг.15 изображает вариант исполнения изобретения, в котором пропеллент создается путем сжатия воздуха вручную.
Фиг.16A изображает вариант исполнения устройства, имеющий камеру композиции в корпусе устройства, позволяющую потоку пропеллента проходить через камеру композиции и обтекать ее. Фиг.16B изображает поперечное сечение устройства по Фиг.16A.
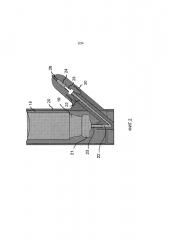
Фиг.17 изображает схематический чертеж устройства, используемого для введения лекарственного препарата 2-PAM крысам в Примере 1.
Фиг.18 демонстрирует результаты испытаний осаждения 2-PAM (затемненный участок) с помощью POD-устройства в назальной полости крысы на обонятельной области (светлая окружность). Незначительное количество лекарственного препарата откладывалось в дыхательной области назальной полости и ничего не было обнаружено в трахее или пищеводе.
Фиг.19 представляет собой график, демонстрирующий POD-введение дозы 2,5 мг 2-PAM, которое приводило к значительно более низким значениям в плазме в любой момент времени в течение первых 60 минут и общим более низким значениям AUC (площадь под кривой) плазмы. *=p<0,05.
Фиг.20 представляет собой график, демонстрирующий POD-введение дозы 2,5 мг 2-PAM, которое приводило к значительно более высоким значениям в мозге в моменты времени 5 и 120 минут и общим более высоким значениям AUC мозга. *=p<0,05.
Фиг.21 изображает модель назальной полости человека, использовавшуюся для испытаний осаждения модельного лекарственного средства флуоресцеина, описанных в Примере 3.
Фиг.22 представляет собой обработанное изображение осаждения в назальной полости человека, как описано в Примере 3. Пять отдельных частей - преддверие, носовые раковины, обонятельная область, основание и пищевод - были проанализированы на осаждение после распыления с помощью устройства. Фиг.22 показывает, что большая часть распыленного материала находится в обонятельной области.
Фиг.23 представляет собой схему экспериментальной установки для испытаний на ударное воздействие, описанных в Примере 4.
Фиг.24 представляет собой схему экспериментальной установки для оценки каких-либо изменений температуры на поверхности, на которую направлено устройство, описанное в Примере 5. Для измерения температуры поверхности мишени был использован лазерный термометр. Устройство распыляло один лишь газообразный ГФА или газообразный ГФА, смешанный с дозой жидкости, и регистрировались любые колебания температуры.
ДЕТАЛЬНОЕ ОПИСАНИЕ ВАРИАНТОВ ИСПОЛНЕНИЯ
Если не указано иное, все технические и научные термины, используемые в данном описании, имеют значения, общеизвестные рядовому специалисту в данной области техники, применимые к описанным способам и композициям. В используемом тут значении следующие термины и фразы имеют приписанные им значения, если не будет указано иное:
В используемом в данном описании значении, термин в единственном числе (в английском тексте - с неопределенными артиклями "a" или "an") может означать один или несколько.
"Диагностический агент" относится к и охватывает атом, молекулу или композицию, пригодные для использования в диагностике болезни. Диагностические агенты включают, без ограничений, радиоизотопы, красители, контрастные агенты, флуоресцентные композиции или молекулы и усиливающие агенты (например, парамагнитные ионы). Нерадиоактивным диагностическим агентом является контрастный агент, пригодный для магниторезонансной визуализации, компьютерной томографии или ультразвуковой диагностики. Диагностический агент может быть использован для проведения позитронно-эмиссионной томографии (ПЭТ), МРВ (магниторезонансной визуализации), рентгена, КТ (компьютерной томографии), ультразвуковой диагностики, оперативной, внутрисосудистой, лапароскопической или эндоскопической процедуры.
“Диффузор” относится к и охватывает устройство для диспергирования или отклонения композиции в различных направлениях.
“Фритта” должна относиться к и охватывать пористый элемент или фильтр.
“Агент визуализации” относится к и охватывает атом, молекулу или композицию, пригодные для использования в детектировании физических изменений или создании изображений внутренних тканей организма. В некоторых аспектах, агент визуализации может быть диагностическим агентом.
“Пропеллент” должен относиться к и охватывать композиции, выполняющие роль носителей для создания движущей силы или толчка.
Термин "терапевтически эффективное количество" относится к и охватывает количество лекарственного средства, эффективное для лечения болезни или расстройства у млекопитающего. В одном аспекте, терапевтически эффективное количество относится к целевой концентрации в ЦНС с подтвержденной эффективностью, например, в замедлении развития болезни. Эффективность может быть измерена обычными способами, в зависимости от состояния, лечение которого проводится.
Термины "лечение" и "лечить" и т.п. относятся к и охватывают терапевтические или сдерживающие мероприятия, направленные на болезнь или расстройство и приводящие к любому клинически желательному или целительному эффекту, включая, без ограничений, смягчение или облегчение одного или нескольких симптомов, регрессию, замедление или приостановку прогрессирования болезни или расстройства. Подтверждением лечения может быть ослабление тяжести симптома, уменьшение числа симптомов или частоты рецидивов.
“Пользователь” или “субъект” должны относиться к и охватывать человека или другое животное. Например, животное может быть приматом или не приматом и может включать кролика, быка, лошадь, свинью, крысу, мышь, собаку или кошку.
Устройство может быть использовано в лечении, профилактике, паллиативном уходе за людьми и в ветеринарных целях. Устройство может быть использовано в исследованиях и в промышленности. Например, устройство может быть использовано для нанесения композиции в сельскохозяйственных целях.
При использовании в данном документе торговых наименований, заявители подразумевают независимое включение композиции продукта с данной торговой маркой, непатентованного лекарственного препарата и активного фармацевтического ингредиента (ингредиентов) продукта с данной торговой маркой.
Для ясности описания и не для ограничений детальное описание изобретения разделено на следующие далее подразделы.
Интраназальное введение композиций обеспечивает некоторые преимущества по сравнению с традиционными хирургическими, внутривенными или пероральными путями введения через гематоэнцефалический барьер (ГЭБ). Интраназальное введение в обонятельную область позволяет избежать разрушения в желудочно-кишечном тракте и метаболизма при первом прохождении через печень, такого как разрушение лекарственных средств ферментами печени, что позволяет экономически эффективно, быстро и прогнозируемо становиться биодоступным большему количеству лекарственного препарата, чем при оральном введении. Интраназальное введение обеспечивает простоту, удобство и безопасность. Интраназальное введение лекарственного препарата обычно является безболезненным (учитывая, что боль может быть субъективным показателем, отличающимся для разных пациентов) и не требует стерильной методики, внутривенных катетеров или других инвазивных приспособлений и обычно может быть немедленно и легко доступным для всех пациентов. Интраназальное введение может обеспечить быстрое достижение терапевтических концентраций лекарственного препарата в мозге и спинном мозге.
Назально вводимые композиции контактируют с верхней обонятельной областью, и молекулярный транспорт происходит напрямую через данную ткань в компартменты центральной нервной системы (Henry, R.J. et al., Pediatr Dent, 1998. 20(5): p. 321-6; Sakane, T. et al., J Pharm Pharmacol, 1991. 43(6): p. 449-51; Banks, W.A. et al., J Pharmacol Exp Ther, 2004. 309(2): p. 469-75; Westin et al., Pharm Res, 2006. 23(3): p. 565-72). Обонятельная слизистая оболочка расположена в верхней части назальной полости, непосредственно под решетчатой пластинкой решетчатой кости черепа. Она содержит обонятельные клетки, которые проходят через решетчатую пластинку решетчатой кости и выступают в полость черепа. При вхождении композиций в контакт с этой специализированной слизистой, они быстро транспортируются непосредственно в мозг в обход ГЭБ и быстро транспортируются прямо в центральную нервную систему, часто быстрее, чем при внутривенном введении композиции.
Обонятельная слизистая оболочка включает обонятельный эпителий. Обонятельный эпителий расположен в верхней части носа между верхней носовой раковиной и крышей назальной полости, непосредственно под решетчатой пластинкой решетчатой кости. У людей она покрывает от примерно 10 до примерно 20 см2 или примерно 8% от общей площади поверхности носа и состоит из четырех основных типов клеток: эпителиальные клетки, нейроны с обонятельными рецепторами, поддерживающие клетки и базальные клетки (Mathison S. et al., (1998) Journal of Drug Targeting 5: 415-441). Хотя обонятельным эпителием занято 3% назальной полости (Morrison and Costanzo, 1990), этот путь является прямым, поскольку обонятельные нейроны не имеют синапса между воспринимающим элементом и афферентным путем (Ding and Даhl, 2003). Обонятельный эпителий имеет глубину, вдвое большую, чем глубина дыхательного эпителия, причем тела обонятельных нервных клеток типично расположены в средней и глубинной областях эпителия, в то время как ядра поддерживающих клеток организованы в виде монослоя, расположенного ближе к мукозальной поверхности. Существует тесный контакт между поддерживающими клетками и между поддерживающими клетками и обонятельными нервными клетками (Morrison E.E. et al. (1992) Journal of Comparative Neurology 297(1): 1-13).
Когда композиция назального лекарственного препарата доставляется вглубь и достаточно высоко в назальную полость, она будет достигать обонятельной слизистой оболочки и будет происходить транспортировка лекарственного препарата в мозг и/или ЦСЖ (цереброспинальную жидкость) через нейроны с обонятельными рецепторами. Перенос композиций из носа в мозг называется носомозговым путем. Носомозговой путь используется, когда лекарственные препараты центрального действия, такие как, без ограничений, седативные средства, противоконвульсивные средства и опиаты вводятся назально. Устройство по настоящему изобретению обеспечивает возможность доставки носомозговым путем, что позволяет почти немедленно доставлять назальные лекарственные препараты в центральную нервную систему и мозг в обход гематоэнцефалического барьера.
Проблема, которая решается в настоящем изобретении, связанная с доставкой лекарственных средств из носа-в-мозг, также вызвана сложной архитектурой носа, которая природно рассчитана на то, чтобы направлять лекарственные средства в нижние носовые воздухоносные пути в направлении легких, что усложняет достижение лекарственными препаратами обонятельной области. Большая часть лекарственного средства, дозируемого из традиционных назальных устройств, таких как распылители или насосы, подвергаются воздействию природного движения воздуха в назальной полости в направлении к пищеводу. Большая часть распыляемого факела, дозируемого традиционными устройствами, встречается с направленным природно вниз воздушным потоком в назальной полости. Остальная часть препарата из традиционных устройств попадает на дыхательный эпителий и удаляется по механизму клиренса реснитчатым эпителием или всасывается в кровоток. Хотя инстилляция с помощью назального катетера и капли в нос в меньшей степени зависят от такого природного направленного вниз движения воздуха, они требуют, чтобы субъекты находились в положении лежа на спине, часто ассоциированы с дискомфортом для пользователя и не являются оптимальными для частого клинического введения.
Кроме того, в верхней части назальной полости существует резервуар остаточного воздуха, который не удаляется при нормальном дыхании, таким образом, оставаясь в обонятельной области и выступая в качестве барьера для отложения. Этот остаточный воздух необходимо вытеснить для стабильной доставки распыленного лекарственного препарата на обонятельный эпителий в верхней части назальной полости. Устройство, описанное в данном документе, доставляет большую часть распыленного лекарственного препарата в верхнюю часть назальной полости для увеличения экспозиции лекарственного средства в обонятельном эпителии, местонахождении пути из носа-в-мозг, путем устранения направленного вниз природного движения воздуха и вытеснения остаточного воздуха верхней части назальной полости.
Устройство по настоящему изобретению предпочтительно и стабильно обеспечивает отложение большей части дозы в более дистальные части назальной полости, такие как обонятельная область. Готовая лекарственная форма (также называемая в данном документе композицией лекарственного средства или назальной лекарственной формой) на скорости выталкивается из устройства в назальную полость.
Фиг.1 изображает один вариант исполнения устройства, в котором контейнер 10 содержит пропеллент. Пропеллент может находиться под давлением. Пропеллент представляет собой текучую среду, например жидкость или газ. В одном аспекте, пропеллент является жидкостью. В другом аспекте, пропеллент является газом. Пропелленты включают фармацевтически пригодные пропелленты. Некоторые примеры фармацевтически пригодных пропеллентов включают гидрофторалкан (ГФА) включая, без ограничений, ГФА, ГФА 227, ГФА 134a, ГФА-FP, ГФА-BP и подобные ГФА. В одном аспекте, пропеллент представляет собой жидкий ГФА. В другом аспекте, пропеллент является газообразным ГФА. Дополнительные примеры пригодных пропеллентов включают азот или хлорфторуглероды (ХФУ). Дополнительно, пропелленты могут быть сжатым воздухом (например, атмосферным воздухом). Контейнер 10 может быть обычным устройством ингалятора с мерными дозами (MDI), включающим находящийся под давлением контейнер, дозирующий клапан (включая шток) для дозирования пропеллента при приведении в действие. В определенных аспектах, пропеллент не дозируется при приведении в действие. В одном аспекте, контейнер 10 не содержит лекарственного средства. В другом аспекте, контейнер включает пропеллент и лекарственное средство.
Контейнер 10 сообщается с диффузором. Например, если диффузор сообщается с контейнером 10, “сообщение” должно относиться к и охватывать конгруэнтность или сообщение по жидкости. Пропеллент из контейнера 10 рассеивается через диффузор. В одном аспекте, большая часть пропеллента рассеивается через диффузор. В другом аспекте, меньшая часть пропеллента рассеивается через диффузор. Большая часть относится к и охватывает по меньшей мере 50 процентов. Меньшая часть относится к и охватывает менее 50 процентов. В другом аспекте, по меньшей мере примерно 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или примерно 100%, включая конечные точки, пропеллента рассеивается через диффузор. Диффузор сообщается с камерой композиции 14. Камера композиции 14 способна удерживать композицию, такую как, без ограничений, лекарственное средство и/или диагностический агент. В одном аспекте, диагностический агент является агентом визуализации. В примере, агент визуализации представляет собой фтордезоксиглюкозу (ФДГ) или фтортимидин (FLT). В другом аспекте, композиция представляет собой лекарственное средство. В другом аспекте, композиция не является агентом визуализации. В одном аспекте, композиция является жидкостью. В другом аспекте, композиция является порошком. В еще одном аспекте, композиция представляет собой интраназальную композицию лекарственного средства в жидком или порошкообразном состоянии. Интраназальная композиция может содержать пригодные интраназальные носители и эксципиенты, известные специалистам.
Пропеллент в контейнере 10 выступает в роли носителя для передачи движущей силы или толчка для выталкивания композиции из камеры композиции 14. Камера композиции 14 сообщается с соплом 16. Движущая сила или толчок пропеллента способны вытолкнуть композицию из камеры композиции 14 и сопла 16, когда он сообщается с камерой композиции 14.
В одном аспекте, когда MDI-устройство приводится в действие, высвобождается дискретное количество находящегося под давлением текучего ГФА. MDI может содержать количество ГФА-пропеллента, достаточное для от примерно 30 до примерно 300 срабатываний, включая конечные точки. Количество текучего пропеллента, высвобождаемое при приведении в действие, может составлять от примерно 20 до примерно 200 мкл жидкого пропеллента, включая конечные точки.
Фиг.2 изображает один из вариантов исполнения устройства. В корпусе привода 20 размещен контейнер 10, в одном аспекте контейнер 10 представляет собой ингалятор с мерными дозами, который включает контейнер пропеллента 18, имеющий шейку 19 и блок дозирующего клапана 21. Шток клапана 23 сообщается с соединительным каналом 22. Пропеллент, выходящий из штока клапана 23, представляет собой текучую среду. Текучая среда может быть жидкостью, газом или их комбинацией. Диффузор 28 сообщается с пропеллентом, выходящим из контейнера 10, и камерой композиции 14.
Пропеллент, выходящий из контейнера 10, входит в контакт с диффузором 28. Диффузор 28 способен преобразовывать жидкий пропеллент, выходящий из контейнера 10, в газообразный пропеллент. В одном аспекте, диффузор 28 способен превращать весь или большую часть жидкого пропеллента в газообразный пропеллент. В другом аспекте, диффузор способен превращать меньшую часть жидкого пропеллента в газообразный пропеллент. Большая часть относится к и охватывает по меньшей мере 50 процентов.
Меньшая часть отно