Способ топической диагностики воспаления в сердце
Иллюстрации
Показать всеИзобретение относится к медицине, радионуклидной диагностике, может найти применение в кардиологии и кардиохирургии. Проводят топическую диагностику воспаления в сердце путем выполнения однофотонной эмиссионной компьютерной томографии (ОФЭКТ) через 18-20 ч после внутривенного введения радиофармпрепарата. Причем перед томографией на тело пациента в 3 межреберье слева по срединно-ключичной линии наносят поверхностную радиоизотопную метку. Затем на нее наклеивают в качестве рентгеноконтрастной метки одноразовый ЭКГ-электрод. Запись ОФЭКТ осуществляют одновременно в 27 проекциях, время сканирования составляет от 400 до 600 сек в зависимости от веса тела пациента. По окончании ОФЭКТ, не меняя положения тела пациента и высоты томографического стола, выполняют рентгеновскую компьютерную томографию грудной клетки высокого разрешения, с толщиной среза 1,25 мм на гибридном ОЭКТ/КТ томографе. Далее по меткам выполняют совмещение сцинтиграфических и рентгеновских томографических изображений путем точного наложения друг на друга радиоизотопной и рентгеноконтрастной меток во фронтальных, сагиттальных и поперечных срезах, определяя наличие и местоположение воспалительного очага в сердце. Способ обеспечивает высокую чувствительность и точность определения наличия и местонахождения воспалительных очагов в сердце, с исключением погрешностей при наложении изображений при визуализации всех камер сердца, сокращение времени исследования, уменьшение лучевой нагрузки на пациента. 3 ил., 2 пр.
Реферат
Изобретение относится к медицине, а именно лучевой диагностике, и может найти применение в кардиологии и кардиохирургии.
Известен способ диагностики миокардита (патент №2508051) [1], заключающийся в выполнении однофотонной эмиссионной компьютерной томографии через 18-20 часов после внутривенного введения радиофармпрепарата, с последующим внутривенным введением 10 мКи 99mTc-технетрила и проведением перфузионной однофотонной эмиссионной компьютерной томографии сердца, по сопоставлению сцинтиграмм судят о местоположении воспалительного очага в сердце, отличающийся тем, что в качестве радиофармпрепарата для диагностики миокардита используют 20 мКи 99mTc-пирофосфата, а перед выполнением каждого из сцинтиграфических исследований сердца на теле пациента ставят поверхностную радиоактивную метку в области 3 межреберья по правой парастернальной линии, по которой совмещают сцинтиграммы.
Недостатками указанного метода являются использование двух радиофармпрепаратов, длительное время его проведения, отсутствие информации об анатомической принадлежности выявленных очагов накопления радиофармпрепарата, находящихся вне контуров левого желудочка, большая лучевая нагрузка (7,55 мЗв).
Задача изобретения - создание способа топической диагностики воспаления в сердце.
Поставленная задача решается техническим решением, представляющим собой способ топической диагностики воспалительных процессов в сердце, включающий в себя внутривенное введение радиофармпрепарата, тройного к воспалению или повреждению ткани (аутолейкоциты, меченные 99mTc-НМРАО или 99mTc-Пирофосфат), с последующим проведением однофотонной эмиссионной компьютерной томографии на гамма-камере, оснащенной твердотельными кадмий-цинк-теллуровыми детекторами, (ОЭКТ) через 18-20 часов после введения РФП. Непосредственно после ОЭКТ пациенту проводят рентгеновскую компьютерную томографию высокого разрешения (КТВР) грудной клетки и сопоставляют томосрезы двух исследований, используя радиоизотопную и рентгеноконтрастную метки.
Новым в предлагаемом способе является использование рентгеноконтрастной метки и совмещение сцинтиграмм с рентгеновскими компьютерными томограммами сердца, что дает возможность исключить появление погрешностей при наложении изображений, сократить время исследования, уменьшить лучевую нагрузку на пациента и при этом визуализировать все камеры сердца.
Сцинтиграфические методы исследования, которые на сегодняшний день применяют для визуализации очагов воспаления в органах средостения, отличаются простотой, а также высокой чувствительностью и специфичностью. Вместе с тем, используя их в качестве моноисследования, ответить на вопрос о месте нахождения воспалительного очага - в пределах миокарда или же нет - очень сложно. В частности, в работе Сазоновой С.И. с соавт. [2], выполненной на фантомах сердца, было показано, что радиоактивность крови от полостей ЛЖ и ПЖ «перекрывает» локальные включения РФП в миокард средней и слабой интенсивности. В связи с этим провести топическую диагностику очаговых накоплений РФП в сердце без дополнительного совмещения сцинтиграмм с изображениями анатомических контуров сердца представляет собой технически сложную задачу. Существующие, на сегодняшний день, методы анатомической визуализиции ограничены возможностями используемой радиоизотопной аппаратуры. Рентгеновская компьютерная томография лишена данных недостатков и позволяет расширить область визуализации.
В связи со стремительным развитием радиодиагностической аппаратуры все большее распространение получают гибридные приборы, позволяющие совмещать изображения различной модальности (ПЭТ-КТ, ОФЭКТ-КТ и др.). Данные технологии позволяют локализовать патологическое накопление РФП не только в миокарде и близлежащих тканях, но и в любой зоне интереса [3, 4]. В настоящее время наиболее доступным является совмещение гамма-сцинтиграфических изображений с рентгеновской компьютерной томографией [5]. Гибридные аппараты ОФЭКТ-КТ активно используются для диагностики заболеваний различных органов и систем, в том числе для радионуклидной индикации в кардиологии и кардиохирургии. При этом используются гамма-камеры Ангеровского типа [6], обладающие меньшей разрешающей способностью в отличие от твердотельных кадмий-цинк-теллуровых (CZT) детекторов, которые являются наиболее предпочтительными для визуализации [7, 8]. Кроме того, в качестве анатомического ориентира принято использовать низкодозную компьютерную томографию (коррекция аттенюации) [6, 9], что приводит к несоответствию данных радионуклидного и рентгенологического методов.
Новые признаки проявили в заявляемой совокупности новые свойства. Идентичной совокупности признаков в известных технических решениях не обнаружено.
Предлагаемый способ может быть использован в здравоохранении.
Исходя из вышеизложенного, предлагаемое изобретение соответствует условиям патентоспособности «Новизна», «Изобретательский уровень» и «Промышленная применимость».
Изобретение будет понятно из следующего описания и приложенных чертежей.
На Фиг. 1 стрелками обозначены изображения поверхностных рентгеноконтрастной (а) и радиоактивной (б) меток на первичных рентгеновских (а) и сцинтиграфических изображениях (б).
На Фиг. 2 показаны наложенные друг на друга сцинтиграммы и рентгеновские компьютерные томограммы, полученные при использовании сцинтиграфии с аутолейкоцитами, меченными 99mTc-HMPAO, и рентгеновской компьютерной томографии высокого разрешения на поперечных (а), фронтальных (б) и сагиттальных (в) срезах.
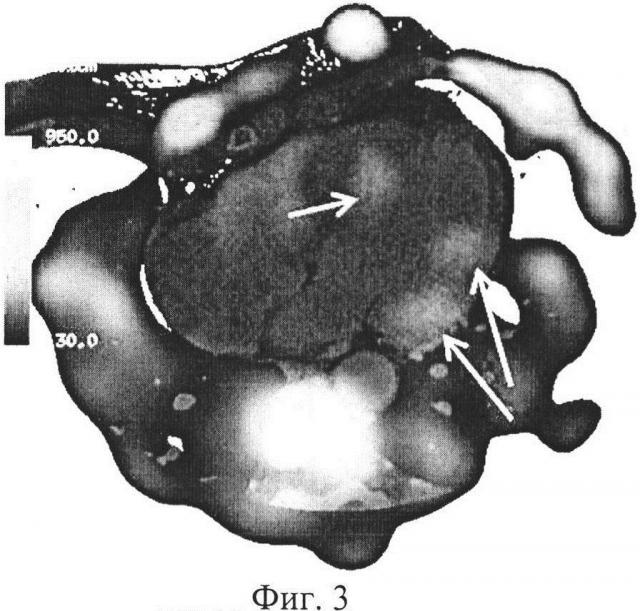
На Фиг. 3 показаны наложенные друг на друга сцинтиграммы и рентгеновские компьютерные томограммы, полученные при использовании сцинтиграфии с 99mTc-пирофосфатом и рентгеновской компьютерной томографии высокого разрешения.
Способ осуществляется следующим образом. На первом этапе исследования проводят ОФЭКТ области средостения на гамма-камере. Пациент располагается на томографическом столе лежа на спине максимально левее к краю стола, с закинутыми за голову руками. Непосредственно перед исследованием на грудь пациента (3 межреберье слева по срединно-ключичной линии) наносится радиоизотопная метка. Сверху на изотопную метку наклеивается одноразовый ЭКГ-электрод, который выполняет функцию рентгеноконтрастной метки. Запись осуществляется одновременно в 27 проекциях, время сканирования составляет от 400 до 600 секунд в зависимости от веса тела пациента. По окончании записи ОФЭКТ, не меняя положения тела пациента и высоты томографического стола, выполняют рентгеновскую компьютерную томографию высокого разрешений грудной клетки по стандартному протоколу с толщиной среза 1,25 мм. Совмещение изображений выполняют путем точного наложения друг на друга радиоизотопной и рентгеноконтрастной меток во фронтальных, сагиттальных и поперечных срезах.
Техническим результатом изобретения являются высокая чувствительность и точность определения наличия и местонахождения воспалительных очагов в сердце, упрощение исследования, сокращение общего времени его проведения, а также снижение лучевой нагрузки на пациента.
Клинический пример 1
Мужчина, 26 лет, находился на лечении в ФГБУ «НИИ кардиологии» СО РАМН (18.06.15-26.07.15).
Предварительный диагноз: Коррегированная Тетрада Фалло. Протезирование легочной артерии клапансодержащим кондуитом, бактериальный эндокардит кондуита клапана легочной артерии.
При поступлении предъявлял жалобы на перебои в работе сердца, повышение температуры тела до субфебрильных цифр, слабость, одышку инспираторного характера, недомогание, быструю утомляемость.
Вышеописанные жалобы беспокоят пациента с 2013 года. В период с 2013 по 2015 год пациент был неоднократно пролечен по поводу пансинусита, бронхита, абсцедирующей пневмонии. При проведении обследования были выявлены носительство цитомегаловирусной инфекции, признаки грибкового поражения пищевода, гепатоспленомегалия, признаки иммунодефицита. Неоднократные посевы крови на стерильность не выявили роста патогенной флоры, однако при посеве мокроты был отмечен рост Candida albicans. В марте 2015 года по данным ультразвукового исследования сердца у пациента определяется вегетация в проекции клапана легочной артерии.
Данные лабораторных исследований:
Общий анализ крови (20.06.15): СОЭ 35 мм/ч, лейкоциты 6,9*103/mm3, Hb 120 г/л, эритроциты 4,3*1012/л, гранулоциты 73%, эозинофилы 1,2%, базофилы 0,3%, лимфоциты 16,8%, моноциты 7,8%, тромбоциты 314*109/л.
Биохимический анализ крови: Пресепсин 351 пг/мл.
Иммунный статус: IgA 1,08 г/л, IgG 37,92 г/л, IgM 2,12 г/л, T-cells 82,5%, B-cells 11,4%, NK-cells 6%, T-cells (CD4+) 38,9%, T-cells (CD3+, CD8+) 40,9%.
Бактериальные посевы крови на стерильность: отрицательные.
Данные инструментальных методов исследования:
Эхокардиография: фракция выброса ЛЖ 68%. Отмечается умеренное увеличение правого желудочка, в области клапана легочной артерии визуализируется подвижное, фиксированное к стенке кондуита образование. Жидкости в перикарде нет.
МСКТ-ангиопульмонография: КТ-признаки флотирующего тромба в легочном стволе.
В связи с необходимостью дифференцировать бактериальный эндокардит (вегетации на клапане) и тромбоз клапана ЛА было решено провести радионуклидное обследование пациента. Для этого больному было внутривенно введено 20 мКи суспензии аутолейкоцитов, меченных 99mTc-НМРАО. Через 18 ч пациента уложили на томографический стол, выставили поверхностную радиоактивную и рентгеноконтрастную метки в области 3 межреберья слева по срединно-ключичной линии (Фиг. 1) и провели однофотонную эмиссионную компьютерную томографию сердца. По окончании исследования, не меняя положения тела пациента и высоты томографического стола, выполнили рентгеновскую компьютерную томографию высокого разрешения грудной клетки. Анализ серии сцинтиграмм показал наличие высокоинтенсивного очагового накопления радиофармпрепарата округлой формы в области переднего средостения слева от грудины, однако точную локализацию очага определить не представлялось возможным. После наложения сцинтиграфических изображений на сканы, полученные после выполнения рентгеновской компьютерной томографии высокого разрешения, анатомическое расположение патологического накопления было локализовано в проекции протеза клапана легочной артерии (Фиг. 2).
Результаты совмещенного ОЭКТ/КТВР исследования были подтверждены данными патоморфологического исследования операционного материала: бактериальный эндокардит с преобладанием грамм-отрицательных кокков.
На основании комплексного обследования был выставлен окончательный диагноз: бактериальный эндокардит кондуита клапана легочной артерии.
Клинический пример 2
Женщина, 51 год, находилась на обследовании и лечении в ФГБУ «НИИ кардиологии» СО РАМН (28.05.15-04.06.15).
Предварительный диагноз: идиопатическое нарушение ритма сердца, персистирующая форма фибрилляции предсердий.
При поступлении предъявляла жалобы на перебои в работе сердца, одышку инспираторного характера при умеренных физических нагрузках, сопровождающихся болью в грудной клетке сжимающего характера.
Данные лабораторных исследований:
Общий анализ крови (30.05.15): СОЭ 19 мм/ч, лейкоциты 6,0*109/л, Нb 132 г/л, эритроциты 3,82*1012 /л, гранулоциты 62%, моноциты 6%, лимфоциты 30%, эозинофилы 1%, базофилы 1%, тромбоциты 23 3*109/л.
Биохимический анализ крови (1.06.2015): СРБ 7 мг/л, ACT 12 Ед/л, АЛТ 10 Ед/л.
Данные инструментальных методов исследования.
ЭКГ (27.05.2015): зарегистрирована постоянная форма фибрилляция предсердий с ЧСС до 74 в минуту.
ЭХО-КГ: расширения полостей сердца не выявлено. Нарушения локальной сократимости стенок ЛЖ не обнаружено. ФВ 62%. Створки МК и ТК интактны. ФВ 65%. Жидкости в перикарде нет.
МСКТ-коронароангиография (02.06.2015): достоверных КТ-признаков коронарного кальциноза и атеросклероза не выявлено.
Учитывая наличие нарушения ритма сердца при ангиографически не измененных коронарных артериях, а также повышение СОЭ и С-реактивного белка, было принято решение о проведении сцинтиграфии миокарда с 99mTc-Пирфотехом, совместно с рентгеновской компьютерной томографией высокого разрешения. Для этого больной было внутривенно введено 20 мКи 99mTc-Пирфотеха. Через 18 ч пациентку уложили на томографический стол, выставили поверхностную радиоактивную и рентгеноконтрастную метку в области 3 межреберья слева по срединно-ключичной линии и провели однофотонную эмиссионную компьютерную томографию сердца. По окончании исследования, не меняя положения тела пациента и высоты томографического стола, выполнили рентгеновскую компьютерную томографию высокого разрешения грудной клетки. Сцинтиграфические и рентгеновские томографические сканы были точно наложены друг на друга по изображениям меток. Анализ серии совмещенных томограмм показал наличие очагового накопления радиофармпрепарата средней интенсивности округлой формы в области средних и базальных отделов боковой стенки, а также средних отделов перегородки (Фиг. 3).
Результаты ОЭКТ/КТВР исследования были подтверждены результатами гистологического исследования эндомиокардиальной биопсии: активный лимфоцитарный миокардит со слабым и умеренно выраженным интерстициальным фиброзом эндокарда.
На основании комплексного обследования был выставлен окончательный диагноз: миокардит, подострое течение, очаговый. Персистирующая форма фибрилляции предсердий.
Предлагаемый способ апробирован на 30 пациентах с подозрением на миокардит и бактериальный эндокардит.
Используемая литература
1. Пат. 2508051 Российская Федерация, МПК A61B 6/00, A61B 6/03, A61K 51/00. Способ диагностики миокардита / С.И. Сазонова, Ю.Б. Лишманов, Ю.Н. Ильюшенкова. - №2013107807/14; заявл. 21.02.2013; опубл. 27.02.2014, Бюл. №6. - 8 с.
2. Сазонова, С.И. Сцинтиграфическая визуализация воспалительных очагов в сердце / С.И. Сазонова, Ю.Б. Лишманов, И.Ю. Проскокова // Медицинская радиология и радиационная безопасность. - 2011. - Т. 56, №5. - С.31-36.
3. Dobrucki, L.W. PET and SPECT in cardiovascular molecular imaging / L.W. Dobrucki, A.J. Sinusas // Nat. Rev. Cardiol. - 2010. - Vol.7. - P. 38-17.
4. Images in cardiovascular medicine. Serial multimodality assessment of myocardial infarction in mice using magnetic resonance imaging and micro-positron emission tomography provides complementary information on the progression of scar formation / S.S. Berr, Y. Xu, R.J. Roy et al. // Circulation. - 2007. - Vol.115. - P. e428-e429.
5. Prior, J.O. Multimodality Imaging in Ischemic Cardiomyopathy / J.O. Prior, H. Farhad, O. Muller // Curr. Cardiovasc. Imaging. Rep. - 2014. - Vol.7. PMC4133026.
6. Erba P.A., Sollini M., Conti U., Bandera F., Tascini C, De Tommasi S.M., et al. Radiolabeled WBC scintigraphy in the diagnostic workup of patients with suspected device-related infections. JACC Cardiovasc Imaging. 2013 Oct;6(10):1075-86. doi: 10.1016/j.jcmg.2013.08.001.
7. Jensen M.M., Schmidt U., Huang C, Zerahn B. Gated tomographic radionuclide angiography using cadmium-zinc-telluride detector gamma camera; comparison to traditional gamma cameras. J Nucl Cardiol. 2014 Apr;24(2):384-96. doi: 10.1007/sl2350-013-9844-6.
8. Chowdhury F.U., Vaidyanathan S., Bould M., Marsh J., Trickett C, Dodds K., et al. Rapid-acquisition myocardial perfusion scintigraphy (MPS) on a novel gamma camera using multipinhole collimation and miniaturized cadmium-zinc-telluride (CZT) detectors: prognostic value and diagnostic accuracy in a 'real-world' nuclear cardiology service. Eur Heart J Cardiovasc Imaging. 2014Mar;15(3):275-83. doi: 10.1093/ehjci/jetl49.
9. Erba P.A., Glaudemans A.W., Veltman N.C, Sollini M., et al. Image acquisition and interpretation criteria for 99mTc-HMPAO-labelled white blood cell scintigraphy: results of a multicentre study. Eur J Nucl Med Mol Imaging. 2014 Apr;41(4):615-23. doi: 10.1007/s00259-013-2631-4.
Способ топической диагностики воспаления в сердце, включающий выполнение однофотонной эмиссионной компьютерной томографии (ОФЭКТ) через 18-20 часов после внутривенного введения радиофармпрепарата, отличающийся тем, что перед выполнением исследования на тело пациента в 3 межреберье слева по срединно-ключичной линии наносят поверхностную радиоизотопную метку, а затем на нее наклеивают в качестве рентгеноконтрастной метки одноразовый ЭКГ-электрод, запись ОФЭКТ осуществляют одновременно в 27 проекциях, время сканирования составляет от 400 до 600 секунд в зависимости от веса тела пациента, затем по окончании ОФЭКТ, не меняя положения тела пациента и высоты томографического стола, выполняют рентгеновскую компьютерную томографию грудной клетки высокого разрешения, с толщиной среза 1,25 мм на гибридном ОЭКТ/КТ томографе, далее по меткам выполняют совмещение сцинтиграфических и рентгеновских томографических изображений путем точного наложения друг на друга радиоизотопной и рентгеноконтрастной меток во фронтальных, сагиттальных и поперечных срезах, определяя наличие и местоположение воспалительного очага в сердце.