Производные фенилгуанидина
Иллюстрации
Показать всеИзобретение относится к применению соединения формулы (I) или его фармацевтически приемлемой соли, или любой из его стереоизомерных форм, или их смесей для лечения патологического состояния, опосредованного Rac1 клеточными белками. В формуле (I) R1 и R1' независимо выбраны из группы, состоящей из Н и CF3 (при условии, что по меньшей мере один из R1 и R1' отличается от Н); А представляет собой карбоциклическую или гетероциклическую кольцевую систему с одним кольцом, где кольцо, образующее кольцевую систему, содержит 5-7 членов, где каждый член независимо друг от друга выбирается из С, N и СН; или представляет собой ароматическое кольцо; при этом А замещен одним или несколькими радикалами, выбранными из группы, состоящей из Н, нитро, прямого или разветвленного (C1-С6)алкила, галоген-(C1-С6)алкила и -SO2NR3R4; где каждый R3 независимо представляет собой Н или прямой или разветвленный (С1-С4)алкил, каждый R4 независимо представляет собой Н или прямой или разветвленный (C1-С6)алкил. Изобретение относится также к соединению формулы (II), способу его получения и фармацевтической композиции, включающей это соединение. В формуле (II) А представляет собой карбоциклическую или гетероциклическую кольцевую систему с одним кольцом, где кольцо, образующее кольцевую систему, содержит 5-7 членов, где каждый член независимо друг от друга выбирается из С, N и СН; или представляет собой ароматическое кольцо. Предлагаемые соединения могут найти применение в качестве агентов для лечения быстрорастущих и/или резистентных опухолей. 4 н. и 10 з.п. ф-лы, 9 ил., 3 табл., 7 пр.
Реферат
По данной заявке испрашивается приоритет предварительной заявки США №61/545804, поданной 11 октября 2011 года, которая включена в настоящее описание посредством ссылки.
Настоящее изобретение относится к новой группе производных фенилгуанидина для ингибирования Rac1, которые блокируют его взаимодействие с гуанозин обменными факторами (GEF), принадлежащими к семейству DBL, в качестве агентов для лечения быстрорастущих и/или резистентных опухолей, а также к процессу их получения, к включающим их фармацевтическим композициям и к их применению в терапии.
Уровень техники
Семейство Rho GTPаз представляет собой молекулярные переключатели, которые контролируют сигнальные пути, регулирующие реорганизацию актинового цитоскелета, экспрессию генов, развитие клеточного цикла, клеточное выживание и другие клеточные процессы. Наряду с другими функциями, они принимают участие в регуляции клеточного цикла и клеточного деления, являются также вовлеченными в секрецию, эндоцитоз, фагоцитоз, мембранный транспорт и апоптоз.
Семейство Rho белков представляет собой одно из трех важнейших ответвлений Ras суперсемейства. На долю Rho белков приходится приблизительно 30 процентов аминокислотной идентичности с Ras белками. По меньшей мере, 23 белка семейства Rho, характерные для млекопитающих, идентифицированы к настоящему времени, включая RhoA, Rac1 и Cdc42.
Опухолевые клетки, помимо того, что они характеризуются нерегулируемым разрастанием, показывают изменения их морфологических характеристик, и в случае метастаз они приобретают способность проходить через тканевые барьеры. Rho GTPазы играют важную роль в контролировании клеточной морфологии и подвижности.
Получение соединений, обладающих способностью специфически ингибировать активность Rho-GTPаз, предоставляет специфическое альтернативное решение в терапии рака.
Синтез и гербицидная активность некоторых производных гуанидина описаны в Chinese Journal of Chemistry, 2008, vol. 26(8), pp. 1481-1485.
Сущность изобретения
В настоящем изобретении предложены соединения, которые представляют собой высокоактивные и селективные ингибиторы Rho GTPазных клеточных белков. А именно, эти соединения могут применяться для ингибирования Rho-зависимого Rac1 GTPазного клеточного белка. Соответственно, эти ингибиторы могут быть использованы для лечения заболеваний, опосредованных характерными для млекопитающих Rac1 клеточными белками, т.e. они могут быть пригодными для лечения любого патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками.
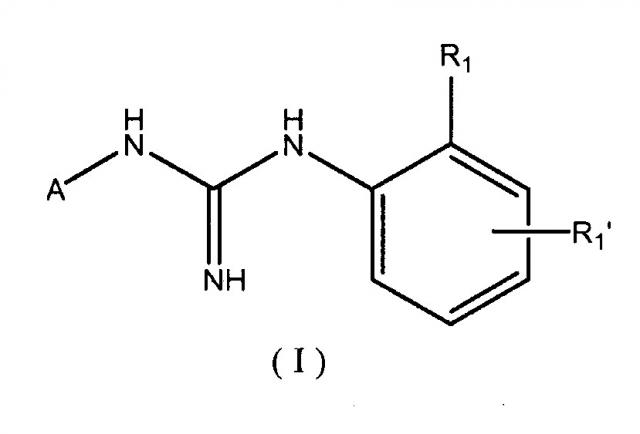
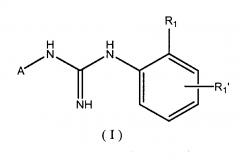
Исходя из вышеизложенного, первый аспект настоящего изобретения касается соединения формулы (I)
или его соли, или любой из его стереоизомерных форм, или их смеси,
в которой:
R1 и R1' независимо выбраны из группы, состоящей из H, (С1-C4)алкила, CF3, F, Cl, Br, I, -CN, OH, NH2, -OCH3 и NO2; при условии, что, по меньшей мере, один из R1 и R1' отличаются от H;
A представляет собой радикал, выбранный из прямого или разветвленного (C1-C6)алкила, или из одной из известных карбоциклических или гетероциклических кольцевых систем с 1-2 кольцами, в которых каждое из колец, образующих кольцевую систему,
содержит 5-7 членов, где каждый член независимо выбран из C, N, O, S, CH, CH2, NH;
представляет собой насыщенное, частично ненасыщенное или ароматическое кольцо;
при этом A замещен одним или несколькими радикалами, выбранными из группы, состоящей из H, галогена, нитро, циано, прямого или разветвленного (C1-C6)алкила, галоген(C1-C6)алкила, прямого или разветвленного (C2-C6)алкенила, -OR2, -COR2, -COOR2, -OC(O)R2, -C(O)NR3R4, -NR3R4, -R5NHR6, -SR2, -SO-R2, -SO2-R2 и -SO2NR3R4;
в которых
каждый R2 независимо представляет собой H или прямой, или разветвленный (C1-C4)алкил,
каждый R3 независимо представляет собой H или прямой, или разветвленный (C1-C4)алкил,
каждый R4 независимо представляет собой H, прямой или разветвленный (C1-C6)алкил, фенил, пиридин или хинолин; при этом кольцевая система фенила, пиридина или хинолина замещена одним или несколькими радикалами, выбранными из H, прямого или разветвленного (C1-C4)алкила и NH2;
R5 и R6 независимо выбраны из H, прямого или разветвленного (C1-C4)алкила,
предназначенного для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками.
Этот первый аспект можно сформулировать как способ лечения патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1, у нуждающегося в этом субъекта, в особенности являющегося человеком, который включает в себя введение субъекту соединения формулы I или его фармацевтически приемлемой соли вместе с фармацевтическими эксципиентами или носителями.
Альтернативно, этот первый аспект может быть сформулирован как применение соединения формулы I или его фармацевтически приемлемой соли для получения лекарственного средства для лечения патологического состояния, опосредованного Rho-GTPазными клеточными белками, в частности, Rac1.
Более предпочтительно, когда патологическое состояние, опосредованное Rac1, представляет собой быстрорастущую и/или резистентную опухоль.
Другой аспект изобретения касается фармацевтической композиции, которая включает в себя, по меньшей мере, одно соединение формулы I или его фармацевтически приемлемую соль и один или несколько фармацевтически приемлемых эксципиентов или носителей.
Предпочтительно, когда фармацевтическая композиция представляет собой противоопухолевую фармацевтическую композицию.
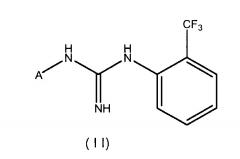
В другом аспекте предлагается соединение формулы II
или его соль, или любая из его стереоизомерных форм или их смесь, в которой:
A представляет собой радикал одной из известных карбоциклических или гетероциклических кольцевых систем с 1-2 кольцами,
в которых каждое из колец, образующих кольцевую систему,
содержит 5-7 членов, где каждый член независимо выбран из C, N, O, S, CH, CH2, NH;
представляет собой насыщенное, частично ненасыщенное или ароматическое кольцо;
при этом A замещен одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2;
при условии, что соединение отличается от N-(4-метил-6-гидроксипиримидин-2-ил)-N'-(2-трифторметилфенил)гуанидина, N-[4,6-бис(метил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидина или N-[(4-метил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидина.
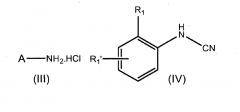
Еще один другой аспект настоящего изобретения касается способа получения соединения формулы I, который включает в себя взаимодействие анилина формулы (III) с цианамидом формулы (IV):
,
в которых A, R1 и R1' представляют собой такие, как определено выше.
Подробное описание изобретения
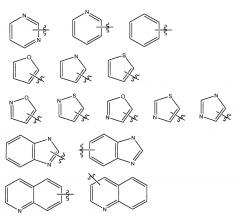
В соответствии с вариантом осуществления первого аспекта, настоящее изобретение относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой A представляет собой кольцевую систему, выбираемую из
и при этом A замещена, как определено выше, или к их соли, или к любой из их стереоизомерных форм, или их смеси, и волнистая линия обозначает место присоединения кольца к сопряженному азоту. Более предпочтительно, когда A выбирают из группы, состоящей из радикала пиридина, пиримидина и фенила; и при этом A замещена, как определено выше, или к их соли, или к любой из их стереоизомерных форм, или их смеси.
В другом варианте осуществления изобретение относится к соединениям формулы I, предназначенным для лечения патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой A представляет собой кольцевую систему, выбираемую из
и при этом A замещена одним или несколькими радикалами, как определено выше, или к их соли, или к любой из их стереоизомерных форм, или их смеси, и волнистая линия обозначает место присоединения кольца к сопряженному азоту. В еще более предпочтительном варианте осуществления изобретения, настоящее изобретение относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой R1 и R1' представляют собой такие, как определено выше; A представляет собой кольцевую систему, выбираемую из
и при этом A замещена одним или несколькими радикалами, как определено выше, или к их соли, или к любой из их стереоизомерных форм, или их смеси, и волнистая линия обозначает место присоединения кольца к сопряженному азоту.
В соответствии с вариантом осуществления первого аспекта, настоящее изобретение относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой A выбирают из метила, этила, н-пропила, изо-пропила, н-бутила, изо-бутила, втор-бутила или н-пентила, и при этом A замещена, как определено выше, или к их соли, или к любой из их стереоизомерных форм, или их смеси.
В другом варианте осуществления изобретение относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, при этом кольцевая система A такая, как определено в любом из вышеприведенных вариантов осуществления изобретения, замещена одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, прямого или разветвленного (C1-C6)алкила, галоген-(C1-C6)алкила, прямого или разветвленного (C2-C6)алкенила, -OR2, -COR2, -COOR2, -OC(O)R2, -C(O)NR3R4, -NR3R4, -R5NHR6, -SR2, -SO-R2, -SO2-R2 и -SO2NR3R4;
в которых
каждый R2 независимо представляет собой H, метил, этил, н-пропил, изо-пропил, н-бутил или трет-бутил;
каждый R3 независимо представляет собой H, метил, этил, н-пропил, изо-пропил, н-бутил или трет-бутил,
каждый R4 независимо представляет собой H, метил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, фенил, пиридин или хинолин;
в которых кольцевая система фенила, пиридина и хинолина замещена одним или несколькими радикалами, выбираемыми из H, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила и NH2;
R5 и R6 независимо выбраны из H, метила, этила, н-пропила, изо-пропила, н-бутила или трет-бутила;
или к их соли, или к любой из их стереоизомерных форм, или их смеси.
В другом варианте осуществления изобретение относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой кольцевая система A такова, как определено в любом из вышеприведенных вариантов осуществления изобретения, замещена одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2;
или к их соли, или к любой из их стереоизомерных форм, или их смеси.
Другой вариант осуществления изобретения относится к соединениям формулы I для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой R1 и R1' независимо выбраны из H, CF3, NH2, метила, этила, F, Cl, Br, I и OH; или к их соли, или к любой из их стереоизомерных форм, или их смеси; при условии, что, по меньшей мере, один из R1 и R1' представляет собой отличающийся от H. Предпочтительными являются такие соединения формулы I, в которых R1 представляет собой CF3 и R1' представляет собой H.
Особо предпочтительными являются такие соединения формулы Ia
,
в которой R1 и R1' независимо выбраны из H, CF3, NH2, метила, этила, F, Cl, Br, I и OH; при условии, что, если R1 представляет собой H, тогда R1' отличается от H, и наоборот;
A представляет собой такие, как определено выше в любом из вариантов осуществления изобретения; или их соль, или любая из их стереоизомерных форм, или их смесь; для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками.
Также предпочтительными являются такие соединения формулы Ia, в которых R1' представляет собой H, и R1 выбирают из CF3, NH2, метила и этила; которые являются особо предпочтительными в случае, когда R1' представляет собой H, и R1 представляет собой CF3; для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками.
В соответствии с конкретным вариантом осуществления этого первого аспекта, в изобретении предлагаются соединения формулы Ia для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой
R1 и R1' независимо выбраны из H, CF3, NH2, метила, этила, F, Cl, Br, I и OH; при условии, что, когда R1 представляет собой H, тогда R1' отличается от H, и наоборот;
A представляет собой радикал одной из известных гетероциклических кольцевых систем с 1-2 кольцами, в которых каждое из колец, образующих кольцевую систему,
содержит 5-7 членов, каждый член независимо выбран из C, N, O, S, CH, CH2, NH;
представляет собой насыщенное, частично ненасыщенное или ароматическое кольцо;
при этом A замещен одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2;
или их соль или сольват, или любая из их стереоизомерных форм, или их смесь.
В соответствии с другим вариантом осуществления, в изобретении предлагаются соединения формулы Ia для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой R1 и R1' независимо выбраны из H, CF3, NH2, метила и этила; при условии, что, когда R1 представляет собой H, тогда R1' отличается от H, и наоборот;
A выбран из группы, состоящей из радикала пиримидина, пиридина, хинолина, имидазола, бензоимидазола и пиррола, где особо предпочтительными являются такие соединения, в которых A представляет собой радикал пиримидина;
при этом A замещен одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2;
или их соль, или любая из их стереоизомерных форм, или их смесь.
В соответствии с другим конкретным вариантом осуществления, в изобретении предлагаются соединения формулы Ia для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой
R1 и R1' независимо выбраны из H, CF3, NH2, метила и этила; при условии, что, по меньшей мере, один из R1 и R1' отличается от H; и
A представляет собой фенил, замещенный одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2; или их соль, или любая из их стереоизомерных форм, или их смесь.
В соответствии с другим конкретным вариантом осуществления, в изобретении предлагаются соединения формулы Ia для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками, в которой
R1 и R1' независимо выбраны из H, CF3, NH2, метила и этила; при условии, что, по меньшей мере, один из R1 и R1' отличается от H; и
A представляет собой прямой или разветвленный (C1-C6)алкил, предпочтительно выбранный из метила, этила, н-пропила, изо-пропила, н-бутила, изо-бутила, втор-бутила или н-пентила, который замещен одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, -CF3, -CH2CF3, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NH CH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -SO2N(CH2CH2CH2CH3)2 и -SO2N(CH2CH2(CH3)2)2; или их соль, или любая из их стереоизомерных форм, или их смесь.
В особо предпочтительном варианте осуществления этого первого аспекта, изобретение относится к соединениям формулы I, которые выбираются из:
N-пиримидин-2-ил-N'-[2-(трифторметил)фенил]гуанидина (1);
N-(4-этил-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (2);
N-(4-метил-6-пропилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (3);
N-(4-изопропил-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (4);
N-(4-бутил-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (5);
N-(4-трет-бутил-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (6);
N-(4,6-диаминопиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (7);
N-(4,6-дихлорпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (8);
N-(4,6-дифторпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (9);
N-[4-метил-6-(трифторметил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидина (10);
N-(4-циано-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (11);
N-(5-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (12);
N-(4-хлор-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (13);
N-(4-фтор-6-метилпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (14);
N-(4-фторпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (15);
N-(5-фторпиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (16);
N-[4,6-бис(трифторметил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидина (17);
N-(4,6-дицианопиримидин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (18);
N-пиридин-2-ил-N'-[2-(трифторметил)фенил]гуанидина (19);
N-пиридин-3-ил-N'-[2-(трифторметил)фенил]гуанидина (20);
N-пиридин-4-ил-N'-[2-(трифторметил)фенил]гуанидина (21);
N-пиримидин-4-ил-N'-[2-(трифторметил)фенил]гуанидина (22);
N-пиримидин-5-ил-N'-[2-(трифторметил)фенил]гуанидина (23);
N-(4,6-диметилпиридин-2-ил)-N'-[2-(трифторметил)фенил]гуанидина (24);
N-(3,5-диметилфенил)-N'-[2-(трифторметил)фенил]гуанидина (25);
N-(2,6-диметилпиридин-4-ил)-N'-[2-(трифторметил)фенил]гуанидина (26);
N-фенил-N'-[2-(трифторметил)фенил]гуанидина (27);
2-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диметилбензолсульфонамида (28);
2-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диэтилбензолсульфонамида (29);
2-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дипропилбензолсульфонамида (30);
2-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дибутилбензолсульфонамида (31);
3-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диметилбензолсульфонамида (32);
3-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диэтилбензолсульфонамида (33);
3-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дипропилбензолсульфонамида (34);
3-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дибутилбензолсульфонамида (35);
4-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диметилбензолсульфонамида (36);
4-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-диэтилбензолсульфонамида (37);
4-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дипропилбензолсульфонамида (38);
4-[(имино{[2-(трифторметил)фенил]амино}метил)амино]-N,N-дибутилбензолсульфонамида (39);
N-(2-нитрофенил)-N'-[2-(трифторметил)фенил]гуанидина (40);
N-(3-нитрофенил)-N'-[2-(трифторметил)фенил]гуанидина (41);
N-(4-нитрофенил)-N'-[2-(трифторметил)фенил]гуанидина (42);
N-2-тиенил-N'-[2-(трифторметил)фенил]гуанидина (43);
N-3-тиенил-N'-[2-(трифторметил)фенил]гуанидина (44);
N-1H-пиррол-2-ил-N'-[2-(трифторметил)фенил]гуанидина (45);
N-1H-пиррол-3-ил-N'-[2-(трифторметил)фенил]гуанидина (46);
N-2-фурил-N'-[2-(трифторметил)фенил]гуанидина (47);
N-3-фурил-N'-[2-(трифторметил)фенил]гуанидина (48);
N-1,3-оксазол-2-ил-N'-[2-(трифторметил)фенил]гуанидина (49);
N-1,3-тиазол-2-ил-N'-[2-(трифторметил)фенил]гуанидина (50);
N-1H-имидазол-2-ил-N'-[2-(трифторметил)фенил]гуанидина (51);
N-изоксазол-5-ил-N'-[2-(трифторметил)фенил]гуанидина (52);
N-1H-бензимидазол-2-ил-N'-[2-(трифторметил)фенил]гуанидина (53);
N-(3,4-диметилизоксазол-5-ил)-N'-[2-(трифторметил)фенил]гуанидина (54);
N-(2-аминофенил)-N'-(4,6-диметилпиримидин-2-ил)гуанидина (55);
N-(4,6-диметилпиримидин-2-ил)-N'-(3-этилфенил)гуанидина (56);
1-(4-(4-амино-2-метилхинолин-7-иламино)пиримидин-2-ил)-3-(2-(трифторметил)фенил)гуанидина (57);
N-(4-амино-2-метилхинолин-7-ил)-N'-[2-(трифторметил)фенил] гуанидина (58);
N-хинолин-7-ил-N'-[2-(трифторметил)фенил]гуанидина (59);
N-метил-N'-[2-(трифторметил)фенил]гуанидина (60);
N-этил-N'-[2-(трифторметил)фенил]гуанидина (61);
Н-пропил-N'-[2-(трифторметил)фенил]гуанидина (62);
N-бутил-N'-[2-(трифторметил)фенил]гуанидина (63);
N-(2-метилфенил)-N'-[2-(трифторметил)фенил]гуанидина (64) и
N-[4,6-бис(метил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидина (65).
Особо предпочтительные соединения формулы I представляют собой N-[4,6-бис(метил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидин (65), N-(3,5-диметилфенил)-N'-[2-(трифторметил)фенил]гуанидин (25), N-фенил-N'-[2-(трифторметил)фенил]гуанидин (27), N-(3-нитрофенил)-N'-[2-(трифторметил)фенил]гуанидин (41), N-[4-метил-6-(трифторметил)пиримидин-2-ил]-N'-[2-(трифторметил)фенил]гуанидин (10) и N-(2-метилфенил)-N'-[2-(трифторметил)фенил]гуанидин (64).
На всем протяжении настоящего описания под термином "лечение" подразумевается устранение, ослабление или нейтрализация причины, результатов воздействия или прогрессирования патологического состояния; и учитывается снижение скорости развития, прекращение скорости развития, нейтрализация патологического состояния, и излечение патологического состояния. Лечение как профилактическая мера (например, профилактика) также учитывается. Термин "лечение" включает комбинирование лечебных процедур и терапии медикаментами, при котором два или несколько лечебных процедур или медикаментов комбинируют, например, последовательно или одновременно. Примеры лечебных процедур и терапии медикаментами включают, но не ограничиваются только приведенными, химиотерапию (введение активных средств, включая, например, лекарства, антитела (например, как в случае иммунотерапии), пролекарства (например, как в случае фотодинамической терапии, GDEPT, ADEPT и др.); хирургическое вмешательство; лучевую терапию; и генную терапию. Для целей этого изобретения лечение включает, но не ограничивается только приведенным, облегчение, уменьшение интенсивности или устранение одного или нескольких симптомов патологического состояния; снижение распространения патологического состояния; стабилизацию (т.e. отсутствие усугубления) статуса патологического состояния; задержку или замедление прогрессирования патологического состояния; уменьшение интенсивности или временное облегчение статуса патологического состояния; и ремиссию патологического состояния (либо частичную, либо полную).
Как показано ниже, соединения формулы I представляют собой ингибиторы Rho GTPазного клеточного белка, а именно, Rac1 клеточного белка, которые пригодны для применения при лечении патологического состояния, опосредованного Rho GTPазным клеточным белком, предпочтительно, патологического состояния, опосредованного Rac1 клеточным белком.
Термин "заболевание, опосредованное Rac1 клеточным белком", при использовании в контексте данного описания, имеет отношение к патологическому состоянию, при котором Rac1 клеточный белок и/или действие Rac1 является важным или необходимым, например, для начала, развития, экспрессии и др. этого патологического состояния.
В связи с тем, что Rho-GTPазные киназы, как известно, играют центральную роль в клеточном цикле, и, в частности, это касается Rac1, то в предпочтительном варианте осуществления настоящего изобретения те заболевания, патологические состояния и/или нарушения, которые могут быть предотвращены, улучшены или вылечены с помощью соединений настоящего изобретения, представляют собой пролиферативные заболевания. При заболевании рассматривается получение положительного результата от снижения активности Rho-GTPазы, в частности, активности Rac1, в том случае, если снижение активности Rac1 составляет, по меньшей мере, 10%, предпочтительно, по меньшей мере, 20%, предпочтительно, по меньшей мере, 30%, что приводит к положительной динамике, по меньшей мере, одного клинического показателя этого заболевания. Примерами таких показателей являются скорость пролиферации, которая, предпочтительно, снижается, клеточная дифференцировка, которая, предпочтительно, стимулируется и др.
Дополнительное предпочтение также заключается в том, что пролиферативные заболевания выбираются из группы, состоящей из предракового состояния; дисплазии; метаплазии; карцином желудочно-кишечного или колоректального тракта, печени, поджелудочной железы, почек, мочевого пузыря, предстательной железы, эндометрия, яичников, семенников, меланомы, диспластической слизистой оболочки полости рта, инвазивных раковых заболеваний ротовой полости, мелкоклеточного и немелкоклеточного рака легких, гормонозависимого рака молочной железы, гормононезависимого рака молочной железы, переходноклеточного и плоскоклеточного рака, неврологических злокачественных опухолей, включая нейробластому, глиомы, глиобластому, астроцитомы, остеосарком, сарком мягких тканей, гемангиом, эндокринологических опухолей, опухолей кроветворной системы, включая лейкемии, лимфомы, и других миелопролиферативных и лимфопролиферативных заболеваний, карцином in situ, гиперпластических патологических изменений, аденом, фибром, гистиоцитозов, хронических воспалительных пролиферативных заболеваний, сосудистых пролиферативных заболеваний и индуцированных вирусами пролиферативных заболеваний, кожных заболеваний, характеризующихся гиперпролиферацией кератиноцитов и/или Т клеток. Особо предпочтительные заболевания, поддающиеся лечению соединениями настоящего изобретения, представляют собой глиобластому, колоректальный рак, рак яичников, рак предстательной железы и рак желудка, и аденокарциномы, более предпочтительны инвазивные аденокарциномы.
Таким образом, в настоящем изобретении также предлагаются активные соединения, которые представляют собой антипролиферативные средства. Термин "антипролиферативное средство", при использовании в настоящем описании, относится к соединению, которое лечит пролиферативное патологическое состояние (т.e., соединение, которое пригодно к использованию при лечении пролиферативного патологического состояния).
Термины "пролиферация клеток", "пролиферативное патологическое состояние", "пролиферативное нарушение" и "пролиферативное заболевание", используются поочередно в данном описании и имеют отношение к нежелательной или к неконтролируемой клеточной пролиферации излишних или аномальных клеток, которая неблагоприятна, к такой как, неопластический или гиперпластический нарост, будь то in vitro, или in vivo. Примеры пролиферативных патологических состояний включают, но не ограничиваются только здесь приведенными, доброкачественную, предраковую и злокачественную клеточную пролиферацию, и злокачественную опухолевую клеточную пролиферацию, включая, но не ограничиваясь только здесь приведенными, неоплазмы и опухолевые новообразования (например, гистиоцитома, глиома, астроцитома, остеома), злокачественные новообразования (например, рак легких, мелкоклеточный рак легких, рак желудочно-кишечного тракта, колоректальный рак, рак толстой кишки, карцинома молочной железы, карцинома яичника, рак предстательной железы, рак яичка, рак печени, рак почки, рак мочевого пузыря, рак поджелудочной железы, рак мозга, саркома, остеосаркома, саркома Капоши, меланома), лейкемии, псориаз, остеопатию, фибропролиферативные нарушения (например, соединительных тканей), и атеросклероз.
В качестве субъекта лечения может быть эукариотический организм, животное, позвоночное животное, млекопитающее, грызуны (например, морская свинка, хомяк, крыса, мышь), мышевидное животное (например, мышь), животное из семейства псовых (например, собака), животное из семейства кошачьих (например, кот), животное из семейства лошадиных (например, лошадь), примат, обезьяноподобное животное (например, мартышка или человекообразная обезьяна), макак (например, обезьяна-игрунка, павиан), человекообразная обезьяна (например, горилла, шимпанзе, орангутан, гиббон) или человек. Предпочтительно, когда субъектом для лечения является человек.
Кроме того, настоящее изобретение охватывает все возможные комбинации специфических и предпочтительных групп, вышеуказанных в данном описании.
Лечение, которому дано определение выше в данном описании, может применяться на практике как монотерапия или может включать, в дополнение к соединению изобретения, стандартное хирургическое вмешательство или лучевую терапию, или химиотерапию.
Также предлагается соединение формулы I для применения в лечении патологического состояния, опосредованного Rac1 клеточными белками, при этом лечение включает введение субъекту одновременно, последовательно или раздельно, по меньшей мере, одного соединения формулы I, как определено выше, и
i) одного или нескольких противоопухолевых препаратов, предпочтительно выбираемых из
гемцитабина, паклитаксела, доцетаксела, капецитабина, децитабина, карбоплатина, цисплатина, винорелбина, иринотекана, доксорубицина, дакарбазина, ритуксимаба или их производных;
ii) лучевую терапию;
iii) стандартное хирургическое вмешательство;
iv) или их смесей.
Далее, также предлагается способ лечения патологического состояния, опосредованного Rac1 клеточными белками, включающий введение одновременно, последовательно или раздельно в организм человека или животного, страдающего от такого патологического состояния, терапевтически эффективного количества, по меньшей мере, одного соединения формулы I, как определено выше, и
i) одного или нескольких противоопухолевых препаратов, предпочтительно выбираемых из
гемцитабина, паклитаксела, доцетаксела, капецитабина, децитабина, карбоплатина, цисплатина, винорелбина, иринотекана, доксорубицина, дакарбазина, ритуксимаба или их производных;
ii) лучевую терапию;
iii) стандартное хирургическое вмешательство;
iv) или их смесей.
Далее, предлагается применять комбинированный лекарственный препарат, включающий, по меньшей мере, одно соединение формулы I и
i) один или несколько противоопухолевых препаратов, предпочтительно выбираемых из
гемцитабина, паклитаксела, доцетаксела, капецитабина, децитабина, карбоплатина, цисплатина, винорелбина, иринотекана, доксорубицина, дакарбазина, ритуксимаба или их производных;
ii) лучевую терапию;
iii) стандартное хирургическое вмешательство;
iv) или их смесей;
для лечения патологического состояния, опосредованного Rac1 клеточными белками.
Альтернативно, предлагается соединение формулы I для применения в лечении патологического состояния, опосредованного Rac1 клеточными белками, в комбинированной терапии, которая включает применение соединения формулы I и
i) одного или нескольких противоопухолевых препаратов, предпочтительно выбираемых из
гемцитабина, паклитаксела, доцетаксела, капецитабина, децитабина, карбоплатина, цисплатина, винорелбина, иринотекана, доксорубицина, дакарбазина, ритуксимаба или их производных;
ii) лучевую терапию;
iii) стандартное хирургическое вмешательство;
iv) или их смесей.
Как указано выше, в настоящем изобретении также предлагаются новые соединения формулы II.
Отмечалось, что общая формула I охватывает такие соединения формулы II. Вследствие этого, соединения формулы II также пригодны для применения в лечении патологического состояния, опосредованного Rho GTPазными клеточными белками, в частности, Rac1 клеточными белками.
В соответствии с вариантом осуществления изобретения, предлагаются новые соединения формулы II, в которой A представляет собой фенил, замещенный одним или несколькими радикалами, выбранными из группы, состоящей из H, F, Cl, Br, I, нитро, циано, метила, этила, н-пропила, изо-пропила, н-бутила, трет-бутила, -CF3, -CH2CF3, прямого или разветвленного (C2-C6)алкенила, -OH, -OCH3, -OCH2CH3, -COH, -COCH3, -COOH, -COOCH3, -COOCH2CH3, -OC(O)H, -OC(O)CH3, -C(O)NH2, -NH2, -NHCH3, -N(CH3)2, -CH2NH2, -CH2NHCH3, -SH2, -SO-CH3, -SO2-CH3, -SO2NH2, -SO2NHCH3, -SO2NHCH2CH3, -SO2N(CH3)2, -SO2N(CH2CH3)2, -SO2N(CH2CH2CH3)2, -