Средства, улучшающие процесс обучения, памяти и когнитивные функции, а также для симптоматической терапии при аутистических расстройствах
Иллюстрации
Показать всеИзобретение относится к средству, обладающему ноотропной и антиаутистической активностью, представляющему собой тетразолсодержащее производное 4-амино-3-фенил-масляной кислоты формулы общей формулы (I):
в которой X=O, N, R2=Н, СН3, Х=O, R1=метил, этил, Н, X=N, R1=2-(пиридин-4-ил)этил, изопропил. Изобретение также относится к фармацевтической композиции, лекарственному средству и способу улучшения процессов обучения, памяти, когнитивных функций. Технический результат: получены средства, эффективные при лечении нарушений конгитивных функций, а также для симптоматической терапии при аутистических расстройствах. 4 н.п. ф-лы, 3 ил., 16 табл., 16 пр.
Реферат
Средства, улучшающие процесс обучения, памяти и когнитивные функции, а также для симптоматической терапии при аутистических расстройствах
Изобретение относится к области медицины, а именно к фармакологии и предназначено для улучшения процессов обучения, памяти, когнитивных функций у здоровых лиц и лиц с психическими дефицитными расстройствами, а также для лечения симптомов аутизма.
После того, как в центральной нервной системе (ЦНС) выявлено присутствие гамма-аминомасляной кислоты (ГАМК) и установлена ее роль в формировании нейромедиаторных процессов, было предложено использовать эту аминокислоту в качестве лечебного средства. В настоящее время существует спектр препаратов с ноотропным действием, в основе которого лежит влияние на ГАМК систему: оксибутират, пикамилон, никотинамид, фенибут и другие.
Известно, что ГАМК является основным ингибирующим нейромедиатором ЦНС млекопитающих. Действие ГАМК реализуется путем ее взаимодействия с ионотропными и метаботропными рецепторами, приводящего к их активации. Рецепторы ГАМК(А) и ГАМК(С) относятся к ионнотропным, а рецепторы ГАМК(В) к метаботропным. ГАМК и ее агонисты используются в качестве средств для лечения различных расстройств ЦНС. Термин агонист используется для обозначения веществ, активирующих клеточный сигналинг, т. е. агонист ГАМК действует посредством активации ГАМК-рецептора.
Особое место среди заболеваний ЦНС занимают аутистические расстройства, которые трудно поддаются лечению медикаментозными средствами. Аутизм является расстройством со сложной симптоматикой, обусловленной нарушением развития головного мозга. К числу основных симптомов заболевания относят задержку умственного развития, трудности в общении с другими людьми вербального и невербального характера, отсутствие друзей, ограниченность интересов, для людей с аутистическими расстройствами характерно стереотипное поведение и мышление, повторение одних и тех же движений. Часто люди, страдающие аутизмом, испытывают страхи, впадают в депрессию или в необъяснимый гнев; случаются приступы эпилепсии, нередко нарушается сон, возникают проблемы с функционированием желудочно-кишечного тракта (ЖКТ).
Для лечения людей с аутизмом применяют антидепрессанты и широкий спектр психотропных средств с целью снижения симптоматики и улучшения поведенческих реакций. Применение психотропных средств оказывает в определенных случаях положительное влияние на поведение больных, но вызывает побочное неблагоприятное действие. В целом современные лекарственные средства имеют ограниченное применение при аутистических расстройствах.
В патенте US 8278276 B2 /A61K31/195, A61K38/00, опубликован 02.10.2012г., в качестве средства для лечения аутизма и других расстройств, связанных с нарушением развития головного мозга предложены композиции, в состав которых входят агонисты ГАМК рецепторов. Например, баклофен (бета-(Аминометил)-4-хлорбензолпропановая кислота), который является агонистом ГАМК(В) рецепторов.
Композиция, содержащая баклофен, обладает способностью снижать выраженность симптомов или частоту их возникновения при аутистических расстройствах. Однако лечебное действие композиции проявлялось избирательно, и степень ее эффективности носила индивидуальный характер (прототип).
Задача, решаемая изобретением, сводится к созданию эффективного средства для симптоматической терапии аутистических расстройств, лишённого указанных недостатков. Технический результат заключается в повышении эффективности лечения нарушений когнитивных функции и расширении числа симптомов, устраняемых препаратом при аутистических состояниях.
Поставленная задача достигается посредством синтеза новых химических соединений тетразолсодержащих производных 4-амино-3-фенилмасляной кислоты формулы (I):
(I)
X = O, N
R2 = H, CH3
X=O, R1 = метил, изопропил, этил, H.
X =N, R1 = фенэтил, 2-(пиридин-4-ил)этил, бензил, бензилпиперазинил, изопропил.
Изобретение также относится к лекарственному средству для улучшения процессов обучения, памяти, когнитивных функций у здоровых лиц и лиц с психическими дефицитными расстройствами, для лечения симптомов аутизма в виде капсул, таблеток или инъекций в фармацевтически приемлемой упаковке, содержащему активное начало и фармацевтически приемлемый носитель, в котором в качестве активного начала содержит эффективное количество соединения формулы (I).
Изобретение также относится к способу улучшения процессов обучения, памяти, когнитивных функций у здоровых лиц и лиц с психическими дефицитными расстройствами, лечения симптомов аутизма, заключающийся во введении пациенту фармакологических средств, содержащих эффективные количества соединений формулы (I) в дозах 0,83-12,5 мг/кг массы тела (в пересчете из эффективной дозы на крысах 5-150 мг/кг массы тела) по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта.
Понятие «эффективное количество», используемое в данной заявке, подразумевает использование того количества соединений формулы (I), которое вместе с их показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной фармацевтической композиции или лекарственной форме.
При необходимости фармацевтические композиции могут содержать вспомогательные средства, такие как наполнители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, например, такие добавки могут быть выбраны из микроцеллюлозы, лактозы, стеарата кальция, крахмала. Выбор и соотношение указанных компонентов зависит от природы и способа назначения и дозировки.
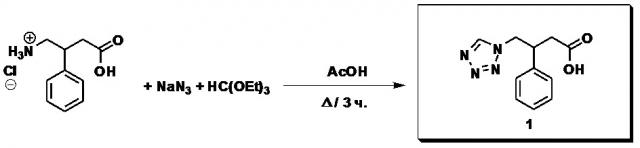
Методика получения соединений формулы (I) описана в статье (Sergey M. Putis, Elena S. Shuvalova, and Vladimir A. Ostrovskii. Tetrazole-containing derivatives of 4-amino-3-phenylbutanoic acid. // ARKIVOC. – 2009. – Vol. iv. – P. 64-68).
Новым в предлагаемом изобретении является то, что в качестве средств для улучшения процессов обучения, памяти, когнитивных функций у здоровых лиц и лиц с психическими дефицитными расстройствами, а также для лечения симптомов аутизма используется вновь синтезированные соединения на основе ГАМК тетразол-содержащих производных 4-амино-3-фенилмасляной кислоты. Для специалиста эти свойства явным образом не вытекают из уровня техники.
Для изучения фармакологической активности заявленных препаратов, проведены модельные эксперименты по выявлению у исследуемых соединений ноотропных свойств и способности снижать выраженность аутистических симптомов или частоту их возникновения.
Статистическую обработку экспериментальных данных проводили с помощью программы «Statistica V. 6.0.», используя однофакторный дисперсионный анализ; непараметрический анализ для независимых переменных (U-тест Манна-Уитни) и парный критерий Стьюдента для внутригрупповых сравнений.
Пригодность заявляемых препаратов подтверждена рядом экспериментальных данных.
Указанные соединения формулы (I) получены по следующей схеме 1 :
Схема 1
Сущность изобретения поясняется примерами конкретного выполнения и рисунками:
На Фиг.1 представлена нумерация отверстий пола актометра, где
1, 2, 3, 4 – угловые отверстия;
5, 6, 7, 8, 9, 10, 11, 12 – пристенные отверстия;
13,14, 15, 16 – отверстия в центре установки
На Фиг. 2 представлено число заглядываний в отверстия арены аутбредных мышей и мышей линии BALB/c, где * обозначено p<0,05 относительно группы «Аутбредные»
На Фиг. 3 - Влияние заявляемого соединения Т-001 на число заглядываний в отверстия арены мышей линии BALB/c, где # обозначено p<0,05 относительно группы «BALB/c»
Пример 1. 3-фенил-4-(1Н-тетразол-1-ил)бутановая кислота (T_001).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 12.23 (уш. с, 1Н, ОН), 9.01 (с, 1Н, НС5), 7.32 (m, 5Н, C6H5), 4.78 (m, 2H, СН2), 3.72 (квинтет, J 8.5, 1Н, СН), 2.74 (m, 2Н, СН2). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 172.4, 151.1, 140.0, 128.5, 127.7, 127.3, 51.9, 42.0, 37.5. ESI MS 233(M++1). Найдено, % C, 56.75; H, 5.28; N, 24.01. C11H12N4O2 (232). Вычислено, %: C, 56.89; H, 5.21; N, 24.12. ИК-спектр, ν, см-1: 3126, 2985, 2929, 1708, 1456, 1260, 1139, 1072, 1018, 981, 734.
Пример 2. Метил-4-(5-метил-1Н-тетразол-1-ил)-3-фенилбутанат (Т_002).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 7.40 (м, 5Н, C6H5), 3.40 (с, 3H, СН3О), 4.73 (м, 2Н, СН2), 3.69 (квинтет, J 8.5 Hz, 1Н, СН), 2.70 (м, 2H, СН2), 2.40 (s, 3Н, СН3-С5). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 171.5, 155.3, 142.1, 128.2, 127.6, 126.8, 52.3, 50.9, 42.1, 37.7. ESI MS 261 (M++1). Найдено, % C, 59.20; H, 6.53; N, 21.01. C13H16N4O2 (260). Вычислено, %: C, 59.99; H, 6.20; N, 21.52. ИК-спектр, ν, см-1: 2980, 2960, 1732, 1450, 1265, 1140, 1070, 1010, 980, 730, 700.
Пример 3. 3-фенил-N-(2-(пиридин-4-ил)этил-4-(1Н-тетразол-1-ил)бутанамид (Т_003).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 8.92 ( с, 1Н, НС5), 8.45 (дд, 2Н, J1 4.38, J2 1.53, СН2 N(пиридин), 7.32 (m, 5Н, C6H5), 7.24 (дд, 2Н, J1 4.38, J2 1.53, СН2 N(пиридин)), 4.82 (m, 2H, СН2), 3.74 (квинтет, J 8.5 Hz, 1Н, СН), 3.42 (м, 2Н, СН2), 2.78 (м, 2Н, СН2), 2.59 (м, 2Н, СН2), Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 171.9, 150.7, 149.2, 147.6, 143.2, 128.1, 127.2, 123.2, 52.1, 42.3, 40.8, 39.1, 34.7. ESI MS 337 (M++1). Найдено, % C, 64.01; H, 5.88; N, 24.91; C18H20N6O (336). Вычислено, %: C, 64.27; H, 5.99; N, 24.98;.
Пример 4. N-фенил-3-фенил-4-(1Н-тетразол-1ил)бутанамид (Т_004).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 8.84 ( с, 1Н, НС5),
7.31-7.05 (m, 10Н, арил), 4.85 (m, 2H, СН2), 3.67 (квинтет, J 8.5 Hz, 1Н, СН),
3.42 (м, 2Н, СН2), 3.34 (м, 2Н, СН2), 2.42 (м, 2Н, СН2). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 172.2, 151.2, 149.5, 148.2, 142.9, 128.1, 126.9, 123.4, 52.6, 43.1, 40.6, 39.5, 33.6. ESI MS 336 (M++1). Найдено, % C, 67.81; H, 6.12; N, 20.67; C19H21N5O (335). Вычислено, %: C, 68.04; H, 6.31; N, 20.88;.
Пример 5. N-изопропил-3-фенил-4-(1Н-тетразол-1-ил)бутанамид (Т_005).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 9.21 (с, 1Н, НС5), 7.45 (m, 5Н, C6H5), 4.69 (m, 2H, СН2), 3.92 (м, 1H, СН(СН3)2), 3.72 (квинтет, J 8.5, 1Н, СН), 2.74 (m, 2Н, СН2). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 168.7, 150.7, 143.2, 127.5, 126.7, 126.3, 52.9, 42.1, 41.9, 39.3, 22.7. ESI MS 274(M++1). Найдено, % C, 61.52; H, 7.01; N, 25.62. C14H19N5O (273). Вычислено, %: C, 61.29; H, 6.93; N, 25.02.
Пример 6. 4-(5-метил-1Н-тетразол-1-ил)-3-фенил-N-(2-(пиридин-4-ил)этил)бутанамид (Т_006).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 8.45 (дд, 2Н, J1 4.38, J2 1.53, СН2 N(пиридин)), 7.32 (m, 5Н, C6H5), 7.24 (дд, 2Н, J1 4.38, J2 1.53, СН2 N(пиридин)), 4.82 (m, 2H, СН2), 3.74 (квинтет, J 8.5 Hz, 1Н, СН), 3.42 (м, 2Н, СН2), 2.78 (м, 2Н, СН2), 2.59 (м, 2Н, СН2), 2.31 (с, 1Н, СН3). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 171.9, 150.7, 149.2, 147.6, 143.2, 128.1, 127.2, 123.2, 52.1, 42.3, 40.8, 39.1, 34.7, 10.8. ESI MS 351 (M++1). Найдено, % C, 64.91; H, 6.18; N, 23.61; C19H22N6O (350). Вычислено, %: C, 65.12; H, 6.33; N, 23.98.
Пример 7. 1-(4-бензилпиперазин-1-ил)-3-фенил-4-(1Н-тетразол-1-ил)бунан-1-он (Т_007).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 9.01 (с, 1Н, НС5), 7.31-7.05 (m, 10Н, арил), 4.92-4.81 (m, 2H, СН2), 3.52-3.37 (m, 2H, СН2, СН), 2.96 (m, 2H, СН2), 2.68 (m, 2H, СН2), 2.38 (m, 2H, СН2). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 167.3, 150.7, 143.4, 137.9, 128.8, 128.1, 127.6, 127.5, 127.3, 127.1, 61.9, 52.1, 51.6, 45.7, 43.1, 40.9, 36.4. ESI MS 391 (M++1). Найдено, % C, 67.41; H, 6.68; N, 21.41; C22H26N6O (390). Вычислено, %: C, 67.67; H, 6.71; N, 21.52.
Пример 8. этил-3-фенил-4-(1Н-тетразол-1-ил)бутанат (Т_008).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 12.23 (уш. с, 1Н, ОН), 9.01 (с, 1Н, НС5), 7.32 (m, 5Н, C6H5), 4.78 (m, 2H, СН2), 3.72 (квинтет, J 8.5, 1Н, СН), 2.74 (m, 2Н, СН2). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 172.4, 151.1, 140.0, 128.5, 127.7, 127.3, 51.9, 42.0, 37.5. ESI MS 233(M++1). Найдено, % C, 56.75; H, 5.28; N, 24.01. C11H12N4O2 (232). Вычислено, %: C, 56.89; H, 5.21; N, 24.12.
Пример 9. Этил-4(-5-метил-1Н-тетразол-1-ил)-3-финилбутанат (Т_009).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 7.40 (м, 5Н, C6H5), 3.40 (с, 3H, СН3О), 4.73 (м, 2Н, СН2), 3.69 (квинтет, J 8.5 Hz, 1Н, СН), 2.70 (м, 2H, СН2), 2.40 (s, 3Н, СН3-С5). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 171.5, 155.3, 142.1, 128.2, 127.6, 126.8, 52.3, 50.9, 42.1, 37.7. ESI MS 275 (M++1). Найдено, % C, 60.21; H, 6.57; N, 20.21. C14H18N4O2 (274). Вычислено, %: C, 61.30; H, 6.61; N, 20.42.
Пример 10. Метил-3-фенил-4(1Н-тетразол-1-ил)-бутанат (Т_010).
Спектр ЯМР 1H (400 MГц, DMSO-d6), δ м.д., J (Гц): 9.01 (с, 1Н, НС5), 7.40 (м, 5Н, C6H5), 3.40 (с, 3H, СН3О), 4.73 (м, 2Н, СН2), 3.69 (квинтет, J 8.5 Hz, 1Н, СН), 2.70 (м, 2H, СН2), 2.40 (s, 3Н, СН3-С5). Спектр ЯМР 13C (75 MГц, CDCl3), δ м.д.: 171.5, 155.3, 142.1, 128.2, 127.6, 126.8, 52.3, 50.9, 42.1, 37.7. ESI MS 245 (M++1). Найдено, % C, 58.40; H, 5.53; N, 22.67. C12H14N4O2 (246). Вычислено, %: C, 58.53; H, 5.73; N, 22.75.
Пример 11. Изучение влияния заявленных соединений на когнитивные функции у животных проведено в сертифицированной установке "Lafayette Instrument Co" (США), используемой как в России, так и за рубежом при изучении веществ, улучшающих когнитивные функции (Воронина, Островская, 2012, Chopin, 1992, Chopin, Briley, 1992, Voronina, 1994 и др.).
Об эффективности препаратов судили по результатам обучения условному рефлексу пассивного избегания (УРПИ) и амнезию этого рефлекса у крыс. Оценку заявленных соединений проводили в сравнительных исследованиях с препаратом-аналогом - фенибут (4-амино-3-фенилбутановая кислота).
Исследования проведены на белых беспородных половозрелых крысах самцах 2-3 месячного возраста массой 210 - 230 г. Животные содержались на постоянном доступе к корму и воде – предоставлялся полный рацион экструдированного брикетированного корма (ГОСТ на корм Р 50258-92) и питьевая вода. Животные содержались при температурном режиме 20-22 градуса по Цельсию, при световом цикле - 12 часов светлый и 12 часов темный периоды, в пластмассовых клетках Т/4А размером 580x375x200 мм, с верхней крышкой из нержавеющей стали с подстилкой обеспыленной из деревянной стружки по 8 крыс в каждой клетке. Опыты проводили в первую половину дня.
Крыс помещали на ярко освещенную платформу перед входом в темную камеру установки хвостом к входному отверстию и регистрировали латентное время рефлекса. Затем в темной камере крыса получала болевое неизбегаемое (закрытая дверь) раздражение электрическим током (0,2-0,З мА) 8 раз продолжительностью 0,2 сек. Тест на воспроизведение УРПИ осуществляли через 24 часа после обучения и проводили при повторном помещении животного в установку с регистрацией в течение 3 мин. латентного периода первого захода крысы в темную экспериментальную камеру, и количества животных, не зашедших в темный отсек камеры в процентах (%).
Для получения амнезии крысам сразу после обучения УРПИ накладывали на роговицы глаз корнеальные электроды и наносили максимальный электрический шок (МЭШ) - 250 V / 122 mА, 0,1 сек.
Для проведения эксперимента крысы были разделены на группы по 9-8 животных:
1 группа: Контроль без амнезии (интактный) физиологический раствор;
2 группа: Контроль с амнезией (с МЭШ) физиологический раствор;
3 группа: амнезия + заявляемое соединение Т-001 в дозе 5 мг/кг/внутрибрюшинно;
4 группа: амнезия +заявляемое соединение Т-001 в дозе 50 мг/кг/внутрибрюшинно;
5 группа: амнезия + заявляемое соединение Т-002 в дозе 5 мг/кг/внутрибрюшинно;
6 группа: амнезия +заявляемое соединение Т-002 в дозе 50 мг/кг/внутрибрюшинно;
7 группа: амнезия + заявляемое соединение Т-003 в дозе 5 мг/кг/внутрибрюшинно;
8 группа: амнезия +заявляемое соединение Т-003 в дозе 50 мг/кг/внутрибрюшинно;
9 группа: амнезия + заявляемое соединение Т-004 в дозе 5 мг/кг/внутрибрюшинно;
10 группа: амнезия +заявляемое соединение Т-004 в дозе 50 мг/кг/внутрибрюшинно;
11 группа: амнезия + заявляемое соединение Т-005 в дозе 5 мг/кг/внутрибрюшинно;
12 группа: амнезия +заявляемое соединение Т-005 в дозе 50 мг/кг/внутрибрюшинно;
13 группа: амнезия + заявляемое соединение Т-006 в дозе 5 мг/кг/внутрибрюшинно;
14 группа: амнезия +заявляемое соединение Т-006 в дозе 50 мг/кг/внутрибрюшинно;
15 группа: амнезия + заявляемое соединение Т-007 в дозе 5 мг/кг/внутрибрюшинно;
16 группа: амнезия +заявляемое соединение Т-007 в дозе 50 мг/кг/внутрибрюшинно;
17 группа: амнезия + заявляемое соединение Т-008 в дозе 5 мг/кг/внутрибрюшинно;
18 группа: амнезия +заявляемое соединение Т-008 в дозе 50 мг/кг/внутрибрюшинно;
19 группа: амнезия + заявляемое соединение Т-009 в дозе 5 мг/кг/внутрибрюшинно;
20 группа: амнезия +заявляемое соединение Т-009 в дозе 50 мг/кг/внутрибрюшинно;
21 группа: амнезия + заявляемое соединение Т-010 в дозе 5 мг/кг/внутрибрюшинно;
22 группа: амнезия +заявляемое соединение Т-010 в дозе 50 мг/кг/внутрибрюшинно;
23 группа: амнезия + Фенибут в дозе 50 мг/кг /внутрибрюшинно.
Вещества растворяли в физиологическом растворе с использованием ТВИН 80. Введение растворов осуществляли однократно за 40 минут до обучения внутрибрюшинно (в/б), из расчета 0,2 мл на 100 г массы тела.
При обучении крыс УРПИ показано, что животные интактного контроля и контроля с МЭШ при первом помещении на освещенную платформу заходили в темную камеру с коротким латентным периодом -14,88 ± 2,40 и 14,56 ± 2,11секунд соответственно (Табл. 1).
На фоне острого введения заявляемых соединений в дозе 5 мг/кг латентный период захода значительно не отличался от контрольных групп, а в дозе 50 мг/кг увеличивался с тенденцией к достоверности. Препарат сравнения фенибут в дозе 50 мг/кг в два раза увеличил время захода в темную камеру, статистически достоверно повышая этот показатель до 34,11 ± 8,83 секунд (Табл. 1).
Таким образом, животные контрольных групп при обучении, проявляя естественное желание избежать освещенной открытой подвесной платформы, осуществляли норковый рефлекс с коротким латентным периодом захода. Заявляемые соединения в дозе 50 мг/кг и фенибут в эквивалентной дозе увеличивали этот показатель в 2 раза, демонстрируя поведение, присущее для веществ с анксиолитической активностью.
При воспроизведении УРПИ через 24 часа после обучения крысы интактного контроля помнили об «опасной» темной камере и не заходили в нее в 100 % случаев. У животных, получивших МЭШ сразу после обучения, при вторичном помещении их на освещенную платформу уменьшался латентный период захода в темный отсек камеры установки до 116,11 ± 23,45 секунд (у интактного контроля 180,0 ± 23,45) и уменьшалось число крыс, воспроизводивших УРПИ до 33 % относительно контрольных значений - 100%. (Табл. 1).
Таким образом, МЭШ достоверно укорачивал длительность латентного периода захода в темную камеру при воспроизведении УРПИ и достоверно уменьшал число животных, не зашедших в темный отсек камеры при воспроизведении УРПИ, т.е. помнящих о нанесенном там накануне аверсивном стимуле. Полученные данные свидетельствуют о выраженном амнезирующем действии МЭШ (Табл. 1).
Таблица 1. Изучение влияния заявляемых соединений на УРПИ, вызванный МЭШ
| Обучение: | Воспроизведение через 24 часа: | |||
| Группа животного | Дозамг/кг | Латентный период первого захода, с | Латентное время рефлекса, с | Количество обучившихся животных |
| Контроль интактный | 14,88 ± 2,40 | 180,00 ± 0,00 | 100 | |
| Контроль с МЭШ | - | 14,56 ± 2,11 | 116,11 ± 15,45* | 33# |
| Заявляемое соединение Т-001 | 5 | 19,00 ± 4,06 | 136,22 ± 14,12 | 69& |
| Заявляемое соединение Т-001 | 50 | 30,22 ± 8,09$1 | 159,56 ± 11,26@ | 81& |
| Заявляемое соединение Т-002 | 5 | 17,01 ± 3,95 | 132,30 ± 23,11 | 67& |
| Заявляемое соединение Т-002 | 50 | 29,11 ± 7,94$1 | 151,32 ± 12,10$2 | 77& |
| Заявляемое соединение Т-003 | 5 | 18,10 ± 4,35 | 133,79 ± 18,45 | 68& |
| Заявляемое соединение Т-003 | 50 | 29,87 ± 7,89$1 | 154,56 ± 13,26$2 | 78& |
| Заявляемое соединение Т-004 | 5 | 17,54 ± 2,67 | 134,34 ± 17,89 | 66& |
| Заявляемое соединение Т-004 | 50 | 27,98 ± 6,23$1 | 153,98 ± 10,37$2 | 76& |
| Заявляемое соединение Т-005 | 5 | 18,89 ± 3,78 | 135,02 ± 17,53 | 69& |
| Заявляемое соединение Т-005 | 50 | 29,68 ± 9,10$1 | 154,90 ± 12,45$2 | 77& |
| Заявляемое соединение Т-006 | 5 | 17,97 ± 2,02 | 133,89 ± 16,10 | 68& |
| Заявляемое соединение Т-006 | 50 | 28,03 ± 7,78$1 | 156,09 ± 14,00$2 | 79& |
| Заявляемое соединение Т-007 | 5 | 18,90 ± 3,32 | 131,92 ± 13,04 | 66& |
| Заявляемое соединение Т-007 | 50 | 29,99 ± 8,11$1 | 155,78 ± 14,44$2 | 75& |
| Заявляемое соединение Т-008 | 5 | 17,87 ± 3,98 | 133,86 ± 16,13 | 67& |
| Заявляемое соединение Т-008 | 50 | 28,88 ± 8,10$1 | 156,16 ± 13,34$2 | 77& |
| Заявляемое соединение Т-009 | 5 | 18,92 ± 2,12 | 132,12 ± 12,12 | 66& |
| Заявляемое соединение Т-009 | 50 | 29,94 ± 7,91$1 | 154,37 ± 14,11$2 | 78& |
| Заявляемое соединение Т-010 | 5 | 17,78 ± 2,15 | 133,35 ± 12,56 | 65& |
| Заявляемое соединение Т-010 | 50 | 30,00 ± 8,29$1 | 154,66 ± 13,45$2 | 76& |
| Фенибут | 50 | 34,11 ± 8,83@ | 115,00 ± 25,13 | 55 |
*-достоверность отличий от интактного контроля, при Р≤0,05 (t-критерий
Стьюдента);
# - достоверность отличий от интактного контроля, при Р≤0,05 (критерий
Фишера);
& - достоверность отличий от контроля с МЭШ, при Р≤0,05 (критерий %2);
$ - тенденция к достоверности отличий от контроля с МЭШ, при Р≤0,1
(критерий Крускала-Уоллиса); $1- Р=0,083, $2 - Р=0,073.
@ - достоверность отличий от контроля с МЭШ, при Р≤0,05 (критерий
Крускала-Уоллиса).
Заявляемые соединения в дозе 5 мг/кг при воспроизведении УРПИ увеличивали латентное время рефлекса до 131,92 – 136,22 секунд и количество животных, воспроизводивших рефлекс до 65-69 % (Табл. 1).
При воспроизведении УРПИ заявляемые соединения в дозе 50 мг/кг значительно уменьшали амнезирующее действие МЭШ, увеличивая латентное время рефлекса до 151,32 - 159,56 с. и количество крыс, воспроизводивших его до 75-81 %. (Табл. 1).
При повторном предъявлении темной «опасной» камеры животным, однократно получившим до обучения фенибут в дозе 50 мг/кг, регистрировалось незначительное увеличение обучившихся навыку крыс до 55 %, но при этом латентный период рефлекса не отличался от значения контрольной группы с МЭШ (Табл. 1).
Таким образом, выполненные исследования показали, что в тесте амнезии УРПИ, вызванной МЭШ, у крыс в установке "Lafayette Instrument Co" (США) заявляемые соединения оказывают антиамнестическое действие в дозе 5 мг/кг и особенно усиленное в дозе 50 мг/кг, что выражается в статистически достоверном увеличении процента животных без амнезии, хорошо помнящих о ситуации и не заходящих в темный «опасный» отсек камеры, где они ранее получали болевое раздражение. Препарат сравнения фенибут в дозе 50 мг/кг незначительно ослабляет амнезию УРПИ, вызванную МЭШ, и уступает по антиамнестическому эффекту заявляемым соединениям.
Проведенные исследования позволяют предположить наличие у заявляемых соединений и Фенибута в дозе 50 мг/кг анксиолитического действия, о чем свидетельствует способность веществ увеличивать латентное время захода в темную камеру с ярко освещенной платформы при обучении рефлекса.
Таким образом, по антиамнестической активности изученные соединения в исследуемых дозах можно расположить в следующей последовательности: заявляемые соединения (50 мг/кг) > заявляемые соединения (5 мг/кг) > Фенибут (50 мг/кг), а по анксиолитической Фенибут (50 мг/кг) > заявляемые соединения (50 мг/кг).
На основании проведенных исследовании был предложен способ улучшения процессов обучения, памяти, когнитивных функций у здоровых лиц и лиц с психическими дефицитными расстройствами, заключающийся во введении пациенту фармакологических средств, содержащих эффективное количество соединений формулы (I) в дозах 0,83-8,33 мг/кг массы тела по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта. Расчет эквивалентных доз для человека проводили в соответствии с Руководством по проведению доклинических исследований лекарственных средств (Часть первая. -М.: Гриф и К, 2012. -944).
Пример 12.
Аутизм диагностируется наличием нескольких критериев, в числе которых:
1. Нарушение социального взаимодействия;
2. Дефицит общения;
3. Стереотипное, повторяющееся поведение, настойчивое требование постоянных, одинаковых условий;
4. Ограниченность интересов;
5. Повышенная тревожность и др.
На основе этих представлений разработаны специальные экспериментальные модели аутизма у животных, позволяющие воспроизвести нарушения ЦНС в эксперименте, а именно на мышах.
Изучение фармакологической активности заявляемых соединений проведено посредством исследования его влияния на аномалии поведения при аутистических расстройствах с использованием специальных экспериментальных моделей аутизма у мышей линии BALB/С, которые широко используются в зарубежных исследованиях (Bielsky et al. 2004; Bielsky, Young 2004; Brodkin 2007; Crawley et al. 2007; Chadman et al. 2008; Roullet and Crawley, 2011; Moy et al. 2004, 2007, 2008; Nadler et.al., 2004; Kwon et al. 2006; Moon J. et al., 2008 и другие) и позволяют оценить такие проявления аутистических состояний, как нарушение социального взаимодействия, дефицит общения, стереотипное, повторяющееся поведение, настойчивое требование постоянных, одинаковых условий, ограниченность интересов, повышенную тревожность и другие. Поскольку подобное поведение характерно для мышей линии BALB/c, именно эта линия животных использовалась в эксперименте для оценки влияния веществ на нарушения ЦНС при аутистических расстройствах.
Изучено влияние заявляемых соединений на обучение пространственному навыку мышей линии BALB/c и на поведение животных после пространственной «сшибки» (переобучения) в водном лабиринте Морриса.
Зацикленное, повторяющееся, стереотипное поведение, активности, ненаправленный на получение конкретного результата являются характерными проявлениями аутизма (South et al. 2005; Roullet and Crawley, 2010). Повторяющееся, стереотипное поведение у мышей включает вращательные движения, повороты назад, повторяющееся обнюхивание одних и тех же мест в пространстве или объектов, а также чрезмерный грумминг и повышенную нецеленаправленную двигательную активность (Crawley 2007b; Moy et al. 2008).
Повторяющееся зацикленное поведение мышей линии BALB/c выявляется в неспособности животных принять решение и осуществить правильное пространственное движение при смене локализации платформы при переобучении в водном лабиринте (Moy et al. 2008).
Эксперимент проводили на мышах-самцах линии BALB/c возрастом 5-7 недель массой 13-15 г. Животные содержались на постоянном доступе к корму и воде – предоставлялся полный рацион экструдированного брикетированного корма (ГОСТ на корм Р 50258-92) и питьевая вода; при температурном режиме 20-22°С, при световом режиме – 12 часов свет/12 часов темнота; в полипропиленовых клетках с решеткой из цинкохромовой стали, с обеспыленной подстилкой из деревянной стружки по 10 мышей в каждой клетке (Т/3С).
Заявляемые соединения использовали в дозах 100 мг/кг и 150 мг/кг. Суспензию соединения готовили с использованием Твина-80. Навеску соединения растирали с каплей Твина-80 и затем добавляли необходимое количество дистиллированной воды.
Заявляемые соединения вводили внутрь (внутрижелудочно) при помощи специального зонда в объеме 0,1 мл на 10 г массы мыши. Контрольным животным вводили внутрь (внутрижелудочно) суспензию с Твином-80 в объеме 0,1 мл на 10 г массы мыши.
Соединения (опытные группы) или суспензию с Твином-80 (контрольные группы) вводили за 40 минут до начала эксперимента.
В настоящем исследовании для оценки влияния заявляемых соединений на аутичные проявления использовалась методика, предложенная Moy SS, Nadler JJ, Young NB et al. (2007). Изучалось влияние соединений на процесс обучения пространственному навыку и на способность осуществить новое пространственное движение при переобучении в водном лабиринте.
Исследование проводили в водном лабиринте Морриса. Лабиринт Морриса представляет собой круглый бассейн диаметром 122 см, глубиной 25 см, заполненный водой температурой 20-22°С. В бассейн помещали круглую платформу диаметром 12 см. Центр платформы располагали на расстоянии 30 см от краев бассейна.
Сначала у мышей проводили предварительное обучение навыку находить платформу в водном лабиринте и воспроизводить этот пространственный навык. А затем животным предъявляли новое местоположение платформы и таким образом осуществляли пространственную «сшибку». При переобучении – смене локализации платформы в водном лабиринте – животные должны принять новое решение и осуществить правильное пространственное движение.
1 этап – отбор животных для эксперимента.
До начала эксперимента проводят отбор животных, пригодных для обучения. Для этого платформу располагают на 0,5 см выше уровня воды. Мышь помещают на платформу на 20 секунд.
Затем мышь опускают в воду на противоположной стороне бассейна и позволяют в течение 60 секунд найти платформу и взобраться на нее, где оставляют животное на 20 секунд. Процесс повторяют, опуская мышь в воду с другой, отличной от первой попытки, стороны бассейна.
Если животное не в состоянии самостоятельно найти платформу в течение 60 секунд, экспериментатор помогает ему переместиться к платформе и взобраться на нее. Если животное не может самостоятельно найти платформу в двух попытках подряд, то оно исключается из опыта.
2 этап. Обучение животных пространственному навыку.
В течение 2-х последующих дней платформа располагается на 0,5 см ниже уровня воды. Ежедневно животным предоставляют по 4 попытки найти платформу в течение 60 секунд. Интервал между попытками составляет 20 секунд, в течение которого они находятся на платформе. Каждый день перед первой попыткой животное на 20 секунд помещают на платформу.
Регистрируют время, прошедшее от момента спуска животного в воду до влезания на платформу, и количество результативных попыток поиска платформы. Животных опускают в воду в 3-х различных точках на половине бассейна, противоположной по отношению к платформе.
3-й этап. Воспроизведение пространственного навыка.
Через 48 часов после второго дня обучения оценивают воспроизведение пространственного навыка: платформу убирают и животных однократно помещают в бассейн на 60 секунд.
Регистрируют время, в течение которого животное находится в квадранте, где в дни обучения располагалась платформа, что служит показателем эффективности обучения и воспроизведения пространственного навыка.
4-й этап. Сшибка пространственного навыка – переобучение.
На следующий день после воспроизведения пространственного навыка платформа, находящаяся ниже уровня воды на 0,5 см при обучении, перемещается в область, диагонально противоположную прежнему её местоположению. Процедура обучения и воспроизведения повторяется по описанной выше схеме.
Влияние заявляемых соединений на обучение и воспроизведение пространственного навыка мышами линии BALB/c в водном лабиринте Морриса
В первый день обучения в водном лабиринте мышей линии BALB/c заявляемые соединения в дозах 100 мг/кг и 150 мг/кг достоверно увеличивали время поиска платформы соответственно на 17,3 % и 14,6 % и снижали количество результативных попыток поиска платформы соответственно в 3,2 и 2,7 раза по сравнению с контрольной группой (Табл. 2). Полученные данные свидетельствуют о негативном влиянии изучаемых соединений на кратковременную память.
Во второй день обучения поведение животных, которым вводились изучаемые соединения в дозах 100 и 150 мг/кг, не отличалось от поведения контрольных мышей. Однако были зафиксированы следующие особенности: если для контрольной группы время поиска платформы было на 11,4 % больше, чем в первый день, то при введении мышам соединений в дозах 100 и 150 мг/кг оно, наоборот, сократилось соответственно на 10,1 % и 10,2 % при сравнении с первым днем обучения. Но эти отличия не являются достоверными.
При воспроизведении пространственного навыка через 48 часов после обучения заявляемые соединения в дозе 150 мг/кг статистически достоверно увеличивали время пребывания в квадранте, где при обучении находилась арена, на 88-90 % (Табл. 2).
Продолжительность нахождения в данном квадранте животных, которым вводили изучаемые соединения в дозе 100 мг/кг, не отличалась от показателя группы контрольных животных (Табл. 2).
Таблица 2 – Влияние заявляемых соединений на обучение и воспроизведение пространственного навыка в водном лабиринте Морриса мышами линии BALB/c (M ± m, n=15)
| Группы | Обучение | Воспроизведение | |||
| Время поиска платформы, сек | Количество результативных попыток, ед. | Время нахождения в квадранте платформы, сек | |||
| 1 день | 2 день | 1 день | 2 день | ||
| Контроль | 48,1 ± 2,7 | 53,6 ± 1,7 | 1,9 ± 0,4 | 1,0 ± 0,2 | 9,2 ± 1,8 |
| Заявляемое соединение Т-001,100 мг/кг | 56,4 ± 1,3* | 50,7 ± 2,7 | 0,6 ± 0,2* | 1,3 ± 0,3 | 10,3 ± 2,1 |
| Заявляемое соединение Т-001, 150 мг/кг | 55,1 ± 1,7* | 49,5 ± 2,9 | 0,7 ± 0,2* | 1,3 ± 0,3 | 17,5 ± 3,6* |
| Заявляемое соединение Т-002,100 мг/кг | 56,2 ± 1,4* | 50,9 ± 2,8 | 0,5 ± 0,3* | 1,4 ± 0,4 | 10,9 ± 1,9 |
| Заявляемое соединение Т-002 150 мг/кг | 54,9 ± 1,6* | 49,8 ± 2,6 | 0,6 ± 0,1* | 1,3 ± 0,2 | 17,8 ± 3,3* |
| Заявляемое соединение Т-003,100 мг/кг | 55,7 ± 1,5* | 51,0 ± 2,5 | 0,5 ± 0,2* | 1,2 ± 0,2 | 11,0 ± 2,6 |
| Заявляемое соединение Т-003, 150 мг/кг | 55,3 ± 1,6* | 49,9 ± 3,0 | 0,6 ± 0,1* | 1,2 ± 0,3 | 17,1 ± 4,0* |
| Заявляемое соединение Т-004,100 мг/кг | 56,8 ± 1,2* | 50,2 ± 2,4 | 0,6 ± 0,3* |