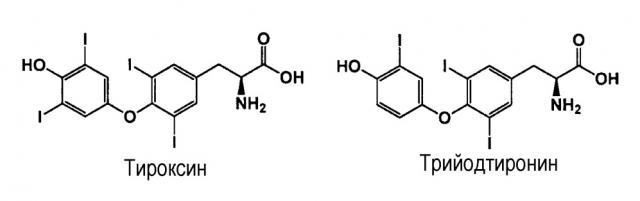
Композиции и способы диагностики и лечения гипертиреоза у животных-компаньонов
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, конкретно к маркерам гипертиреоза, и может быть использовано в медицине для диагностики гипертиреоза у кошки. Способ диагностики гипертиреоза у кошки включает: (a) определение уровня нуклеиновой кислоты, кодирующей пептид натрий-йодного симпортера кошки с SEQ ID NO: 2, в биологическом образце кошки; и (b) сравнение уровня нуклеиновой кислоты с референсным уровнем указанной нуклеиновой кислоты, определенным у контрольных кошек без гипертиреоза, где биологический образец содержит ткань, клетку или биологическую жидкость, содержащую ДНК или РНК. При этом повышенный уровень указанной нуклеиновой кислоты в образце от кошки по сравнению с референсным уровнем является диагностическим для гипертиреоза у кошки. Настоящее изобретение позволяет повысить эффективность диагностики гипертиреоза кошки. 6 н. и 2 з.п. ф-лы, 2 табл., 12 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет по предварительной заявке США № 61/577373, зарегистрированной 19 декабря 2011 года, включенной в настоящее описание в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выделенной молекуле ДНК, кодирующей часть белка NIS кошек, а также применению этого фрагмента гена в способах получения пищевых композиций для животных, подходящих для введения животным-компаньонам из семейства кошачьих, страдающих гипертиреозом, а также композициям и способам лечения гипертиреоза у животных-компаньонов из семейства кошачьих.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка включает список последовательностей, поданный с помощью EFS-Web и включенный, таким образом, в настоящее описание в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 15 декабря 2011 года, названа 9344P-00-HL_Sequence_Listing_ST25.txt и имеет размер 3 KB.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Гипертиреоз является относительно распространенным эндокринным нарушением, в частности, преобладающим у пожилых кошек. Он является опасным состоянием здоровья, являющимся результатом гиперпластического роста тиреоидной ткани и гиперпродукции тиреоидного гормона. Общепринятые способы лечения гипертиреоза включают постоянное введение антитиреоидного лекарственного средства, хирургическое удаление щитовидной железы и/или терапию радиоактивным йодом. Эти способы лечения являются дорогостоящими и имеют ограничения и побочные эффекты. Например, т.к. большинство антитиреоидных лекарственных средств вводят перорально, соблюдение режима лечения часто нарушается. Для хирургического вмешательства необходима анестезия, и это часто невозможно для пожилых кошек, в частности, кошек, страдающих также и другими заболеваниями. Терапия радиоактивным йодом доступна только в учреждениях, лицензированных для использования радиоактивных материалом, и для нее необходима госпитализация кошек до тех пор, пока их уровни радиоактивности не станут безопасными.
Т.к. для продукции тиреоидного гормона необходим поступающий с пищей йод, разрабатывают способы лечения гипертиреоза у кошек, включающие кормовые рационы с ограниченным содержанием йода. Желательно дополнять такие рационы с ограниченным содержанием йода ингредиентами, снижающими захват йода щитовидной железой, и ингредиентами, ингибирующими синтез тиреоидного гормона.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и реагентам для определения пищевых ингредиентов, снижающих захват йода щитовидной железой и ингибирующих синтез тиреоидного гормона. Способы, представленные в настоящем описании, включают использование выделенного фрагмента гена, кодирующего часть натрий-йодного симпортерного белка кошек (белка NIS), для получения данных профиля экспрессии гена в присутствии и отсутствие тестовых материалов. Используя эти способы, можно определять материалы, которые можно включать в рацион кошки, страдающей гипертиреозом, для лечения этого состояния.
Настоящее изобретение относится к выделенному фрагменту гена, кодирующему часть натрий-йодного симпортерного белка кошек (белка NIS), имеющему нуклеотидную последовательность SEQ ID NO:1 и кодирующему пептид, имеющий аминокислотную последовательность SEQ ID NO:2.
Настоящее изобретение также относится к рекомбинантным векторам и трансформированным клеткам, содержащим выделенный фрагмент гена NIS кошек. Настоящее изобретение также относится к способам, включающим использование таких выделенных молекул ДНК для определения профилей экспрессии гена для гена NIS кошек у здоровых и больных животных и измерения профилей экспрессии гена NIS в присутствии и отсутствие пищевых ингредиентов и их экстрактов для получения пищевых композиций для животных, подходящих для введения животным-компаньонам из семейства кошачьих, страдающим гипертиреозом. Настоящее изобретение также относится к композициям и способам лечения гипертиреоза у кошек.
Настоящее изобретение также относится к способу получения корма для домашних животных, подходящего для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом, включающему: (a) осуществление доступа по меньшей мере к одной первой базе данных, содержащей первый набор данных, относящий функциональный профиль гена в образце биологической жидкости или ткани животного к физиологическому состоянию и, необязательно, генотипу животного, где функциональный профиль гена является функциональным профилем гена NIS кошек, (b) осуществление доступа по меньшей мере к одной второй базе данных, содержащей второй набор данных, относящийся к эффектам биоактивных компонентов рациона на функциональный профиль гена из этапа (a); (c) обработку исходных данных, определяющих физиологическое состояние и, необязательно, генотип субпопуляции, например, кошек, страдающих гипертиреозом, с помощью первого алгоритма, использующего первый и второй наборы данных, для получения пищевого состава, применимого для выбора и получения пищевой композиции для этой субпопуляции животных; и (d) получение пищевой композиции на основе пищевого состава, где эта пищевая композиция подходит для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом.
В определенных аспектах этого варианта изобретения первый набор данных получают из образцов, собранных от множества отдельных животных, представляющих диапазон генотипов и физиологических состояний, включающих животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В одном из аспектов каждый такой образец от отдельного животного связан с записью о происхождении, содержащей зоографические данные отдельного животного, относящиеся к определению генотипа и физиологического состояния, на момент забора образца. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к генотипу, выбранных из группы, состоящей из породы, пород родителей, родословной, пола, типа шерстного покрова и очевидных наследственных состояний и нарушений, в частности, гипертиреоза. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к физиологическому состоянию, выбранному из группы, состоящей из возраста, массы, ветеринарного анамнеза, репродуктивного анамнеза, состояния здоровья в настоящее время или состояния заболевания, аппетита, уровня физической активности, умственной деятельности, поведенческих аномалий и характера, и, в частности, наличия и степени гипертиреоза.
В конкретном аспекте этого способа первый набор данных содержит данные, относящиеся к анализу образца в отношении одного или нескольких компонентов, выбранных из группы, состоящей из ДНК, РНК, белков, метаболитов в качестве биомаркеров, в то время как второй набор данных получают при контролируемых экспериментах, включающих подвергание модели на животных воздействию различных уровней одного или нескольких биоактивных компонентов рациона.
Настоящее изобретение также относится к композициям и способам диагностики гипертиреоза у кошек, а также способам определения материалов и составления пищевых композиций, содержащих эти материалы, которые будут применимыми для лечения гипертиреоза у кошек.
В другом конкретном аспекте этого способа исходные данные содержат зоографические данные, относящиеся к определению генотипа и физиологического состояния животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В другом аспекте этого способа исходные данные содержат аналитические данные для образца биологической жидкости или ткани, полученного от животных-компаньонов из семейства кошачьих, не страдающих гипертиреозом. В других конкретных аспектах этого способа исходные данные содержат аналитические данные для образца биологической жидкости или ткани, полученного от животных-компаньонов из семейства кошачьих, страдающих легким гипертиреозом, а также от животных-компаньонов из семейства кошачьих, страдающих тяжелым гипертиреозом.
Настоящее изобретение также относится к пищевым композициям для животных, полученным указанным выше способом, для получения корма для домашних животных, иллюстративные примеры которого представлены в настоящем описании ниже, применимого для введения животным-компаньонам из семейства кошачьих, страдающим гипертиреозом.
Таким образом, настоящее изобретение относится к способам рационального получения рациона для животного, страдающего заболеванием или состоянием, включающим определение биоактивных компонентов рациона, применимых в снижении эффектов заболевания или состояния, которым страдает животное. В конкретном иллюстративном аспекте этого варианта осуществления заболеванием или состоянием является гипертиреоз, а страдающим животным является животное-компаньон из семейства кошачьих.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В другом варианте осуществления настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В конкретных аспектах этих вариантов осуществления животное-компаньон с гипертиреозом, нуждающееся в лечении, кормят пищевой композицией для домашних животных, содержащей эффективное количество биоактивного компонента рациона, достаточное для подавления экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или их обоих, в качестве неограничивающих примеров, таких как активность гена NIS кошек, представленного в настоящем описании.
В определенных вариантах осуществления полипептид, ингибируемый биоактивными компонентами рациона, выбран из группы, состоящей из тиреоидной пероксидазы, натрий-йодного симпортера (NIS), тиреоидной оксидазы, интратиреоидной 5'-дейодиназы типа I, рецептора тиреотропного гормона, пендрина, монокарбоксилат-транспортера 8 и их комбинаций.
Настоящее изобретение также относится к способу составления рациона, подходящего для лечения заболевания или состояния у животного.
Дополнительные области применения настоящего изобретения станут очевидными из подробного описания, представленного далее в настоящем описании. Следует понимать, что, хотя в подробном описании и конкретных примерах указан предпочтительный вариант осуществления изобретения, они предназначены исключительно для иллюстративных целей, а не для ограничения объема изобретения.
Дополнительные варианты осуществления и цели настоящего изобретения будут очевидны специалистам в этой области.
В другом варианте осуществления изобретение относится к способу лечения гипертиреоза у нуждающейся в этом кошки, включающему диагностику наличия гипертиреоза, например, с использованием описываемых выше способов, и контроль состояния, например, исключительно с помощью рациона или в комбинации с соответствующим лекарственным средством. В одном из аспектов этого варианта осуществления рацион включает один или несколько компонентов, определяемых способами, представленными в настоящем описании, применимых для снижения захвата йода щитовидной железой или для ингибирования синтеза тиреоидного гормона, включая, в том числе, компоненты, способные подавлять или ингибировать экспрессию гена NIS или снижать или ингибировать функцию белка NIS.
В дополнительном варианте осуществления изобретение относится к реагентам, необязательно меченым, применимым в определении уровня экспрессии биомаркера NIS у кошки. Такие реагенты могут включать, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие белок NIS кошек, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие пептид SEQ ID NO:2. Другие такие реагенты включают аптамеры, например, аптамеры нуклеиновых кислот или пептидные аптамеры, распознающие или избирательно распознающие белок NIS кошек или пептид SEQ ID NO:2, а также олигонуклеотидные зонды, способные избирательно гибридизоваться с геном NIS кошек или нуклеотидной последовательностью SEQ ID NO:1.
В дополнительном варианте осуществления настоящее изобретение относится к набору для диагностики, прогнозирования или мониторинга гипертиреоза у кошки, содержащему средства для измерения экспрессии гена NIS кошек в биологическом образце от кошки и инструкции по использованию таких средств для измерения экспрессии гена NIS в биологическом образце от кошки и оценки наличия процесса, приводящего к гипертиреозу у кошки. Набор предназначен для измерения одного или нескольких биомаркеров с помощью одного или нескольких нуклеиновых кислот-зондов, с помощью которых можно определять экспрессию гена NIS, способных избирательно гибридизоваться с нуклеиновой кислотой SEQ ID NO:1 в строгих условиях.
В других аспектах этих вариантов изобретения средствами для измерения одного или нескольких биомаркеров являются одно или несколько антител, с помощью которых можно определять экспрессию гена NIS посредством избирательного распознавания экспрессируемого белка NIS или посредством избирательного распознавания пептида SEQ ID NO:2. Такие наборы могут находиться в формате ELISA, содержащем антитело, с помощью которого можно определять белок NIS, включая выделенный, очищенный или рекомбинантный белок NIS, соответствующий экспрессируемому белку или пептидной последовательности SEQ ID NO:2, и буфер.
В других аспектах этого варианта осуществления средствами для измерения биомаркера NIS являются один или несколько аптамеров, например, как представлено в настоящем описании выше, с помощью которых можно определять экспрессию гена, кодирующего белок NIS, или посредством распознавания экспрессируемого белка NIS.
Дополнительные области применения настоящего изобретения станут очевидными из подробного описания, представленного далее в настоящем описании. Следует понимать, что, хотя в подробном описании и конкретных примерах указан предпочтительный вариант осуществления изобретения, они предназначены исключительно для иллюстративных целей, а не для ограничения объема изобретения.
ПОДРОБНОЕ ОПИСАНИЕ
Следующее описание предпочтительных вариантов осуществления носит исключительно иллюстративный характер и никоим образом не предназначено для ограничения изобретения или его применения.
Определения
Как применяют в настоящем описании и формуле изобретения, термины в единственном числе включают множественное число, если контекст четко не указывает на иное, например, упоминание "варианта" включает множество вариантов. Кроме того, определенные термины включают варианты терминов, используемые в соответствующем грамматическом контексте, например, термин "специфически связывается" включает "специфическое связывание" и другие формы термина. Аналогично, слова "содержат", "содержит" и "содержащий" следует интерпретировать включительно, а не исключительно.
Термин "антитело" означает любой иммуноглобулин, связывающийся с конкретным антигеном, включающий антитела IgG, IgM, IgA, IgD и IgE. Термин включает поликлональные, моноклональные, моновалентные, гуманизированные антитела, гетероконъюгат, композиции антител с полиэпитопной специфичностью, химерные, биспецифические антитела, диатела, одноцепочечные антитела и фрагменты антител, такие как Fab, Fab', F(ab')2 и Fv, или другие антигенсвязывающие фрагменты. Специфичность антител можно определять с использованием способов и анализов, известных в этой области, включая, в качестве неограничивающих примеров, конкурентные анализы и использование систем фагового дисплея. Таким образом, антитело, специфически связывающееся, например, с белком NIS кошек, является антителом со скоростью ассоциации/диссоциации и/или аффинностью связывания, значительно большей для пептида SEQ ID NO:2 или его части, субфрагмента или части пептида, чем для гомологичного белка другого вида, например, для белка NIS человека. В этом контексте термин "значительно" означает, что скорости ассоциации/диссоциации и/или аффинность связывания субъекта отличается по меньшей мере в 1,1, 1,2, 1,5, 2, 5, 10, 50, 100, 1000 или 10000 раз или более.
Термин "чип" означает упорядоченное расположение по меньшей мере двух зондов на субстрате. По меньшей мере один из зондов является контролем или стандартом, и по меньшей мере один из зондов является диагностическим зондом. Расположение от приблизительно двух до приблизительно 40000 зондов на субстрате гарантирует, что размер и интенсивность сигнала каждого меченого комплекса, образующегося между зондом и полинуклеотидом или полипептидом в образце, являются индивидуально различимыми. Коллекцию молекул, нанесенных на чип, можно получать синтетически или биосинтетически. Чип может иметь множество форм, включая библиотеки растворимых молекул, библиотеки соединений, связанных с зернами смолы, чипами из диоксида кремния или другими твердыми подложками. Чип с нуклеиновой кислотой может включать библиотеки нуклеиновых кислот, которые можно получать нанесением в виде пятен нуклеиновых кислот по существу любой длины (например, от 1 до приблизительно 1000 нуклеотидов в длину) на субстрат. Чип с нуклеиновыми кислотами-зондами предпочтительно содержит нуклеиновые кислоты, связанные с субстратом в известных местах. В других вариантах осуществления система может включать твердую подложку или субстрат, такой как мембрана, фильтр, предметное стекло, лунка микропланшета, пробирка для образца, бусина, цепочка бусин или т.п. Твердую подложку можно получать из различных материалов, включая бумагу, целлюлозу, нейлон, полистирол, поликарбонат, пластмассу, стекло, керамику, нержавеющую сталь или т.п. Твердая подложка предпочтительно может иметь жесткую или полужесткую поверхность и предпочтительно может являться сферической (например, бусиной) или по существу плоской (например, плоской поверхностью) с подходящими лунками, выпуклыми областями, вытравленными канавками или т.п. Твердая подложка также может включать гель или матрицу, в которые можно погружать нуклеиновые кислоты.
Термин "биомаркеры" относится к генам и продуктам генов, кодируемым геном по изобретению или его гомологом, в частности, его гомологом у кошек, где определено, что ген дифференциально экспрессируется в результате заболевания, состояния, нарушения или введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, и где такие гены и продукты генов по изобретению определены, например, в SEQ ID NO:1. Биомаркер может являться полинуклеотидом, полипептидом, белком, РНК, включая РНК-транскрипт или продукт ее транскрипции, ДНК, кДНК, метаболит одной или нескольких из указанных выше молекул или применимый вариант любой из указанных выше молекул, дифференциальная экспрессия которого ассоциирована с гипертиреозом кошек, где корреляцию такой дифференциальной экспрессии в образце, взятом у тестового животного, с дифференциальной экспрессией в образце, взятом у контрольного животного, можно использовать в диагностике, прогнозировании, мониторинге или лечении состояния, заболевания или нарушения у нуждающегося в этом животного. Кроме того, биомаркер, как правило, можно использовать в отношении любой части или сегмента такого гена или белка, с помощью которой можно определять полноразмерный ген или белок, или которая может коррелировать с полноразмерным геном или белком, например, в анализе или другом способе по изобретению. Экспрессию биомаркера также можно определять посредством определения трансляции биомаркера (т.е. определения биомаркерного белка в образце). Способы, подходящие для определения биомаркерных белков, включают любой подходящий способ определения и/или измерения белков из клетки или клеточного экстракта. Такие способы включают, в качестве неограничивающих примеров, иммуноблоттинг (например, Вестерн-блоттинг), твердофазный иммуноферментный анализ (ELISA), радиоиммунологический анализ (RIA), иммунопреципитацию, иммуногистохимию и иммунофлуоресценцию. Особенно предпочтительные способы определения белков включают любой клеточный анализ, включая иммуногистохимию и иммунофлуоресценцию. Такие способы хорошо известны в этой области.
Термин "по сравнению", используемый для сравнения экспрессии в тестовом образце и контрольном образце, должен означать признаки такого свойства и количество и должен включать, в качестве неограничивающих примеров, значения в пределах одного стандартного отклонения от среднего значения, с которым осуществляют указанное сравнение, и значения, включающие дифференциальную экспрессию между тестовым образцом и контрольным образцом.
Термины "дифференциально экспрессирующийся ген", "дифференциальная экспрессия гена", "дифференциальная экспрессия" или "дифференциально экспрессируемый" и их синонимы, используемые взаимозаменяемо, относятся к гену, экспрессия которого активируется до более высокого или более низкого уровня у субъекта, страдающего заболеванием, состоянием или нарушением, или в результате введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, относительно его экспрессии у нормального или контрольного субъекта. Термины также включают гены, экспрессия которых активируется до более высокого или более низкого уровня на разных стадиях одного заболевания. Также следует понимать, что дифференциально экспрессируемый ген можно активировать или ингибировать на уровне нуклеиновой кислоты или уровне белка, или можно подвергать альтернативному сплайсингу, приводящему к другому полипептидному продукту. Такие различия можно подтверждать изменением уровней мРНК, поверхностной экспрессии, секреции или, например, другим разделением полипептида. Дифференциальная экспрессия гена может включать сравнение экспрессии двух или более генов или их продуктов, или сравнение соотношений экспрессии двух или более генов или их продуктов, или даже сравнение двух по-разному процессирующихся продуктов одного и того же гена, отличающихся среди нормальных субъектов и субъектов, страдающих заболеванием, состоянием или нарушением, или в результате введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, или между разными стадиями одного и того же заболевания, состояния или нарушения, или в результате введения различных количеств вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций. Дифференциальная экспрессия включает и количественные, и качественные различия временного или клеточного профиля экспрессии гена или продуктов его экспрессии, например, в нормальных и пораженных клетках или в клетках, прошедших различные события в течение заболевания или стадии заболевания. В целях настоящего изобретения считают, что присутствует "дифференциальная экспрессия гена", если существует изменение количества транскрибированных полинуклеотидов или транслируемого белка в образце по меньшей мере приблизительно в 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,25 раз.
При использовании в качестве меры дифференциальной экспрессии гена термин "кратный" означает уровень экспрессии гена у кошки, являющийся кратным количеством или долей экспрессии гена, сравниваемым с уровнем экспрессии гена у кошки сравнения, например, у кошки, страдающей гипертиреозом, по сравнению с животным, не демонстрирующим такого состояния. Например, ген, экспрессирующийся у животного в 2 раза сильнее, чем у животного сравнения, имеет 2-кратную дифференциальную экспрессию гена, и ген, экспрессирующийся у животного вполовину слабее, чем у животного сравнения, также имеет 2-кратную дифференциальную экспрессию гена.
Термин "фрагмент" означает (1) олигонуклеотид или полинуклеотидную последовательность, являющуюся частью полной последовательности или содержащую ее, и имеющую ту же или схожую активность для конкретного использования в качестве полной полинуклеотидной последовательности, или (2) пептид или полипептидную последовательность, являющуюся частью полной последовательности или содержащую ее, и имеющую ту же или схожую активность для конкретного использования в качестве полной полипептидной последовательности. Такие фрагменты могут содержать любое количество нуклеотидов или аминокислот, считающихся подходящими для конкретного использования. Как правило, олигонуклеотидные или полинуклеотидные фрагменты содержат по меньшей мере приблизительно 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 200, 400, 600, 800 или 1000 или более нуклеотидов, и полипептидные фрагменты содержат по меньшей мере приблизительно 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48 или 50 или более последовательных аминокислот из полной последовательности. Термин включает полинуклеотидные и полипептидные варианты фрагментов. Например, полинуклеотид можно разбивать или фрагментировать на множество сегментов.
Различные способы фрагментирования нуклеиновых кислот хорошо известны в этой области. Например, эти способы могут являться по своей природе химическими или физическими. Химическая фрагментация может включать частичную деградацию ДНКазой; частичную депуринизацию кислотой; использование ферментов рестрикции; использование кодируемых интронами эндонуклеаз; способы расщепления на основе ДНК, такие как способы с образованием триплекса и гибрида, основанные на специфической гибридизации сегмента нуклеиновой кислоты для локализации расщепляющего средства в конкретном месте в молекуле нуклеиновой кислоты; или другие ферменты или соединения, расщепляющие ДНК в известном или неизвестном месте. Способы физической фрагментации могут включать подвергание ДНК воздействию высокой скорости сдвига. Высокие скорости сдвига можно получать, например, перемещая ДНК через камеру или канал с углублениями или шипами, или пропуская образец ДНК через канал ограниченного размера, например, отверстие, имеющее поперечный размер микронного или субмикронного порядка. Другие физические способы включают обработку ультразвуком и распыление. Аналогично можно использовать комбинации физических и химических способов фрагментации, такие как фрагментация нагреванием и ион-опосредованный гидролиз. См., например, Sambrook et al., "Molecular Cloning: A Laboratory Manual," 3rd Ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (2001) ("Sambrook et al"), включенную в настоящее описание в качестве ссылки для всех целей. Эти способы можно оптимизировать для расщепления нуклеиновой кислоты на фрагменты с выбранным диапазоном размеров. Применимые диапазоны размеров могут составлять от 25, 50, 100, 200, 400, 700 или 1000 до 500, 800, 1500, 2000, 4000 или 10000 пар оснований. Однако большие диапазоны размеров, такие как от 4000, 10000 или 20000 до 10000, 20000 или 500000 пар оснований, также могут являться применимыми.
Термин "ген" или "гены" означает полный или частичный сегмент ДНК, участвующий в продукции полипептида, включая области перед и после кодирующей области (лидерную и трейлерную последовательность) и промежуточные последовательности (интроны) между отдельными кодирующими сегментами (экзонами). Термин включает любую последовательность ДНК, гибридизующуюся с комплементарной цепью кодирующих последовательностей гена.
Термин "гомолог" означает (1) полинуклеотид, включая полинуклеотиды из того же или другого вида животных, имеющий более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%-ое сходство последовательности с полинуклеотидом, имеющий те же или по существу те же свойства и осуществляющий ту же или по существу ту же функцию, что и полный полинуклеотид, или имеющий способность специфически гибридизоваться с полинуклеотидом в строгих условиях, или (2) полипептид, включая полипептиды из того же или другого вида животных, имеющий более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сходство последовательности с полипептидом, идентифицированным по экспрессирующимся полинуклеотидам, и имеющий те же или по существу те же свойства и осуществляющий ту же или по существу ту же функцию, что и полный полипептид, или имеющий способность специфически связываться с полипептидом, идентифицированным по экспрессии полинуклеотидов. Сходство последовательности двух полипептидных последовательностей или двух полинуклеотидных последовательностей определяют с использованием способов, известных специалистам в этой области, например, алгоритма Karlin и Altschul (Proc. Natl. Acad. Sci. USA 87: 2264-2268 (1990)). Такой алгоритм включен в программы NBLAST и XBLAST Altschul et al. (J. Mol. Biol. 215: 403-410 (1990)). Для получения выравнивания с пропусками в целях сравнения можно использовать Gapped Blast, как описано в Altschul et al. (Nucl. Acids Res. 25: 3389-3402 (1997)). При использовании программ BLAST и Gapped BLAST используют программы по умолчанию соответствующих программ (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov.
Термин "гибридизация" относится к процессу, в котором два одноцепочечных полинуклеотида нековалентно связываются с образованием стабильного двухцепочечного полинуклеотида. Термин "гибридизация" также может относиться к трехцепочечной гибридизации. Получаемый (как правило) двухцепочечный полинуклеотид является "гибридом". Доля популяции полинуклеотидов, образующих стабильные гибриды, в настоящем описании обозначают как "степень гибридизации".
Реакции гибридизации можно осуществлять в абсолютных или дифференциальных форматах гибридизации. В абсолютном формате гибридизации полинуклеотиды, полученные из одного образца, гибридизуют с зондами в чипе с нуклеиновыми кислотами. Сигналы, определяемые после образования гибридизационных комплексов, коррелируют с уровнями полинуклеотида в образце. В формате дифференциальной гибридизации полинуклеотиды, полученные из двух образцов, метят различными веществами для мечения. Смесь этих по-разному меченых полинуклеотидов добавляют на чип с нуклеиновыми кислотами. Затем чип с нуклеиновыми кислотами исследуют в условиях, в которых излучение от двух разных меток определяют по отдельности. В одном из вариантов осуществления для формата дифференциальной гибридизации в качестве веществ для мечения используют флуорофоры Cy3 и Cy5 (Amersham Pharmacia Biotech, Piscataway, N.J.).
Сигналы, полученные от чипов с нуклеиновыми кислотами, можно анализировать с использованием коммерчески доступного программного обеспечения, такого как программное обеспечение, поставляемое Affymetrix или Agilent Technologies. Предпочтительно, в эксперименты по гибридизации включают контроли, такие как контроли чувствительности сканирования, мечения зонда и квантования кДНК или кРНК. Сигналы гибридизации можно масштабировать или нормировать до проведения дальнейшего анализа. Например, сигналы гибридизации для каждого отдельного зонда можно нормировать для учета изменений интенсивностей гибридизации при использовании нескольких чипов в аналогичных условиях тестирования. Также сигналы гибридизации можно нормировать с использованием интенсивностей, полученных от внутренних контролей для нормирования, содержащихся в каждом чипе. Кроме того, гены с относительно постоянными уровнями экспрессии среди образцов можно использовать для нормирования уровней экспрессии других генов. В одном из вариантов осуществления зонды для конкретных генов "домашнего хозяйства" включают в чип с нуклеиновыми кислотами по настоящему изобретению. Эти гены выбирают потому, что они демонстрируют стабильные уровни экспрессии в различных тканях. Сигналы гибридизации можно нормировать и/или масштабировать, учитывая уровни экспрессии этих генов "домашнего хозяйства".
Термин "гибридизационный комплекс" означает комплекс, образующийся между полинуклеотидами в образце, когда пурины одного полинуклеотида образуют водородные связи с пиримидинами комплементарного полинуклеотида, например, 5'-A-G-T-C-3' образует пары оснований с 3'-T-C-A-G-5'. Степень комплементарности и использование аналогов нуклеотида влияет на эффективность и точность реакций гибридизации.
Термин "зонды для гибридизации" включает нуклеиновые кислоты (такие как олигонуклеотиды), способные связывать с комплементарной цепью нуклеиновой кислоты с образованием пар оснований. Такие зонды включают пептид-нуклеиновые кислоты, как описано в Nielsen et al., Science 254: 1497-1500 (1991), Nielsen Curr. Opin. Biotechnol., 10: 71-75 (1999), и другие аналоги нуклеиновых кислот и имитации нуклеиновых кислот. См. патент США № 6156501, зарегистрированный 3 апреля 1996 года.
"Последовательность нуклеиновой кислоты" означает олигонуклеотид, нуклеотид или полинуклеотид и его фрагменты или части, и относится к ДНК или РНК геномного или синтетического происхождения, которая может являться одно- или двухцепочечной, и представляет смысловую или антисмысловую цепь.
Термин "полинуклеотид" или "олигонуклеотид" означает полимер нуклеотидов. Термин включает молекулы ДНК и РНК (включая кДНК и мРНК), одно- или двухцепочечные, и, в случае одноцепочечной молекулы, ее комплементарную последовательность в линейной или кольцевой форме. Термин также включает фрагменты, варианты, гомологи и аллели, при необходимости, в случае последовательностей, имеющих те же или по существу те же свойства и осуществляющих ту же или по существу ту же функцию, что и исходная последовательность. Последовательности могут являться полностью комплементарными (без несовпадений) при выравнивании или могут иметь несовпадения до приблизительно 30% последовательности. В случае полинуклеотидов цепь содержит от приблизительно 20 до 10000, от 50 до 8000, от 100 до 5000 или от 150 до 3500 нуклеотидов. В случае олигонуклеотидов цепь содержит от приблизительно 2 до 100, от 3 до 80, от 4 до 60, от 5 до 40 или от 6 до 30 нуклеотидов. Точный размер полинуклеотида или олигонуклеотида будет зависеть от различных факторов и от конкретного использования полинуклеотида или олигонуклеотида. Термин включает нуклеотидные полимеры, синтезированные и выделенные и очищенные из природных источников. Термин "полинуклеотид" включает "олигонуклеотид".
Термин "полипептид", "пептид" или "белок" означает полимер аминокислот. Термин включает природные и неприродные (синтетические) полимеры и полимеры, в которых искусственными химическими имитациями замещают одну или несколько аминокислот. Термин также включает фрагменты, варианты и гомологи, имеющие те же или по существу те же свойства и осуществляющие ту же или по существу ту же функцию, что и исходная последовательность. Термин включает полимеры любой длины, предпочтительно полимеры, содержащие от приблизительно 2 до 1000, от 4 до 800, от 6 до 600 и от 8 до 400 аминокислот. Термин включает полимеры аминокислот, синтезированные и выделенные и очищенные из природных источников. В некоторых случаях в настоящем описании термины "полипептид", "пептид" или "белок" используют взаимозаменяемо.
Термин "зонд" означает (1) олигонуклеотид или полинуклеотид РНК или ДНК, существующий в природе в виде очищенного продукта расщепления ферментами рестрикции или полученный синтетически, способный отжигаться или специфически гибридизоваться с полинуклеотидом с последовательностями, комплементарными зонду; или (2) пептид или полипептид, способный специфически связываться с конкретным белком или фрагментом белка, по существу, для исключения других белков или фрагментов белков. Олигонуклеотидный или полинуклеотидный зонд может являться одно- или двухцепочечным. Точная длина зонда будет зависеть от многих факторов, включая температуру, источник и использование. Например, в случае диагностического применения в зависимости от сложности последовательности-мишени, олигонуклеотидный зонд, как правило, содержит от приблизительно 10 до 100, от 15 до 50 или от 15 до 25 нуклеотидов. В случае конкретного диагностического применения полинуклеотидный зонд содержит приблизительно 100-1000 нуклеотидо