Вещества, обладающие ангиогенной активностью
Иллюстрации
Показать всеГруппа изобретений относится к области фармакологии и экспериментальной медицины и касается применения низкомолекулярных пептидных миметиков фактора роста нервов: гексаметилендиамида бис-(N-моносукцинил-глутамил-лизина) - соединения ГК-2; гексаметилендиамида бис-(N-ацетил-лизил-глутаминовой кислоты) - соединения ГК-4; амида N-аминокапроил-глицил-лизина - соединения ГК-5; гексаметилендиамида бис-(N-аминокалроил-глицил-лизина) - соединения ГК-6, в качестве соединений, обладающих ангиогенной активностью. Группа изобретений обеспечивает создание новых высокоэффективных средств для стимуляции неоангиогенеза при различных ишемических процессах. 4 н.п. ф-лы, 3 ил., 2 табл., 3 пр.
Реферат
Изобретение относится к медицине, в частности к фармакологии, и касается применения описанных ранее (Середенин С.Б., Гудашева Т.А. Патент РФ №2410392) низкомолекулярных пептидных миметиков фактора роста нервов: гексаметилендиамида бис-(N-моносукцинил-глутамил-лизина) - соединения ГК-2; гексаметилендиамида ,бис-(N-ацетил-лизил-глутаминовой кислоты) - соединения ГК-4; амида N-аминокапроил-глицил-лизина - соединения ГК-5; гексаметилендиамида бис-(N-аминокапроил-глицил-лизина) -соединения ГК-6, в качестве соединений, обладающих ангиогенной активностью.
Изобретение относится к разделу Экспериментальная медицина и в дальнейшем может быть использовано для создания новых оригинальных высокоэффективных лекарственных средств для стимуляции неоангиогенеза при различных ишемических процессах.
Основной областью применения ангиогенных лекарственных средств является ишемическая болезнь сердца, в том числе острый инфаркт миокарда, и хроническая ишемия нижних конечностей, особенно в тех случаях, когда применение хирургических методов лечения, в частности эндоваскулярной реваскуляризации, и/или невозможно, и/или недостаточно эффективно, и/или сопряжено с риском развития тяжелых осложнений, а также в неврологии и травматологии. Например, количество такого рода пациентов среди больных ишемической болезнью сердца согласно данным различных источников, колеблется в пределах 30-45% (Cao Y. Discov. Med., 2010, 9(46): 179-184; Mitsos S. et al. Angogenesis, 2012, 15(1):1-22 и др.), а у больных, страдающих хроническим облитерирующим эндартериитом, из-за невозможности проведения полномасштабного хирургического вмешательства ампутация проводится более чем в 25% случаях, летальность же при этой патологии составляет 20-25% (Smith L. Nurs. Times, 2012, 108(43):12-14; Ouma G.O. et al. 2012, 17(3):174-192 и др.).
Теоретические подходы, обосновывающие целесообразность фармакологической стимуляции ангиогенеза, были сформулированы в конце XX века, а само направление получило название «терапевтический ангиогенез» или «биологическое шунтирование» (Isner J.M. Clin. Immunol. Immunopathol., 1996, 80(3 Pt2):S82-91). В настоящее время под термином «терапевтический ангиогенез» понимают стимуляцию ангиогенеза при помощи лекарственных средств, преимущественно биоподобных препаратов, обладающих способностью улучшать перфузию ишемизированных тканей с помощью усиления естественных, но недостаточных в критических ситуациях, процессов неоваскуляризации тканей, т.е. стимулировать рост и ветвление (арборизацию) кровеносных сосудов и/или модулировать функции эндотелия (Mima Y. et al. PLoS One, 2012, 7(4):e35199; Chu H., Wang Y. Ther. Deliv., 2012, 3(6):693-714). Наиболее перспективным в этом плане представляется разработка и внедрение в клиническую практику экзогенных аналогов эндогенных факторов роста и/или химических соединений, обладающих способностью активировать факторы роста, а также использование генетически модифицированных прогениторных клеток (Парфенова Е.В., Ткачук В.А. Кардиологический вестник, 2007, т.II (XIV), №2, С.5-14; Semeraro F. et al. chit. Vasc. PharmacoL, 2011, 9(5):629-646; Machalinska A. et al. Klin. Oczna, 2012, 114(1):63-67; Fariha M.M. et al. J. Cell. Mol. Med., 2013).
Одним из возможных подходов к решению этой проблемы является использование для стимуляции неоангиогенеза низкомолекулярных пептидных миметиков первой (соединения ГК-4, ГК-5, ГК-6) и четвертой (соединение ГК-2) петель фактора роста нервов (NGF).
В настоящее время накоплен достаточно убедительный литературный материал, свидетельствующий о том, что фактор роста нервов, помимо ЦНС, синтезируется и экскретируется эндотелиальными и гладкомышечными клетками сосудов, а на их клеточной мембране представлены специфические для NGF TrkA рецепторы (Meloni M. et al. Circ. Res., 2010, 106(7):1275-1284; Saygili E. et al. J. Mol. Cell. Cardiol., 2010, 49(1):79-87 и др.), посредством взаимодействия с которыми NGF реализует свои ангиогенные эффекты. NGF-опосредованная активация TrkA рецепторов, расположенных на клеточных мембранах эндотелиальных и гладкомышечных клеток сосудов, влечет за собой активацию PI3K-Akt, Ras-MAPK и PLCγ1-IP3 внутриклеточных сигнальных путей, инициирующих неоангиогенез (Caporali A., Emanueli С., 2009, 80: 279-308 и др.). Этот феномен описан как для нормальных, так и патологически измененных тканей. В эндотелиальных клетках сосудов конечным этапом NGF-опосредованной активации TrkA рецепторов является активация матриксной металлопротеиназы-2 (ММР-2), относящейся к семейству цинкозависимых эндопротеиназ. Опосредованная NGF активация ММР-2, в свою очередь, инициирует активацию фактора транскрипции генов АР-2 (Park M.-J. et al. J. Biol. Chem., 2007, 282(42): 30485-30496), который транслоцируется в ядро клетки, где запускает каскад реакций, стимулирующих пролиферацию, миграцию и инвазию эндотелиальных клеток. Помимо этого имеются данные о том, что этот процесс может быть инициирован и посредством активации NGF фактора роста эндотелия сосудов - VEGF-A (Lazarovici P. et al. Endothelium, 2006, 13(1):51-59). В гладкомышечных клетках сосудов активация Ras-MAPK-сигнального пути влечет за собой активацию металлопротеиназы-9 (ММР-9), которая, в отличие от ММР-2, активирует лишь процессы миграции и инвазии клеток (Lucchesi P.A. et al. Circulation, 2004, 110:3587-3593). Миграция гладкомышечных клеток сосудов может быть инициирована и путем NGF-опосредованной активации PI3K-Akt и PLCγ1-IРЗ внутриклеточных сигнальных каскадов (Kraemer R. et al. Arterioscler. Thromb. Vasc. Biol., 1999,19:1041-1050).
В результате многолетних фундаментальных исследований в НИИ фармакологии имени В.В. Закусова РАМН синтезирован ряд низкомолекулярных пептидных миметиков NGF, обладающих свойствами агонистов (соединения ГК-2, ГК-4, ГК-5, ГК-6) TrkA рецепторов (Гудашева Т.А. с соавт. Доклады Академии Наук, 2010, 434(4): 549-551) и выявлена их ангиогенная активность.
Следующие примеры иллюстрируют ангиогенную активность гексаметилендиамида бис-(N-моносукцинил-глутамил-лизина) - соединения ГК-2; гексаметилендиамида бис-(N-ацетил-лизил-глутаминовой кислоты) - соединения ГК-4; амида N-аминокапроил-глицил-лизина - соединения ГК-5; гексаметилендиамида бис-(N-аминокапроил-глицил-лизина) - соединения ГК-6.
Пример 1. Влияние соединений ГК-2, ГК-4, ГК-5, ГК-6 на длину капилляров в ишемизированной конечности у крыс.
Опыты проводили на беспородных крысах-самцах массой 180-200 г. Животных рандомизировали на 5 групп: 1-я (n=23) - контрольная и 2-я - n=15, 3-я - n=8, 4-я - n=10 и 5-я - n=14, получавшие соединения ГК-2, ГК-4, ГК-5 и ГК-6 соответственно. Ишемию задних конечностей у анестезированных крыс (тиопентал натрия, 50 мг/кг, в/б) вызывали путем одномоментной резекции участка бедренной артерии, после чего рану послойно ушивали. Изучаемые соединения (1 мг/кг) вводили внутрибрюшинно в течение 14 дней от момента резекции бедренной артерии. Первую инъекцию осуществляли через 1 ч после окончания операции. Контрольным животным по аналогичной схеме внутрибрюшинно вводили 0,3 мл физиологического раствора. Через сутки после последней инъекции животных забивали и извлекали икроножную мышцу из ишемизированной конечности. Для визуализации капилляров использовали 1%-ный раствор синьки Эванса, который вводили за 5 мин до забоя животных. При помощи световой микроскопии оценивали суммарную длину капилляров в 1 мм2 ишемизированной ткани, что позволяло судить об интенсивности роста сосудов под влиянием изучаемых соединений. Значимость различий определяли с помощью однофакторного дисперсионного анализа с дальнейшей обработкой методом множественных сравнений по Даннету.
Анализ полученных результатов свидетельствует о том, что изучаемые соединения в той или иной проявляют ангиогенную активность (табл.1). Так, например, у животных, получавших соединение ГК-6, суммарная длина капиллярного русла была на 32% больше, чем в контроле (р=0,008). Наибольшую ангиогенную активность проявляло соединение ГК-2: у животных, получавших это соединение, показатель суммарной длины капилляров был более чем на 50% выше, чем у контрольных животных - соответственно 21024±1344 и 13607±715 мкм/мм2 (р<0,001).
Таким образом, приведенные результаты скрининговых исследований свидетельствуют о том, что рассматриваемые соединения в той или иной мере стимулируют ангиогенез. При этом наибольшей ангиогенной активностью обладает соединение ГК-2.
Пример 2. Ангиогенная и противоишемическая активности низкомолекулярного пептидного миметика NGF - соединения ГК-2.
Опыты проводили на беспородных крысах-самцах массой 180-200 г. Животных рандомизировали на 2 группы: контрольную (n=18) и основную (n=17). В этой серии экспериментов, выполненных на модели ишемии задних конечностей крыс (протокол эксперимента аналогичен таковому, изложенному в примере 1), оценивали не только ангиогенные, но и противоишемические эффекты соединения ГК-2. Для этой цели изучали влияние соединения ГК-2 на интенсивность васкуляризации и некробиотических процессов, протекающих в ишемизированной икроножной мышце. Для оценки интенсивности некробиотических процессов, протекающих в ишемизированной икроножной мышце, использовали световую микроскопию, для чего мышцу фиксировали в 10%-ном нейтральном растворе формалина, при помощи замораживающего микротома изготовляли срезы толщиной 5 мкм, которые окрашивали гематоксилин-эозином по стандартной методике. Для визуализации капилляров использовали синьку Эванса. Для каждого поля зрения рассчитывали суммарную длину сосудов и их количество в 1 мм2. О степени васкуляризации судили по величине индекса васкуляризации, за который принимали произведение длины капилляров и их количества в 1 мм2 ищемизированной ткани. Статистическую значимость изменений, вызываемых соединением ГК-2, определяли с помощью критерия Манна-Уитни. Значимость различий между сериями экспериментов определяли с помощью критерия точной вероятности Фишера.
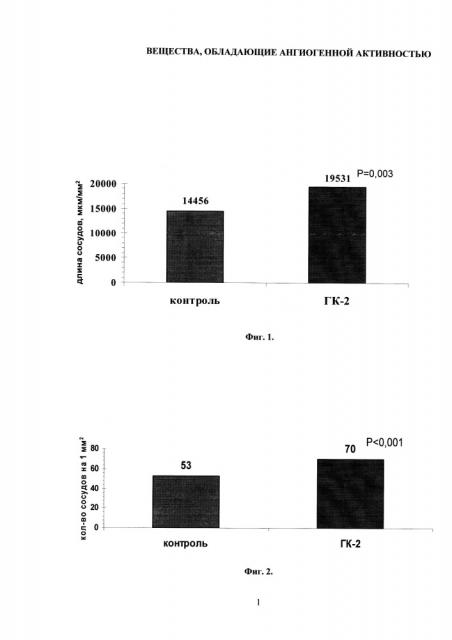
Полученные результаты свидетельствуют о том, что у животных, получавших соединение ГК-2, суммарная длина капиллярного русла статистически значимо больше (р<0,003), чем у контрольных животных - 19531(16085÷24511) и 14420(10901÷17404) мкм/мм2 соответственно (фиг.1. Влияние соединения ГК-2 (в/б, 1 мг/кг/сут, 14 дней) на суммарную длину сосудов в 1 мм ткани в условиях ишемии задней конечности крысы). Количество сосудов в 1 мм2 ишемизированной ткани у животных, получавших соединение ГК-2, также было больше (р<0,001): 71(71÷78) и 53(50÷57) соответственно (фиг.2. Влияние соединения ГК-2 (в/б, 1 мг/кг/сут, 14 дней) на количество сосудов в 1 мм2 ткани в условиях ишемии задней конечности крысы). Математический анализ полученных результатов свидетельствует о том, что интенсивность васкуляризации ишемизированной ткани у животных, получавших соединение ГК-2, практически в 2 раза выше, чем в контроле - 27794(25218÷35941) и 14725(9030÷19630) соответственно (р<0,001).
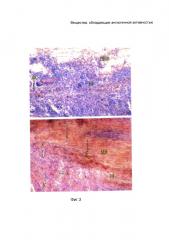
Согласно данным световой микроскопии у контрольных животных основу ткани составляет некробиотически измененная мышца с участками восковидного некроза. Саркоплазма ярко окрашена, гомогенна, поперечная исчерченность отсутствует (фиг. 3а. Морфологическая картина задней икроножной мышцы крысы (х 10)). Отмечается большое количество воспалительных инфильтратов. Ядра поперечно-полосатых мышц мелкие, гиперхромные или отсутствуют. Сосуды полнокровны, околососудистый отек хорошо выражен, капилляры извитые, мелкие, тонкие, плохо различимы. Таким образом, в результате удаления участка бедренной артерии в икроножной мышце наблюдаются выраженные некротические и некробиотические изменения, сопровождающиеся воспалительной реакцией и расстройством кровообращения. У животных, получавших соединение ГК-2, микроскопическая картина икроножной мышцы существенно отличается от таковой в контроле - интенсивность альтеративных процессов в мышце этих крыс менее выражена, количество и размер участков восковидного некроза значимо меньше, чем у контрольных крыс. Площадь воспалительных инфильтратов незначительна. В отличие от контрольных животных эндомизий сосудов четко выражен. Поперечная исчерченность скелетной мускулатуры сохранена. Капиллярная сеть хорошо различима, капилляры идут прямо и располагаются вдоль мышечных волокон (фиг.3б).
Таким образом, пример свидетельствует о том, что соединение ГК-2 проявляет не только выраженную ангиогенную, но и противоишемическую активность, которая, по всей видимости, связана со способностью соединения стимулировать неоангиогенез в поврежденной икроножной мышце.
Пример 3. Влияние соединения ГК-2 на формирование трубчатых структур (тубулогенез) в культуре клеток эндотелия человека HUVEC.
Оценку ангиогенной активности соединения ГК-2 в экспериментах in vitro проводили на культуре изолированных клеток эндотелия человека HUVEC. Такой подход обусловлен тем, что согласно литературным данным образование трубчатых структур (тубулогенез) является начальной стадией ангиогенеза. В начестве эталона использовали NGF.
Клетки эндотелия рассаживали в среде ДМЕМ, содержащую 20 мМ Hepes, 2 мМ L-глутамина, гепарин (5 Ед/мл), ECGF (20 мкг/мл), 10% FBS с плотностью 3,5 тыс. на 96-луночные планшеты, покрытые полилизином. ГК-2 (10-6 М) и NGF (10-9 М) вносили через 30 мин после рассеивания клеток на планшеты и затем каждые 48 ч (всего 3 внесения). После чего для оценки влияния соединения ГК-2 и NGF на формирование трубчатых структур эндотелиальные клетки фотографировали с использованием фотокамеры Canon инвертированного микроскопа Nikon Eclipse TS-100F. Для обсчета тубулогенеза использовали программу ImageJ. Измеряли длину микротрубочек в 5 полях зрения каждой лунки.
Полученные результаты обобщены в таблице 2, из которых следует, что длина микротрубочек в культуре клеток эндотелия, в которую вносили соединение ГК-2, статистически значимо (р<0,001) больше, чем в контроле и сравнима с таковой при внесении NGF.
Таким образом, результаты экспериментов in vitro свидетельствуют о том, что ГК-2 подобно NGF активирует тубулогенез - начальную стадию ангиогенеза.
Описание чертежей
Фиг.1. Влияние соединения ГК-2 (в/б, 1 мг/кг/сут, 14 дней) на суммарную длину сосудов в 1 мм2 ткани в условиях ишемии задней конечности крысы.
По оси ординат - длина сосудов в мкм/мм. По оси абсцисс - группы животных.
Из фиг. 1 видно, что у животных, получавших соединение ГК-2, суммарная длина сосудов в 1 мм ткани ишемизированной конечности статистически значимо больше (Р=0,003), чем в контроле.
Фиг.2. Влияние соединения ГК-2 (в/б, 1 мг/кг/сут, 14 дней) на количество сосудов в 1 мм2 ткани в условиях ишемии задней конечности крысы.
По оси ординат - количество сосудов в 1 мм. По оси абсцисс - группы животных.
Из фиг. 2 видно, что у животных, получавших соединение ГК-2, количество сосудов в 1 мм2 ткани ишемизированной конечности статистически значимо больше (Р<0,001), чем в контроле.
Фиг.3. Морфологическая картина задней икроножной мышцы крысы (х 10).
Верхняя панель - контроль (а), нижняя - ГК-2 (в/б, 1 мг/кг/сут, 14 дней) (б).
ЗВ - зона воспаления, НМВ - некротизированные мышечные волокна; MB - мышечные волокна, ФС - фрагмент сосуда; К - капилляры.
| Таблица 1 | |||||
| Влияние соединений ГК-2, ГК-4, ГК-5, ГК-6 (1 мг/кг, в/б) на плотность сосудистого русла в ишемизированной мышце крыс (арифметические средние, их стандартные ошибки и 95% доверительные интервалы). | |||||
| Показатель | Соединения | ||||
| Контроль, n=23 | ГК-2, n=15 | ГК-4, n=8 | ГК-5 n=10 | ГК-6, n=14 | |
| Плотность сосудистого русла, мкм/мм2 | 13607±715 12123÷15091 | 21024±1344 18142÷23906 Р<0,001 | 14363±812 10443÷15284 р≈0,822 | 15201±1411 11216÷16002 р≈0,057 | 17937±1185 15376÷20497 p≈0,008 |
| Таблица 2 | |||
| Влияние соединения ГК-2 (10-6) и NGF(10-9 M) на формирование микротрубочек в культуре изолированных клеток эндотелия человека-HUVEC (указаны медианы, нижний и верхний квартили). | |||
| Показатель | Экспериментальные группы | ||
| Контроль, n=92 | NGF, n=78 | ГК-2, n=54 | |
| Суммарная длина микротрубочек, мкм | 20 | 36 | 38 |
| 14÷29 | 26÷49 | 27÷53 | |
| p<0,001 | |||
| P<0,001 |
1. Применение гексаметилендиамида бис-(N-моносукцинил-глутамил-лизина) в качестве средства, обладающего ангиогенной активностью.
2. Применение гексаметилендиамида бис-(N-ацетил-лизил-глутаминовой кислоты) в качестве средства, обладающего ангиогенной активностью.
3. Применение амида N-аминокапроил-глицил-лизина в качестве средства, обладающего ангиогенной активностью.
4. Применение гексаметилендиамида бис-(N-аминокапроил-глицил-лизина) в качестве средства, обладающего ангиогенной активностью.