Способ прогнозирования неблагоприятного течения постинфарктного периода у пациентов трудоспособного возраста
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к кардиологии. Определяют наличие бета-адреноблокаторв среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение ближайшего года после перенесенного инфаркта миокарда, госпитализация в специализированный стационар. Определяют наличие в анамнезе перенесенного ранее инфаркта миокарда, а также нарушений углеводного обмена различного характера (нарушение толерантности к глюкозе, нарушенная гликемия натощак или сахарный диабет 2 типа) путем опроса или анализа медицинской документации. Рассчитывают вероятность развития летального исхода (р) по оригинальной формуле. При значении р≥0,6 прогнозируют неблагоприятное течение постинфарктного периода. Способ позволяет выявлять лиц с неблагоприятным течением постинфарктного периода и провести соответствующую коррекцию лечебно-диагностической стратегии у пациентов трудоспособного возраста. 1 табл., 2 пр.
Реферат
Изобретение относится к области медицины, а именно к кардиологии.
Инфаркт миокарда может стать дебютом ИБС либо быть проявлением ИБС у лиц с уже установленным диагнозом.
Данные о частоте инфаркта миокарда позволяют оценить бремя ИБС в популяции. Заболеваемость острыми формами ИБС среди молодого населения, как и случаи первичной заболеваемости, характеризуют эффективность проводимых в популяции превентивных мероприятий. Само понятие «инфаркт миокарда» несет в себе не только патофизиологический смысл, но и может иметь психологический и юридический аспект как для конкретного человека, так и для популяции в целом [1]. С целью уменьшить возможность отягощенного течения постинфарктного периода (развитие повторных случаев инфаркта миокарда, эпизодов прогрессирования сердечной и коронарной недостаточности), необходимо использовать индивидуальные (персонифицированные) прогнозные шкалы и формулы [2].
Попытки прогнозирования неблагоприятного течения постинфарктного периода предпринимались многими авторами в различной интерпретации с различным набором предикторов и с различным сроком отдаленного наблюдения за пациентами. Причины этому весьма понятны. Ведь развитие повторных коронарных событий или усугубление симптомов сердечной недостаточности являются предвестниками неблагоприятного исхода и свидетельствуют о неудовлетворительном коронарном резерве. Недостатком созданных ранее расчетных моделей является то, что осуществлялись они на клиническом материале с четкими критериями включения, которые зачастую ограничивались территориально, по тендерному признаку, возрасту и т.д. Так, например, в 1994 г. в Томске была создана формула для прогноза неблагоприятного течения постинфарктного периода с учетом генетического полиморфизма у женщин в течение 10-летнего наблюдения [3]. Другие авторы изучали биохимические критерии с позиции возможных предикторов [4], не учитывая при этом клинические характеристики. Отличием предлагаемого способа является то, что инициировался он на основе исследования эпидемиологического характера и включении больных, перенесших инфаркт миокарда, методом сплошной выборки. Единственным критерием включения был возрастной состав больных, поскольку исследование интерполировалось на пациентов трудоспособного возраста: мужчины не старше 60 лет, женщины - не старше 55 лет. Преимуществом выполненного популяционного исследования является сбор данных с использованием стандартизованных критериев, на основании которых верифицируется острый инфаркт миокарда. Таким образом, мы минимизировали возможность влияния на прогнозный расчет возраста больных и усилили приоритеты на особенностях развития, клинического течения, стратегии ведения в остром и ближайшем периодах и особенностях медикаментозной поддержки, что впоследствии можно было бы использовать в качестве модифицируемых критериев изменения прогноза у каждого конкретного пациента.
Приоритетным направлением научных трудов последних десятилетий стала разработка возможностей предотвращения негативных проявлений социально опасных заболеваний. Касается этот прогнозный анализ не только характера неблагоприятных проявлений (от осложненного течения до развития летального исхода), но и сроков их развития. Большинство исследований ограничивались изучением ближайшего периода острого инфаркта миокарда, что дополнительно ограничивает возможность применения подобных предикторных формул для описания характера течения постинфарктного периода в долгосрочной перспективе. Прогноз пациентов с острым инфарктом миокарда неоднозначен и зависит от множества факторов. Систематизация этих факторов, основанная на длительном проспективном наблюдении однородного клинического материала позволит объективизировать данные и создать приближенную к реальности математическую формулу прогнозирования.
Создание регистров по-прежнему считается наиболее объективным способом получения информации о конкретном заболевании в рамках настоящего времени с учетом всех возможных прогнозных факторов. Главной и преимущественной особенностью функционирования регистров, осуществляющих унифицированную и организованную работу по централизованному сбору данных стандартного характера, является то, что аналитическая информация обрабатывается из всех лечебных учреждений города.
В изученной медицинской и патентной литературе адекватного прототипа не обнаружено.
Задача изобретения - разработать способ прогнозирования неблагоприятного течения постинфарктного периода у пациентов трудоспособного возраста.
Поставленная задача решается путем определения основных параметров, характеризующих анамнестические данные, на фоне которых развивается коронарная катастрофа, а также особенности лечения острого инфаркта миокарда, включающие характер медикаментозного лечения на момент выписки из стационара и тип лечебного учреждения, в котором пациент проходил лечение. К таким параметрам относятся характеристика технической оснащенности стационара (в частности, возможность своевременного выполнения интервенционных процедур в остром периоде индексного инфаркта миокарда) и рекомендации по медикаментозному сопровождению пациента после выписки из лечебного учреждения и/или в течение ближайшего года после инфаркта миокарда (наличие бета-адреноблокаторов). Затем определяют наличие в анамнезе перенесенного ранее инфаркта миокарда, а также нарушений углеводного обмена различного характера (нарушение толерантности к глюкозе, нарушенная гликемия натощак или сахарный диабет 2 типа) путем опроса или анализа медицинской документации.
Вероятность развития летального исхода определяют по формуле:
где р - вероятность развития летального исхода;
z - значение дискриминантной функции.
Индивидуальная количественная оценка риска летального исхода вычисляется по зависимости риска от интегрального показателя, который определяют как сумму произведений показателей и соответствующих им весовых коэффициентов, полученных на предварительном этапе разработки способа.
Определяют значение дискриминантной функции по формуле:
где k - константа, определяемая при составлении уравнения мультипредикторной модели, x1-x4 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты a, b, c, d - весовые коэффициенты соответствующих показателей,
k=0,642,
x1 - наличие бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
а=-0,836 - есть бета-адреноблокаторы среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
а=0 - при отсутствии бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
x2 - госпитализация в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
b=-0,738 - госпитализация в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
b=0 - при отсутствии госпитализации в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
х3 - нарушение углеводного обмена,
с=0,485 - нарушение углеводного обмена,
с=0 - при отсутствии нарушения углеводного обмена,
x4 - перенесенный в анамнезе инфаркт миокарда,
d=0,817 - перенесенный в анамнезе инфаркт миокарда,
d=0 - при отсутствии перенесенного в анамнезе инфаркта миокарда.
При значении p≥0,6 прогнозируют неблагоприятное течение постинфарктного периода. Для представления вероятности неблагоприятного исхода перенесенного инфаркта миокарда в % умножают р на 100 (процентная интерпретация более понятна врачу).
Неблагоприятное течение постинфарктного периода характеризуется случаями прогрессирования коронарной и сердечной недостаточности, в том числе и повторные эпизоды инфаркта миокарда.
Нами определены факторы, обладающие весомой прогнозной значимостью. Кроме того, предложена многофакторная регрессионная модель, позволяющая рассчитать вероятность развития летального исхода в течение последующих лет жизни у пациентов трудоспособного возраста после перенесенного инфаркта миокарда.
Была сформулирована задача: выявить факторы, значимо влияющие на неблагоприятное течение постинфарктного периода, и разработать прогностическую модель для его предсказания.
В анализ были включены следующие признаки (факторы):
• Пол (мужской, женский);
• Перенесенный в анамнезе инфаркт миокарда (да, нет);
• Наличие патологии углеводного обмена (да, нет);
• Наличие дислипидемии (да, нет);
• Локализация индексного инфаркта миокарда (боковой, передний, задний, нижний, циркулярный);
• Наличие осложнений острого периода инфаркта миокарда (да, нет);
• Характер осложнений острого периода инфаркта миокарда (постинфарктная стенокардия, аневризматическая деформация левого желудочка, рецидивирующее течение, нарушения ритма и проводимости, шок различного генеза, отек легких);
• Фармакологическая реваскуляризация в остром периоде (да, нет);
• Внутрисосудистая реваскуляризация миокарда за период 5-летнего наблюдения (да, нет);
• Мощность нагрузки, выполненной при выписке, по уровню ТФН (≤75 Вт,>75 Вт);
• Окклюзия шунтов (да, нет);
• Рестеноз имплантированных ранее стентов (да, нет);
• Сочетание фармакологической реваскуляризации в остром периоде и выполнение агентирования в ближайший год после перенесенного инфаркта миокарда (да, нет).
• Уровень фракции выброса левого желудочка по данным эхокардиографического исследования, выполненного во время госпитализации по поводу индексного инфаркта миокарда (>45%,≤45%;≤35%, 36-49%,>50%);
• Наличие статинов среди лекарственных препаратов, рекомендованных при выписке из стационара (да, нет);
• Наличие бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда (да, нет);
• Наличие ингибиторов ангиотензин-превращающего фермента среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда (да, нет);
• Госпитализация в первые 3 часа от начала заболевания (да, нет);
• Госпитализация в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения (да, нет).
Необходимо было выяснить, наличие каких из перечисленных факторов является наиболее неблагоприятным в плане развития летального исхода и степень влияния каждого из них.
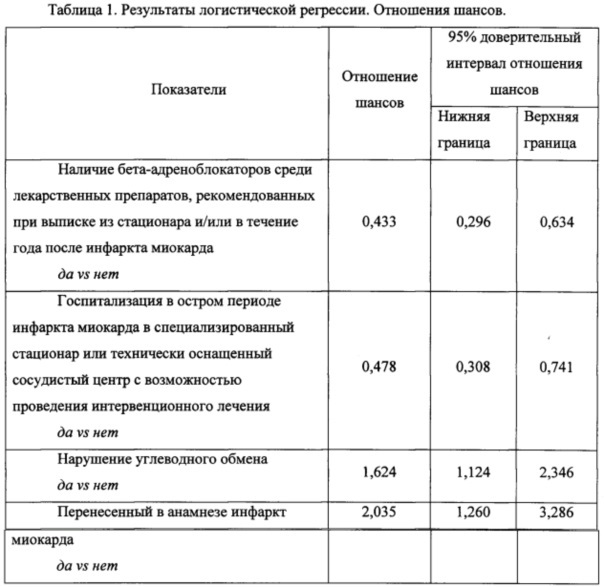
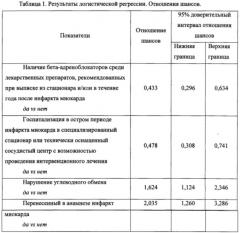
Построение модели происходило пошаговым методом условного включения переменных в модель. Были определены переменные, статистически значимые с исходом и вносящие достоверные различия в дискриминацию групп, с благоприятным и неблагоприятным исходом, рассчитаны отношения шансов и построена прогностическая функция. В результате пошаговой процедуры отбора значимых факторов в модель вошли следующие показатели:
1) наличие бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда (р<0,001) (да/нет);
2) госпитализация в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения (р=0,001) (да/нет);
3) нарушение углеводного обмена (р=0,01) (да/нет);
4) перенесенный в анамнезе инфаркт миокарда (р=0,004) (да/нет).
Наличие у пациента верифицированного нарушения углеводного обмена увеличивает риск неблагоприятного течения постинфарктного периода в 1,6 раза.
Наличие перенесенного в анамнезе инфаркта миокарда увеличивает риск неблагоприятного течения постинфарктного периода в 2 раза.
Новым в предлагаемом изобретении является выделение основных параметров, влияющих на течение отдаленного постинфарктного периода у социально активной категории населения.
Общий процент правильно классифицированных исходов (коэффициент конкордации) - 57,1. Чувствительность модели - 70,5%, специфичность - 86,7%. Процент ложноположительных результатов классификации - 13,3%, процент ложноотрицательных результатов - 29,5%.
Полученная модель статистически значима (объединенный тест коэффициентов модели, хи-квадрат = 178,3, р<0,001). Качество подгонки модели удовлетворительное (критерий Хосмера-Лемешова, хи-квадрат = 3,1, р=0,361). Согласованность модели с данными недостаточная - R2 Найджелкерка - 0,412.
Модель позволила выявить совокупность факторов, значимо связанных с летальным исходом, и определить, какие факторы увеличивают, а какие из них снижают этот шанс.
Клинический пример №1.
Пациент А., 60 лет. В анамнезе: перенес в прошлом инфаркт миокарда и ишемический инсульт. Выявлены следующие факторы риска ИБС: нарушение углеводного обмена (сахарный диабет 2 типа, верифицированный до индексного инфаркта миокарда), артериальная гипертензия, курение. В сентябре 2005 г. госпитализировался в неспециализированный стационар с повторным субэндокардиальным инфарктом миокарда передней стенки левого желудочка. Острый период заболевания протекал без осложнений. При выписке рекомендованы нитраты короткого действия для купирования сердечно-болевого синдрома, антиагреганты и триметазидин.
При оценке вероятности неблагоприятного течения постинфарктного периода была использована разработанная модель:
умножаем на 100, получаем 87.
Таким образом, вероятность неблагоприятного течения постинфарктного периода в долгосрочной перспективе острого инфаркта миокарда составила 87%.
Действительно, 10 апреля 2007 года пациент перенес повторный (третий) инфаркт миокарда.
Клинический пример №2.
Пациент Б., 50 лет. Анамнез не отягощен ранее перенесенными сердечно-сосудистыми событиями. Выявлены следующие факторы риска ИБС: артериальная гипертензия и курение. В марте 2005 г. госпитализировался в специализированное лечебное учреждение с первичным острым инфарктом миокарда с подъемом сегмента ST нижней стенки левого желудочка. Острый период заболевания протекал без осложнений. При выписке пациенту рекомендован прием бета-адреноблокатора и ингибитора АПФ.
При оценке риска развития летального исхода была использована разработанная модель:
умножаем на 100, получаем 28.
Таким образом, вероятность неблагоприятного течения постинфарктного периода составила 28%.
Действительно, пациент преодолел рубеж 5-летнего наблюдения, посетив кардиолога в июне 2013 г. За время динамического наблюдения не зарегистрировано неблагоприятных сердечно-сосудистых событий.
Предполагаемый в качестве изобретения способ апробирован на 500 больных и позволяет прогнозировать неблагоприятный характер течения постинфарктного периода у пациентов трудоспособного возраста и провести соответствующую коррекцию лечебно-диагностической стратегии у данной категории пациентов.
Список литературы
1. Третье универсальное определение инфаркта миокарда // Приложение 1 Российский кардиологический журнал. - 2013. - №2 (100).
2. Марцевич С.Ю. Люберецкое исследование смертности (исследование ЛИС): факторы, влияющие на отдаленный прогноз жизни после перенесенного инфаркта миокарда / С.Ю. Марцевич, М.Л. Гинзбург // Профилактическая кардиология. - 2013. - №2. - С. 32-38.
3. Филимонов С.Н. Клиническое значение определения генетических и фенетических маркеров у больных инфарктом миокарда. - автореф. канд. мед. наук. 14.00.06. - Томск. - С. 20.
4. Виноградов А.В. Прогнозирование течения инфаркта миокарда по биохимическим маркерам / А.В. Виноградов, И.А. Журавлева, Н.Ю. Воеводина и др. // Кардиология. - 1999. - №2. - С. 39-40.
Способ прогнозирования неблагоприятного течения постинфарктного периода у пациентов трудоспособного возраста, характеризующийся тем, что определяют основные параметры: наличие бета-адреноблокаторв среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение ближайшего года после перенесенного инфаркта миокарда, госпитализация в специализированный стационар, наличие нарушений углеводного обмена, наличие перенесенного инфаркта миокарда в анамнезе и вероятность неблагоприятного течения постинфарктного периода определяют по формуле:
p=1/1+exp(-z)
где р - вероятность развития летального исхода;
z - дискриминантная функция,
а значение дискриминантной функции определяют по формуле:
z=-k+ax1+bx2+cx3+dx4,
где k - константа, определяемая при составлении уравнения мультипредикторной модели, x1-x4 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты a, b, c, d - весовые коэффициенты соответствующих показателей,
k=0,642,
x1 - наличие бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
а=-0,836 - есть бета-адреноблокаторы среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
а=0 - при отсутствии бета-адреноблокаторов среди лекарственных препаратов, рекомендованных при выписке из стационара и/или в течение года после инфаркта миокарда,
x2 - госпитализация в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
b=-0,738 - госпитализация в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
b=0 - при отсутствии госпитализации в остром периоде инфаркта миокарда в специализированный стационар или технически оснащенный сосудистый центр с возможностью проведения интервенционного лечения,
х3 - нарушение углеводного обмена,
с=0,485 - нарушение углеводного обмена,
с=0 - при отсутствии нарушения углеводного обмена,
x4 - перенесенный в анамнезе инфаркт миокарда,
d=0,817 - перенесенный в анамнезе инфаркт миокарда,
d=0 - при отсутствии перенесенного в анамнезе инфаркта миокарда,
и при значении p≥0,6 прогнозируют неблагоприятное течение постинфарктного периода.