Способ жидкофазного синтеза многокомпонентного керамического материала в системе zro2-y2o3-gd2o3-mgo для создания электролита твердооксидного топливного элемента
Иллюстрации
Показать всеИзобретение может быть использовано для создания электролита твердооксидного топливного элемента. Жидкофазный синтез многокомпонентного керамического материала в системе ZrO2-Y2O3-Gd2O3-MgO осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O, Gd(NO3)3⋅6H2O и Mg(NO3)2⋅6H2O. Из указанных солей готовят разбавленные растворы. Осуществляют обратное осаждение гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов и получения осадка. Гелеобразный осадок фильтруют и подвергают замораживанию при -25°С в течение 24 часов. Синтезированный порошок твердого раствора (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 подвергают термообработке при 800°С. Затем методом одноосного прессования при давлении 150 МПа формуют компакты. Указанные компакты обжигают при температуре 1400°С в трубчатой печи с изотермической выдержкой в 2 часа и скоростью нагрева 350-400°С/ч. Изобретение позволяет снизить степень агломерации осадка, повысить его дисперсность и гомогенность, а также полноту осаждения гидроксидов. 4 ил., 2 табл.
Реферат
В настоящее время поиск новых эффективных источников энергии, компактных, энергоемких, удовлетворяющих экологическим требованиям, является актуальной проблемой энерготехники.
Топливный элемент (ТЭ) - электрохимическая ячейка, напрямую преобразующая химическую энергию реакции восстановителя (топлива) и окислителя в электрическую энергию. Для работы ТЭ требуется постоянный подвод окислителя и восстановителя. При этом топливом могут служить любые углеводороды, а окислителем - воздух. Низкотемпературное электрохимическое сгорание топлива обеспечивает высокую экологичность процесса получения электроэнергии. Основными составляющими частями топливного элемента являются электролит, катод и анод. На катоде происходит восстановление окислителя с образованием аниона (например, иона О2-), а на аноде - окисление восстановителя с образованием катиона (например, иона Н+). Ион транспортируется через электролит, далее на одном из электродов происходит реакция окисления топлива с образованием продуктов реакции. Электроны при этом проходят через внешнюю цепь, создавая полезную энергию электрического тока.
Достоинствами топливных элементов являются высокий КПД (до 80%); продолжительная непрерывная работа, определяемая в основном запасами топлива; способность к значительным и продолжительным перегрузкам без заметного снижения напряжения; умеренные рабочие температуры и давление; бесшумность работы и отсутствие выделений; возможность использования воздуха как окислителя, возможность работы как на водороде любого качества, так и на любом углеводородном топливе (природный газ, легкие и тяжелые углеводороды и т.д.).
Твердооксидные топливные элементы (ТОТЭ) представляют собой привлекательные электрохимические генераторы, эффективно преобразующие химическую энергию взаимодействия водорода с кислородом в электрическую при минимальном воздействии на окружающую среду. На основе таких элементов созданы опытные установки мощностью до 100 кВт. ТОТЭ применимы, главным образом, для энергоустановок большой мощности, в которых возможно свести к минимуму относительную долю тепловых потерь в окружающее пространство. Одним из главных преимуществ этого типа топливных элементов является отсутствие жидкого электролита и возможность создание миниатюрного единичного элемента, состоящего из тонких слоев электродов и электролита.
Однако высокие рабочие температуры ТОТЭ (800-1000°С) обуславливают две основные проблемы, характерные для данного типа топливных элементов. Во-первых, для выхода на рабочую температуру ТОТЭ приходится нагревать с небольшой скоростью (менее 300°С ч-1) во избежание разрушения керамических элементов конструкции вследствие разницы их коэффициентов термического расширения (КТР). Во-вторых, высокая температура приводит к окислению или коррозии большинства металлов, диффузии материалов электродов в электролит с образованием непроводящих соединений, возникновению механических напряжений вследствие различных КТР. Снижение интервала рабочих температур ТОТЭ является важной задачей при разработке новых материалов для энергетики.
Диоксид циркония (ZrO2), стабилизированный оксидами редкоземельных металлов, является наиболее применяемым твердым электролитом при производстве ТОТЭ, работающих при температурах 900-1000°С. Существующая тенденция к удешевлению себестоимости ТОТЭ требует уменьшения интервала рабочих температур и, как следствие, использование, как новых материалов, так и новых технологий получения компонентов ТОТЭ. Перспективными, в данном случае, являются нанотехнологии формирования компонентов с использованием нанокристаллических порошков, позволяющих уменьшить энергетические затраты на производство, за счет снижения температур спекания электролита на 300-400°.
Из уровня техники известен цельнокерамический твердооксидный элемент по патенту РФ №2479075, который содержит анодный слой, катодный слой и электролитный слой, заключенный между анодным слоем и катодным слоем. Электролитный слой содержит легированный диоксид циркония и имеет толщину от 40 до 300 мкм. Анодный и катодный слои оба содержат легированный оксид церия или оба содержат легированный диоксид циркония. Многослойная структура, образованная анодным слоем, электролитным слоем и катодным слоем, является симметричной структурой. Изобретение позволяет создать ТОЭ, обладающий повышенной электродной производительностью и длительным сроком службы.
Известен твердооксидный топливный элемент (ТОТЭ) по патенту РФ №2128384, который включает тонкослойные пористые катодный и анодный катализаторы, диффузионно сцепленные с поверхностью твердого электролита. Катализаторы состоят из кластеров веществ с высокой каталитической активностью, а также из веществ, содержащих элементы переменной валентности, включенных в твердый электролит. Контактирующий с ними твердый электролит по крайней мере на глубину 2 мкм имеет аксиальную кристаллографическую текстуру с размером блоков 100-300 ангстрем и содержит не более чем на 0,1 общей толщины твердого электролита кластеры элементов переменной валентности. Способ изготовления ТОТЭ магнетронным напылением включает получение методом магнетронного синтеза кристаллических пористых слоев твердого электролита, содержащих кластеры каталитически активных веществ и элементов переменной валентности, диффузионно сцепленных с газоплотными слоями твердого электролита, имеющими по крайней мере на глубину 2 мкм аксиальную кристаллографическую текстуру и содержащими не более чем на 0,1 общей толщины твердого электролита кластеры элементов переменной валентности. Технический результат - повышение полезной электрической мощности ТОТЭ.
Эти патенты относятся к конструкции полной (собранной) топливной ячейки, состоящей из 2-х электродов и электролита. В них катоды и электролит состоят из твердооксидной керамики.
Задачей изобретения является создание одной части топливного элемента, а именно, твердооксидного керамического электролита, путем направленного жидкофазного синтеза на базе метода совместного осаждения гидроксидов для получения порошков-прекурсоров и керамических оксидных нанокомпозитов заданного химического состава в системе ZrO2-Y2O3-Gd2O3-MgO с улучшенными электрофизическими свойствами.
Выбор данного сложного состава обусловлен необходимостью стабилизации кубической структуры диоксида циркония в широком диапазоне температур (100-1200°С), что возможно достичь легированием ZrO2 оксидами с более низкой валентностью (Y2O3, Gd2O3, MgO). Это позволяет осуществить гетеровалентное замещение ионов в катионной подрешетке кубической кристаллической решетки ZrO2 и тем самым увеличить концентрацию кислородных вакансий, и, следовательно, улучшить электрофизические свойства керамики, а именно ионную долю проводимости, которая является основным критерием материала электролита при изготовлении ТОТЭ.
Для получения нанопорошков на основе диоксида циркония часто используют так называемые методы «мягкой» химии, одним из которых является метод химического осаждения. При синтезе многокомпонентных керамических композиций данным методом необходимо учитывать химические свойства каждого из реагентов, которые участвуют в синтезе. В связи с этим технология получения твердого раствора (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02 была разработана индивидуально.
Согласно изобретению способ жидкофазного синтеза многокомпонентного керамического материала в системе ZrO2-Y2O3-Gd2O3-MgO для создания электролита твердооксидного топливного элемента осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O, Gd(NO3)3⋅6H2O и Mg(NO3)2⋅6H2O, из которых приготавливают разбавленные растворы и осуществляют обратное осаждения гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов и получения осадка, затем гелеобразный осадок фильтруют и подвергают замораживанию при -25°С в течение 24 часов, после чего синтезированный порошок твердого раствора (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 подвергают термообработке при 800°С, затем методом одноосного прессования при давлении 150 МПа формуют компакты, которые обжигают при температуре 1400°С в печи фирмы «Nabertherm» с изотермической выдержкой в 2 часа и скоростью нагрева - 350-400°С/ч.
Технический результат, достигаемый при использовании заявленной совокупности существенных признаков, заключается в следующем. Использование разбавленных растворов при осаждении более целесообразно, чем концентрированных, так как это позволяет получить более дисперсный продукт осаждения. Метод обратного осаждения обеспечивает полное осаждение всех гидроксидов и получения осадка с высокой степенью гомогенности. Быстрое замораживание геля ослабляет силы взаимодействия кристаллических частиц осадка между собой и способствует снижению степени его агломерации.
Сущность изобретения поясняется чертежами, где на фиг. 1 представлена последовательность образования керамического нанокомпозита состава (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02: а - ксерогель (обжиг при 150°С, 1 ч), б - нанопорошок (обжиг 800°С, 1 ч), в - нанопорошок (обжиг 1400°С, 2 ч), (обозначения: - кубический твердый раствор на основе ZrO2 со структурой флюорита. (а=5,411 ), на фиг. 2 - стадии процесса термолиза ксерогеля состава (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02, полученного методом совместного осаждения, а) без замораживания ксерогеля; б) после замораживания ксерогеля при -25°С (24 ч), на фиг. 3 - микроструктура твердого раствора (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02, после спекания при 1400°С (2 ч), на фиг. 4 - температурная зависимость удельной электропроводности твердых растворов структуры флюорита на основе ZrO2 в интервале температур 350-870°С.
(1 - (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02; 2 - (ZrO2)0,92(Y2O3)0,05(MgO)0,03)
Заявленный способ осуществляют следующим образом.
В качестве исходных реагентов выбраны соли ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O, Gd(NO3)3⋅6H2O и Mg(NO3)2⋅6H2O, из которых были приготовлены разбавленные растворы (~0.1 М). Использование разбавленных растворов при осаждении более целесообразно, чем концентрированных, так как это позволяет получить более дисперсный продукт осаждения. Методом потенциометрического титрования установлено, что осаждение гидроксидов из соответствующих солей водным раствором аммиака (NH4OH) происходит в различных интервалах рН, поэтому для полного осаждения всех гидроксидов и получения осадка с высокой степенью гомогенности, был использован метод обратного осаждения. Величину рН в реакторе поддерживали буферным раствором NH4Cl в интервале 12.3-12.5. Экспериментально установлено, что концентрация водного раствора аммиака должна быть ~ 1 М, так как повышение концентрации NH4OH хотя бы до 3 М приводит к значительному укрупнению агломерированных частиц осадка (250 нм → 600 нм), данный факт связан с процессом коагуляции частиц осаждаемых гидроксидов.
Гидроксид циркония является основным компонентом продукта совместного осаждения в системе ZrO2-Y2O3-Gd2O3-MgO и для него характерны реакции гидролиза и полимеризации с образованием тетрамерных гидроксильных комплексов [Zr(OH)2⋅nH2O]48+, которые приводят к образованию «жестких» агломератов. Поэтому необходимо, чтобы время нахождения осадка в маточном растворе было минимальным.
Гелеобразный осадок фильтровали, а затем замораживали при -25°С (24 ч), в результате чего был получен рентгеноаморфный ксерогель, фиг. 1а, с площадью удельной поверхности 150 м2/г и средним размером пор ~3-4 нм. Быстрое замораживание геля ослабляет силы взаимодействия кристаллических частиц осадка между собой и способствует снижению степени его агломерации. Следует учитывать, что температура замораживания осадка не должна быть очень низкой, поскольку при быстром замораживании, например, при температуре жидкого азота, криокристаллизация гидроксидов может протекать лишь частично и есть вероятность сохранения некоторого количества аморфной фазы в гранулах образовавшегося ксерогеля, что приведет к нарушению гомогенности конечного продукта.
Процессы термолиза полученного ксерогеля исследовали методом ДТА, фиг. 2(а, б). Для сравнения на фиг. 2(а) приведены данные термического анализа для осадка, не подвергнутого низкотемпературной обработке при -25°С, из которых следует, что на кривой ДТА фиксируется два тепловых эффекта: эндотермический с максимумом ~140°С и экзотермический в области 435°С. Экзоэффект на кривой ДТА (450°С), по данным РФА, свидетельствует о процессе кристаллизации твердого раствора на основе диоксида циркония в метастабильной кубической структуре типа флюорита (f-ZrO2). На кривой ДТА, фиг. 2б, характеризующей процесс термолиза ксерогеля после замораживания при -25°С, отсутствует эндотермический эффект, соответствующий дегидратации, то есть удаление большей части воды происходит в процессе заморозки осадка. Потеря массы в замороженном ксерогеле составляет 10%. На кривой ДТА также фиксируется снижение температуры кристаллизации метастабильной фазы f-ZrO2 (450°С → 420°С), это связано с тем, что низкотемпературная обработка осадка позволяет законсервировать частицы в наносостоянии и увеличить химическую активность ксерогеля. Средний размер кристаллитов в синтезированном порошке твердого раствора (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 составляет 4-5 нм. Повышение температуры термообработки до 800°С приводит к образованию стабильной кубической структуры типа CaF2, фиг. 1б. При дальнейшем обжиге в интервале температур 800-1400°С сохраняется однофазность кубической структуры твердого раствора, фиг. 1в.
Из порошка на основе ZrO2, термообработанного при 800°С, методом одноосного прессования при давлении 150 МПа формовали компакты, которые обжигали при температуре 1400°С в трубчатой печи с программным управлением фирмы Nabertherm. Изотермическая выдержка составляла 2 ч, а скорость нагрева - 350-400°С/ч. Достаточно большая скорость нагрева была выбрана, чтобы уменьшить скорость роста кристаллитов. Также ранее было установлено, что плотность твердого раствора (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 зависит не только от скорости нагрева образцов, но и от скорости охлаждения.
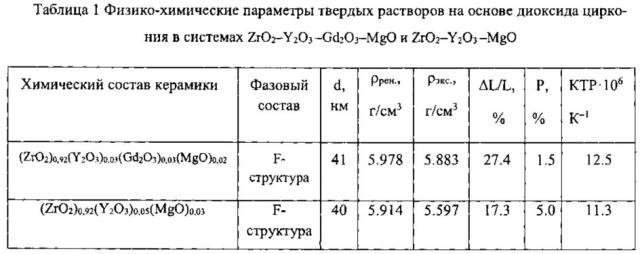
Свойства спеченной керамики состава (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 приведены в табл. 1. Для сравнения в таблице даны свойства керамики (ZrO2)0.92(Y2O3)0.05(MgO)0.03.
Методом электронной микроскопии исследована микроструктура керамики состава (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02, спеченной при 1400°С, фиг. 3. Из фиг. 3 очевидно, что данная керамика является однофазной, высокоплотной с четкой формой кристаллитов, размер которых составляет 40-45 нм, что соответствует размеру кристаллитов порошка, рассчитанных из данных РФА.
Проводимость легированного диоксида циркония зависит от концентрации легирующей примеси. Система на основе (ZrO2)0,92(Y2O3)0,08 широко используется в качестве материала электролита при изготовлении высокотемпературных твердооксидных топливных элементов ввиду удовлетворительных значений его ионной проводимости и стабильности в окислительных и восстановительных средах, однако физико-химические свойства твердых растворов состава (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02 не изучены.
Процессы дефектообразования в кубической решетке ZrO2 при добавлении Y2O3 происходят в соответствии со следующим квазихимическим уравнением:
где Y'Zr - ион иттрия на месте иона Zr4+с отрицательным зарядом, Voʺ - кислородная вакансия с положительным зарядом, компенсирующим заряд допанта. Аналогичный эффект (образование кислородных вакансий) достигается и при введении в ZrO2 других оксидов с более низкой степенью окисления металла, чем у циркония (MgO, Cd2O3). На фиг. 4 представлены кривые температурной зависимости удельной электропроводности синтезированных твердых растворов на основе ZrO2, а в таблице 2 - соотношение ионной и электронной долей проводимости твердых растворов состава (ZrO2)0,92(Y2O3)0,03(Gd2O3)0,03(MgO)0,02 и (ZrO2)0,92(Y2O3)0,05(MgO)0,03.
Как видно из фиг. 4 и табл. 2, температурная зависимость удельной электропроводности изучаемых твердых растворов на основе ZrO2 носит полупроводниковый характер, полученные твердые растворы обладают кислородно-ионным механизмом проводимости с числами переноса ионов tu=0,98, tu=0,89 и энергией активации 0,68, 0,60 эВ соответственно.
Полученный керамический нанокомпозит по своим механическим (открытая пористость, плотность, коэффициент термического расширения) и электрофизическим (величина, тип и механизм электропроводности) свойствам перспективен в качестве твердооксидного электролита и может быть использован в качестве электролита для ТОТЭ.
При создании новых материалов для современной энергетики ключевым вопросом является разработка технологий получения высококачественных оксидных нанокомпозитов с заданными физико-химическими, электрическими и механическими свойствами. В результате исследований, проведенных в данной работе, предложена технология жидкофазного синтеза многокомпонентного керамического материала в системе ZrO2-Y2O2-Gd2O3-MgO для создания электролита твердооксидного топливного элемента. Подобрано соотношение оксидов и оптимальные условия получения нанокристаллического мезопористого порошка твердого раствора на основе диоксида циркония и выявлены условия его консолидации. Установлено, что размер кристаллитов кубического твердого раствора типа флюорита (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 (а=5,411 ) не превышает 45 нм в интервале температур 400-1400°С; открытая пористость 1-3%, КТР - 11,6 10-6 К-1. Полученные электролитные материалы обладают кислородно-ионной электропроводностью, tн=98% в интервале температур 700-1000°С, σ=8,2⋅10-1См⋅см-1 при 800°С.
Таким образом, полученные результаты свидетельствуют о перспективности применения предложенной технологии синтеза керамики состава (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 для получения твердого электролита на основе диоксида циркония для твердооксидных топливных элементов.
Способ жидкофазного синтеза многокомпонентного керамического материала в системе ZrO2-Y2O3-Gd2O3-MgO для создания электролита твердооксидного топливного элемента осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O, Gd(NO3)3⋅6H2O и Mg(NO3)2⋅6H2O, из которых приготавливают разбавленные растворы и осуществляют обратное осаждение гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов и получения осадка, затем гелеобразный осадок фильтруют и подвергают замораживанию при -25°С в течение 24 часов, после чего синтезированный порошок твердого раствора (ZrO2)0.92(Y2O3)0.03(Gd2O3)0.03(MgO)0.02 подвергают термообработке при 800°С, затем методом одноосного прессования при давлении 150 МПа формуют компакты, которые обжигают при температуре 1400°С в трубчатой печи с изотермической выдержкой в 2 часа и скоростью нагрева 350-400°С/ч.