Устройство для исследования эффекта намагничивания растворов при их вращении
Иллюстрации
Показать всеИзобретение относится к электрохимии и физике магнетизма, в частности к электролитической диссоциации некоторых растворов, ионы которых существенно отличаются по их атомной массе. Заявлено устройство для исследования эффекта намагничивания растворов при их вращении, состоящее из последовательно связанных регулируемого источника постоянного тока, двигателя постоянного тока, датчика угловой скорости оси вращения двигателя постоянного тока, цилиндрического сосуда с осью его вращения из немагнитного материала, заполненного испытываемым раствором, измерителя напряженности магнитного поля, возникающего в испытываемом растворе, и устройства управления и обработки информации, второй вход которого связан с выходом датчика угловой скорости вращения оси двигателя, а управляющий выход соединен с регулируемым источником постоянного тока. Заявляемое техническое решение позволяет исследовать различные виды растворов на предмет возникновения их намагничивания и электрической поляризации при вращении, что дает дополнительную информацию о физико-химической структуре растворов и о природе электролитической диссоциации. 1 ил.
Реферат
Изобретение относится к электрохимии и физике магнетизма, в частности к электролитической диссоциации некоторых растворов, ионы которых существенно отличаются по их атомной массе.
Известно намагничивание ферромагнетика при его вращении - эффект Барнетта, а также намагничивание заряженных тел при их вращении под действием амперовых токов.
Известно, что диссоциация (от лат. dissociatio - разъединение) - это распад частицы (молекулы, радикала, иона) на несколько более простых частиц. Отношение числа распавшихся при диссоциации частиц к общему их числу до распада называется степенью диссоциации. В зависимости от характера воздействия, вызывающего диссоциацию, различают термическую диссоциацию, фотодиссоциацию, электролитическую диссоциацию, диссоциацию под действием ионизирующих излучений. Электролитическая диссоциация - полный или частичный распад молекул растворенного вещества на катионы и анионы. Электролитической диссоциацией называют также распад на катионы и анионы ионных кристаллов при растворении или расплавлении. Электролитическая диссоциация, как правило, происходит в полярных растворителях. Электролит - вещество, расплав или раствор, которое проводит электрический ток вследствие диссоциации на ионы. Примерами электролитов могут служить растворы кислот, солей и оснований. Электролиты - проводники второго рода, вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов и обладающие вследствие этого ионной проводимостью. Исходя из степени диссоциации, все электролиты делятся на две группы: сильные электролиты - электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора (сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты HCl, HBr, HNO3, HPO3), и слабые.
Наибольший интерес для оценки эффекта намагничивания растворов типа электролитов с высокой степенью диссоциации при их вращении представляют кислоты: азотная HNO3, метафосфорная HPO3 и ортофосфорная H3PO4, поскольку для них характерно высокое соотношение атомных масс положительных и отрицательных ионов в растворе. Реакции диссоциации для этих кислот записываются так:
| - соотношение атомных масс ионов 1:62 | |
| - соотношение атомных масс тонов 1:76 | |
| - соотношение атомных масс ионов 1:94 |
В этих реакциях диссоциации сверхтяжелыми являются отрицательные ионы (катионы).
В слабых растворах соли AgCl, наоборот, тяжелыми являются положительные ионы серебра (анионы) с соотношением атомных масс ионов 108:35.
Растворы кислот в воде, которая, в свою очередь, диссоциирует на ионы:
H2O↔H++OH-,
формируются в ионные диполи со структурой: отрицательные ионы воды связываются с положительными ионами кислоты, а положительные ионы воды связываются с отрицательными ионами кислоты. Например, для раствора азотной кислоты можно это изобразить как:
- соотношение атомных масс связанных ионов 63:18
Для мето- и ортофосфорных кислот эти соотношения масс равны соответственно как 77:18 и 95:18. При этом такие связанные ионы равнораспределены в объеме растворов и взаимно независимы. Каждый из таких связанных ионов представляет собой электрический диполь, а ориентация электрических диполей является произвольной (хаотической в температурном поле), так что в целом раствор является электронейтральным, то есть не заряженным.
Учитывая различие атомных весов для положительных и отрицательных связанных ионов, можно полагать, что под действием гравитационного поля Земли может произойти частичная поляризация таких растворов кислот, так как более тяжелые ионы в составе связанных ионов под действием силы тяготения будут стремиться развернуться вдоль вектора гравитационного поля, занимая при этом нижнее положение по сравнению с положением более легких ионов. Однако действие теплового поля, вызывающего броуновское движение связанных ионов, разрушает такую тенденцию к выстраиванию связанных ионов вдоль вектора гравитационного поля, и поляризации растворов под действием гравитационного поля Земли практически не наблюдается.
С целью увеличения ориентационного эффекта диполей связанных ионов с существенно различными атомными массами их компонент в данном техническом решении предлагается использовать вращательное движение сосуда с раствором, при котором под действием центростремительного ускорения a=ω2r, где ω - угловая скорость вращения сосуда с раствором, r - радиус - расстояние от оси вращения до рассматриваемого связанного иона в растворе на последний действуют пары сил: F1(r)=m-ω2r и F2(r)=m+ω2r, где m- и m+ - соответственно атомные массы отрицательных и положительных ионов в составе связанного свободного иона. Для рассматриваемых кислот массы отрицательных ионов существенно больше масс положительных, поэтому всегда F1(r)>>F2(r). Например, соотношение этих сил для связанной пары ионов в растворе азотной кислоты будет равно p=F1(r)/F2(r)=63/18=3,5. Для других указанных выше кислот эти соотношения сил будут равны соответственно как 4,28 и 5,28.
Неравенство этих сил с учетом длины d диполя связанного иона, а также его угловой ориентации β по отношению к вектору центростремительной силы, расположенной по соответствующему радиусу, приводит (без учета силы тяготения Земли) к возникновению вращательного момента M(r,β), действующего на такой диполь, равного M(r,β)=(F1(r)-F2(r))dcosβ=m+ω2r(p-1)dcosβ. Поскольку при достаточно быстром вращении сосуда с раствором возникает эффект ориентации диполей связанных ионов вдоль радиусов вращения, притом тем больший, чем больше длина r по радиусу расположения данного связанного иона во вращающемся сосуде от его оси вращения, то возникает электрическая поляризация раствора - отрицательные ионы связанных ионов становятся обращенными к периферии сосуда, и раствор становится как бы заряженным отрицательным зарядом на наружной цилиндрической поверхности (для рассматриваемых кислот), оставаясь в целом незаряженным, электронейтральным.
Если сосуд, выполненный из немагнитного материала, например стеклянный, имеет форму цилиндра радиуса R с его осью вращения, связанной с осью двигателя 3, то на его наружной стенке формируется отрицательный заряд q=2πRhejAη(δm-ω2R2/kT), где h -- длина цилиндрического сосуда, заполненного раствором кислоты, e - заряд электрона, j - поверхностная плотность тяжелых ионов [1/м2], A=(m--m+)/m+ (для азотной кислоты A=61), η(δm-ω2R2/kT) - некоторая безразмерная сложная функция, определяемая опытным путем, от параметров эксперимента и зависящая от абсолютной температуры T раствора (которая определяет степень хаоса броуновского движения ионов), δ - искомый безразмерный коэффициент, k - постоянная Больцмана. Тогда на основании закона об электромагнитной индукции Фарадея [1] вращение заряда q по замкнутому контуру с радиусом R приводит к возникновению магнитного момента MH от действия амперовых токов I=ωq/2π в контуре сечением s=πR2 и намагничиванию раствора при его вращении с величиной магнитного момента MH=IBs [Дж], где B - магнитная индукция, связанная с напряженностью магнитного поля выражением B(r)=μOH(r), где μO=1,256⋅10-6 Гн/м - магнитная постоянная. Поскольку в случае использования раствора кислот заряд q является отрицательным, то намагничивание происходит аналогично тому, как это имеет место в соленоиде с постоянным током в его обмотке (при круговом движении свободных электронов в проводнике). Магнитная полярность определяется по известному «правилу буравчика». Напряженность поля H(r) неоднородна по сечению s.
Аналоги заявляемого технического решения заявителем не выявлены.
Целью изобретения является установление факта намагничивания некоторых растворов при их вращении, а также получение дополнительной информации о физико-химической структуре растворов и о природе электролитической диссоциации.
Указанная цель достигается в устройстве для исследования эффекта намагничивания растворов при их вращении, состоящем из последовательно связанных регулируемого источника постоянного тока, двигателя постоянного тока, датчика угловой скорости оси вращения двигателя постоянного тока, цилиндрического сосуда с осью его вращения из немагнитного материала, заполненного испытываемым раствором, измерителя напряженности магнитного поля, возникающего в испытываемом растворе, и устройства управления и обработки информации, второй вход которого связан с выходом датчика угловой скорости вращения оси двигателя, а управляющий выход соединен с регулируемым источником постоянного тока.
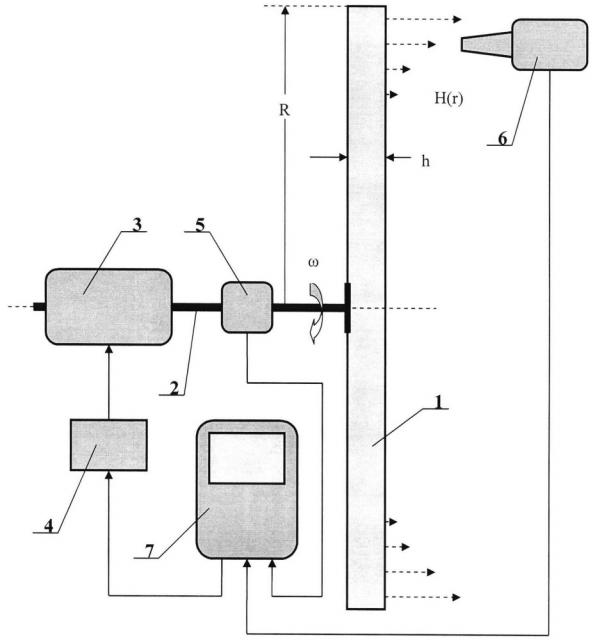
Заявляемое техническое решение понятно из прилагаемого чертежа. Оно содержит:
1 - цилиндрический сосуд из немагнитного материала, например стеклянный, заполненный исследуемым раствором, например раствором азотной кислоты,
2 - ось вращения цилиндрического сосуда, единая для элементов 3 и 5,
3 - двигатель постоянного тока, регулируемый по скорости вращения его ротора,
4 - регулируемый источник постоянного тока питания двигателя 3,
5 - датчик угловой скорости ω вращения оси 2 двигателя 3,
6 - сканирующий измеритель напряженности H(r) магнитного поля, индуцируемого в растворе,
7 - устройство управления и обработки информации (персональный компьютер).
Работа устройства понятна из его структуры. С помощью устройства управления и обработки информации 7 - персонального компьютера - задается скорость вращения цилиндрического сосуда 1 с исследуемым раствором, например, азотной, мета- или ортофосфорной кислоты, так что возникающие центростремительные ускорения существенно превосходят ускорение силы тяжести земной гравитации, за счет чего проявляется эффект ориентации диполей связанных ионов вдоль радиусов вращающегося цилиндрического сосуда, что приводит также и к вращению самого исследуемого раствора в установившемся режиме. Намагничивание раствора при этом объясняется ориентацией на внутренней поверхности цилиндрического сосуда более тяжелых отрицательных ионов раствора, то есть к наведенному на этой поверхности отрицательному заряду, вращение которого по контуру радиуса R создает намагничивание, фиксируемое сканирующим измерителем напряженности магнитного поля 6. При заданной конструкции устройства напряженность магнитного поля H(r) пропорциональна угловой скорости ω и кубу радиуса R цилиндрического сосуда и достаточно сложным образом зависит от параметров устройства, величины диполя d связанных ионов исследуемого раствора, типа раствора, концентрации его ионов и внешней температуры, действие которой приводит к хаотической ориентации электрических диполей связанных ионов раствора, снижая величину возникающего магнитного момента MH. Ясно, что при возрастании угловой скорости вращения ω раствора и радиуса r (в пределах 0≤r≤R) угол ориентации β уменьшается. Так называемое «магнитное насыщение» раствора максимально при β=0 теоретически при ω→∞. Этому процессу свойственно понятие «магнитной вязкости», как для ферромагнетиков, но по отношению к изменению угловой скорости ω вращения раствора. В растворах, характеризуемых параметром p→1, намагничивание практически не возникает.
Заявляемое техническое решение позволяет исследовать различные виды растворов на предмет их намагничивания (и электрической поляризации) при вращении, что дает дополнительную информацию о физико-химической структуре растворов и о природе электролитической диссоциации.
Литература
1. Ландау Л.Д., Лифшиц Е.М. Теория поля, изд. 7-е, исправленное. – М.: Наука, 1988, 512 с. (Теоретическая физика, том II).
Устройство для исследования эффекта намагничивания растворов при их вращении, состоящее из последовательно связанных регулируемого источника постоянного тока, двигателя постоянного тока, датчика угловой скорости оси вращения двигателя постоянного тока, цилиндрического сосуда с осью его вращения из немагнитного материала, заполненного испытываемым раствором, измерителя напряженности магнитного поля, возникающего в испытываемом растворе, и устройства управления и обработки информации, второй вход которого связан с выходом датчика угловой скорости вращения оси двигателя, а управляющий выход соединен с регулируемым источником постоянного тока.