Прибор для автоматизированного бесклеточного получения белков и способ получения белков с применением данного прибора
Иллюстрации
Показать всеГруппа изобретений относится к области биохимии. Предложена автоматизированная система бесклеточного получения белка, способ бесклеточного получения белка и реакционный набор для автоматизированного бесклеточного получения белка. Система включает блок реакции экспрессии белка, блок контроля температуры реакции, массив пипеток, блок перемещения массива пипеток, блок очистки белков и блок крепления многолуночных планшетов с многолуночным планшетом. Причём блок реакции экспрессии белка содержит реакционный сосуд с диализной трубкой. Блок очистки белков включает устройство применения магнитного поля для крепления целевого белка к магнитным микросферам с последующим прикреплением магнитных микросфер к стенке, а многолуночный планшет обеспечен растворами, необходимыми для получения белков. Способ включает стадии получения смеси для бесклеточной экспрессии белка, экспрессии белка, очистки белка с использованием магнитных частиц и диализа очищенного белка. Реакционный набор содержит набор многолуночных планшетов с индивидуальными лунками для хранения раствора с аминокислотами, необходимыми для транскрипции и трансляции, источником энергии и буфером, диализные трубки с диализной мембраной. Изобретения обеспечивают повышение уровня экспрессии белка. 3 н. и 21 з.п. ф-лы, 11 ил., 8 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к автоматизированной системе бесклеточного получения белка и к способу получения белка с применением данной системы. Более конкретно, настоящее изобретение относится к автоматизированной системе бесклеточного получения белка, включающей: блок реакции экспрессии белка, содержащий реакционный сосуд, который включает множество диализных трубок, каждая из которых включает диализную мембрану и открыта сверху; блок контроля температуры реакции, сконфигурированный для нагревания или охлаждения реакционного сосуда; массив пипеток, включающий множество пипеток и сконфигурированный для набора или для слива растворов с помощью пипеток; блок движения массива пипеток, сконфигурированный для движения массива пипеток в направлении вверх и вниз, в прямом и в обратном направлении или в направлении влево и вправо, для того, чтобы перемещать растворы; блок очистки белка, включающий устройство применения магнитного поля; и блок закрепления многолуночного планшета, содержащий закрепленный в нем набор многолуночных планшетов, сконфигурированный для подачи растворов, которые используются для получения белка, и к способу получения белка с использованием данной системы.
Кроме того, более конкретно, настоящее изобретение относится к автоматизированной системе получения белка и к способу, с помощью которого можно синтезировать свободный от аффинной метки чистый белок и с помощью которого можно автоматизировано и быстро заменять раствор элюата, содержащий конечный очищенный белок с целевым буфером для хранения белка с помощью многостадийного диализа, и таким образом, можно автоматизировано и удобно получать множество белков в больших количествах.
Кроме того, настоящее изобретение относится к реакционному набору для автоматизированного бесклеточного получения белка, который включает набор многолуночных планшетов для хранения раствора, необходимого для получения белка, и диализную трубку, включающую диализную мембрану.
Уровень техники
Обычно способы получения рекомбинантных белков осуществляют с использованием различных клеточных линий, таких как Е. coli, дрожжевые и животные клетки. Эти способы включают трансформацию вектора, экспрессирующего рекомбинантый белок, в клеточную линию, культивирование клеточной линии для экспрессии целевого белка и лизис клеток для очистки целевого белка.
Этим способам необходим процесс отбора штамма по стабильной экспрессии рекомбинантного белка с последующим осуществлением ряда процессов, включающих культивирование клеток, разрушение клеток и очистку белка. Таким образом, эти способы требуют большие количества времени и усилий.
Кроме того, цитотоксические белки или мембранные белки трудно экспрессировать. Таким образом, в случае этих белков необходимо предпринять множество усилий, таких как подбор различных условий экспрессии. Поэтому существует проблема, которая заключается в том, что для получения одного белка необходимо потратить от нескольких дней до нескольких месяцев.
Для преодоления этой проблемы были разработаны бесклеточные способы экспрессии белка для экспрессии белка в реакционном сосуде, таком как пробирка, в течение короткого периода времени без использования клеток, а также были разработаны ассоциированные с этими способами продукты. Эти способы предназначены для экспрессии целевого белка без клеточной культуры. В этих способах используется вектор, содержащий ген-мишень, клеточный экстракт, полученный с помощью выделения/очистки после культивирования клеток, и раствор для экспрессии белка, включающий аминокислоты, трифосфат рибонуклеиновую кислоту, источник энергии и буфер. В этих способах ген, кодирующий целевой белок, транскрибируется в мРНК с помощью РНК-полимеразы, содержащейся в клеточном экстракте, и мРНК транслируется в белок с использованием рибосомы, тРНК и тому подобного, содержащихся в клеточном экстракте.
Бесклеточный способ экспрессии белка был коммерциализирован «Roche», «Promega» и другими. В данном способе матричная ДНК (например, экспрессирующий вектор, ПЦР-продукт и т.д.), способная экспрессировать белок, клеточный лизат и раствор для экспрессии, включающий аминокислоты, трифосфат рибонуклеиновые кислоты и источник энергии добавляют в пробирку, и затем дают возможность пройти реакции при подходящей температуре (30-40°С) в течение подходящего времени (1-3 часа) для экспрессии целевого белка. Данный способ предпочтителен по отношению к способу экспрессии белка с использованием клеток в том, что требуется значительно меньшее количество времени, а также могут экспрессироваться цитотоксические белки или мембранные белки.
Кроме того, были разработаны системы, способные продуцировать белки подходящим образом с помощью автоматизированного осуществления бесклеточной экспрессии белка.
Такие системы включают RTS (Система быстрой трансляции), разработанную «Roche». RTS может осуществлять бесклеточную экспрессию белка с высокой эффективностью. В данной системе диализная мембрана располагается на дне реакционного сосуда для предотвращения остановки реакции из-за истощения источника энергии и накопления ингибитора белкового синтеза, такого как фосфорная кислота, в ходе бесклеточной экспрессии белка. Для диализа данный реакционный сосуд помещают, по меньшей мере, в сосуд 10-кратного объема, содержащий раствор низкомолекулярных соединений для экспрессии с целью максимизации реакции. Как описано у Kim, D.-M. and Choi, C.-Y., Biotechnol. Prog., 12(5):645, 1996, данный принцип основан на принципе, согласно которому уровень экспрессии белка может быть повышен до 10 раз путем непрерывной замены раствора низкомолекулярных соединений для экспрессии, содержащего трифосфат рибонуклеиновую кислоту, аминокислоты и источник энергии, через диализную мембрану.
Однако данный способ имеет проблему, которая заключается в том, что также должен использоваться раствор низкомолекулярных соединений для экспрессии, имеющий объем, соответствующий, по меньшей мере, 10-кратному объему раствора для экспрессии, при этом общий объем реакционного сосуда становится больше и, таким образом, размер системы значительно повышается, когда одновременно в одной параллели необходимо синтезировать различные типы белков. Кроме того, система не автоматизирована и может осуществлять только функцию перемешивания реакционного раствора при определенной температуре. Таким образом, по окончании реакции должен быть осуществлен отдельный процесс, такой как очистка синтезированного белка.
Институт RIKEN (Япония) сконструировал крупномасштабную систему автоматизированной экспрессии белка, хотя подробная структура системы не была объяснена (Alexander Spirin & James R. Swartz, Cell-Free Protein Synthesis, p103, Fig 6.3B). Yaeta Endo et al. разработали бесклеточный способ экспрессии белка с использованием экстракта зародышей пшеницы и разработали автоматизированную систему на основе принципа, отличного от системы RTS. Кроме того, Yaeta Endo et al. смогли повысить выход белковой экспрессии путем разведения раствора для бесклеточной экспрессии белка раствором низкомолекулярных соединений для экспрессии и концентрированием разведения (US 2006/0257997 A1).
Однако вышеописанная автоматизированная система имеет проблемы, заключающиеся в том, что система является дорогостоящей из-за своей сложной структуры, в ней отсутствует функция очистки белка, как в системе RTS, и с помощью нее затруднительно получать несколько типов белков.
При этом образец, содержащий рекомбинантный белок, экспрессированный с помощью клеточной культуры или с помощью метода бесклеточной экспрессии, включает различные типы белков дополнительно к белку-мишени. Для того, чтобы легко очистить белок-мишень из данного образца используется технология прикрепления аффинной метки (гистидиновая метка). В данной технологии при введении в матричный ген последовательности, кодирующей гистидиновую метку, ее прикрепляют к С- или к N-концу белка, экспрессируемого с матричного гена, и белок-мишень может быть легко получен с высокой чистотой путем выделения/очистки белка с использованием аффинности между меткой и ионами металлов (ионы никеля, ионы кобальта и т.д.).
Однако аффинная метка, которая используется для очистки, может оказывать отрицательное воздействие на активность и структуру целевого белка. По этой причине для получения белков-мишеней для исследования белковой функции и в медицинских целях необходим способ удаления метки.
Авторы изобретения (Bioneer) разработали автоматизированную систему белкового синтеза «ExiProgen™» (Публикации корейских патентов No. 10-2011-0121588 и 10-2013-0023091) и связанный набор реактивов. Данную систему сконфигурировали для автоматизированного проведения бесклеточной реакции белковой экспрессии и очистки экспрессированного белка. В данной системе матричная ДНК и растворы, требуемые для реакции, могут автоматизированно смешиваться с целью автоматизированного осуществления реакции белковой экспрессии и могут поддерживаться при подходящей температуре реакции. Кроме того, все процессы, включающие синтез РНК из ДНК и экспрессию белка из РНК, могут поддерживаться при оптимальной температуре. Кроме того, для облегчения очистки целевого белка из смеси образца, содержащей экспрессированный белок, аффинную метку, такую как олигогистидин, присоединяют к белку-мишени, и в таком состоянии белок-мишень экспрессируют и автоматизировано очищают с использованием магнитных микросфер, включающих ионы металлов (ионы никеля, кобальта и т.д.). Вышеописанные «ExiProgen™» и набор реактивов могут одновременно экспрессировать и очищать различные типы белков, но имеются проблемы, заключающиеся в том, что из-за массовой экспрессии белка источник энергии истощается с течением времени, и экспрессия белка прекращается при накоплении ингибитора экспрессии белка, и, таким образом, конечный уровень экспрессированного белка низкий.
Для повышения уровня экспрессии белка одновременно должны поставляться раствор низкомолекулярных соединений для экспрессии, содержащий трифосфат рибоуклеиновые кислоты, аминокислоты и источник энергии и удаляться ингибиторы экспрессии белка. Для автоматизированного осуществления таких операций требуются новые типы реактора и система.
Авторы настоящего изобретения предприняли усилия для разработки системы и набора реактивов, которые могут преодолеть недостатки низкой эффективности экспрессии белка автоматического белкового синтезатора «ExiProgen™», и в то же время повысить уровень экспрессии целевого белка при этом с исключением необходимости повышения размера системы благодаря применению раствора низкомолекулярных соединений для экспрессии в 10-кратном количестве или более по отношению к количеству раствора для экспрессии. В результате авторы настоящего изобретения разработали систему, способную повышать уровень экспрессии целевого белка путем одновременного снабжения раствором низкомолекулярных соединений для экспрессии с помощью диализной мембраны в процессе реакции бесклеточной экспрессии белка и удаления ингибиторов экспрессии белка.
Было обнаружено, что система, разработанная авторами настоящего изобретения, обладает эффектом повышения эффективности экспрессии белка при автоматизированном снабжении в течение нескольких стадий, может автоматизировано очищать экспрессированный белок как в стандартной системе «ExiProgen™», и может автоматизировано заменять раствор целевого белка, который содержит высококонцентрированный элюат, на буфер для хранения целевого белка после очистки.
Кроме того, авторы настоящего изобретения обнаружили, что при получении белка с удаляемой аффинной меткой, используемой для очистки, чистый белок может быть получен при автоматизированном удалении аффинной метки во время очистки белка путем обработки протеазой, которая распознает и расщепляет специфичную аминокислотную последовательность белка, что завершает настоящее изобретение.
Публикации предшествующего уровня техники
Патентные документы
Патентный документ 1: Корейский патент с регистрационным номером 10-0385298 В1 (13 мая 2003 года)
Патентный документ 2: Корейский патент с регистрационным номером 10-0534558 B1 (1 декабря 2005 года)
Патентный документ 3: Корейский патент с регистрационным номером 10-0733712 B1 (23 июня 2007 года)
Патентный документ 4: Заявка на патент США No. 2006-0257997 A1 (16 ноября 2006 года)
Непатентные документы:
Cheolju Lee, et al., Development of High-Throughput Protein Production Technology, Ministry of Science and Technology, 17-30, 2005
Alexander Spirin & James R. Swartz, Cell-Free Protein Synthesis, p103, Fig 6.3B
Описание изобретения
Техническая проблема
Цель настоящего изобретения заключается в обеспечении автоматизированной системы бесклеточного получения белка, которая может повышать уровень экспрессии целевого белка с помощью автоматизированного и одновременного снабжения небольшим количеством раствора низкомолекулярных соединений для экспрессии через диализную мембрану в процессе реакции бесклеточной экспрессии белка и удаления ингибиторов экспрессии белка во время реакции, и в обеспечении способа получения белка с использованием данной системы.
Техническое решение
Для осуществления вышеописанной задачи в настоящем изобретении предлагается автоматизированная система бесклеточного получения белка, содержащая: блок реакции экспрессии белка, содержащий реакционный сосуд, который включает множество диализных трубок, каждая из которых включает диализную мембрану и открыта сверху; блок контроля температуры реакции, сконфигурированный для нагревания или охлаждения реакционного сосуда; массив пипеток, включающий множество пипеток и сконфигурированный для забора или для слива растворов с использованием пипеток; блок движения массива пипеток, сконфигурированный для движения массива пипеток в направлении вверх и вниз, в прямом и в обратном направлении или в направлении влево и вправо, для перемещения растворов; блок очистки белка, включающий устройство применения магнитного поля; и блок закрепления многолуночного планшета, содержащий закрепленный в нем набор многолуночных планшетов, сконфигурированный для подачи растворов, которые используются при получении белка.
В настоящем изобретении также предлагается способ автоматизированного бесклеточного получения белка, включающий стадии: (a) приготовления смеси бесклеточной экспрессии белка (S1); (b) экспрессии белка с использованием раствора низкомолекулярных веществ для экспрессии (S2); (c) очистки белка с использованием магнитных микросфер (S3); и (d) диализа очищенного белка с использованием буфера для хранения белка (S4).
В настоящем изобретении также предлагается способ автоматизированного бесклеточного получения белка, включающий стадии: (a) приготовления смеси бесклеточной экспрессии белка (S1); (b) экспрессии белка с использованием раствора низкомолекулярных веществ для экспрессии (S2); стадии (c') очистки чистого целевого белка без аффинной метки (S3'); и (d) диализа очищенного белка с использованием буфера для хранения белка (S4).
В настоящем изобретении также предлагается набор реактивов для автоматизированного бесклеточного получения белка, который содержит набор реактивов с многолуночным планшетом, содержащим индивидуальные отдельные лунки для хранения раствора, требующегося для бесклеточного получения белка, а также предлагается диализная трубка, включающую диализную мембрану.
Краткое описание чертежей
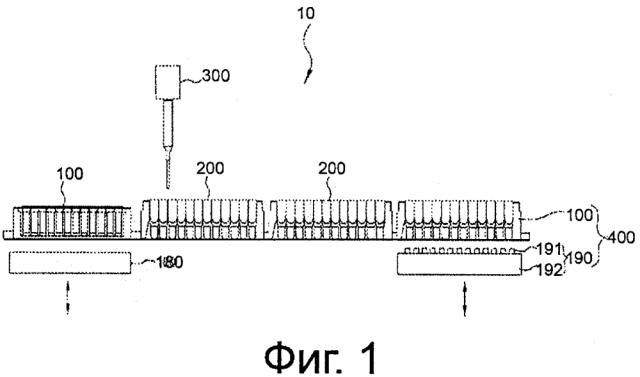
Фиг. 1 представляет собой схематическое изображение автоматизированной системы бесклеточного получения белка согласно настоящему изобретению.
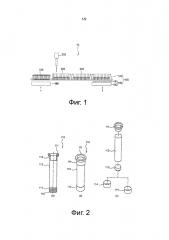
Фиг. 2 представляет собой изображение в разрезе (a), перспективное изображение (b) и внутренний вид (c) диализной трубки согласно настоящему изобретению.
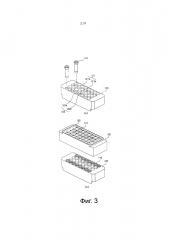
Фиг. 3 представляет собой перспективное изображение и внутренний вид первого реакционного сосуда согласно настоящему изобретению.
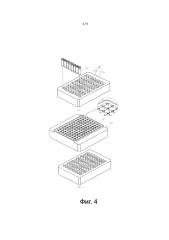
Фиг. 4 представляет собой перспективное изображение и внутренний вид второго реакционного сосуда согласно настоящему изобретению.
Фиг. 5 представляет собой перспективное изображение и внутренний вид третьего реакционного сосуда согласно настоящему изобретению.
Фиг. 6 представляет собой перспективное изображение и внутренний вид четвертого реакционного сосуда согласно настоящему изобретению.
Фиг. 7 представляет собой фронтальное изображение массива пипеток согласно настоящему изобретению.
Фиг. 8 представляет собой схема работы (А) автоматизированного способа бесклеточного получения белка согласно настоящему изобретению и перспективное изображение (В) набора многолуночных планшетов согласно настоящему изобретению.
Фиг. 9 представляет собой схему работы способа получения белка с использованием автоматизированной системы бесклеточного получения белка согласно настоящему изобретению.
Фиг. 10 представляет собой результаты анализа полученного согласно настоящему изобретению целевого белка на геле SDS-PAGE.
(А): М: Маркер размера белка Bioneer AccuLadder™ (низкомолекулярный); Е: экспрессированный образец AcGFP; Р: очищенный образец AcGFP; (В): М: Маркер размера белка Bioneer AccuLadder™ (низкомолекулярный); AcGFP: очищенный образец AcGFP; RFP: очищенный образец RFP; CAT: очищенный образец CAT; AcGFP (ПЦР-продукт): очищенный образец ПЦР-продукта AcGFP.
Фиг. 11 представляет собой результаты анализа SDS-PAGE и Вестерн-блот-анализа чистого целевого белка, не содержащего аффинную метку, полученного согласно настоящему изобретению.
(А): Результаты SDS-PAGE анализа TEV-AcGFP; М: Маркер размера белка Bioneer AccuLadder™ (низкомолекулярный); Е: образец экспрессированного AcGFP; Р: образец очищенного AcGFP; (В) сравнение образцов по присутствию или отсутствию гистидиновой метки; Контроль: TEV-AcGFP, очищенный с помощью метода очистки целевого белка с аффинной меткой; Без аффинной метки: образец TEV-AcGFP, очищенный с помощью метода очистки целевого белка, не содержащего аффинную метку.
Цифровые обозначения:
10: автоматизированная система бесклеточного получения белка
100: реакционный блок экспрессии белка
110: диализная трубка 111: верхняя структура
112: диализная мембрана 113: нижняя структура
114: эластичная трубка 120: первый реакционный сосуд
121а: отверстие диализной трубки
121b: отверстие для раствора низкомолекулярных веществ для экспрессии
122а: отверстие диализной трубки 122b: отверстие для диализного раствора
130: крышка первого реакционного сосуда 131: отверстие
132: пленка, предотвращающая выпаривание
140: второй реакционный сосуд
141а: отверстие диализной трубки
141b: отверстие для раствора низкомолекулярных веществ для экспрессии
150: крышка первого реакционного сосуда 151: отверстие
152: пленка, предотвращающая выпаривание
160: третий реакционный сосуд
161: сосуд для раствора низкомолекулярных веществ для экспрессии
162: крышка сосуда с раствором
163: вход 164: выход
165: насос-дозатор 166: многоканальный клапан
167: контейнер с раствором 168: контрольный клапан
169: контейнер для отходов 170: четвертый реакционный сосуд
171: сосуд для раствора низкомолекулярных веществ для экспрессии
172: крышка сосуда для раствора
173: прохождение раствора 174: реверсивный насос-дозатор 175: многоканальный клапан 176: контейнер для раствора
177: контейнер для отходов
180: блок контроля температуры реакции
190: устройство применения магнитного поля 191: магнит
192: блок крепления магнита 200, 200': набор многолуночных плашнетов
300: массив пипеток 310: пипетка
320: блок движения массива пипеток
400: блок очистки белка
S1-S4: автоматизированный способ бесклеточного получения белка
Лучший вариант осуществления изобретения
Если иное не определено, все технические и научные термины, использованные здесь, имеют те же смыслы, которые вкладываются в них обычным специалистом области, к которой принадлежит данное изобретение. Как правило, номенклатура, используемая в данном документе, и экспериментальные методы хорошо известны и традиционно используются в данной области.
В одном аспекте, настоящее изобретение относится к автоматизированной системе бесклеточного получения белка, содержащей: блок реакции экспрессии белка, содержащий реакционный сосуд, который включает множество диализных трубок, каждая из которых включает диализную мембрану и открыта сверху; блок контроля температуры реакции, сконфигурированный для нагревания или охлаждения реакционного сосуда; массив пипеток, включающий множество пипеток и сконфигурированный для всасывания или для слива растворов с использованием пипеток; блок движения массива пипеток, сконфигурированный для движения массива пипеток в направлении вверх и вниз, в прямом и в обратном направлении или в направлении влево и вправо для движения растворов; блок очистки белка, включающий устройство применения магнитного поля; и блок крепления многолуночного планшета, содержащий закрепленный в нем набор многолуночных планшетов, сконфигурированный для подачи растворов, которые используются для получения белка.
Каждая из диализных трубок содержит: цилиндрическую диализную мембрану, имеющую определенную длину; нижнюю структуру, встроенную на дне диализной мембраны и имеющую форму диска; и верхнюю структуру, встроенную сверху диализной мембраны и имеющую кольцевую структуру с тавровым профилем.
Каждая из диализных трубок дополнительно включает эластичные трубки, встроенные вокруг внешней периферической поверхности участков диализной мембраны, которые вступают в контакт с верхней структурой и с нижней структурой.
Реакционный сосуд дополнительно включает крышку реакционного сосуда, сконфигурированную для закрытия реакционного сосуда для предотвращения выпаривания раствора из диализных трубок, причем крышка реакционного сосуда имеет множество прорезей, которые позволяют вставлять пипетки диализные трубки.
Блок реакции экспрессии белка содержит: множество отверстий для диализных трубок, сформированных сверху и сконфигурированных для приема диализных трубок; и множество отверстий для раствора низкомолекулярных веществ для экспрессии для жидкостного сообщения с отверстиями диализных трубок.
Блок реакции экспрессии белка дополнительно содержит блок диализа белка, включающий: множество отверстий для диализных трубок, сформированных сверху и сконфигурированных для приема диализных трубок; и множество отверстий для диализного раствора, образованных по соседству с отверстиями диализных трубок, для жидкостного сообщения с отверстиями диализных трубок и сконфигурированных для приема буфера для хранения белка.
Блок реакции экспрессии белка содержит: открываемый/закрываемый выход, сконфигурированный так, чтобы дать возможность раствору вытекать из реакционного сосуда; контейнер для отходов, связанный с выходом так, чтобы было жидкостное сообщение с выходом; вход, сконфигурированный так, чтобы посредством него была возможность введения раствора в реакционный сосуд; насос-дозатор, сконфигурированный для подачи раствора на вход; и один или несколько контейнеров для растворов, связанных с насосом-дозатором.
Блок реакции экспрессии белка дополнительно включает многоканальный клапан, сконфигурированный так, чтобы одна его сторона была связана с насосом-дозатором, а другая его сторона имела жидкостное сообщение с любым выбранным контейнером среди контейнеров для растворов.
Блок реакции экспрессии белка содержит: канал для раствора, сконфигурированный так, чтобы дать возможность раствору подаваться или вливаться в реакционный сосуд или из реакционного сосуда; реверсивный насос-дозатор, связанный с каналом для раствора и сконфигурированный для подачи или вливания раствора в реакционный сосуд или из реакционного сосуда; один или несколько контейнеров для раствора, связанных с реверсивным насосом-дозатором; один или несколько контейнеров для отходов, связанных с реверсивным насосом-дозатором; и многоканальный клапан, сконфигурированный так, чтобы одна его сторона была связана с реверсивным насосом-дозатором, а другая его сторона была связана с контейнерами для растворов и с контейнерами для отходов, так чтобы любой выбранный контейнер из числа контейнеров для растворов или контейнеров для отходов имел жидкостное сообщение с реверсивным насосом-дозатором посредством многоканального клапана.
Массив пипеток содержит 1-96 пипеток, расположенных в 1-12 рядов согласно размеру реакционного сосуда и количеству пипеток и сконфигурирован так, чтобы у пипеток была возможность автоматически присоединяться или отсоединяться, и сконфигурирован для всасывания или сбрасывания целевого количества раствора.
Далее настоящее изобретение будет описано более подробно.
Фиг. 1 иллюстрирует общую конфигурацию автоматизированной системы 10 бесклеточного получения белка согласно настоящему изобретению.
Согласно фиг. 1, автоматизированная система бесклеточного получения белка по настоящему изобретению содержит блок 100 реакции экспрессии белка, блок 180 контроля температуры реакции, массив пипеток 300, блок 320 движения массива пипеток, блок 400 очистки белка, и встроенный блок многолуночных планшетов, который можно оборудовать наборами многолуночных планшетов 200 и 200'.
Блок 100 реакции экспрессии белка представляет собой сосуд, имеющий множество гнезд, в которых могут располагаться диализные трубки 110, содержащие цилиндрическую диализную мембрану 112 и открытые сверху, так что их верхняя часть экспонирована из гнезд, и они располагаются на определенном расстоянии друг от друга в вертикальном и в горизонтальном направлениях. Сосуд может принимать раствор низкомолекулярных веществ для экспрессии или что-то подобное. Блок 100 реакции экспрессии белка содержит реакционный сосуд 120, 140, 160 или 170, сконфигурированный для добавления или удаления раствора низкомолекулярных веществ для экспрессии для контакта с внешней областью диализной мембраны 112.
Блок 180 контроля температуры реакции помещают под реакционным сосудом 120, 140, 160 или 170, и он служит для нагревания или охлаждения реакционного сосуда 120, 140, 160 или 170.
Массив пипеток 300 содержит множество пипеток 310, имеющих такое же расположение, что и множество диализных трубок 110, которые вставляются в блок 100 реакции экспрессии белка, и сконфигурирован для всасывания или для сброса раствора с помощью пипеток 310.
Блок 320 движения массива пипеток сконфигурирован для движения массива пипеток 300 в направлении вверх и вниз, в прямом и в обратном направлении или в направлении влево и вправо так, чтобы переносить раствор из блока реакции экспрессии белка, из набора многолуночных планшетов или т.п.
Блок 400 очистки белка содержит устройство применения магнитного поля 190, сконфигурированный для прикрепления целевого белка к магнитным микросферам с последующим прикреплением магнитных микросфер к стенке.
Устройство применения магнитного поля 190 содержит блок крепления магнита 192, содержащий встроенный магнит 191, которое служит для перемещения блока крепления магнита вверх или вниз для применения или удаления магнитного поля.
Кроме того, блок 180 контроля температуры реакции и устройство применения магнитного поля 190 могут быть сконструированы отдельно, или могут быть сконструированы для одновременного контроля в одном и том же положении. Другими словами, как представлено на чертежах, блок очистки белка 400 не предоставляется отдельно, а каждый из реакционных сосудов 120, 140, 160 и 170 может включать одновременно блок 100 реакции экспрессии белка и блок 400 очистки белка, и блок 180 контроля температуры реакции и устройство применения магнитного поля 190 могут передвигаться и помещаться под каждым реакционным сосудом.
Далее конфигурация диализной трубки 110 по настоящему изобретению будет подробно описана со ссылкой на фиг. 2.
Согласно фиг. 2, то диализная трубка 110 по настоящему изобретению содержит диализную мембрану 112, нижнюю структуру 113, верхнюю структуру 111 и эластичную трубку 114.
Диализная мембрана 112 придана цилиндрическая форма, имеющая определенный размер, и нижняя структура 113 имеет форму диска и вставляется в дно диализной мембраны. Кроме того, верхняя структура 111 представляет собой кольцевую структуру, имеющую тавровый профиль, вставляется в верхнюю часть диализной мембраны 112, и имеет отверстие, в которое можно вводить раствор.
Диализная трубка 110 предпочтительно включает эластичную трубку 114, расположенную вокруг внешней области диализной мембраны 112, которая вступает в контакт с верхней структурой 111 и нижней структурой 113 с целью повышения адгезии между ними.
Кроме того, верхняя структура 111 имеет диаметр больше, чем диаметр дна диализной трубки 110 так, что она может быть остановлена верхним концом отверстия диализной трубки 121а или 141а реакционного сосуда 120, 140, 160 или 170, когда диализная трубка 110 вставляется в отверстие для диализной трубки.
Более конкретно, для монтирования диализной трубки 110 по стандартному 96-луночному формату, верхняя структура 111 предпочтительно имеет диаметр 9 мм или менее, а диализная мембрана 112 предпочтительно имеет диаметр 6,37 мм или 7,62 мм.
В предшествующем уровне техники, диализная мембрана устанавливается внизу реакционного сосуда, тогда как в настоящем изобретении диализная мембрана 112 является цилиндрической по форме и, таким образом, имеет большую поверхность контакта с низкомолекулярным раствором для экспрессии, позволяя, таким образом, эффективно осуществить реакцию.
Далее конфигурация реакционных сосудов 120, 140, 160 и 170 по настоящему изобретению будет подробно описана со ссылкой на фиг. 3-6.
Фиг. 3-6 представляют различные воплощения реакционных сосудов 120, 140, 160 и 170 по настоящему изобретению. Конкретно, фиг. 3 представляет первый реакционный сосуд 120, способный принимать 16 диализных трубок; фиг. 4 представляет второй реакционный сосуд 140, способный принимать 48 диализных трубок; фиг. 5 представляет третий реакционный сосуд 160, способный принимать 96 диализных трубок; и фиг. 6 представляет четвертый реакционный сосуд 170, способный принимать 96 диализных трубок.
Первый реакционный сосуд 120 и второй реакционный сосуд 140 сконфигурированы так, что отверстие 121b или 141b для раствора низкомолекулярных веществ для экспрессии, способное принимать раствор низкомолекулярных веществ для экспрессии, сформировано для жидкостного сообщения с диализной трубкой. Третий реакционный сосуд 160 и четвертый реакционный сосуд 170 сконфигурированы так, что в них формируется область, способная принимать раствор низкомолекулярных веществ для экспрессии, а раствор низкомолекулярных веществ для экспрессии, буфер для хранения белка или т.п. могут туда подаваться или извлекаться оттуда с помощью насоса 165 или 174.
В соответствии с фиг. 3 теперь будет подробно описан первый реакционный сосуд 120.
В первом реакционном сосуде 120 формируется множество отверстий 121а для диализных трубок, в которые вставляется диализная трубка 110, и формируется множество отверстий 121b для раствора низкомолекулярных веществ для экспрессии, которые прилегают к отверстиям 121а диализных трубок и имеют жидкостное сообщение с отверстиями 121а диализных трубок. Предпочтительно, количество отверстий 121а диализных трубок составляет 16 так, что туда могут быть вставлены 16 диализных трубок 110.
Кроме того, первый реакционный сосуд 120 сконфигурирован так, что он делится на блок 100 реакции экспрессии белка, в который вставлены 8 диализных трубок 110 и в котором осуществляется экспрессия белка, и блок 122 диализа белка, который диализует очищенный белок относительно буфера для хранения белка.
Блок 122 диализа белка содержит: множество отверстий 122а для диализных трубок, в которые вставляется диализная трубка 110; и множество отверстий 122b для диализного раствора, которые сформированы по соседству с отверстиями 122а диализных трубок так, чтобы было жидкостное сообщение с отверстиями 122а диализных трубок и чтобы они были способны принимать буфер для хранения белка.
Кроме того, первый реакционный сосуд 120 дополнительно содержит крышку 130 первого реакционного сосуда с целью предотвращения выпаривания раствора в диализной трубке 110.
Крышка 130 первого реакционного сосуда имеет отверстия 131, сформированные для соответствия с отверстиями 121b для раствора низкомолекулярных веществ для экспрессии и с отверстиями 121а для диализных трубок, сформированных в реакционном сосуде 120. Кроме того, выше отверстий 131 установлена пленка 132, предотвращающая испарение с целью предотвращения испарения раствора из диализной трубки 110. Кроме того, области пленки 132 для предотвращения испарения, которые соответствуют отверстиям 121а для раствора низкомолекулярных веществ для экспрессии и отверстиям 121b для диализных трубок, могут быть надрезаны так, чтобы пипетки 310 могли быть легко туда вставлены. Эти области предпочтительно надрезаются в форме "+", без ограничения этим способом.
В соответствии с фиг. 4 будет подробно описан второй реакционный сосуд 140 по настоящему изобретению.
Второй реакционный сосуд 140 содержит множество отверстий 141а для диализных трубок, в которые вставляется диализная трубка, и содержит множество отверстий 141b для раствора низкомолекулярных веществ для экспрессии, которые прилегают к отверстиям 141а для диализных трубок так, чтобы было жидкостное сообщение с отверстиями 141а для диализных трубок. Предпочтительно, количество отверстий 141а для диализных трубок составляет 48 так, что туда могут быть вставлены 48 диализных трубок 110. В данном описании некоторые из отверстий для раствора низкомолекулярных веществ для экспрессии могут использоваться в качестве блока диализа белка.
Кроме того, второй реакционный сосуд 140 дополнительно содержит крышку 150 второго реакционного сосуда для предотвращения выпаривания раствора в диализной трубке 110.
Крышка 150 второго реакционного сосуда имеет отверстия 151, сформированные для соответствия с отверстиями 141b для раствора низкомолекулярных веществ для экспрессии и с отверстиями 141а для диализных трубок, сформированных во втором реакционном сосуде 140. Выше отверстий 151 устанавливается пленка 152, предотвращающая испарение, для предотвращения испарения раствора из диализной трубки 110. Кроме того, области пленки 152 для предотвращения испарения, которые соответствуют отверстиям 141а для раствора низкомолекулярных веществ для экспрессии и отверстиям 141b диализных трубок, могут быть надрезаны так, чтобы пипетки 310 могли быть легко туда вставлены. Эти области предпочтительно надрезаются в форме "+" без ограничения этим способом.
В соответствии с фиг. 5 будет подробно описан третий реакционный сосуд 160 по настоящему изобретению.
Третий реакционный сосуд 160 содержит: сосуд 161 с низкомолекулярным раствором для экспрессии, имеющий область, способную принимать раствор низкомолекулярных веществ для экспрессии или буфер для хранения белка; и крышку 162 сосуда с раствором, которая служит в качестве крышки сосуда 161 для раствора низкомолекулярных веществ для экспрессии и имеет отверстия для диализных трубок, в которые вставляется диализная трубка 110. Предпочтительно, количество отверстий диализных трубок составляет 96 так, что туда могут быть вставлены 96 диализных трубок 110.
Кроме того, третий реакционный сосуд 160 содержит вход 163, сконфигурированный для введения раствора низкомолекулярных веществ для экспрессии или для буфера для хранения белка, и выход 164, сконфигурированный для сброса раствора низкомолекулярных веществ для экспрессии или буфера для хранения белка после завершения реакции.
Вход 163 соединен с насосом-дозатором 165, с многоканальным клапаном 166 и, по меньшей мере, с одним контейнером 167 для раствора. Конкретно, с целью введения раствора низкомолекулярных веществ для экспрессии или буфера для хранения белка через вход 163, многоканальный клапан 166 соединяется, по меньшей мере, с одним из контейнеров 167 для раствора, и раствор низкомолекулярных веществ для экспрессии или буфер для хранения белка в контейнере 167 для раствора подается в третий реакционный контейнер 160 посредством насоса-дозатора 165.
Выход 164 соединен с контрольным клапаном 168 и с контейнером 169 для отходов. Когда раствор низкомолекулярных веществ для экспрессии