Производные тетрагидрохинолина в качестве активаторов амрк
Иллюстрации
Показать всеИзобретение относится к новым производным тетрагидрохинолина формулы (I) или к его фармацевтически приемлемой соли, где R1: водород, низший алкил, галоген или карбокси; R2: водород, низший алкил, гало-низший алкил, галоген, циано или карбокси; R3 и R4: низший алкил; R5 и R6 выбраны из водорода, карбокси-низший алкиламино, карбоксициклопропиламино, низший алкилсульфониламино, фенилсульфониламино, галофенилсульфониламино, низший алкилфенилсульфониламино, галофенилкарбониламино, пиридинилсульфониламино, низший алкиламиносульфонила и галофениламиносульфонила; при условии, что оба R5 и R6 не представляют собой водород одновременно; R7: водород или низший алкил. Также изобретение относится к фармацевтической композиции на основе соединения формулы (I) и применению соединения формулы (I). Технический результат: получены новые производные тетрагидрохинолина, полезные в качестве активатора АМФ-активированной протеинкиназы (АМРК). 4 н. и 16 з.п. ф-лы, 1 табл., 94 пр.
Реферат
Изобретение относится к соединениям, которые представляют собой активаторы АМФ-активированной протеинкиназы (AMPK от AMP-activated protein kinase) и которые являются полезными в лечении или профилактике заболеваний, которые связаны с регуляцией AMPK, таких как ожирение, дислипидемия, гипергликемия, диабет 1-го или 2-го типа и злокачественные новообразования.
В частности, изобретение относится к соединению формулы (I)
где
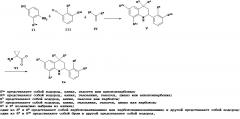
R1 представляет собой водород, алкил, галоалкил, галоген, циано или карбокси;
R2 представляет собой водород, алкил, галоалкил, галоген, циано или карбокси;
R3 и R4 независимо представляют собой алкил;
R5 и R6 независимо выбраны из водорода, карбоксиалкиламино, карбоксициклоалкиламино, алкилсульфониламино, фенилсульфониламино, галофенилсульфониламино, алкилфенилсульфониламино, фенилкарбониламино, галофенилкарбониламино, пиридинилсульфониламино, алкиламиносульфонила и галофениламиносульфонила; при условии, что оба R5 и R6 не представляют собой водород одновременно;
R7 представляет собой водород или алкил; или его фармацевтически приемлемой соли или эфиру.
Также изобретение относится к способу изготовления этих новых соединений и лекарствам, содержащим их. Соединения по изобретению обладают эффектом активации АМФ (аденозин-монофосфат)-активированной протеинкиназы, который приводит к пониженным уровням глюкозы и липидов в крови. Таким образом, изобретение также относится к применению подобных соединений для лечения или профилактики заболеваний, которые связаны с регуляцией AMPK, таких как ожирение, дислипидемия, гипергликемия, диабет 1-го или 2-го типа и злокачественные новообразования.
Ожирение и диабет 2-го типа, гипертензия и сердечно-сосудистое заболевание представляют собой заболевания, которые характеризуются серьезными нарушениями в метаболизме глюкозы или липидов, которые сильно влияют на здоровье и качество жизни пораженных болезнью людей. Кроме того, известно, что метаболизм раковых клеток отличается от нормального клеточного метаболизма. Увеличивающееся распространение этих заболеваний делает поиск новых лекарственных средств для лечения этих синдромов неотложной задачей.
АМФ-активированная протеинкиназа действует как клеточный датчик и регулятор энергии. Она активируется в ходе увеличения клеточного соотношения АМФ: АТФ под воздействием метаболического усиления, гормональной команды и сигналов питательных веществ и других клеточных механизмов, таких как фосфорилирование и белок-белковое взаимодействие. После активации AMPK включает катаболические проводящие пути, что порождает АТФ, и выключает АТФ-потребляющие анаболические проводящие пути в ходе резкого регулирования активности ключевых ферментов при метаболизме и хронического регулирования экспрессии основных факторов транскрипции (Hardie, DG. Nature reviews 8 (2007b), 774-785; Woods, A et al. Molecular and cellular biology 20 (2000), 6704-6711). Растущее доказательство влияния регулирования AMPK на метаболизм глюкозы и липидов делает это потенциальное лекарственное средство мишенью для лечения диабета, метаболического синдрома и злокачественного новообразования (Carling, D. Trends Biochem Sci 29(2004), 18-24; Hardie, DG. Annual review of pharmacology and toxicology 47 (2007a), 185-210; Kahn, BB et al. Cell metabolism 1 (2005), 15-25; Long, YC et al. The Journal of clinical investigation 116 (2006), 1776-1783).
На физиологическом уровне данная концепция подтверждена двумя адипокинами, лептином и адипонектином, оба из которых оказывают превосходное влияние на метаболизм глюкозы и липидов (Friedman, JM and Halaas, JL. Nature 395 (1998), 763-770; Muoio, DM et al. Diabetes 46 (1997), 1360-1363; Yamauchi, T et al. Nature medicine 7 (2001), 941-946). Недавние исследования показывают, что лептин и адипонектин оказывают свое антидиабетическое влияние, активируя AMPK. Лептин стимулирует окисление жирных кислот в мышцах, активируя AMPK непосредственно или через гипоталамически-адренергический путь (Minokoshi, Y et al. Nature 415 (2002), 339-343). Адипонектин стимулирует поглощение глюкозы и окисление жирных кислот in vitro при активации AMPK. Кроме того, он оказывает свой гипогликемический эффект, уменьшая экспрессию РЕРСК и G6Pase, тогда как введение доминантного отрицательного α1 аденовируса полностью изменяет эффект in vivo (Yamauchi, Т et al. Nature medicine 8 (2002), 1288-1295).
На фармакологическом уровне концепция AMPK в качестве потенциальной мишени для лечения метаболического синдрома, кроме того, подтверждается открытием двух основных классов существующих антидиабетических средств: тиазолидиндионы (росиглитазон, троглитазон и пиоглитазон) и бигуаниды (метформин и фенформин) активируют AMPK в культивируемых клетках и in vivo. Традиционно считается, что росиглитазон является агонистом PPARy и проявляет свои антидиабетические эффекты посредством дифференциации адипоцитов (Semple, RK et al. The Journal of clinical investigation 116 (2006), 581-589). Недавние результаты указывают на то, что AMPK может принимать участие в антидиабетических эффектах росиглитазона (Brunmair, В et al. The Journal of biological chemistry 277 (2002), 25226-25232; Kadowaki, T et al. The Journal of clinical investigation 116(2006), 1784-1792). В случае метформина, существующий антидиабетический агент без определенного механизма действия, недавние исследования показывают, что он мог активировать AMPK in vitro и in vivo, ингибируя комплекс I (El-Mir, MY et al. The Journal of biological chemistry 275 (2000), 223-228; Owen, MR et al. The Biochemical journal 348 Pt 3 (2000), 607-614; Zhou, G et al. The Journal of clinical investigation 108 (2001), 1167-1174), и гипогликемический эффект мог быть блокирован полностью выключением его вышерасположенной киназы LKB1, что подтверждает ключевую роль AMPK в опосредовании антидиабетического эффекта метформина (Shaw, RJ et al. Science (New York) N.Y. 310(2005), 1642-1646).
Совсем недавно Cool и коллеги обнаружили небольшой прямой AMPK активатор, А-769662, который проявляет антидиабетические эффекты in vivo (Cool, В et al. Cell metabolism 3 (2006), 403-416). Лаборатория Li также обнаружила небольшой AMPK активатор, РТ1, который активирует неактивные формы AMPK α2398 и α1394 с микромолярной активностью и проявляет некоторые клеточные эффекты (Pang, Т et al. The Journal of biological chemistry 283 (2008), 16051-16060).
Найдено, что соединения по настоящему изобретению представляют собой эффективные AMPK активаторы. Следовательно, соединения по изобретению полезны в лечении или профилактике заболеваний, которые связаны с регуляцией AMPK, таких как ожирение, дислипидемия, гипергликемия, диабет 1-го или 2-го типа и злокачественные новообразования.
Как используется здесь, термин «алкил», отдельно или в сочетании, означает насыщенную, линейную или разветвленную алкильную группу, содержащую 1-8, предпочтительно 1-6, более предпочтительно 1-4 атомов углерода, например метил, этил, пропил, изопропил, 1-бутил, 2-бутил и трет-бутил. Предпочтительными алкильными группами являются метил, этил, изопропил и трет-бутил.
Термин «циклоалкил», отдельно или в сочетании, относится к насыщенному углеродному кольцу, содержащему от 3 до 7 атомов углерода, предпочтительно от 3 до 6 атомов углерода, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил. Предпочтительными циклоалкильными группами являются циклопропил, циклопентил и циклогексил.
Термин «галоген» означает фтор, хлор, бром или йод. Галоген предпочтительно представляет собой фтор, хлор или бром.
Термин «галоалкил» означает алкил, замещенный одним - семью атомами галогена, предпочтительно одним - тремя атомами галогена, предпочтительно фтором. Предпочтительный галоалкил представляет собой трифторметил.
Термин «галофенил» означает фенил, замещенный галогеном.
Термин «карбокси», отдельно или в сочетании, относится к группе -COOH.
Термин «карбонил», отдельно или в сочетании, относится к группе -С(O)-.
Термин «амино», отдельно или в сочетании, относится к первичному (-NH2-), вторичному (-NH-) или третичному амину (-N-).
Термин «сульфонил», отдельно или в сочетании, относится к группе -S(O)2-.
Соединения по настоящему изобретению могут существовать в форме их фармацевтически приемлемых солей. Термин «фармацевтически приемлемая соль» относится к традиционным солям присоединения кислоты или солям присоединения основания, которые сохраняют биологическую эффективность и свойства соединений формулы (I) и образованы подходящими нетоксичными органическими или неорганическими кислотами или органическими или неорганическими основаниями. Соли присоединения кислоты включают, например те, что получены из неорганических кислот, таких как соляная китслота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота и азотная кислота, и те, что получены из органических кислот, таких как п-толуолсульфоновая кислота, салициловая кислота, метансульфоновая кислота, щавелевая кислота, янтарная кислота, лимонная кислота, яблочная кислота, молочная кислота, фумаровая кислота. Соли присоединения основания включают те, что получены из гидроксидов аммония, калия, натрия и четвертичного аммония, такого как, например гидроксид тетраметиламмония. Химическое превращение фармацевтического соединения в соль является методикой, хорошо известной химикам-фармацевтам для получения соединений с улучшенными физической и химической стабильностью, гигроскопичностью, текучестью и растворимостью. Это, например, описано у Bastin R.J., et. al. organic Process Research & Development 2000, 4, 427-435; или у Ansel, H., et. al., In: Pharmaceutical Dosage Forms and Drug Delivery Systems, 6th ed. (1995), pp.196 and 1456-1457. Предпочтительной является натриевая соль соединения формулы (I).
«Фармацевтически приемлемый эфир» означает, что соединение общей формулы (I) может быть преобразовано по функциональным группам, что даст производные, которые способны превращаться обратно в исходные соединения in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически подвижные эфирные производные, такие как метоксиметиловые эфиры, метилтиометиловые эфиры и пивалоилоксиметиловые эфиры. Кроме того, любые физиологически приемлемые эквиваленты соединений общей формулы (I), подобные метаболически подвижным эфирам, которые способны давать исходные соединения общей формулы (I) in vivo, находятся в объеме данного изобретения. Предпочтительными являются метиловые и этиловые эфиры соединений формулы (I).
Изобретение относится, в частности, к соединению формулы (I), где оба R1 и R2 не представляют собой водород одновременно.
В особом воплощении изобретения R1 представляет собой водород, алкил, галоген или карбокси.
В другом особом воплощении изобретения R1 представляет собой водород, метил или хлор.
В еще особом воплощении изобретения R2 представляет собой галоалкил, галоген, циано или карбокси.
В дополнительном воплощении изобретения R2 представляет собой трифторметил, хлор, циано или карбокси.
В другом особом воплощении изобретения оба R3 и R4 представляют собой метил одновременно.
Изобретение относится, в частности, к соединению формулы (I), где R5 представляет собой водород, алкилсульфониламино, галофенилсульфониламино, карбоксиалкиламино, карбоксициклоалкиламино, галофенилкарбониламино, пиридинилсульфониламино или фенилсульфониламино.
В частности, изобретение также относится к соединению формулы (I), где R5 представляет собой водород, карбоксиалкиламино, галофенилсульфониламино, пиридинилсульфониламино или фенилсульфониламино.
Изобретение также относится к соединению формулы (I), где R5 представляет собой водород, карбоксиизопропиламино, фенилсульфониламино, фторфенилсульфониламино или пиридинилсульфониламино.
Кроме того, изобретение относится к соединению формулы (I), где R6 представляет собой водород, карбоксиалкиламино, карбоксициклоалкиламино, алкилсульфониламино, фенилсульфониламино, галофенилсульфониламино, алкилфенилсульфониламино, галофениламиносульфонил, пиридинилсульфониламино или алкиламиносульфонил.
В дополнительном воплощении этого изобретения R6 представляет собой водород, карбоксиалкиламино или карбоксициклоалкиламино.
В другом воплощении изобретения R6 представляет собой водород, карбоксиизопропиламино или карбоксициклопропиламино.
Также изобретение относится, в частности, к соединению формулы (I), где R7 представляет собой водород или метил.
Особые соединения формулы (I) по изобретению могут быть выбраны из 2-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(1-Карбокси-циклопропиламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-8-карбоновой кислоты;
2-[3-(1-Карбокси-циклопропиламино)-фенил]-6-хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-8-карбоновой кислоты;
2-[3-(1-Карбокси-циклопропиламино)-фенил]-6-хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-8-карбоновой кислоты;
1-[3-(6-Циано-4,4,8-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
2-Метил-2-[3-(1,4,4-триметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-пропионовой кислоты;
2-[3-(6-Циано-4,4,8-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(1,4,4-Триметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-3-фтор-бензолсульфонамида;
2-[3-(1-Карбокси-1-метил-этиламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-8-карбоновой кислоты;
[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
1-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
1-[3-(8-Хлор-6-циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-фтор-бензолсульфонамида;
2-[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
1-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
N-[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
2-[3-(6-Циано-1,4,4-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(6-Фтор-4,4,8-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
1-[3-(6-Циано-1,4,4-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(8-Хлор-6-циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
2-Метил-2-[3-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-пропионовой кислоты;
2-[3-(6-Фтор-4,4,8-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
2-[2-(4-Фтор-бензоиламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-(2-Этансульфониламино-фенил)-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
4,4-Диметил-2-[2-(пиридин-3-сульфониламино)-фенил]-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-[2-(2-Фтор-бензоиламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
[2-(6-хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты;
2-[2-(3-Фтор-бензоиламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
2-[2-(2-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-[2-(4-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-(2-Бензолсульфониламино-фенил)-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-[2-(3-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
N-[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-3-фтор-бензолсульфонамида;
N-[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
N-[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-фтор-бензолсульфонамида;
[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
N-[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
N-[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пропан-2-сульфоновой кислоты;
N-[2-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
3-Фтор-N-[2-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[2-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты;
[2-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты;
[3-(4)4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-фтор-бензолсульфонамида;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-3-фтор-бензолсульфонамида;
[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пропан-2-сульфоновой кислоты;
N-[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-метил-бензолсульфонамида;
[3-(4,4-Диметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты;
4-Фтор-N-[3-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
2-Фтор-N-[3-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
3-Фтор-N-[3-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[3-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
4-Метил-N-[3-(4,4,6-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[3-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
[3-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
[3-(4,4,6-Триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-3-фтор-бензолсульфонамида;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-фтор-бензолсульфонамида;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амидапропан-2-сульфоновой кислоты;
N-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-метил-бензолсульфонамида;
[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амидапиридин-3-сульфоновой кислоты;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-фтор-бензолсульфонамида;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-4-метил-бензолсульфонамида;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-бензолсульфонамида;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-3-фтор-бензолсульфонамида;
N-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-метансульфонамида;
3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-N-метил-бензолсульфонамида;
[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида этансульфоновой кислоты;
3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-N-(4-фтор-фенил)-бензолсульфонамида и
[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-амида пиридин-3-сульфоновой кислоты.
Дополнительные особые соединения формулы (I) могут быть выбраны из 2-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
2-Метил-2-[3-(1,4,4-триметил-6-трифторметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-пропионовой кислоты;
2-[3-(6-Циано-4,4,8-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
2-[2-(6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
N-[2-(6-Хлор-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фенил]-2-фтор-бензолсульфонамида;
2-[3-(6-Циано-1,4,4-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
1-[3-(6-Циано-1,4,4-триметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-циклопропанкарбоновой кислоты;
2-[3-(8-Хлор-6-Циано-4,4-диметил-1,2,3,4-тетрагидро-хинолин-2-ил)-фениламино]-2-метил-пропионовой кислоты;
4,4-Диметил-2-[2-(пиридин-3-сульфониламино)-фенил]-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-[2-(2-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-[2-(4-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты;
2-(2-Бензолсульфониламино-фенил)-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты и
2-[2-(3-Фтор-бензолсульфониламино)-фенил]-4,4-диметил-1,2,3,4-тетрагидро-хинолин-6-карбоновой кислоты.
Соединения по настоящему изобретению могут быть получены любыми обычными способами. Подходящие процессы синтеза этих соединений приведены на схемах ниже и в примерах. На следующих схемах R1-R7 являются такими, как определено выше, если не указано иное.
Аббревиатуры:
| д: | день или дни |
| г: | грамм |
| ч: | час или часы |
| ВЭЖХ: | высокоэффективная жидкостная хроматография |
| Гц: | герц |
| мг: | миллиграмм |
| мин: | минута или минуты |
| мл: | миллилитр |
| ммоль: | миллимоль |
| мМ: | миллимоль на литр |
| ЖХ/МС: | жидкостная хроматография/масс-спектрометрия |
| МС: | масс-спектрометрия |
| ЭСИ: | ионизация электрораспылением |
APCI: химическая ионизация при атмосферном давлении
Схема 1
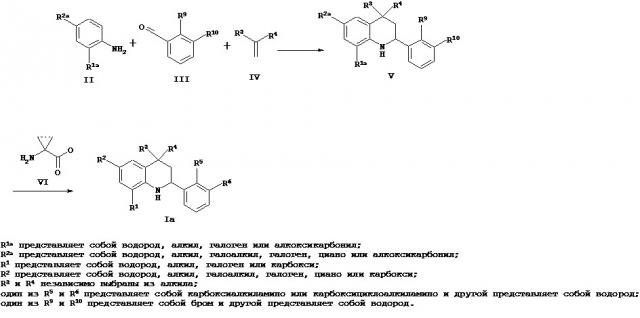
Соединение формулы Ia можно получить в соответствии со Схемой 1. Тетрагидрохинолин V можно синтезировать с использованием трех компонентов аза реакции Дильса-Альдера анилина II, альдегида III и метилен-алкена IV. Реакция связывания по Ульману между тетрагидрохинолином V и аминокислотой VI дает в результате соединение Ia.
Соединение V можно получить в ходе аза реакции Дильса-Альдера между тремя компонентами анилином II, альдегидом III и метилен-алкеном IV. Эту реакцию Дильса-Альдера можно проводить в присутствии кислоты Льюиса, такой как трифторметансульфонат иттербия (III) (Yb(OTf)3), трифторметансульфонат скандия (III) (Sc(OTf)3), трифторметансульфонат лантана (III) (La(OTf)3), трифторметансульфонат индия (III) (In(OTf)3), трихлорид индия (InCl3) или трифторид бора - диэтиловый эфир (BF3⋅Et2O), или протонсодержащей кислоты, такой как трифторуксусная кислота (ТФК) или п-толуолсульфоновая кислота, в растворителе, таком как ацетонитрил, дихлорметан, тетрагидрофуран, нитрометан, N,N-диметилформамид, 2,2,2-трифторэтанол или их смесь, при температуре между 25 и 100°C в течение нескольких часов (ссылка: Kiselyov, A. S. et al., Tetrahedron 54 (1998) 5089).
Реакцию связывания по Ульману, как показано на Схеме 1, можно проводить в присутствии источника меди, такого как иодид меди (I) (Cul) или трифторметансульфонат меди (II), и лиганда, такого как 2,2’-бипиридин, пролин, N,N’-диметил-глицин или этиленгликоль, в присутствии подходящего основания, такого как триэтиламин, карбонат натрия, карбонат калия, карбонат цезия, метилат натрия, трет-бутилат натрия, трет-бутилат калия. Реакцию можно проводить в подходящем растворителе, таком как 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид или N-метилпирролидинон, при температуре между 100 и 180°C в течение 15-60 минут в условиях микроволнового излучения. Альтернативно, реакции можно проводить без применения микроволнового излучения при повышенной температуре, такой как 130°C, в течение длительного времени (ссылка: Ley, S. V. et al., Angew. Chem. Int. Ed. 42 (2003) 5400).
Схема PAGE15
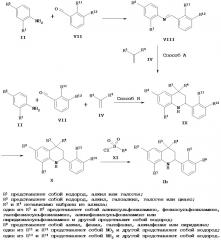
Соединение формулы Ib можно получить согласно Схеме 2. Анилин II взаимодействует с альдегидом VII, что дает имин VIII. Имин VII взаимодействует с метилен-алкеном IV, что дает тетрагидрохинолин IX. Альтернативно, тетрагидрохинолин IX можно синтезировать посредством трехкомпонентной аза реакции Дильса-Альдера между анилином II, альдегидом VII и метилен-алкеном IV. Восстановление тетрагидрохинолина IX с последующим связыванием с сульфонилхлоридом XI дает в результате соединение Ib.
В способе, указанном на Схеме 2, имин VIII можно получить в ходе реакции конденсации замещенного анилина II и замещенного альдегида VII в органическом растворителе, таком как толуол, метанол или этанол и их смеси, при температуре между 80 и 140°C в течение 2-16 часов.
Соединение IX можно получить либо в ходе аза реакции Дильса-Альдера между имином VIII и метилен-алкеном IV, либо в ходе трехкомпонентной аза реакции Дильса-Альдера между анилином II, альдегидом VII и метилен-алкеном IV. Эту реакцию Дильса-Альдера можно проводить в присутствии кислоты Льюиса, такой как трифторметансульфонат иттербия (III) (Yb(OTf)3), трифторметансульфонат скандия (III) (Sc(OTf)3), трифторметансульфонат лантана (III) (La(OTf)3), трифторметансульфонат индия (III) (In(OTf)3), трихлорид индия (InCl3) или трифторид бора - диэтиловый эфир (BF3⋅Et2O), или протонсодержащей кислоты, такой как трифторуксусная кислота (ТФК) или п-толуолсульфоновая кислота, в растворителе, таком как ацетонитрил, дихлорметан, тетрагидрофуран, нитрометан, N,N-диметилформамид, 2,2,2-трифторэтанол или их смесь, при температуре между 25 и 100°C в течение нескольких часов (ссылка: Kiselyov, A. S. et al., Tetrahedron 54 (1998) 5089).
Восстановление нитросоединения IX до соответствующего производного амина X может быть выполнено с использованием способов, хорошо известных квалифицированному специалисту в данной области техники. Реакцию обычно проводят в кислотных условиях, используя соляную кислоту или хлорид аммония в смеси этанола и воды при нагревании с обратным холодильником в течение нескольких часов.
Превращение амина X в соответствующий сульфонамид Ib с подходящим сульфонилхлоридом XI может быть легко выполнено при использовании способов, хорошо известных квалифицированному специалисту в данной области техники. Реакцию обычно проводят в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин, метилат натрия, трет-бутилат натрия, трет-бутилат калия, гидрид натрия или диметил-пиридин-4-ил-амин, в подходящем инертном растворителе, таком как дихлорметан, ацетонитрил, 1,4-диоксан, тетрагидрофуран или их смесь, при комнатной температуре в течение нескольких часов.
Схема 3
Соединение формулы Ic можно получить в соответствии со Схемой 3. В данном способе соединение формулы V можно синтезировать, как проиллюстрировано на Схеме 1. Алкилирование соединения V с последующей реакцией сочетания по Ульману с аминокислотой VI дает в результате соединение Ic.
Алкилирование соединения формулы V можно легко выполнить, используя способы, хорошо известные квалифицированному специалисту в данной области техники. Реакцию обычно проводят в присутствии основания, такого как триэтиламин, пиридин, метилат натрия, трет-бутилат натрия, трет-бутилат калия, гидрид натрия или диметил-пиридин-4-ил-амин, в подходящем инертном растворителе, таком как дихлорметан, ацетонитрил, 1,4-диоксан, тетрагидрофуран или их смеси, при комнатной температуре в течение нескольких часов.
Реакцию связывания по Ульману, как показано на Схеме 3, можно проводить в присутствии источника меди, такого как иодид меди (I) (CuI) или трифторметансульфонат меди (II), и лиганда, такого как 2,2’-бипиридин, пролин, N,N’-диметил-глицин или этилен гликоль, в присутствии подходящего основания, такого как триэтиламин, карбонат натрия, карбонат калия, карбонат цезия, метилат натрия, трет-бутилат натрия, трет-бутилат калия. Реакцию можно проводить в подходящем растворителе, таком как 1,4-диоксан, N,N-диметилформамид, диметилсульфоксид или N-метилпирролидинон, при температуре между 100 и 180°C в течение 15-60 минут в условиях микроволнового излучения. Альтернативно, реакции можно проводить без применения микроволнового излучения при повышенной температуре, такой как 130°C, в течение длительного времени (ссылка: Ley, S.V. et al., Angew. Chem. Int. Ed. 42 (2003) 5400).
Схема 4
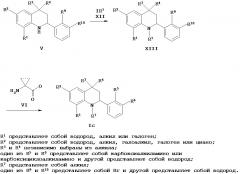
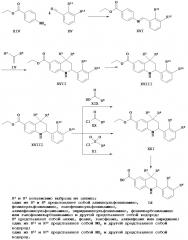
Соединение формулы Id можно получить в соответствии со Схемой 4. Анилин XIV взаимодействует с альдегидом XV, что дает имин XVI. Имин XVI взаимодействует с метилен-алкеном IV, что дает тетрагидрохинолин XVII. Восстановление тетрагидрохинолина XVII с последующим сочетанием с карбоновой кислотой XIX, карбонилхлоридом XX или сульфонилхлоридом XI дает в результате соединение XXI. Гидролиз этилового эфира XXI дает в результате продукт Id.
В способе, указанном на Схеме 4, имин XVI можно получить в ходе реакции конденсации замещенного анилина XIV и замещенного альдегида XV в органическом растворителе, таком как толуол, метанол или этанол и их смеси, при температуре между 80 и 140°C в течение 2-16 часов.
Соединение XVII можно получить в ходе аза реакции Дильса-Альдера между имином XVI и метилен-алкеном IV. Эту реакцию Дильса-Альдера можно проводить в присутствии кислоты Льюиса, такой как трифторметансульфонат иттербия (III) (Yb(OTf)3), трифторметансульфонат скандия (III) (Sc(OTf)3), трифторметансульфонат лантана (III) (La(OTf)3), трифторметансульфонат индия (III) (In(OTf)3), трихлорид индия (InCl3) или трифторид бора - диэтиловый эфир (BF3⋅Et2O), или протонсодержащей кислоты, такой как трифторуксусная кислота (ТФК) или п-толуолсульфоновая кислота, в растворителе, таком как ацетонитрил, дихлорметан, тетрагидрофуран, нитрометан, N,N-диметилформамид, 2,2,2-трифторэтанол или их смесь, при температуре между 25 и 100°C в течение нескольких часов (ссылка: Kiselyov, A.S. et al., Tetrahedron 54 (1998) 5089).
Восстановление нитросоединения XVII до соответствующего производного амина XVIII может быть выполнено с использованием способов, хорошо известных квалифицированному специалисту в данной области техники. Реакцию обычно проводят в кислотных условиях, используя соляную кислоту или хлорид аммония в смеси этанола и воды при нагревании с обратным холодильником в течение нескольких часов.
Превращение амина XVIII в соответствующий амид XXI с подходящей карбоновой кислотой XIX можно легко выполнить, используя способы, хорошо известные квалифицированному специалисту в данной области техники. Реакцию обычно проводят в присутствии связующего реагента, такого как дициклогексилкарбодиимид (ДЦК), бензотриазол-1-ил-окси-трис-пирролидинофосфония гексафторфосфат (РуВор), о-(7-азабензотриазол-1-ил)-N,N,N’,N’-тетраметилурония гексафторфосфат (HATU), о-(1Н-бензотриазол-1-ил)-N,N,N’,N’-тетраметилурония гексафторфосфат (HBTU) или 1-этил-3-(3’-диметиламино)карбодиимида гидрохлорид (EDCI), в присутствии или отсутствии гидроксибензотриазола (HOBt), в присутствии основания, такого как триэтиламин, или N,N-диизопропилэтиламин, или N,N-диметиламинопиридин (ДМАП). Реакцию можно проводить в растворителе, таком как дихлорметан или N,N-диметилформамид, при комнатной температуре в течение нескольких часов (ссылка: Montalbetti, С.A. G.N. et al., Tetrahedron 61 (2005) 10827).
Альтернативно, превращение амина XVIII в соответствующий амид XXI может быть легко выполнено при связывании амина XVIII с подходящим карбонилхлоридом XX в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин или диметил-пиридин-4-ил-амин, в подходящем инертном растворителе, таком как дихлорметан, ацетонитрил, 1,4-диоксан, тетрагидрофуран или их смесь, при комнатной температуре в течение нескольких часов. Карбонилхлорид имеется в продаже или образуется в реакционной смеси при обработке карбоновой кислоты оксихлоридом фосфора.
Превращение амина XVIII в соответствующий сульфонамид XXI с подходящим сульфонилхлоридом XI может быть легко выполнено при использовании способов, хорошо известных квалифицированному специалисту в данной области техники. Реакцию обычно проводят в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин, метилат натрия, трет-бутилат натрия, трет-бутилат калия, гидрид натрия или диметил-пиридин-4-ил-амин, в подходящем инертном растворителе, таком как дихлорметан, ацетонитрил, 1,4-диоксан, тетрагидрофуран или их смесь, при комнатной температуре в течение нескольких часов.
Гидролиз этиловых эфиров XXI до окончательных продуктов Id может быть выполнен в присутствии водного неорганического основания, такого как гидроксид лития, гидроксид натрия или гидроксид калия, в растворителе, таком как метанол, 1,4-диоксан, тетрагидрофуран или их смеси, при комнатной температуре или при нагревании с обратным холодильником в течение нескольких часов.
Схема 5
Соединение формул Ie можно получить в соответствии со Схемой 5. Исходный амин XXII можно получить в соответствии со Схемой 2. Превращение амина XXII до сульфонилхлорида с последующим образованием сульфонамида дает в результате соединение If.
Превращением амина XXII до сульфонилхлорида XXIII можно легко выполнить, обрабатывая раствор соли диазония в уксусной кислоте и соляной кислоте раствором диоксида серы в уксусной кислоте в присутствии хлорида меди. Раствор соли диазония можно получить при обработке амина XXII нитритом натрия в растворе уксусной кислоты и соляной кислоты.
Превращение сульфонилхлорида XXIII до окончательного сульфонамида Ie с подходящим амином XXIV можно легко выполнить, используя способы, хорошо известные квалифицированному специалисту в данной области техники. Реакцию обычно проводят в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин, пиридин, метилат натрия, трет-бутилат натрия, трет-бутилат калия, гидрид натрия или диметил-пиридин-4-ил-амин, в подходящем инертном растворителе, таком как дихлорметан, ацетонитрил, 1,4-диоксан, тетрагидрофуран или их смесь, при комнатной температуре в течение нескольких часов.
Схема 6
Соединение формулы Ie можно получить в соответствии со Схемой 6. В этом способе соединение формулы IX можно синтезировать, как проиллюстрировано на Схеме 2. Алкилирование соединения IX дает XXV. Восстановление тетрагидрохинолина XXV с последующим связыванием с сульфонилхлоридом XI дает в результате соединение Ie.
Алкилирование соединения формулы IX можно легко выполнить, используя способы, хорошо известные квалифицированному специалисту в данной облас