Способ регулирования полового поведения самцов млекопитающих
Иллюстрации
Показать всеГруппа изобретений относится к области ветеринарии и предназначена для регулирования полового поведения самцов животных. Фармацевтическая композиция для трансдермального введения имеет pH в интервале от 4,0 до 6,0 и имеет следующий состав, мас.%: гестаген 0,9÷2,0, мелатонин 10÷17,2, α-адреноблокатор, тропный к задним ядрам гипоталамуса, 0,9÷2,0, N-метил-N-(1,2R,3R,4R,5S-пентагидроксигексил)-октадеканамид 0,5, D-пантенол 0,5, полиоксиэтилированный α-токоферол 10, полиоксиэтилированный ланолин 1, 3-(октадецилокси)-1,2-пропандиол 0,1, стеариновая кислота 1,1, N,N-диэтилтолуамид 15, 1,2-изопропилиденглицерол 20, 1,2,3-триацетоксипропан до 100. Способ регулирования полового поведения самцов животных включает введение заявленной фармацевтической композиции. Использование заявленной группы изобретений позволяет эффективно регулировать половое поведение самцов млекопитающих при отсутствии побочных эффектов. 2 н. и 2 з.п. ф-лы, 10 табл., 33 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области ветеринарии, а именно, к способу временного блокирования или торможения половых функций самцов млекопитающих животных, включая поведенческие феномены (поиск партнера, дромомания, внутривидовая агрессия и агрессия по отношению к хозяину, «мечение» территории, вокализация и т.п.). Способ предполагает одно/двукратное введение животному фармацевтической композиции, включающей в качестве действующих веществ α-адреноблокатор, тропный к задним ядрам гипоталамуса, мелатонин и стероидное соединение с гестагенной активностью. Способ позволяет при минимальной дозе опасного для здоровья животных стероидного гормона блокировать половое поведение самцов на срок от нескольких недель до полугода. Фармацевтическая композиция вводится трансдермально в форме «Спот-он».
Уровень техники
Половое поведение самцов собак и кошек в весенний период (удлиняющийся - длинный световой день) активизируется, что ведет к неприятным для владельцев животных изменениям в их поведении. Самцы становятся агрессивными (в том числе нередко и по отношению к хозяину), беспокойными, активно ищут партнера, что сопровождается дромоманией - «убеганием», при этом животные часто теряются, резко возрастает вероятность заражения зоонозными заболеваниями, включая бешенство. Мало приятны также особенности поведения самцов, такие как «мечение» территории, вокализация, животные могут царапать и грызть предметы домашней обстановки и т.п. Поэтому проблема подавления в первую очередь поведенческих феноменов полового поведения самцов в ветеринарии мелких домашних животных крайне актуальна. Наиболее эффективным методом решения этих проблем является стерилизация самцов животных, тем более что хирургическое вмешательство в случае самцов проще, безопаснее и дешевле, чем в случае самок. Однако в ряде случаев необратимая кастрация самцов может быть неприемлема - к примеру, при использовании ценных животных для разведения, для выставочных и служебных собак и т.п. Кастрация существенно изменяет поведение животного, придает черты апатичности и пассивности, значительно влияет на обмен веществ и экстерьер животных (в частности, резко возрастает склонность к ожирению, развитию диабета, рвотные позывы, артериальная гипертензия, тромбофлебиты, тромбоэмболия, гинекомастия). Таким образом, существует необходимость в фармацевтическом управлении половыми функциями самцов, не сопровождающимися необратимыми изменениями органов и систем животного. В гуманной медицине известно применение временной химической кастрации (как женщин, так и мужчин) введением в виде депо (пролонгированные инъекционные формы) повышенных количеств гипоталамических рилизинг-гормонов, это ведет к нарушению синхронизации системы гипоталамус-гипофиз, и в конечном итоге к блокированию на время поступления в кровь продуцируемых гипофизом гонадотропинов [Щекина Е.Г. Мужская контрацепция - завтрашний день! // Провизор. 2004. Вып. 11]. Преимущественно данный метод применяют в онкологии, для лечения гормонозависимых опухолей [Машковский М.Д. Лекарственные средства. - 16-е издание, переработанное, исправленное и дополненное / М.: Новая волна, 2012]. Для применения этого метода в ветеринарии мелких домашних животных необходима разработка удобных инъекционных форм с более медленным высвобождением и адекватными дозами. Применение ограничивает также и высокая стоимость как самих рилизинг-гормонов, так и компонентов пролонгированных инъекционных форм. Наибольшее распространение получило введение самцам больших доз гестагенов, аналогично самкам, что в итоге по механизму обратной связи ингибирует продукцию гонадотропинов и вызывает эффекты временной химической кастрации. В России широко используют те же препараты на основе мегестрола ацетата, что и применяемые для контрацепции самок [RU 2163809, опубл. 10.03.2001]. Однако для развития достоверного и быстрого подавления полового поведения самцов необходимо введение гестагенов более длительно и (или) в повышенных дозах, т.к. отклик гипофизарных структур у самцов ниже ввиду специфичности рецепторов. Применение гестагенов для воздействия на половое поведение самцов сопровождается большим количеством побочных эффектов, часто необратимых: угнетается кора надпочечников и нарушается выделение кортикостероидов, нередко повреждается поджелудочная железа, с развитием в той или иной степени диабета, практически всегда обнаруживаются гепатотоксические эффекты, возникают холециститы. В особенности для котов характерно развитие инфекций мочеполовой системы, с проявлением циститов и пиелонефритов и последующим уролитиазом (мочекаменная болезнь). Для молодых самцов нередко обнаруживают акромегалию. Почти всегда обнаруживается гиперплазия молочных желез с частым возникновением в последующем аденокарциномы. Поведение животных становится пассивным, они набирают избыточный вес. В значительной степени и на длительное время нарушается функционирование гонад, что приводит к неудачным вязкам спустя длительное время после прекращения введения гестагенов. Медленное развитие эффектов подавления полового поведения часто не спасает от «убегания» по следу самки в состоянии течки, со всеми последующими проблемами. Таким образом, попытки оказать воздействие на половое поведение самцов одним лишь введением гестагенов оставляют желать лучшего решения проблемы.
Известно применение для целей контрацепции у женщин сочетания гестагенов и мелатонина с возможным дополнительным введением эстрогена [RU 2114621, опубл. 10.06.1998], а также сочетания гестагенов и более активных производных мелатонина [ЕР 0641565, опубл. 08.03.1995]. Мелатонин является гормоном эпифиза, нормализует биологические ритмы, оказывает адаптогенное действие на организм, относительно безвредное вещество и используется в широком терапевтическом интервале и широком диапазоне доз. Так в терапевтических дозах он используется для улучшения мужского и женского гаметогенеза [ЕР 2253228, опубл. 24.11.2010]. Однако в повышенных дозах мелатонин подавляет овуляцию, а в сочетании со стероидами позволяет снизить дозу последних в препарате, что нивелирует их побочное действие [Хунданов Л., Гладков А., Левашова В. Жить долго и счастливо. Ученых заинтересовал мелатонин // Мед. вестн. 1997. №10 (77). С. 1-3.]. Для целей контрацепции овец, коз и других племенных животных используют мелатонин и его производные в форме имплантата как для самок (с целью задержки течки), так и для самцов (снижение спермопроизводства) [ЕР 0246910, опубл. 25.11.1987]. Недостатком изобретения является сложный процесс изготовления имплантата, а также трудности для хозяев домашних животных введения его под кожу беспокойным питомцам.
Известно сочетание α-адреноблокаторов с гестагенами и (или) эстрогенами с целью контрацепции и с целью снижения половой активности как самцов, так и самок в ветеринарии [Корхов В.В. и др. Посткоитальные стероиды и нестероидные контрацептивы // Фармакология и токсикология, 1980, Т. 43 (1), С. 94-96; Корхов В.В., Вещилова Т.П. Контрацептивная активность сочетания стероидов и антиадренергических препаратов // Бюл. эксперим. биол. и мед., 1975, Т. 79 (4), С. 77-79; RU 2233586, опубл. 10.08.2004]. Недостатком данного изобретения является невысокий контрацептивный эффект комбинации (55%) и недоступность на рынке используемого синтетического гестагена.
Задачей предлагаемого изобретения является нахождение максимально безопасного и удобного в применении способа временного блокирования половых функций самцов млекопитающих, включая поведенческие феномены (поиск партнера, вокализация, и т.п.). Технический результат данного изобретения заключается в получении высокоэффективной фармацевтической композиции для нанесения «Спот-он» в любой период полового цикла, которая позволяет легко решить вопросы изменения полового поведения самцов млекопитающих.
Раскрытие изобретения
При исследовании контрацептивных эффектов сочетания мелатонина и гестагенов с целью получения, по меньшей мере, эффекта подавления агрессивных реакций у «гуляющих» самцов нами был дополнительно введен известный неселективный α-адреноблокатор пророксан [Машковский М.Д. Лекарственные средства. - 16-е издание, переработанное, исправленное и дополненное / М.: Новая волна, 2012], который взаимодействует с альфа-адренорецепторами задних ядер гипоталамуса, ответственных за формирование полового поведения. Пророксан снижает возбуждение, подавляет агрессивность, нормализует вестибулярную функцию без проявления значимых седативных и других побочных эффектов. Неожиданно было обнаружено, что в этом случае коррекция активного полового поведения самцов животных происходит после одного/двух применений описанного выше сочетания биологически активных веществ и продолжается сроком от нескольких недель до полугода. Эффект развивается быстро (от 12 часов), при этом блокируются поведенческие феномены полового поведения - поиск партнера, вокализация, агрессивность, возбуждение и т.п., и проявляются явно ювенильные особенности - активизация игрового и исследовательского поведения, животное становится дружелюбным. Данная комбинация активных веществ для снижения активного полового поведения не была обнаружена нами в литературе.
Введение только гестагена, либо введение гестагена в сочетании только с мелатонином либо только с α-адреноблокатором, также как и введение мелатонина только с α-адреноблокатором, не позволило получить значительную эффективность композиции и максимально возможно снизить дозу стероидного компонента в препарате.
В качестве гестагена нами был выбран ципротерона ацетат, который обладает высокой аффинностью к андрогенным рецепторам как в структурах гипоталамуса, так и гипофиза у самцов и блокирует их, не проявляя андрогенного воздействия, препятствующего быстрому купированию половой активности. Замена обычно используемого мегестрола ацетата на ципротерона ацетат позволила существенно увеличить эффект, снизить нагрузку прогестагенным гормоном и увеличить физиологичность воздействия на организм самцов. Эффективность этого воздействия при этом выше при введении препарата в вечернее время, что делает правомерной гипотезу о преобладающем значении мелатонина в развитии эффекта. Введение в композицию α-адреноблокатора позволило максимально быстро и пролонгированно купировать симптомы возбужденного поведения самцов.
В качестве неселективного α-адреноблокатора можно использовать близкие по свойствам пророксан или (и) бутироксан (см. пример 16, 17, 18 и др.), либо аналогичные по фармакологическим и химическим свойствам биологически активные вещества (БАВ). Другие проверенные селективные и неселективные α-адреноблокаторы не оказались столь эффективными и описанный эффект не вызывали (см. пример 31), что, по-видимому, обуславливается специфическим воздействием пророксана и бутироксана на структуры мозга.
В качестве прогестинового компонента используют гестагены, обладающие наибольшей аффинностью к соответствующим рецепторам: 6-хлор-1β,2β-дигидро-17-гидрокси-3'Н-циклопропа[1,2]прегна-1,4,6-триен-3,20-дионацетат (ципротерона ацетат) или (и) 17α-цианометил-17β-гидроксиэстра-4,9-диен-3-он (диеногест), или (и) (6R,7R,8R,9S,10R,13S,14S,15S,16S,17S)-1,3',4',6,6a,7,8,9,10,11,12,13,14,15,15а,16-гексадекагидро-10,13-диметилспиро-[17Н-дициклопропа-[6,7:15,16]циклопента[а]фенантрен-17,2'(5'Н)-фуран]-3,5'(2Н)дион (дроспиренон). Применение ципротерона ацетата наиболее актуально из-за коммерческой доступности гормона.
Для гестагена и α-адреноблокатора дозы не должны превышать обычно используемые терапевтические, т.к. в противном случае резко возрастает вероятность неблагоприятных побочных эффектов. Мелатонин же практически безопасен при очень значительном превышении доз.
Можно было ожидать, что мелатонин и пророксан в составе трансдермальных форм будут обладать хорошей транскутанной биодоступностью, а гестаген, концентрации которого в крови животного не столь критичны для выраженности эффекта, также при определенном составе трансдермальной фармацевтической композиции, попадет в достаточном количестве в кровоток и окажет системное действие при минимальных местных эффектах. Была подобрана фармацевтическая композиция, предназначенная для трансдермального введения, содержащая (масс. %):
| Гестаген | Терапевтические количества |
| Мелатонин | Терапевтические количества |
| α-Адреноблокатор, тропный к задним ядрам гипоталамуса | Терапевтические количества |
| N-метил-N-(1,2R,3R,4R,5S-пентагидроксигексил)-октадеканамид (Стеариламид меглюмина) | 0,5 |
| D-пантенол | 0,5 |
| Полиоксиэтилированный α-токоферол | 9,3-10,2 |
| Полиоксиэтилированный ланолин | 1 |
| 3-(октадецилокси)-1,2- | 0,1 |
| пропандиол (Батилол) | |
| Карбоновая кислота | 0,1-1,1 |
| N,N-диэтилтолуамид | 13,9-15,3 |
| 1,2-изопропилиденглицерол | 18,6-20,4 |
| 1,2,3-триацетоксипропан | до 100 |
которая обеспечила биологический эффект при введении «Спот-он», идентичный оральным способам введения, но применение препарата значительно более удобно. При этом не обнаруживается раздражения кожи, животные не ощущают момент нанесения и дискомфорт в зоне нанесения, поэтому отсутствует расчесывание и вылизывание.
Наилучшие результаты были отмечены при сочетании следующих компонентов (масс. %):
| Ципротерона ацетат | 0,9÷2,0 |
| Мелатонин | 10÷17,2 |
| Пророксан основание | 0,94÷2,0 |
| N-метил-N-(1,2R,3R,4R,5S- | 0,5 |
| пентагидроксигексил)- | |
| октадеканамид | |
| D-пантенол | 0,5 |
| полиоксиэтилированный | 10 |
| α-токоферол | |
| полиоксиэтилированный | 1 |
| ланолин | |
| 3-(октадецилокси)-1,2- | 0,1 |
| пропандиол | |
| Стеариновая кислота | 1,1 |
| N,N-диэтилтолуамид | 15 |
| 1,2-изопропилиден глицерола | 20 |
| 1,2,3-триацетоксипропан | До 100 |
Нижние концентрации биологически активных веществ выбраны из условия минимальных количеств БАВ, вызывающих гарантированный эффект при технически допустимом объеме готовой лекарственной формы «Спот-он» для данного вида животных (см. пример 9, 12, 19). Так для котов оптимальная разовая объемная доза - 0,5-2 мл, т.к. при большем количестве раствор растекается на недопустимо большой площади и смачивает шерсть. Верхние пределы концентраций пророксана и ципротерона ацетата выбраны исходя из известных данных токсичности этих компонентов при удобных количествах наносимой формы «Спот-он» и растворимости их в фармацевтической композиции (см. пример 20, 24). Верхний предел концентрации мелатонина определяется его растворимостью в выбранном составе растворителей (см. пример 22).
Важным также оказалась необходимость стабилизации значения рН композиции на уровне 4-6, т.к. при большем значении рН быстро разрушается БАВ (например, ципротерона ацетат), а при меньшем существует вероятность раздражения кожи животного (см. пример 32, 33). Данное значение рН легко получить необходимой добавкой при ионометрическом контроле подходящей карбоновой кислоты: глицирризиновой или (и) янтарной или (и) молочной, или (и) пировиноградной, или (и) лимонной, или (и) яблочной, или (и) винной, или (и) стеариновой, или (и) миристиновой, или (и) октановой или (и) лауриновой кислоты (см. примеры 16, 18, 21 и др.) и др. Как показала практика необходимое количество карбоновой кислоты колеблется в зависимости от молекулярной массы и степени диссоциации от 0,1 до 1,1 масс %.
Проведенные биологические испытания (см. пример 6-15) показали, что разработанная фармацевтическая композиция при однократном (реже двукратном) нанесении самцам быстро и полностью блокирует поведенческие феномены активного полового поведения, при этом эффект развивается в течение 12-72 часов и сохраняется обычно от одного месяца до полугода, что позволяет свести к минимуму количество вводимого в организм животного стероидного соединения, а следовательно вероятность тяжелейших, часто летальных побочных эффектов, развивающихся при длительном системном введении животному гормонально активных стероидов. Проявляющиеся после применения препарата ювенильные особенности поведения животного - игровое и познавательное поведение при отсутствии агрессивности - комфортно для владельцев животных. Препарат не влияет на навыки служебных собак, ингибирование полового поведения благоприятно сказывается на продуктивности их работы. Препарат обратимо блокирует фертильные функции самцов, которые восстанавливаются сразу после прекращения его действия. Фармацевтическая композиция удобна в применении - используется для трансдермального введения в форме «Спот-он» в любой период полового цикла. Присутствующий в композиции мелатонин по литературным данным [Катцунг Б.Г. Базисная и клиническая фармакология. Т. 2 / М.: Бином. 2008. 784 с] улучшает эмоциональный фон, обладает сильным антиоксидантным и адаптогенным действием, нормализует сон.
Таким образом, предложен безопасный и удобный способ временного блокирования половых функций самцов млекопитающих, включая поведенческие феномены, и найдена фармацевтическая композиция для его осуществления.
Осуществление изобретения
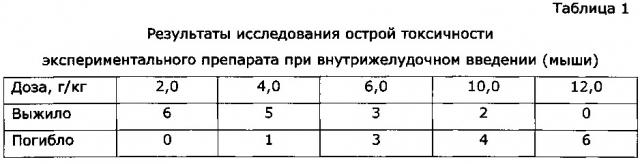
Пример 1. (Исследование острой токсичности у белых мышей)
Материалы и методы:
Исследование острой токсичности препарата, приготовленного по примеру 16, проводили на клинически здоровых самцах белых мышей массой 23-25 г, предварительно выдержанных на 15 дневном карантине. Статистические группы состояли из 6 особей. Всего было сформировано 5 групп. За животными вели наблюдение в течение двух недель после введения препарата, отмечая сроки гибели, общее состояние животных, сохранение двигательных функций, аппетита, состояние шерстяного покрова, дыхания, реакцию на внешние раздражители.
Испытания проводились в соответствии с «Методическими рекомендациями по изучению общетоксического действия фармакологических веществ», утвержденных Минздравом России, 2005 г.
Экспериментальный препарат вводили белым мышам внутрижелудочно через атравматичный металлический зонд в возрастающих дозах по Литчфилду-Уилкоксону: 2,0 г/кг, 4,0 г/кг, 6,0 г/кг, 10,0 г/кг и 12,0 г/кг. Контрольные животные получали воду в тех же объемах. Результаты представлены в Таблице 1.
ЛД50 составило 7,2 г/кг (рассчитано по формуле Кербера) при стандартной ошибке 0,97 (по формуле Гаддама).
С помощью графического метода анализа зависимости «доза-эффект» определили LD16 и LD84, которые составили 3,48 г/кг и 11,5 г/кг соответственно.
Результаты:
Установлено, что LD50 (в/ж) = 7,2±0,97 г/кг, что позволяет отнести данный препарат к 4 классу опасности (малотоксичное соединение) по ГОСТ 12.1.007-76.
Клиника острого отравления характеризовалась выраженным угнетением, вялостью животных почти сразу после введения. Затем наступал наркоз, из которого часть животных выходила, а часть погибала на 2-3 сутки. При проведении патологоанатомического вскрытия у погибших животных была отмечена гиперемия слизистой желудка, кровоизлияния на ходу кровеносных сосудов, полнокровие печени и почек.
Пример 2. (Исследование кожно-резорбтивного действия предлагаемого препарата)
Материалы и методы:
Изучение кожно-резорбтивного действия препарата, приготовленного по примеру 16, изучалось в однократном и повторном (5 дней) опытах на белых крысах-самцах массой 180-200 г. Для исследования были отобраны клинически здоровые особи без видимых повреждений кожного покрова. Животные были разделены на три группы:
1 группа - контроль (10 животных).
2 группа - однократная обработка (10 животных).
3 группа - пятикратная обработка (10 животных).
Целью однократного опыта являлось определение смертельных доз и соответственно определение кожно-орального коэффициента (К к/о):
Для этого, препарат в объеме 1 мл (5,0 г/кг) наносился на выстриженный участок кожи спины крысы размером 4×4 (2 раза в течение двух часов). Суммарная доза составила 10 г/кг.
Результаты:
Клиническая картина интоксикации животных после однократной обработки практически не отличалась от контроля. Животные были активны, подвижны, хорошо поедали корм. Гибель животных не отмечалась. Аналогичные результаты получены в пятикратном эксперименте, где препарат наносился ежедневно в дозе 5,0 г/кг (1,0 мл на крысу).
Не было отмечено раздражающего действия препарата на кожу ни в одном из опытов. Не наблюдалось покраснения кожи, расчесов, отека, утолщения кожной складки.
Вывод: таким образом, полученные данные свидетельствуют о том, что препарат не обладает кожно-резорбтивным действием.
Пример 3. (Изучение переносимости предлагаемого препарата на кобелях)
Материалы и методы:
Исследование по переносимости препарата, приготовленного по примеру 16, проводили на 6 клинически здоровых кобелях метисах в возрасте от 15 месяцев до 4-х лет и массой 3,5-4,7 кг. Животные были разделены на 3 группы по 2 особи в каждой:
1 группа - каждое животное обрабатывали 1 мл препарата.
2 группа - каждое животное обрабатывали 3 мл препарата.
3 группа - контрольная (без обработки).
Препарат наносили на неповрежденную кожу вдоль позвоночника между лопатками в течение 10 дней с перерывом на 3 и 6 дни. Особей контрольной группы обрабатывали дистиллированной водой. Клинические наблюдения проводили за сутки до нанесения препарата и через 1, 2 и 5 суток после первого применения. Обследование животных включало измерение температуры тела, подсчета количества сердечных сокращений и дыхательных движений, визуальную оценку общего состояния и определение гематологических показателей.
Результаты:
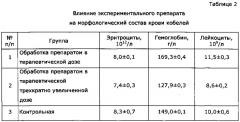
Многократное нанесение препарата в терапевтической и превышающей ее в три раза дозах не вызывало никаких отклонений от нормы в физиологическом статусе животных. Температура тела варьировала от 38,0 до 38,5°C (при физиологической норме 37,5-39,0°C). Частота пульса находилась в пределах колебаний от 70 до 77 ударов в минуту (норма 70-80). Количество дыхательных движений было от 15 до 30 (норма 10-30). Общее состояние кобелей опытных групп не отличалось от состояния контрольных животных. Отмечено угнетение и отказ от корма особей второй группы в последние 2 дня опыта. Результаты гематологического исследования представлены в таблице 2.
Таким образом, препарат при многократном (в течение 10 дней с перерывом на 3 и 6 дни) нанесении кобелям разных возрастных групп в терапевтической дозе и превышающей ее в три раза хорошо переносится животными, не оказывает отрицательного влияния на физиологическое состояние организма и гематологические показатели.
Пример 4. (Изучение переносимости предлагаемого препарата на котах)
Материалы и методы:
Исследование переносимости препарата, приготовленного по примеру 16, на котах проводили на 9 клинически здоровых метисах в возрасте от 15 месяцев до 3,5 лет массой 3,5-5,0 кг. Животные были разделены на 3 группы по три особи в каждой:
1 группа - животные, получавшие 1 мл препарата.
2 группа - животные, получавшие 3 мл препарата.
3 группа - контрольная.
Препарат наносили на кожу спины между лопатками. Животных обрабатывали ежедневно в течение 8 дней с перерывом на 3 и 6 дни. Особям третьей группы вводили дистиллированную воду.
Клинические наблюдения проводили за сутки до применения препарата, а затем через 1, 6, 12 часов и 1, 2, 5 дней после первого нанесения препарата. Обследование животных включало осмотр, измерение температуры тела, частоты пульса и дыхания, а также изучение гематологических и биохимических показателей крови.
Результаты:
Никаких отклонений от нормы в физиологическом статусе животных не отмечалось, аппетит сохранен, температура тела варьировала от 38,5 до 39,0°C, частота пульса находилась в пределах 100-110 ударов в минуту (норма 100-125), частота дыхания 20-25 (норма 20-30) дых. движ./мин, общее состояние опытных животных не отличалось от состояния контрольных.
Применение препарата не вызвало изменений в гематологических и биохимических показателях крови животных (таблица 3, 4).
Вывод: коты хорошо переносили экспериментальный препарат при его многократном применении в терапевтической дозе и превышающей ее в 3 раза.
Пример 5. (Изучение субхронической токсичности на крысах)
Материалы и методы:
Изучение субхронической токсичности проводили на 15 беспородных клинически здоровых крысах-самцах. Животные были разделены на три группы по 5 особей в каждой. Воздействие препарата на организм животных изучали в течение 15 дней в дозах 1/100 и 1/1000 от LD50. Препарат, приготовленный по примеру 16, наносили ежедневно накожно в область спины 1-й группе в дозе 0,07 г/кг и 2-й группе в дозе 0,007 г/кг. Третьей группе никаких препаратов не наносили. В ходе исследования анализировались гематологические и биохимические показатели крови животных до начала эксперимента и через 5 дней после последнего нанесения препарата, а также было проведено макро- и микроскопическое исследование внутренних органов (см. таблицу 5, 6).
Результаты:
Гематологические и биохимические показатели крови крыс 1 и 2 групп были на уровне показателей в контроле (3 группа) и соответствовали физиологической норме для животных данного пола и возраста.
Макро- и микроскопическое исследования внутренних органов крыс показали: серозные оболочки гладкие, блестящие, дыхательные пути свободны. Сердце, печень, почки, селезенка, органы желудочно-кишечного тракта, поджелудочная железа, надпочечники, тимус, семенники обычной консистенции, окраски, размеров. Печень у всех крыс нормальной гистоструктуры, у одной из 1-ой группы была отмечена умеренная, очаговая зернистая дистрофия гепатоцитов. Почки - во всех случаях полнокровие капилляров, особенно в составе клубочков, а также в интерстиции, эпителий прямых и извитых канальцев не изменен. Сердце - кардиомиоциты обычного вида, адекватная васкуляризация. Легкие - бронхиальное дерево без особенностей. Селезенка - увеличение доли красной пульпы, реакция фолликулов в виде размытых границ, без светлых центров размножения. Поджелудочная железа - во всех случаях дольки разделены жировой тканью, в паренхиме - нормальные островки и паренхима. Надпочечники - нормальные соотношения и полнокровие слоев. Тимус - крупные дольки со сливающимися светлыми центрами, умеренное полнокровие. Семенники - как в контроле, так и в опыте содержали зрелые нормальные сперматозоиды в придатке. Тонкая кишка - во всех случаях соответствовала возрастной гистоструктуре.
Массовые коэффициенты внутренних органов крыс представлены в таблице 6.
Вывод: проведенные исследования показали, что длительное применение экспериментального препарата в дозах выше терапевтических не вызывает изменения гематологических и биохимических показателей крови лабораторных животных и не оказывает отрицательное воздействие на морфологию внутренних органов.
Пример 6. (Исследование регулирующего половое поведение предлагаемого препарата на котах)
Материалы и методы:
Испытания регулирующего половое поведение препарата, полученного по примеру 16, проводились на 4 домашних беспородных клинически здоровых котах, живущих у разных хозяев, в период с мая 2013 по ноябрь 2014 г (см. таблицу 9).
Препарат животным наносили на второй день проявления половой охоты в вечернее время в количестве 1 мл на спину между лопатками.
Результаты:
После применения препарата хозяевами котов отмечалось исчезновение проявлений половой охоты, успокоение животных, снижение агрессивности, снижение проявлений вокализации.
У одного кота половая охота возобновились спустя 2 месяца после применения препарата, у одного кота - спустя 6 месяцев, у двух - спустя 3 месяца.
Побочных эффектов препарата не было отмечено.
Вывод: экспериментальный препарат показал высокую эффективность в качестве регулятора полового поведения на срок от 2 до 6 месяцев у котов.
Пример 7. (Исследование регулирующего половое поведение предлагаемого препарата на котах)
Материалы и методы:
Испытания по определению эффективности применения препарата, приготовленного по примеру 16, с целью снижения половой активности и коррекции нежелательного поведения (повышенная агрессивность и вокализация, поиск полового партнера, мечение территории мочой) проводились на базе приюта для бездомных животных СГОБФ «Зоозащита плюс» Серпуховского района Московской области в период с февраля по апрель 2014 г на 10 клинически здоровых котах в возрасте от 12 месяцев до 3 лет массой 3,3-4,8 кг.
Животных разделили на две группы - опытную и контрольную, по 5 особей в каждой. Котам опытной группы препарат наносили однократно во время вечернего осмотра путем капельного нанесения на сухую неповрежденную кожу в области спины между лопатками в дозе 1 пипетка-капельница (1 мл) на животное. Животные контрольной группы никаких препаратов не получали. Котов опытной и контрольной группы осматривали 1 раз в день.
Результаты:
При отсутствии должного эффекта в течение 24 часов двум котам опытной группы, препарат наносили повторно в той же дозе. При применении препарата побочных явлений и осложнений у котов не наблюдалось. Признаки полового возбуждения и связанного с ним поведения не отмечали у опытных животных в течение всего периода наблюдения (67 дней), эффект наступал на 1-2 сутки.
Вывод: экспериментальный препарат показал высокую эффективность в качестве регулятора полового поведения у котов. Эффект развивался быстро за 1-2 суток и сохранялся в течение 67 дней наблюдения.
Пример 8. (Исследование регулирующего половое поведение предлагаемого препарата на котах)
Материалы и методы:
Испытания по определению терапевтической эффективности препарата, приготовленного по примеру 16, проводились в период с января по февраль 2015 г в ООО «Калининградский областной центр ветеринарной медицины» на 14 клинически здоровых котах в возрасте от 10 месяцев до 4 лет массой 2,5-4,0 кг.
Животных разделили на две группы - опытную и контрольную, по 7 особей в каждой. Котам опытной группы в период повышенной половой активности на 2-3 день проявления признаков наносили испытуемое средство однократно во время вечернего приема в клинике путем капельного нанесения на сухую неповрежденную кожу в области спины между лопатками или в области шеи у основания черепа в дозе 1 мл (20 капель) на животное. Животные контрольной группы никаких препаратов не получали и продолжали «гулять». Котов опытной и контрольной группы осматривали в клинике 1 раз в неделю.
Результаты:
При отсутствии должного эффекта в течение 24 часов двум котам опытной группы, препарат нанесли повторно в той же дозе. Применение препарата побочных явлений и осложнений у котов не выявило. Половая активность у 5 котов опытной группы прекратилась на 2-ые сутки, у 2 - на 3-тьи сутки. За 30 дней исследования у 4 котов контрольной группы половая активность регистрировалась трижды, у 3 котов дважды. У всех котов опытной группы половая активность за 30 дней проведения опыта не наступила.
Вывод: экспериментальный препарат показал высокую эффективность в качестве регулятора полового поведения у котов. Эффект развивался за 2-3 суток и сохранялся в течение 30 дней наблюдения.
Пример 9. (Исследование регулирующего половое поведение предлагаемого препарата на котах)
Материалы и методы:
Испытания по определению терапевтической эффективности препарата, приготовленного по примеру 19, проводились в период с января по март 2015 г в ООО «Калининградский областной центр ветеринарной медицины» на 14 клинически здоровых котах в возрасте от 11 месяцев до 4 лет массой 2,5-4,5 кг.
Животных разделили на две группы - опытную и контрольную, по 7 особей в каждой. Котам опытной группы в период повышенной половой активности наносили испытуемый препарат однократно путем капельного нанесения на сухую неповрежденную кожу в области спины между лопатками или в области шеи у основания черепа в дозе 1 мл (20-25 капель) на животное. Коты содержались в квартирных условиях. Животные контрольной группы никаких препаратов не получали и продолжали «гулять». Котов опытной и контрольной группы осматривали в клинике 1 раз в неделю.
Результаты:
При отсутствии должного эффекта в течение 24 часов трем котам опытной группы, препарат нанесли повторно в той же дозе. При применении препарата побочных явлений и осложнений у животных не наблюдалось. Половая активность у 4 котов опытной группы прекратилась на третьи сутки, у 3 - на четвертые сутки. За 40 дней исследования у котов контрольной группы половая активность не прекратилась, животные «метили» территорию. У всех котов опытной группы половая активность за 28 дней не наступила. На 33-ий день 2 кота пометили территорию, на 35-ый день 2 кота загуляли, периодически кричали и беспокоились. Остальные животные опытной группы стали беспокойными, 2 кота на 38-ой день опыта пометили территорию, стали агрессивными.
Вывод: экспериментальный препарат показал высокую эффективность в качестве регулятора полового поведения у котов. Эффект развивался за 3-4 суток и сохранялся минимум в течение 28 дней наблюдения.
Пример 10. (Исследование регулирующего половое поведение предлагаемого препарата на кобелях)
Материалы и методы:
Испытания по оценке эффективности применения препарата, приготовленного по примеру 16, для коррекции полового поведения проводились на базе приюта для бездомных животных СГОБФ «Зоозащита плюс» Серпуховского района Московской области в период с февраля по май 2014 г на 12 клинически здоровых кобелях в возрасте от 1,5 до 5 лет массой 7-35 кг. Животные содержались на базе приюта.
Животных разделили на две группы - опытную и контрольную, по 6 особей в каждой. Кобелям опытной группы препарат наносили однократно во время вечернего осмотра путем капельного нанесения на сухую неповрежденную кожу в области спины между лопатками в дозе 2 мл на животное массой от 5 до 15 кг и 4 мл на животное массой от 15 до 35 кг. Животные контрольной группы никаких препаратов не получали. Кобелей опытной и контрольной группы осматривали 1 раз в день.
Результаты:
При отсутствии должного эффекта в течение 24 часов двум животным опытной группы, препарат наносили повторно в той же дозе. При применении препарата побочных явлений и осложнений у кобелей не наблюдалось. Признаки снижения агрессивности и