Способ моделирования патофизиологического химического ожога пищевода у экспериментальных животных
Иллюстрации
Показать всеИзобретение относится к медицине и может быть использовано для изучения особенностей формирования химического ожога пищевода в эксперименте. Способ включает введение в пищевод животного, подобранного по величине просвета пищевода зонда, имеющего боковые отверстия, и доставку по зонду химического агента. При этом используют градуированный, слепо заканчивающийся полый зонд со свободно вставленной в его просвет до слепого конца струной-проводником. Зонд имеет два длинных продольных, соразмерных длине пищевода, расположенных друг напротив друга боковых отверстия. Последние выполнены таким образом, чтобы они при установке располагались в просвете всего пищевода и проксимальная вырезка отверстий находилась ниже глоточно-пищеводного сфинктера, а дистальная - над кардиальным жомом. Наличие между отверстиями узких перемычек практически не меняет щелевидную форму и объем пищевода животного при установлении зонда. Предлагаемый способ обеспечивает создание патофизиологического химического ожога пищевода, формируя его протяженный характер при использовании различных коррозивных жидкостей. 1 пр., 4 ил.
Реферат
Предлагаемый способ относится к области медицины, а именно к экспериментальной хирургии, и может быть использован для изучения особенностей формирования послеожогового рубца пищевода и влияния различных медикаментов на процесс рубцевания.
Из наиболее известных и близких по технической сущности является способ моделирования химического ожога пищевода в эксперименте с применением зонда с одним боковым отверстием, марлевым тампоном на дистальном конце и вставленным в просвет трубки капилляром для подведения коррозивной жидкости [Устройство для моделирования локального ожога пищевода у экспериментальных животных. Никольский В.И., Климашевич А.В., Шабров А.В. RU Пат. №134422, МПК А61В 18/14].
К недостаткам данного устройства следует отнести то, что расположенное на дистальном конце зонда отверстие является единственным выходом для коррозивной жидкости, способствуя тем самым появлению трудно контролируемого по глубине локального ожога пищевода и увеличивая вероятность перфорации в этой зоне. Пропитанный реагентом тампон не обеспечивает строгой дозировки подводимой коррозивной жидкости и напрямую зависит от степени гигроскопичности материала, что трудно учесть в эксперименте. Указанная модель не совмещает возможность получения химического ожога и дальнейшую оценку эффективности проводимой местной терапии, поскольку процесс патологических изменений на ограниченном участке стенки пищевода не предполагает локального внутрипищеводного подведения препаратов непосредственно к зоне повреждения.
Наиболее близким к заявленному способу, позволяющему создать ожог пищевода, может служить модель Ю.А. Пархисенко и соавт. (2003), представляющая собой полиэтиленовую трубку с четырьмя боковыми отверстиями и торцевой заглушкой на дистальном конце [Устройство для создания экспериментальной модели химического ожога пищевода у крыс. Пархисенко Ю.А., Булынин В.В., Лейбович Б.Е., Трофимов Д.П. Удостоверение на рационализаторское предложение №2639 от 28.10.2003].
Однако устройство Ю.А. Пархисенко и соавт. (2003) для моделирования ожога имеет ряд недостатков. При установке устройства зачастую отмечается перегиб его в области отверстий, расположенных конструктивно друг напротив друга, что лишает зонд первоначальной жесткости. При использовании полиэтиленовой трубки с несколькими боковыми отверстиями происходит первоначальный контакт коррозивной жидкости со слизистой пищевода в зоне боковых отверстий, прилегающих к стенке органа, с последующим распространением ее вдоль трубки по оси органа. Сама трубка при этом выполняет кратковременную каркасную функцию, расширяя физиологически щелевидный пищевод, что неизбежно приводит к увеличению объема поступающей коррозивной жидкости в пищевод с целью создания равномерного давления вещества на стенку органа. Ввиду ограниченности пищевода к расширению отмечается более плотный нефизиологический контакт коррозивной жидкости со слизистой оболочкой с созданием кратковременной «муфты» из жидкости вокруг трубки. Указанный эффект можно назвать «эффектом тугого наполнения» за счет большего объема вводимого вещества.
Все вышесказанное приводит к формированию циркулярного химического ожога тяжелой степени с наиболее вероятной перфорацией пищевода в областях напротив отверстий, откуда коррозивная жидкость выходит под высоким давлением, что вызывает преждевременную гибель животных, а в случае выживания приводит к формированию грубого рубца, ограничивающего возможность проведения и изучения воздействия лекарственных препаратов в качестве местной терапии.
Задачей заявленного способа является устройство, которое создает приближенный к реальности по площади и глубине химический ожог пищевода с возможностью в перспективе внутрипищеводного подведения лекарственных препаратов с последующей морфометрической оценкой их эффективности.
Техническим результатом предлагаемого устройства является создание патофизиологической модели химического ожога пищевода за счет конструктивных особенностей устройства.
Эта задача решается способом, заключающимся в том, что выкраивание боковых отверстий зонда осуществляется с учетом анатомо-физиологических особенностей пищевода у крыс.
Сущность предлагаемого способа заключается в том, что для моделирования патофизиологического ожога согласно предлагаемой полезной модели в качестве устройства доставки коррозивной жидкости используют градуированный зонд со вставленной в его просвет струной-проводником. Отличительными особенностями устройства является наличие двух длинных продольных, расположенных друг напротив друга, боковых отверстий для создания патофизиологического ожога, что позволяет приблизить эксперимент к условиям ожога у человека. Струна-проводник и шкала делений обеспечивают контролируемую установку устройства в просвете пищевода таким образом, что два боковых отверстия располагаются строго в просвете всего пищевода, проксимальная вырезка отверстий находится ниже глоточно-пищеводного сфинктера, а дистальная - над кардиальным жомом. При этом струна-проводник предупреждает сгибание зонда в области боковых отверстий при установке. Сохраненные перемычки трубки между отверстиями практически не меняют щелевидную форму и объем пищевода, что позволяет вводить меньший объем реагента, а также обеспечивают безопасность при установке и извлечении зонда. В результате коррозивная жидкость поступает в просвет органа наиболее физиологично и в меньшем количестве. Подобранный по величине просвета пищевода животного внешний диаметр устройства предупреждает заброс в дыхательные пути крысы коррозивной жидкости. Слепой конец препятствует попаданию коррозивной жидкости в желудок, что создает необходимую экспозицию контакта агента со стенкой пищевода.
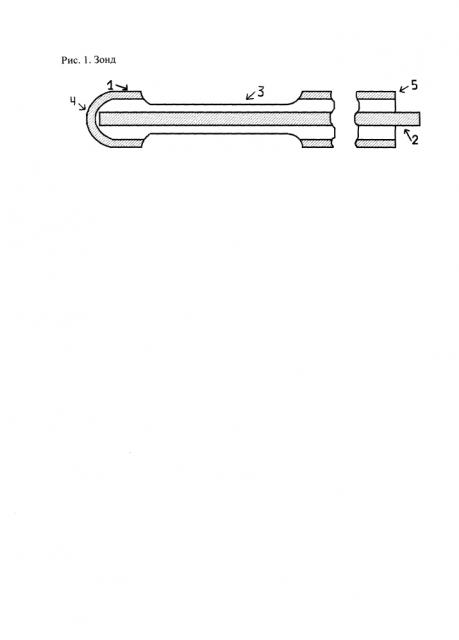
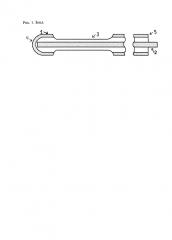
Предлагаемое устройство для моделирования ожога пищевода представлено градуированным зондом из эластичного материала с двумя продольными длинными боковыми отверстиями, дистальный конец зонда округлой формы, заканчивающийся слепо, внутри него свободно установлена металлическая струна-проводник. Проксимальный конец свободен.
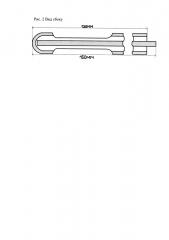
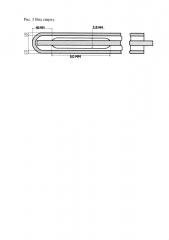
Устройство иллюстрируется чертежами-рисунками (рис. 1, рис. 2, рис. 3, рис. 4), где 1 - полиэтиленовая градуированная трубка со струной-проводником - 2, боковыми отверстиями - 3, слепо заканчивающимся концом - 4, проксимальный конец - 5 свободный.
Пример.
Применяли устройство следующим образом. Под общей анестезией животному вводили устройство со струной-проводником в пищевод, не доходя до кардиального жома. Создавали ожог путем экспозиции 20% уксусной кислоты в течение 1 минуты, в объеме 0,5 мл. Для этого под общей анестезией вводили зонд с внешним диметром 2,0 мм, имеющий 2 продольных боковых отверстия размером 50×1,2 мм (длина отверстий обусловлена длиной пищевода у крысы - 80 мм), отступив на 10 мм проксимально от слепо заканчивающегося конца на струне-проводнике диаметром 1,0 мм, упирающейся в слепой конец. Длина зонда, введенного в пищевод, должна составлять 10,0-11,0 см, что соответствует расстоянию от резцов до супракардиального отдела пищевода у крысы [Трофимов Д.П. Профилактика формирования послеожогового рубцового стеноза пищевода (экспериментально-клиническое исследование): дис. … канд. мед. наук. - Воронеж, 2004. - 146 с.]. Удаляли струну-проводник. По зонду болюсно вводили 0,75 мл. 20% уксусной кислоты с учетом того, что 0,25 мл прижигающего агента остаются в полой проксимальной части трубки. Указанный объем (0,25 мл) определен до начала эксперимента. В последующем после эвакуации оставшейся уксусной кислоты шприцем быстро удаляли зонд. В течение 30 минут контролировали состояние животных до выхода из наркоза.
Таким образом, устройство для моделирования патофизиологического химического ожога пищевода у экспериментальных животных обеспечивает создание патофизиологического химического ожога в пищеводе, формируя его протяженный характер, а по площади и глубине сопоставимо с химическим ожогом у человека. Экспериментальный ожог пищевода позволяет изучать влияние различных лекарственных препаратов, подводимых через заявленное устройство, физических факторов и другое на формирование рубцовой ткани, максимально приближенных к человеку. Устройство позволяет получить в эксперименте химический ожог при использовании различных коррозивных жидкостей без учета их вязкости, поверхностного натяжения, благодаря достаточной ширине отверстий и сохраненным эластичным перемычкам конструкции, которые «расходятся» при введении вещества любой консистенции. Гибкий проводник обеспечивает щадящее проведение и безопасное извлечение зонда при различных видах и формах образующихся сужений пищевода в результате ожога.
Указанный способ одинаково применим для создания и изучения патофизиологического ожога, особенностей воздействия местной лекарственной терапии у других экспериментальных животных (собака, кролик) с конструированием аналогичного устройства, учитывающего видовые анатомические особенности строения верхнего отдела пищеварительной трубки.
Способ моделирования химического ожога пищевода у экспериментальных животных, включающий введение в пищевод подобранного по величине просвета пищевода зонда, имеющего боковые отверстия, и доставку по зонду химического агента, отличающийся тем, что используют градуированный, слепо заканчивающийся полый зонд со свободно вставленной в его просвет до слепого конца струной-проводником и наличием на зонде двух длинных продольных, соразмерных длине пищевода, расположенных друг напротив друга боковых отверстий, которые выполнены таким образом, чтобы они при установке располагались в просвете всего пищевода, проксимальная вырезка отверстий находилась ниже глоточно-пищеводного сфинктера и дистальная - над кардиальным жомом, при наличии между ними узких перемычек, практически не меняющих щелевидную форму и объем пищевода животного при установлении зонда.