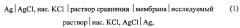Способ одновременной оценки потенциала доннана в восьми электромембранных системах
Иллюстрации
Показать всеИзобретение относится к области потенциометрических методов анализа и мембранных технологий и может быть использовано для совместного определения органических и неорганических ионов в многокомпонентных водных средах. Способ одновременной оценки потенциала Доннана в восьми электромембранных системах заключается в измерении ЭДС восьми электрохимических цепей с помощью девятисекционной ячейки из непроводящего материала, в которой каждая из восьми ионообменных мембран одним концом погружена в центральный корпус с исследуемым раствором, а другим концом - в одну из восьми секций с раствором сравнения, при этом измерение откликов восьми хлоридсеребряных электродов, погруженных в секции с раствором сравнения, осуществляют одновременно относительно хлоридсеребряного электрода, погруженного в корпус с исследуемым раствором, с помощью многоканального потенциометра, при этом каждая из восьми электрохимических цепей замыкается вдоль мембраны и диффузия в мембранах является бесконечно медленной относительно времени эксперимента. Технический результат: точная экспрессная оценка потенциала Доннана одновременно в восьми электромембранных системах. 5 ил., 2 пр.
Реферат
Изобретение относится к области потенциометрических методов анализа и мембранных технологий. Оно может быть использовано для одновременного экспресс-определения компонентов, совместно присутствующих в полиионных растворах, а также экспрессного исследования электрохимических свойств ионообменных мембран, в том числе вблизи межфазной границы мембрана/раствор.
Наиболее близким является способ определения потенциала Доннана (патент РФ №2364859, 2009 [1]). Способ заключается в измерении ЭДС двухэлектродной ячейки, в которой полоса ионообменной мембраны, подобно солевому мостику, погружена одним концом в раствор, концентрация которого близка к концентрации внутреннего раствора мембраны, а другим - в исследуемый раствор. Измерение производится с помощью двух электродов сравнения, контактирующих соответственно с исследуемым и концентрированным растворами, при этом электрохимическая цепь замыкается вдоль мембраны, а диффузия в фазе мембраны и примембранных слоях является бесконечно медленной относительно времени эксперимента. Данный способ позволяет выполнять оценку потенциала Доннана на границе ионообменная мембрана / раствор электролита только в одной электромембранной системе и не может быль использован для одновременного определения компонентов полиионных растворов или для экспрессной оценки электродноактивных свойств партии мембран.
Заявляемое изобретение заключается в разработке способа одновременной оценки потенциала Доннана в восьми электромембранных системах, предназначенного для совместного определения органических и неорганических ионов в многокомпонентных водных средах (пищевых, фармацевтических, медицинских и промышленных), содержащих аминокислоты, витамины, лекарственные вещества, меркаптаны и неорганические электролиты, а также для экспрессной оценки электродноактивных свойств ионообменных мембран в полиионных растворах.
Технический результат заключается в возможности реализации поставленной задачи.
Технический результат достигается тем, что электрохимическая ячейка включает следующие составные части: центральный корпус (d=4.5 см, h=4 см) для исследуемого раствора, второй корпус с одной секцией (d=5 см, h=3 см) для центрального корпуса и восьмью секциями (V=28 см3) для раствора сравнения, ионообменные мембраны (от 1 до 8 шт.), штатив для электродов, стеклянный рН-селективный электрод, хлоридсеребряные электроды сравнения (от 2 до 9 шт.) и электронный высокоомный многоканальный потенциометр с выходом на персональный компьютер. Корпуса для растворов выполнены из непроводящего материала. Оба корпуса имеют по восемь фиксаторов для мембран (8 шт. расположены на внутренней стороне центрального корпуса и по 1 шт. в каждой секции второго корпуса). Ионообменные мембраны выполнены из полимерного материала в форме пленок, трубок или стержней длиной 6-8 см. Каждая из восьми мембран одним концом погружена в центральный корпус с исследуемым раствором, а другим концом - в одну из восьми секций с раствором сравнения. Состав раствора в мембране (или в части мембраны, контактирующей с раствором сравнения) и состав раствора сравнения не должны отличаться. Хлоридсеребряный электрод, подключенный к входу многоканального потенциометра для электрода сравнения, погружен в центральный корпус, а хлоридсеребряные электроды, подключенные к измерительным входам, - в каждую из восьми секций. Стеклянный электрод погружен в центральный корпус и подключен к измерительному входу потенциометра. Измерение откликов хлоридсеребряных электродов (от 1 до 8 шт.), погруженных в секции с раствором сравнения, и стеклянного электрода осуществляется одновременно относительно хлоридсеребряного электрода, погруженного в корпус с исследуемым раствором, с помощью многоканального потенциометра. Реализация способа состоит в одновременном измерении электродвижущей силы (ЭДС) восьми электрохимических цепей вида (1) для восьми различных мембран и цепи вида (2).
Общая ЭДС цепи (1) складывается из скачков потенциала на отдельных границах:
где - стандартные потенциалы электродов сравнения; и и - разности потенциалов на границе раствора сравнения и исследуемого раствора с насыщенным раствором КСl электродов сравнения; и - потенциалы Доннана на границе мембраны с раствором сравнения и исследуемым раствором соответственно; - диффузионный потенциал в фазе мембраны.
В электрохимической ячейке используются хлоридсеребряные электроды с равными стандартными потенциалами (), которые в цепи (1) направлены противоположно и компенсируют друг друга.
Потенциалы жидкостного соединения и , рассчитанные по уравнению Гендерсона для растворов сравнения НСl, NaCl, КСl, СаСl2 с концентрацией 1 М и исследуемых растворов тех же электролитов с минимальной концентрацией (1.0⋅10-4 М), составляют ~1.0 мВ и ~-5.4 мВ соответственно.
Нивелирование величины потенциала Доннана на границе мембраны с раствором сравнения () достигается близостью концентраций раствора сравнения и фиксированных ионообменных групп в мембране. Значение на границе 1 М раствора 1,1-валентного электролита и ионообменной мембраны с сильнокислотными или сильноосновными группами при обменной емкости 1 ммоль/г составляет 2-10 мВ (учитывая, что при концентрации внешнего раствора 1 М снижается степень диссоциации фиксированных групп и электронейтральный раствор присутствует во всех порах с радиусом >1.5-1.8 нм).
Расстояние между границами ионообменной мембраны с исследуемым раствором и раствором сравнения соответствует длине мембраны. Время диффузии 1 моль электролита через 6 см мембраны с сечением (1.6-5)⋅10-2 см2 составляет 5.6⋅106 ч (с учетом среднего значения интегрального коэффициента проницаемости мембраны Р≈10-7 см2⋅с-1 [2]). Это на порядки превышает время установления квазиравновесия в электромембранной системе (≤15 мин). Благодаря этому квазиравновесия, формирующиеся на границах мембраны с исследуемым раствором и раствором сравнения, устойчивы во времени и независимы друг от друга, а ионный состав в объеме мембраны не изменяется. Поэтому складывается из двух диффузионных потенциалов в фазе мембраны вблизи границ с исследуемым раствором и раствором сравнения. На границе мембрана / исследуемый раствор выравнивание концентраций противо- и коионов в растворе и мембране ограничивается ее селективностью, то есть потоки ионов через межфазную границу после установления квазиравновесия стремятся к нулю. На границе мембрана / раствор сравнения диффузионные потоки ионов нивелируются благодаря близости концентраций противо- и коионов в связанных порах вблизи межфазной границы и в объеме мембраны (состав растворов сравнения выбирается в зависимости от ионной формы мембраны: 1.0 М растворы XClz для пленок Хz+-формах, где Xz+ - неорганический или органический катион).
Таким образом, суммарный вклад скачков потенциала на всех межфазных границах электрохимической цепи (1), кроме потенциала Доннана на границе мембрана / исследуемый раствор, составляет от -3 мВ до 5 мВ. При этом для систем с мембранами обменной емкостью 1-3 ммоль/г и исследуемыми растворов электролитов концентрацией 1.0⋅10-4-1.0⋅10-1 М экспериментальные значения ЭДС цепи (1) варьируются в интервале 20-200 мВ. Таким образом, можно считать, что определяющий вклад в ЭДС цепи (1) вносит потенциал Доннана на границе мембрана / исследуемый раствор.
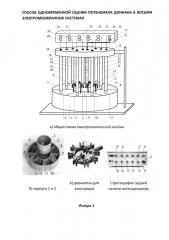
На фигуре 1 представлена схема электрохимической ячейки для одновременной оценки потенциала Доннана в шести электромембранных системах; на фигуре 2 - время установления квазиравновесия и дрейф потенциала Доннана в системах с гибридными мембранами и раствором 1,0⋅10-3 М NovHCl+1,0⋅10-3 M LidHCl; на фигуре 3 - значения коэффициентов градуировочных зависимостей потенциала Доннана от концентрации ионов NovH+, LidH+ и Н3O+ в растворах NovHCl+LidHCl для ряда гибридных мембран; на фигуре 4 - результаты совместного определения ионов ΝοvΗ+ и LidH+ в присутствии ионов Н3O+ в водных растворах с помощью пар гибридных мембран различного состава; на фигуре 5 - систематические и случайные ошибки определения катионов ΝοvΗ+ и LidH+ в водных растворах с использованием гибридных мембран различного состава.
Работа реализуется следующим образом. Корпус 1 заполняется исследуемым раствором объемом 15 см3. В корпусе 2 секции 3-10 заполняются раствором сравнения объемом 10 см3. Корпус 1 помещается в секцию 11 корпуса 2. Образцы мембран 12 (1-8 шт., длиной 6-8 см) в набухшем состоянии одним концом 13 закрепляются в фиксаторе корпуса 1, а другим концом 14 - в секциях 3-10. В корпус 1 погружаются хлоридсеребряный электрод 15, подключенный к входу 16 (вход для электрода сравнения) многоканального потенциометра 17, и стеклянный электрод 18, подключенный к измерительному входу 19. В секции 3-10 погружаются хлоридсеребряные электроды 20-27, подключенные к измерительным входам 28-35 потенциометра. Все электроды закреплены в держателе 36 штатива и их погружение в исследуемый раствор и раствор сравнения осуществляется одновременно. Измерение откликов электродов 18, 20-27 относительно электрода 15 осуществляется одновременно с помощью электронного высокоомного многоканального потенциометра 17 и автоматически выводятся на персональный компьютер.
Достоинствами способа являются низкие время и трудоемкость анализа, малый объем анализируемого раствора, снижение накопления ошибок за счет одновременного измерения ЭДС электрохимических цепей.
ПРИМЕР 1
Способ одновременной оценки потенциала Доннана в восьми электромембранных системах позволяет проводить экспрессное определение электродноактивных свойств ионообменных мембран в полиионных водных растворах.
Исследованы свойства гибридных материалов на основе перфторированных сульфокатионитных мембран МФ-4СК и Nafion. Методом экструзии с последующим in situ введением допанта были получены мембраны Nafion, содержащие наночастицы гидратированного диоксида циркония. Концентрация ZrO2 варьировалась от 2.0 до 2.8 масс. %. Методом отливки были получены мембраны МФ-4СК, содержащие наночастицы гидратированного диоксида кремния с поверхностью, функционализированной 3-аминопропил- (R1) и 3-(2-имидазолин-1-ил)пропил- (R2). Концентрация SiO2 составляла 3 масс. %, концентрации R1 - 5, 10 мол. %, R2 - 5 мол. % от количества SiO2. Во всех материалах лишь 1/2 длины пленки содержала допант. Конец этой части мембраны контактировал с исследуемым раствором в процессе эксперимента. Часть пленки, контактирующая с раствором сравнения, не была модифицирована. Отсутствие допанта в этой части было необходимо для обеспечения близости составов раствора внутри мембраны и раствора сравнения. Образцы гибридных мембран были предоставлены Лабораторией ионики функциональных материалов ИОНХ РАН (заведующий лабораторией - проф., д.х.н., член.-корр. РАН А.Б. Ярославцев). Синтез мембран и определение содержания в них допантов выполнен с. н.с. ИОНХ РАН к.х.н. Е.Ю. Сафроновой.
Электродноактивные свойства мембран исследовали в водных растворах, содержащих гидрохлориды новокаина (NovHCl) и лидокаина (LidHCl) с концентрациями от 1.0⋅10-4 до 1.0⋅10-2 М. Интервал рН растворов NovHCl+LidHCl составлял от 4.05±0.05 до 6.09±0.05. Ионный состав исследуемых растворов представлен ионами NovH+, LidH+, Н3O+ и Сl-.
Анализ проводили следующим образом. Для оценки времени установления квазиравновесия и дрейфа потенциала Доннана определяли одновременно ЭДС цепей вида (1) для восьми образцов мембран, погруженных модифицированными концами в исследуемый раствор (1,0⋅10-3 М NovHCl+l,0⋅10-3 M LidHCl), в течение 1-1.5 ч. Временем установления квазиравновесия считали время, за которое ЭДС цепи достигала постоянного значения (изменялось незначимо). Дрейф потенциала Доннана рассчитывали как изменение ЭДС цепи после установления квазиравновесия в единицу времени. Для оценки чувствительности потенциала Доннана к ионам NovH+, LidH+ и Н3O+, совместно присутствующим в водных растворах, определяли его величину одновременно для восьми образцов мембран и величину отклика стеклянного электрода в растворах NovHCl+LidHCl с различным соотношением концентраций компонентов. Время одного измерения составляло 12 мин (время установления квазиравновесия). Дублирование эксперимента составляло 6-8 раз. На основании полученных данных методом многомерной регрессии рассчитывали градуировочные зависимости потенциала Доннана от концентрации ионов NovH+, LidH+ и Н3О+ в водных растворах:
где ΔϕD (мВ) - потенциал Доннана на границе мембрана/исследуемый раствор; pNovH и pLidH - отрицательные логарифмы концентрации NovH+ и LidH+ в растворе; b0 (мВ) - свободный член градуировочного уравнения; b1 (мВ/рС), b2 (мВ/рС), b3 (мВ/рН) - коэффициенты чувствительности потенциала Доннана к ионам NovH+, LidH+ и Н3O+ соответственно.
Хронопотенциометрически определено, что время установления квазиравновесия и дрейф потенциала Доннана для экструзионных мембран ниже, чем для мембран, полученных отливкой (фигура 2). Кроме того, наблюдалось влияние размера и концентрации привитых групп на стабильность потенциала: среди мембран, полученных отливкой, наибольшая стабильность потенциала получена для образца МФ-4СК+3 мас. % SiO2 (10 мол. % R1) (фигура 2).
Согласно данным, представленным на фигуре 3, введение в мембраны допантов, обладающих протоноакцепторными свойствами, приводит к сохранению высокой чувствительности потенциала Доннана к ионам LidH+, NovH+ и понижению чувствительности к Н3О+. Наибольшая чувствительность потенциала Доннана к NovH+ и LidH+ по сравнению с таковой к Н3O+ получена для образцов Nafion+2.4 мас. % ZrO2, Nafion+2.8 мас. % ZrO2, МФ-4СК+3 мас. % SiO2 (5 мол. % R1), МФ-4СК+3 мас. % SiO2 (10 мол. % R1) (фигура 3). Для всех пленок, полученных экструзией, чувствительность потенциала Доннана к NovH+ выше, чем к LidH+, а для пленок, полученных отливкой - наоборот (фигура 3).
ПРИМЕР 2
Потенциал Доннана может быть аналитическим сигналом для определения ионов в водных растворах. При этом одновременная оценка потенциала Доннана для нескольких мембран, погруженных в многокомпонентый раствор, позволяет выполнять совместное определение ионов в нем подобно мультисенсорной системе.
На основании результатов исследования электродноактивных свойств гибридных мембран были выбраны три пары образцов, обеспечивающие высокую чувствительность к ионам NovH+ и LidH+, низкую чувствительность к мешающим их определению ионам Н3О+ и наименьшую корреляцию между величинами потенциала (корреляцию между значениями потенциала Доннана для пар мембран оценивали по r-критерию Пирсона):
1) Nafion+2.4 мас. % ZrO2 и Nafion+2.8 мас. % ZrO2;
2) МФ-4СК+3 мас. % SiO2 (5 мол. % R1) и МФ-4СК+3 мас. % SiO2 (10 мол. % R1);
3) Nafion+2.4 мас. % ZrO2 и МФ-4СК+3 мас. % SiO2 (10 мол. % R1).
Для каждой мембраны были получены градуировочные зависимости потенциала Доннана от концентрации ионов NovH+, LidH+ и Н3O+ в растворах NovHCl+LidHCl с концентрациями электролитов от 1.1⋅10-4 до 1.0⋅10-2 М (фигура 3):
Анализ проводили следующим образом. Определяли величину потенциала Доннана одновременно для шести выбранных образцов мембран и величину отклика стеклянного электрода в исследуемом растворе NovHCl+LidHCl с заданными концентрациями компонентов (Свв). Время одного измерения составляло 12 мин (время установления квазиравновесия). Дублирование эксперимента составляло 3-5 раз. На основании полученных данных с помощью систем градуировочных уравнений для каждой пары мембран рассчитывали концентрации компонентов в исследуемом растворе (фигура 4). Правильность результатов характеризовали относительной погрешностью концентрации , а воспроизводимость - относительным стандартным отклонением (sr) определения среднего значения концентрации (фигура 5).
Согласно данным, представленным на фигурах 4 и 5, наибольшая точность совместного определения NovH+ и LidH+ получена при использовании пары мембран Nafion+2.4 мас. % ZrO2 и МФ-4СК+3 мас. % SiO2 (10 мол. % R1).
Источники информации
1. Патент 2364859 РФ. Способ определения доннановского потенциала / Бобрешова О.В., Кулинцов П.И., Агупова М.В., Паршина А.В., заявитель и патентообладатель Ворон. гос. ун-т.- №2008115703; заявл. 21.04.08, опубл. 20.08.09; бюл. №23, 8 с.
2. Заболоцкий В.И. Перенос ионов в мембранах / В.И. Заболоцкий, В.В. Никоненко. - М.: Наука, 1996. - 395 с.
Способ одновременной оценки потенциала Доннана в восьми электромембранных системах, заключающийся в измерении ЭДС восьми электрохимических цепей с помощью девятисекционной ячейки из непроводящего материала, в которой каждая из восьми ионообменных мембран одним концом погружена в центральный корпус с исследуемым раствором, а другим концом - в одну из восьми секций с раствором сравнения, измерение откликов восьми хлоридсеребряных электродов, погруженных в секции с раствором сравнения, осуществляется одновременно относительно хлоридсеребряного электрода, погруженного в корпус с исследуемым раствором, с помощью многоканального потенциометра, при этом каждая из восьми электрохимических цепей замыкается вдоль мембраны и диффузия в мембранах является бесконечно медленной относительно времени эксперимента.