Новое производное оксазолидинона и включающая его фармацевтическая композиция
Иллюстрации
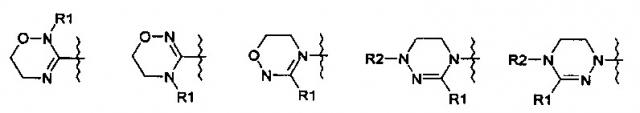
Показать всеИзобретение относится к производному оксазолидинона, представленному формулой (1), где R означает гетероциклическую группу, выбираемую из следующих групп, представленных формулой (1а), R1 означает водород, C1-С6-алкил или С3-С6-циклоалкил; R2 означает водород, C1-С6-алкил, -СН2-СН=СН2, -СН2-С≡СН, -С(O)СН(ОН)СН2ОН, -СН2-С(О)ОС2Н5, -СН2СН2ОН, -СН2С(O)ОН, -СН2С(O)ОС(СН3)3, -С(O)СН2ОН, -С(O)СН2ОС(O)СН3, или (СН2)mC(=O)R21, где R21 означает водород, (СН2)nNHR211, где R211 означает водород или C1-С6 алкил, или СН(ОН)СН2ОН, и m и n, каждый, независимо означают целое число от 0 до 3; и Q означает OR3, NHR3 или 1,2,3-триазол, где R3 означает водород, C1-С6-алкил, -C(=O)R31 или гетероароматическую циклическую группу, выбираемую из изоксазол-3-ила или изоксазол-5-ила, R31 означает водород, C1-С6-алкил, С3-С6-циклоалкил или О-(C1-С6)алкил. Изобретение также относится к пролекарству оксазолидинона, представленному соединением, выбираемым из соединений формул (5)-(7), где Q означает те же заместители, которые указаны для соединения формулы (1), и М+ представляет собой ион щелочного металла, такой как Na+ или K+, или ион аммония. Соединения по изобретению также относятся к конкретным производным оксазолидинона, приведенным в формуле изобретения. Соединения по изобретению предназначены для изготовления фармацевтической композиции для антибиотика, включающей (а) терапевтически эффективное количество производного оксазолидинона и (b) фармацевтически приемлемый носитель, разбавитель, эксципиент или их комбинацию. Технический результат – производные оксазолидинона, обладающие активностью антибиотика. 4 н. и 2 з.п. ф-лы, 1 табл., 113 пр.
, (1а),
, ,
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому производному оксазолидинона. Более конкретно, настоящее изобретение относится к новому производному оксазолидинона, имеющему циклическую амидоксимную или циклическую амидразоновую группу. Кроме того, настоящее изобретение относится к фармацевтической композиции, обладающей активностью антибиотика, которая включает, в качестве активного ингредиента, производное оксазолидинона, его пролекарство, его гидрат, его сольват, его изомер или его фармацевтически приемлемую соль.
Предпосылки создания изобретения
С тех пор как о линезолиде, который является оксазолидиноновым антибиотиком, впервые было сообщено в 1984 г. (см. Публикацию Европейского Патента №127902), о множестве производных оксазолидинона сообщалось различными фармацевтическими фирмами. Однако, лекарственные средства, во время разработки, не обладают превосходящими свойствами перед линезолидом (название продукта: Zyvox) с точки зрения токсичности и эффективности. Вследствие таких проблем линезолид еще привлекает внимание в качестве наилучшей альтернативы ванкомицину при лечении заболеваний, вызванных метициллин резистентным staphylococcus aureus (MRSA). Если резистентные к линезолиду бактерии, о которых недавно сообщалось, продолжают распространяться, возникнут очень серьезные проблемы, то есть, отсутствие лечения заболеваний, вызванных резистентными к линезолиду бактериями.
По этой причине существует очень срочная необходимость в создании лекарственных средств, обладающих превосходящими свойствами перед линезолидом с точки зрения эффектов или токсичности и проявляющих эффективность против резистентных к линезолиду бактерий. В заявке на патент Кореи №10-2008-0093712, зарегистрированной авторами настоящего изобретения 24 сентября 2008 г., раскрывается, что оксазолидиноновый антибиотик, имеющий циклическую амидразоновую или циклическую амидоксимную группу, обладает превосходящими свойствами перед линезолидом с точки зрения эффективности и токсичности и оксазолидиноновый антибиотик имеет многие преимущества за счет введения циклической амидразоновой группы.
В частности, циклическая амидразоновая группа является слабо основной и, таким образом, образует соль. Когда циклическая амидразоновая группа образует гидрохлорид, гидрохлорид имеет кислотность, подобную уксусной кислоте, то есть, рКа составляет около 5. Вследствие такой слабой кислотности, антибактериальные эффекты не ухудшаются, и растворимость гидрохлорида в воде может быть значительно увеличена.
Однако, оксазолидиноновый антибиотик, раскрытый в вышеуказанной заявке на патент, также обладает незначительным воздействием на резистентные к линезолиду бактерии и, таким образом, не может быть использован для эффективного лечения инфекций из-за резистентных к линезолиду бактерий при данных обстоятельствах, что бактерии продолжают распространяться.
Техническая проблема
Как результат ряда обширных и интенсивных исследований и экспериментов для решения проблем, как описано выше, авторы настоящего изобретения обнаружили, что, как описано ниже, новые производные оксазолидинона, представленные нижеприводимой формулой (1), в частности, новые производные оксазолидинона, имеющие циклическую амидоксимную или циклическую амидразоновую группу, оказывают превосходное воздействие на резистентные к линезолиду бактерии, обладают более высокой антибактериальной активностью, чем обычные антибиотики, и имеют высокую растворимость, что дает возможность производным оксазолидинона быть легко переработаны в пероральные и инъецируемые лекарственные средства, таким образом, завершая настоящее изобретение, базирующееся на данном раскрытии.
В частности, настоящее изобретение относится к соединению, представленному нижеприводимой формулой (1).
Настоящее изобретение также относится к пролекарству соединения, сольвату соединения, изомеру соединения или фармацевтически приемлемой соли соединения.
Настоящее изобретение также относится к фармацевтической композиции, включающей соединение, и способу лечения антибиотиком, используя эффективное количество соединения.
Техническое решение
В соответствии с одним аспектом настоящего изобретения, оно относится к новому производному оксазолидинона, представленному нижеприводимой формулой (1), в частности, к новому производному оксазолидинона, имеющему циклическую амидоксимную или циклическую амидразоновую группу. Кроме того, настоящее изобретение также относится к новому производному оксазолидинона, представленному нижеприводимой формулой (1), его пролекарству, его гидрату, его сольвату, его изомеру и его фармацевтически приемлемой соли:
где
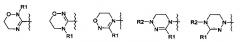
R означает гетероциклическую группу, выбираемую из следующих групп:
R1 означает водород, C1-С6-алкил или С3-С6-циклоалкил;
R2 означает водород, C1-С6-алкил или (СН2)mC(=O)R21, где R21 означает водород, (СН2)nNHR211, где R211 означает водород или C1-С6-алкил, CH2OH или СН(ОН)СН2ОН, и m и n, каждый, независимо означают целое число от 0 до 3; и
Q означает OR3, NHR3 или где R3 означает водород, C1-С6-алкил, -C(=O)R31, где R31 означает водород, C1-С6-алкил, С3-С6-циклоалкил или О-(C1-С6)-алкил или гетероароматическую циклическую группу, выбираемую из следующих групп:
Соединение представляет собой новое соединение, химическую структуру которого редко исследовали. Так, за счет введения циклической амидоксимной или циклической амидразоновой группы в оксазолидиноновый антибиотик, может быть значительно улучшена абсорбционная способность и может быть значительно увеличена растворимость соединения в воде, так как циклическая амидоксимная или циклическая амидразоновая группа обладает подходящей основностью и, таким образом, образует соль. Вследствие увеличения растворимости в воде соединение может быть получено в форме, пригодной для инъекции, без получения пролекарственной формы, и соединение имеет незначительную токсичность.
Производное оксазолидинона проявляет антибактериальную способность в отношении грамположительных бактерий, как например Staphylococcus aureus, Enterococcus faecalis и т.п., и грамотрицательных бактерий, как например Haemophilus influenza, Moraxella catarrhalis и т.п., которые резистентны к существующим антибиотикам, при гораздо более низкой концентрации, чем коммерчески доступный линезолид. В особенности, производное оксазолидинона обладает превосходной антибактериальной способностью против резистентной к линезолиду Enterococcus faecium.
Термин «алкил», как используется в данном контексте, включает линейные или разветвленные структуры. Например, C1-С6-алкил включает все возможные изомеры положения и геометрические изомеры, как например, метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, гексил и т.п.
Термин «С3-С6-циклоалкил» включает все изомеры положения циклического типа и геометрические изомеры, как например циклопропил, циклобутил, циклопентил, циклогексил, циклопропилметил и т.п.
Предпочтительно, производное оксазолидинона формулы (1) может представлять собой соединение, соответствующее соединению, выбираемому из соединений формул (2)-(4):
где R2 и Q имеют такие же значения, как указано выше, что касается формулы (1).
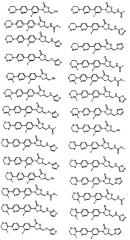
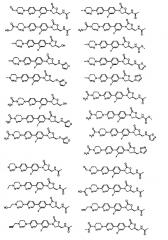
Производное оксазолидинона согласно настоящему изобретению может представлять собой одно из следующих соединений, но не исчерпывающим образом:
Производное оксазолидинона согласно настоящему изобретению может быть получено в виде пролекарства, гидрата, сольвата, изомера или фармацевтически приемлемой соли для усиления биодоступности или растворимости. Таким образом, пролекарство, гидрат, сольват, изомер и фармацевтически приемлемая соль производного оксазолидинона также входят в рамки настоящего изобретения.
В дальнейшем должны быть кратко описаны термины, как используемые в данном контексте.
Термин «фармацевтически приемлемая соль» относится к составам соединения, которые не вызывают тяжелого раздражения в организме, в который введено соединение, и не ухудшают биологической активности и физических свойств соединения. Термины «гидрат», «сольват», «изомер» и «пролекарство» также имеют значения такие же, как указано выше. Фармацевтически приемлемые соли включают фармацевтически приемлемые, содержащие анион, нетоксичные аддитивные соли, образуемые с кислотами, например, с неорганическими кислотами, как например хлороводородная (соляная) кислота, серная кислота, азотная кислота, фосфорная кислота, бромоводородная кислота, иодоводородная кислота и т.п., с органическими кислотами, как например винная кислота, муравьиная кислота, лимонная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, глюконовая кислота, бензойная кислота, молочная кислота, фумаровая кислота, малеиновая кислота, салициловая кислота, и т.п., и с сульфоновыми кислотами, как например метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота и т.п. Примеры фармацевтически приемлемых солей карбоновых кислот включают соли (щелочных) металлов или соли щелочноземельных металлов лития, натрия, калия, кальция, магния и т.п., соли аминокислот, как например лизин, аргинин, гуанидин и т.п., и органические соли, как например дициклогексиламин, N-метил-D-глюкамин, трис(гидроксиметил)-метиламин, диэтаноламин, холин, триэтиламин и т.п. Соединение формулы (1) может быть превращено в соль, используя обычный способ.
Термин «гидрат» относится к соединению или его соли согласно настоящему изобретению, которое(которая) содержит стехиометрические или нестехиометрические количества воды, связанной с ним(ней) за счет нековалентной межмолекулярной силы.
Термин «сольват» относится к соединению или его соли согласно настоящему изобретению, которое(которая) содержит стехиометрические или нестехиометрические количества растворителя, связанного с ним(ней) за счет нековалентной межмолекулярной силы. В этом отношении, предпочтительными растворителями могут быть летучие растворители, нетоксичные растворители и/или растворители, подходящие для введения людям.
Термин «изомеры» относится к соединениям или их солям согласно настоящему изобретению, которые имеют одну и ту же химическую или молекулярную формулу, но различные структурные формулы. Такие изомеры включают структурные изомеры, такие как таутомеры и т.п., R- или S-изомеры, имеющие асимметрический углеродный центр, и стереоизомеры, такие как геометрические изомеры (транс-, цис-) и т.п. Все изомеры и их смеси также входят в рамки настоящего изобретения.
Термин «пролекарство» относится к агенту, который in vivo превращается в исходное лекарственное вещество. В некоторых случаях пролекарства часто используют из-за более легкого введения, чем исходные лекарственные вещества. Например, пролекарства обладают биодоступностью, при введении перорально, тогда как исходные лекарственные вещества могут не обладать биодоступностью. Кроме того, пролекарство может обладать улучшенной растворимостью в случае фармацевтической композиции по сравнению с исходным лекарственным веществом. Например, пролекарство может представлять собой in vivo гидролизуемый сложный эфир соединения согласно настоящему изобретению или его фармацевтически приемлемую соль. Кроме того, пролекарство может быть короткоцепочечным пептидом (полиаминокислота) со связанным с ним кислотным радикалом, который метаболизируется, так, что пептид открывает активный сайт.
Другие термины, которые используются в данном контексте, могут быть интерпретированы как обычно понимаемые в области, к которой имеет отношение настоящее изобретение.
В уровне техники известны различные типы пролекарств, и не являющиеся исчерпывающими примеры цитируемых ссылок включают:
a) Desin of Prodrugs, под ред. H. Bundgaard (Elsevier, 1985) и Methods in Enzymology, том 42, cc. 309-396, под ред. K. Widder и др. (Academic press, 1985);
b) A Textbook of Drug Design and Development, под ред. Krogsgaard-Larsen и H. Bundgaard, глава 5 «Design and Application of Prodrugs», H. Bundgaard, cc. 113-191 (1991);
c) H. Bundgaard, Advanced Drug Delivery Reviews, 8, 1-38 (1992);
d) H. Bundgaard и др., Journal of Pharmaceutical Sciences, 77, 285 (1988); и
e) N. Kakeya и др., Chem. Pharm. Bull., 32, 692 (1984).
Например, пролекарство согласно настоящему изобретению может представлять собой одно из следующих соединений:
или представлять собой соединение, выбираемое из соединений формул (5)-(7):
где Q означает OR3, NHR3 или где R3 означает водород, C1-С6-алкил, -C(=O)R31, или гетероароматическую циклическую группу, выбираемую из следующих групп:
где R31 означает водород, C1-С6-алкил, С3-С6-циклоалкил или O-(C1-С6)алкил; и М+ представляет собой ион щелочного металла, такой как Na+ или K+, или ион аммония.
Более предпочтительно, производное оксазолидинона формулы (1) может представлять собой соединение вышеприведенной формулы (2), (3) или (4), где Q означает NHC(=O)CH3, NHC(=O)OCH3, или и R2 означает метил, С(=O)CH2OH, C(=O)CH2NH2 или С(=O)СН(ОН)CH2OH.
Как проиллюстрировано в предшествующих примерах, фосфонатная или ацетильная группа может быть присоединена по гидроксильной группе, так что пролекарство после введения превращается в активный метаболит. Согласно другому воплощению, может быть присоединена аминокислота или может быть использован способ получения в карбонатной форме. Такое пролекарство главным образом используют тогда, когда растворимость является относительно низкой или абсорбционная способность является низкой. Использование пролекарств может приводить к улучшению абсорбции, распределения, метаболизма и экскрекции (ADME) и профиля PK, в дополнение, к повышению растворимости и абсорбционной способности.
Соединение согласно настоящему изобретению имеет хиральный центр в положении С-5 оксазолидинонового цикла. Предпочтительный диастереоизомер производного оксазолидинона согласно настоящему изобретению представлен формулой (1), приведенной выше, и, по сравнению с эпимером, представленным формулой (1b), приводимой ниже, диастереоизомер проявляет превосходное действие.
Когда используют смесь эпимеров относительно формы хирального центра оксазолидинона, количество используемой смеси может быть установлено принимая во внимание доли диастереоизомеров в целях достижения такого же фармацевтического эффекта, как когда используют один зеркальный изомер.
Соединение формулы (1) или его соль может быть таутомеризовано(на) и, таким образом, хотя химические формулы или реакционные схемы, как используемые согласно данному контексту, представляют только один возможный таутомер, настоящее изобретение не ограничено одним таутомером, представленным химическими формулами или реакционными схемами, и произвольные таутомерные формы, обладающие антибактериальной активностью, также входят в объем настоящего изобретения.
Кроме того, соединение согласно настоящему изобретению может проявлять полиморфизм и, таким образом, все полиморфные соединения, обладающие антибактериальной активностью, также входят в объем настоящего изобретения.
Новое производное оксазолидинона согласно настоящему изобретению может быть получено, используя различные известные способы в зависимости от его заместителей. Например, производное оксазолидинона может быть получено, используя один из способов, проиллюстрированных на нижеприводимых реакционных схемах. Способы получения, представленные на нижеприводимых реакционных схемах, предусмотрены только для иллюстративных целей и ясно, что способы получения могут быть легко изменены квалифицированным специалистом в данной области в соответствии с конкретными заместителями. Таким образом, способ получения производного оксазолидинона согласно настоящему изобретению не ограничивается способами получения, проиллюстрированными на нижеприводимых реакционных схемах. В дополнение, если не указано иным образом, определение заместителей на нижеприводимых реакционных схемах является таким же, как указано в случае вышеприведенной формулы (1).
Получение производных оксазолидинона формулы (1) представлено на нижеприводимой реакционной схеме 1:
Реакционная схема 1
Как проиллюстрировано на вышеприведенной реакционной схеме 1, соединение формулы (1) синтезируют посредством реакции связывания между бромпиридиновой частью, имеющей циклическую амидоксимную или циклическую амидразоновую группу, то есть, частью А, и частью В, имеющей оксазолидиноновую группу. После реакции связывания, добавляют различные производные по отношению к сайту R' для превращения группы R' в группу R и группу Y превращают в группу Q за счет реакции У с различными производными, таким образом, завершая синтез соединения формулы (1). В дополнение, такая же группа, как Q, указанная в вышеприведенной формуле (1), может быть введена в сайт Y и Y может быть выбран из различных промежуточных реакционных групп, включая Q. Подобным образом, R' также может быть выбран из различных промежуточных реакционных групп, включая группу R, указанную в вышеприведенной формуле (1).
Сначала, бромпиридиновые производные, каждое, имеющее циклическую амидразоновую группу, согласно части А реакционной схемы 1, могут быть синтезированы согласно нижеприводимой реакционной схеме 2.
Реакционная схема 2
Как представлено на реакционной схеме 2, соединение I синтезируют путем введения во взаимодействие 2-амино-5-бромпиридина с (Вос)2O и соединение II синтезируют путем введения во взаимодействие соединения I с аллилбромидом. Соединение II превращают в альдегид III, используя OsO4 и NaIO4, и затем подвергают реакции с BocNHNH2, получая соединение IV. Синтезированное соединение IV обрабатывают кислотой с получением соединения V и затем подвергают реакции со сложным ортоэфиром, получая соединение A-I.
Однако способ согласно реакционной схеме 2 включает использование OsO4, который является относительно дорогостоящим и является очень токсичным, и, таким образом, может быть предложен другой способ, согласно которому не используют OsO4, и который осуществляют в соответствии с нижеприводимой реакционной схемой 3.
Реакционная схема 3
Как представлено на реакционной схеме 3, этаноламин подвергают реакции с Cbz-Cl и затем окисляют с помощью SO3-Py, получая альдегид, и альдегид подвергают реакции с BocNHNH2 для синтеза соединения VII. Затем соединение VII подвергают реакции с pmb-Cl для синтеза соединения VIII и Cbz-группу удаляют из полученного соединения с помощью Pd/C в присутствии водорода и подвергают реакции с дибромпиридином, получая соединение IX. После этого соединение IX обрабатывают соляной кислотой, получая соединение X, и полученное соединение X подвергают реакции со сложным ортоэфиром для синтеза соединения A-II.
Соединение, местоположение амина в котором отличается от такового циклического амидразона, синтезируют согласно нижеприводимой реакционной схеме 4.
Реакционная схема 4
Boc-группу присоединяют к соединению IX, полученному путем введения во взаимодействие дибромпиридина с этилендиамином, получая соединение XII. Соединение XII подвергают аминированию с помощью NaNO2 и Zn, обработанного кислотой, и затем подвергают реакции со сложным ортоэфиром, получая соединение А-III. В качестве другого способа, синтез производного, имеющего введенную в него алкильную группу, осуществляют таким образом, что соединение XII подвергают алкилированию, получая соединение XV, имеющее введенную в него алкильную группу, и затем подвергают аминированию и циклизации с помощью сложного ортоэфира, синтезируя соединение А-IV, имеющее введенную в него алкильную группу.
Способы синтеза бромпиридинов, каждого, имеющих циклическую амидоксимную группу, представлены на нижеприводимой реакционной схеме 5.
Реакционная схема 5
Сначала синтезируют соединение XVII путем введения во взаимодействие дибромпиридина с этаноламином и затем путем осуществления реакции Mitsunobu с гидроксифталимидом, получая соединение XVIII, из него удаляют фталимидную группу при использовании гидразина и после этого полученное в результате соединение подвергают циклизации с помощью сложного ортоэфира, получая соединение A-V.
Способ синтеза производного бромпиридина, имеющего другой тип циклической амидоксимной группы, представлен на реакционной схеме 6.
Реакционная схема 6
Соединение XX получают путем введения во взаимодействие N-алкилэтаноламина с Boc2O и затем путем осуществления реакции Mitsunobu с гидроксифталимидом, полученное в результате соединение обрабатывают соляной кислотой для удаления Boc-группы и фтал-имидную группу удаляют из него при использовании гидразина, получая соединение XXI, в которое введена алкильная группа R1. Кроме того, в качестве способа введения алкильной группы R1 позже, сначала соединение XXII может быть получено из этаноламина посредством реакции Mitsunobu и затем может быть обработано соляной кислотой, получая соединение XXIII, соединение XXIII может быть подвергнуто реакции с альдегидом, получая соединение XXIV, в которое введена алкильная группа R1, и затем фталимидная группа может быть удалена из соединения XXIV при использовании гидразина, получая соединение XXI.
Кроме того, в качестве способов синтеза других соединений, местоположение R1 в которых является отличным от местоположения в вышеуказанном соединении, сначала из соединения XXII удаляют фталимидную группу при использовании гидразина и затем подвергают реакции с алкилальдегидом, получая соединение XXVI, в которое введена алкильная группа, и полученное в результате соединение обрабатывают соляной кислотой, получая соединение XXVII, из которого удаляют Boc-группу. Полученные соединения XXI и XXVII, каждое, подвергают реакции с цианобромпиридином XXVIII для синтеза соединений A-VI, A-VII и A-VIII. Между тем, соединения формулы (1), где R1 означает водород, можно не подвергать реакции с алкилальдегидом для получения каждого результирующего соединения.
На вышеприведенной реакционной схеме 1, способы синтеза соединений В-части, имеющих оксазолидиноновую группу, представлены на нижеприводимой реакционной схеме 7.
Реакционная схема 7
Соединение XXIX получают путем введения во взаимодействие 3-фтор-4-броманилина с Cbz-Cl и затем его вводят во взаимодействие с (R)-глицидилбутиратом для синтеза хирального соединения B-I. Спиртовую группу соединения B-I превращают в различные типы производных соединений Y, синтезируя соединения В-II, В-III, В-IV, B-V и B-VI, с последующим связыванием с А-частью, или бром-группу соединения B-I превращают в пинаколборановую группу, получая соединение B-VII, и затем подвергают связыванию, таким образом завершая синтез соединения формулы (1).
Настоящее изобретение также относится к фармацевтической композиции антибиотика, которая включает: (а) терапевтически эффективное количество нового производного оксазолидинона формулы (1), его пролекарства, его гидрата, его сольвата, его изомера или его фармацевтически приемлемой соли; и (b) фармацевтически приемлемый носитель, разбавитель, эксципиент или их комбинацию.
Термин «фармацевтическая композиция», как используемый в данном контексте, означает смесь соединения согласно настоящему изобретению и других химических компонентов, как например разбавитель или носитель. Фармацевтическая композиция облегчает введение соединения в организм. Введение соединения может быть осуществлено, используя различные способы. Примеры различных способов введения включают, но не исчерпывающим образом, пероральное введение, инъекцию, аэрозольное введение, парентеральное введение и локальное введение. Фармацевтическая композиция может быть получена через посредство реакции с кислотой, как например соляная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота или т.п.
Как используется в данном контексте, термин «терапевтически эффективное количество» означает эффективное количество активного ингредиента фармацевтической композиции для облегчения или уменьшения одного или более симптомов нарушений, подвергаемых лечению композицией, или для замедления стимулирования клинических маркеров или симптомов заболеваний, необходимых для предотвращения. Таким образом, термин «терапевтически эффективное количество» означает количество, которое обладает эффектом: (1) реверсирования скорости прогрессирования заболеваний, (2) до некоторой степени ингибирования дальнейшего прогрессирования заболеваний и/или (3) до некоторой степени ослабления (предпочтительно, устранения) одного или более связанных с заболеваниями симптомов. Терапевтически эффективное количество может быть экспериментально определено путем испытания соединения на известной in vivo и in vitro модельной системе для заболеваний, нуждающихся в лечении.
Термин «носитель» определяют как соединение, которое облегчает доставку соединения в клетки или ткани. Например, диметилсульфоксид (ДМСО) представляет собой обычно используемый носитель, который облегчает введение многих органических соединений в клетки или ткани организма.
Термин «разбавитель» определяют как соединение, которое стабилизирует биологически активную форму соединения-мишени и разводится в воде, используемой для растворения соединения. Соли, растворенные в буферных растворах, используют в качестве разбавителей в уровне техники. Обычно используемым буферным раствором является забуференный фосфатом солевой раствор, так как он обладает подобной соленостью человеческому организму. Буферные соли могут регулировать значение pH раствора при низких концентрациях и, таким образом, забуференный разбавитель редко модифицирует биологическую активность соединения.
Используемое соединение может быть введено пациенту индивидуально или может быть введено пациенту в виде фармацевтической композиции, получаемой путем смешивания соединения с другими активными ингредиентами или с соответствующим носителем или эксципиентом, как в случае комбинированной терапии. Способы получения готовой лекарственной формы и введения соединения согласно настоящей заявке можно найти в «Remington's Pharmaceutical Sciences», Mack Publishing Co, Easton, PA, восемнадцатое издание, 1990.
Фармацевтическая композиция согласно настоящему изобретению может быть получена известным образом посредством способов, как например обычное смешивание, растворение, грануляция, дражирование, растирание в порошок, эмульгирование, инкапсуляция, улавливание или лиофилизация.
Таким образом, фармацевтические композиции для применения согласно настоящему изобретению могут быть получены обычным образом, используя один или более фармацевтически приемлемых носителей, включая эксципиенты или вспомогательные агенты, которые облегчают обработку активных соединений до готовых лекарственных форм для фармацевтического применения. Подходящая готовая лекарственная форма зависит от выбранного пути введения. Любые подходящие хорошо известные способы, носители и эксципиенты могут быть использованы, как подразумеваемые в уровне техники, например, согласно указанному выше руководству «Remingston's Pharmaceutical Sciences». Соединение формулы (1) согласно настоящему изобретению может быть использовано для получения готовой лекарственной формы для инъекции, перорального введения или т.п. в соответствии с предназначенным применением.
Для инъекции, композиция согласно настоящему изобретению может быть получена в виде водного раствора, предпочтительно, физиологически приемлемого буфера, как, например, раствор Хэнкса, раствор Рингера или физиологический солевой буфер. Для трансмукозального введения, в композиции используют неинвазивные агенты, пригодные для барьера, через который проходит композиция. Такие неинвазивные агенты обычно известны в уровне техники.
Для перорального введения, соединения могут быть использованы для получения композиции путем комбинирования активных соединений с фармацевтически приемлемыми носителями, известными в уровне техники. Такие носители дают возможность использования соединений согласно настоящему изобретению для получения готовых лекарственных форм в виде таблеток, пилюль, порошков, гранул, драже, капсул, жидкостей, гелей, сиропов, взвесей, суспензий, и т.п. Предпочтительными являются капсулы, таблетки, пилюли, порошки и гранулы и, в особенности, могут быть использованы капсулы и таблетки. Таблетки и пилюли могут быть получены с энтеросолюбильными покрытиями. Фармацевтические композиции для перорального использования могут быть получены путем смешивания одного или более твердых эксципиентов с одним или более соединениями согласно изобретению, необязательно измельчая полученную в результате смесь, и обработки смеси до гранул, после добавления вспомогательных агентов, если желательно, для получения таблеток или ядер драже. Подходящие эксципиенты включают, в особенности, наполнители, как например лактоза, сахароза, маннит или сорбит; вещества на основе целлюлозы, как например кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза и/или поливинилпирролидон (PVP). Если желательно, могут быть добавлены дезинтегрирующие агенты, как например сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, как например, альгинат натрия, смазочные вещества, как например стеарат магния, и носители, как например связующие вещества, и т.п.
Фармацевтические композиции, которые могут быть введены перорально, включают твердые капсулы, сделанные из желатина, а также мягкие, герметизированные капсулы, сделанные из желатина, и пластификатор, как например глицерин или сорбит. Твердые капсулы могут содержать активные ингредиенты в смеси с наполнителем, как например лактоза, связующим веществом, как например крахмал, и/или смазочным веществом, как например тальк или стеарат магния. В случае мягких капсул, активные соединения могут быть растворены или суспендированы в подходящих жидкостях, как например жировые масла, жидкий парафин или жидкий полиэтиленгликоль. В дополнение, могут быть добавлены стабилизаторы. Все готовые лекарственные формы для перорального введения должны быть в дозировках, подходящих для такого введения.
Соединения могут быть использованы для получения готовой лекарственной формы для парентерального введения путем инъекции, например, путем инъекции ударной дозы вещества или непрерывной инфузии. Композиции для инъекции могут быть предусмотрены в виде стандартной лекарственной формы, например, в ампулах или многодозовых контейнерах, с добавленным консервантом. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных средах, и могут содержать агенты для приготовления лекарственной формы, как например суспендирующие агенты, стабилизаторы и/или диспергаторы.
Кроме того, соединения могут быть в форме сухого порошка, которую используют после растворения в стерильной непирогенной воде.
Соединения могут быть использованы для получения готовой лекарственной формы в виде суппозиториев, включая обычные вещества для суппозитория, как например масло какао или другие глицериды, или в виде композиций для ректального введения, как например удерживающая клизма.
Фармацевтические композиции, подходящие для использования согласно настоящему изобретению, включают композиции, где активные ингредиенты содержатся в количестве, эффективном для достижения предназначенной им цели. Более конкретно, термин «терапевтически эффективное количество» означает количество соединения, эффективное для продления продолжительности существования субъекта, подвергаемого лечению, или для предотвращения, ослабления или уменьшения интенсивности симптомов заболеваний. Определение терапевтически эффективного количества может быть в пределах компетенции квалифицированного специалиста в данной области, в особенности, с точки зрения предусмотренного в данном контексте подробного описания.
Когда получают готовую лекарственную форму в виде стандартной лекарственной формы, фармацевтическая композиция может включать соединение формулы (1) в качестве активного ингредиента в стандартной дозе приблизительно от 0,1 мг до 1500 мг. Подходящую дозу соединения формулы (1) вводят в соответствии с предписанием докторов в зависимости от факторов, как, например, масса тела и возраст пациентов и конкретных свойств и тяжести заболеваний. Однако включенное в готовую лекарственную форму соединение может быть введено от одного до трех раз в сутки для лечения взрослых, согласно частоте и интенсивности введения, и его доза обычно находится в диапазоне от примерно 1 мг до примерно 1500 мг. Когда вводят взрослому внутримышечно или внутривенно, фармацевтическая композиция может быть введена от одного до трех раз в сутки и доза соединения обычно может составлять от примерно 1 мг до примерно 1500 мг. Для некоторых пациентов, однако, может быть использована более высокая доза.
Фармацевтическая композиция согласно настоящему изобретению может быть составлена вместе, по меньшей мере, с одним известным лекарственным средством, выбираемым из клинически пригодных антибактериальных агентов (например, β-лактам, макролид, хинолон и аминогликозид) и противовоспалительных агентов (например, противогрибковый триазол или амфотерицин), или может быть совместно введена вместе с одним или более известных лекарственных средств. Соединение согласно настоящему изобретению может быть использовано для получения готовой лекарственной формы вместе с, или совместно вводимым, повышающим бактерицидность/проницаемость белком (BPI) или ингибитором насоса оттока, для увеличения активности против грамотрицательных бактерий и антибиотика, резистентного к бактериям.
Соединение согласно настоящему изобретению может быть использовано для получения готовой лекарственной формы вместе с витаминами или может быть введено вместе с витаминами, например, витамином В2, витамином В6 или витамином В12, и фолиевой кислотой. Соединение согласно настоящему изобретению может быть использовано для получения готовой лекарственной формы вместе с ингибитором циклооксигеназы (СОХ) или может быть введено вместе с ингибитором циклоокси