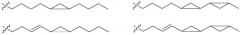Новые низкомолекулярные катионные липиды для доставки олигонуклеотидов
Иллюстрации
Показать всеНастоящее изобретение относится к новому катионному липиду по формуле А, или его любой фармацевтически приемлемой соли, которые используются для формирования липидных наночастиц (LNP) для доставки олигонуклеотидов, к композиции липидных наночастиц (LNP), содержащей предлагаемый катионный липид, и к применению катионного липида. В формуле А значения R1, R2, R3, R', Rʺ, n, L1 и L2 такие, как указаны в формуле изобретения. 7 н. и 3 з.п. ф-лы, 14 ил., 2 табл., 9 пр.
Реферат
Предпосылки к созданию изобретения
Настоящее изобретение относится к новым катионным липидам, которые могут быть использованы в комбинации с другими липидными компонентами, такими как холестерин и PEG-липиды, для формирования липидных наночастиц с олигонуклеотидами, для облегчения клеточного поглощения и эндосомального выделения и к нокдаун мРНК-мишени как in vitro, так и in vivo.
Ранее были раскрыты катионные липиды и использование катионных липидов в липидных наночастицах для доставки олигонуклеотидов, в частности, миРНК и микроРНК. Ранее были раскрыты липидные наночастицы и использование липидных наночастиц для доставки олигонуклеотидов, в частности, миРНК и микроРНК. Ранее были раскрыты олигонуклеотиды (в том числе миРНК и микроРНК) и синтез олигонуклеотидов (Смотрите патентные заявки США: US 2006/0083780, US 2006/0240554, US 2008/0020058, US 2009/0263407 и US 2009/0285881 и патентные заявки PCT: WO 2009/086558, WO 2009/127060, WO 2009/132131, WO 2010/042877, WO 2010/054384, WO 2010/054401, WO 2010/054405 и WO 2010/054406). Смотрите также Semple S.C. et al., Rational design of Cationic lipids for siRNA delivery, Nature Biotechnology, 2010, 28, 172-176.
Другие катионные липиды раскрыты в патентных заявках США: US 2009/0263407, US 2009/0285881, US 2010/0055168, US 2010/0055169, US 2010/0063135, US 2010/0076055, US 2010/0099738 и US 2010/0104629.
Общепринятые катионные липиды, такие как CLinDMA и DLinDMA, использовали для доставки миРНК в печень, но для них характерна неоптимальная эффективность доставки в пределах печени с печеночной токсичностью при более высоких дозах. Задачей данного изобретения является обеспечение каркасного катионного липида, который проявляет повышенную эффективность вместе с более низкой печеночной токсичностью в результате снижения уровней липида в печени. В настоящем изобретении используются низкомолекулярные катионные липиды с одной короткой липидной цепью для усиления эффективности и иммунности доставки in vivo миРНК.
Краткое описание изобретения
Настоящее изобретение обеспечивает новые катионные липиды, которые можно использовать в комбинации с другими липидными компонентами, такими как холестерин и PEG-липиды, для формирования липидных наночастиц с олигонуклеотидами. Задачей данного изобретения является обеспечение каркасного катионного липида, который проявляет повышенную эффективность вместе с более низкой печеночной токсичностью в результате снижения уровней липида в печени. В настоящем изобретении используются низкомолекулярные катионные липиды с одной короткой липидной цепью для усиления эффективности и иммунности доставки in vivo миРНК.
Краткое описание чертежей
Фиг.1. Эффективность LNP (соединение 1) у мышей.
Фиг.2. Эффективность LNP (соединения 32 и 33) у крыс (миРНК ApoB).
Фиг.3. Уровни катионного липида (соединения 32 и 33) в печени крыс.
Фиг.4. Эффективность LNP (соединения 32 и 33, миРНК ApoB) в NHP.
Фиг.5. Эффективность LNP (соединения 32 и 33, миРНК β-катенина) в NHP.
Фиг.6. Пиковые уровни ALT в NHP после дозы LNP (соединения 32 и 33).
Фиг.7. Уровни катионного липида (соединения 32 и 33) в печени NHP.
Фиг.8. KD миРНК β-катенина в печени у мышей TRE-Met (соединение 33).
Фиг.9. KD миРНК β-катенина опухоли у мышей TRE-Met (соединение 33).
Фиг.10. Ингибирование роста опухоли (соединение 33) у мышей TRE-met.
Фиг.11. Эффективность LNP (соединения 32 и 33) у мышей.
Фиг.12. KD миРНК β-катенина печени у мышей TRE-Met (соединение 32).
Фиг.13. KD миРНК β-катенина опухоли у мышей TRE-Met (соединение 32).
Фиг.14. Ингибирование роста опухоли (соединение 32) у мышей TRE-met.
Подробное описание изобретения
Различные аспекты и варианты осуществления данного изобретения направлены на практичность новых катионных липидов, эффективных в липидных наночастицах для доставки олигонуклеотидов, в частности, миРНК и микроРНК, к любому гену-мишени (Смотрите патентные заявки США: US 2006/0083780, US 2006/0240554, US 2008/0020058, US 2009/0263407 и US 2009/0285881, и патентные заявки PCT: WO 2009/086558, WO 2009/127060, WO 2009/132131, WO 2010/042877, WO 2010/054384, WO 2010/054401, WO 2010/054405 и WO 2010/054406). Также смотрите Semple S. C. et al., Rational design of Cationic lipids for siRNA delivery, Nature Biotechnology, 2010, 28, 172-176.
Катионные липиды по настоящему изобретению представляют собой эффективные компоненты в липидных наночастицах для доставки олигонуклеотидов, в особенности миРНК и микроРНК.
В первом варианте осуществления этого изобретения данные катионные липиды представлены формулой А:
в которой:
R1 и R2 независимо друг от друга выбраны из H, алкила (C1-C6), гетероциклила и полиамина, где указанный алкил, гетероциклил и полиамин, необязательно, являются замещенными одним-тремя заместителями, выбранными из R’, или R1 и R2 могут быть взяты совместно с азотом, к которому они присоединены для образования моноциклического гетероцикла с 4-7 членами, необязательно содержащего в себе, в дополнение к данному азоту, один или два дополнительных гетероатомов, выбранных из N, O и S, указанный моноциклический гетероцикл, необязательно, является замещенным с использованием от одного до трех заместителей, выбранных из R’;
R3 независимо выбран из H и алкила (C1-C6), указанный алкил, необязательно, является замещенным с использованием от одного до трех заместителей, выбранных из R’;
R’ независимо выбран из галогена, R", OR", SR", CN, CO2R" или CON(R")2;
R" независимо выбран из H и алкила (C1-C6), где указанный алкил, необязательно, является замещенным с использованием галогена и OH;
n равен 0, 1, 2, 3, 4 или 5;
L1 выбран из алкила C4-C24 и алкенила C4-C24, указанные алкил и алкенил, необязательно, являются замещенными с использованием от одного или нескольких заместителей, выбранных из R’; и
L2 выбран из алкила C3-C9 и акленила C3-C9, указанные алкил и алкенил, необязательно, являются замещенными с использованием одного или нескольких заместителей, выбранных из R’;
или любая фармацевтически приемлемая соль или его стереоизомер.
Во втором варианте осуществления данное изобретение описывает соединение, имеющее формулу А, где:
R1 и R2, каждый, представляет собой метил;
R3 представляет собой H;
n равен 0;
L1 выбран из алкила C4-C24 и алкенила C4-C24; и
L2 выбран из алкила C3-C9 и алкенила C3-C9;
или любая фармацевтически приемлемая соль или его стереоизомер.
В третьем варианте осуществления данное изобретение описывает соединение, имеющее формулу А, где:
R1 и R2, каждый, представляет собой метил;
R3 представляет собой H;
n равен 2;
L1 выбран из алкила C4-C24 и алкенила C4-C24; и
L2 выбран из алкила C3-C9 и алкенила C3-C9;
или любая фармацевтически приемлемая соль или его стереоизомер.
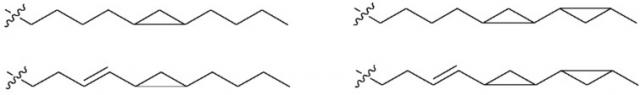
Специфические катионные липиды представляют собой:
(20Z,23Z)-N,N-диметилнонакоза-20,23-диен-10-амин (соединение 1);
(17Z,20Z)-N,N-диметилгексакоза-17,20-диен-9-амин (соединение 2);
(16Z,19Z)-N,N-диметилпентакоза-16,19-диен-8-амин (соединение 3);
(13Z,16Z)-N,N-диметилдокоза-13,16-диен-5-амин (соединение 4);
(12Z,15Z)-N,N-диметилгеникоза-12,15-диен-4-амин (соединение 5);
(14Z,17Z)-N,N-диметилтрикоза-14,17-диен-6-амин (соединение 6);
(15Z,18Z)-N,N-диметилтетракоза-15,18-диен-7-амин (соединение 7);
(18Z,21Z)-N,N-диметилгептакоза-18,21-диен-10-амин (соединение 8);
(15Z,18Z)-N,N-диметилтетракоза-15,18-диен-5-амин (соединение 9);
(14Z,17Z)-N,N-диметилтрикоза-14,17-диен-4-амин (соединение 10);
(19Z,22Z)-N,N-диметилоктакоза-19,22-диен-9-амин (соединение 11);
(18Z,21Z)-N,N-диметилгептакоза-18,21-диен-8-амин (соединение 12);
(17Z,20Z)-N,N-диметилгексакоза-17,20-диен-7-амин (соединение 13);
(16Z,19Z)-N,N-диметилпентакоза-16,19-диен-6-амин (соединение 14);
(22Z,25Z)-N,N-диметилгентриаконта-22,25-диен-10-амин (соединение 15);
(21Z,24Z)-N,N-диметилтриаконта-21,24-диен-9-амин (соединение 16);
(18Z)-N,N-диметилгептакоз-18-ен-10-амин (соединение 17);
(17Z)-N,N-диметилгексакоз-17-ен-9-амин (соединение 18);
(19Z,22Z)-N,N-диметилоктакоза-19,22-диен-7-амин (соединение 19); и
N,N-диметилгептакозан-10-амин (соединение 20);
(20Z,23Z)-N-этил-N-метилнонакоза-20,23-диен-10-амин (соединение 21);
1-[(11Z,14Z)-1-нониликоза-11,14-диен-1-ил]пирролидин (соединение 22);
(20Z)-N,N-диметилгептакоз-20-ен-10-амин (соединение 23);
(15Z)-N,N-диметилгептакоз-15-ен-10-амин (соединение 24);
(14Z)-N,N-диметилнонакоз-14-ен-10-амин (соединение 25);
(17Z)-N,N-диметилнонакоз-17-ен-10-амин (соединение 26);
(24Z)-N,N-диметилтритриаконт-24-ен-10-амин (соединение 27);
(20Z)-N,N-диметилнонакоз-20-ен-10-амин (соединение 28);
(22Z)-N,N-диметилгентриаконт-22-ен-10-амин (соединение 29);
(16Z)-N,N-диметилпентакоз-16-ен-8-амин (соединение 30);
(12Z,15Z)-N,N-диметил-2-нонилгеникоза-12,15-диен-1-амин (соединение 31);
(13Z,16Z)-N,N-диметил-3-нонилдокоза-13,16-диен-1-амин (соединение 32);
N,N-диметил-1-[(1S,2R)-2-октилциклопропил]гептадекан-8-амин (соединение 33);
1-[(1S,2R)-2-гексилциклопропил]-N,N-диметилнонадекан-10-амин (соединение 34);
N,N-диметил-1-[(1S,2R)-2-октилциклопропил]нонадекан-10-амин (соединение 35);
N,N-диметил-21-[(1S,2R)-2-октилциклопропил]геникозан-10-амин (соединение 36);
N,N-диметил-1-[(1S,2S)-2-{[(1R,2R)-2-пентилциклопропил]метил}циклопропил]нонадекан-10-амин (соединение 37);
N,N-диметил-1-[(1S,2R)-2-октилциклопропил]гексадекан-8-амин (соединение 38);
N,N-диметил-1-[(1R,2S)-2-ундецилциклопропил]тетрадекан-5-амин (соединение 39);
N,N-диметил-3-{7-[(1S,2R)-2-октилциклопропил]гептил}додекан-1-амин (соединение 40)
1-[(1R,2S)-2-гептилциклопропил]-N,N-диметилоктадекан-9-амин (соединение 41);
1-[(1S,2R)-2-децилциклопропил]-N,N-диметилпентадекан-6-амин (соединение 42);
N,N-диметил-1-[(1S,2R)-2-октилциклопропил]пентадекан-8-амин (соединение 43); и
(11E,20Z,23Z)-N,N-диметилнонакоза-11,20,23-триен-10-амин (соединение 44);
или любая фармацевтически приемлемая соль или его стереоизомер.
В другом варианте осуществления данные раскрытые катионные липиды являются пригодными при получении липидных наночастиц.
В другом варианте осуществления данные раскрытые катионные липиды являются пригодными компонентами в липидных наночастицах для доставки олигонуклеотидов.
В другом варианте осуществления данные раскрытые катионные липиды являются пригодными компонентами в липидных наночастицах для доставки миРНК и микроРНК.
В другом варианте осуществления данные раскрытые катионные липиды являются пригодными компонентами в липидной наночастице для доставки миРНК.
Данные катионные липиды по настоящему изобретению могут иметь ассиметричные центры, хиральные оси и хиральные плоскости (как описано у E.L. Eliel and S.H. Wilen, Stereochemistry of Carbon Compoundes, John Wiley & Sons, New York, 1994, pages 1119-1190), и встречаться в виде рацематов, рацемических смесей, и в виде отдельных диастериоизомеров, со всеми возможными изомерами и их смесями, включая оптические изомеры, входящие в данное изобретение. Кроме того, раскрытые здесь катионные липиды могут присутствовать в виде таутомеров, и обе таутомерные формы предназначены для включения в диапазон данного изобретения, несмотря на то, что описана только одна таутомерная структура.
Понятно, что заместители и схемы замещения в катионных липидах по настоящему изобретению могут быть выбраны специалистом, владеющим обычными практическими навыками в данной области, для обеспечения катионных липидов, которые являются химически стабильными и которые можно без труда синтезировать с использованием технологических приемов, известных в данной области, а также и тех методов, которые описаны ниже, из легкодоступных исходных материалов. Если сам заместитель является замещенным более чем одной группой, понятно, что эти множественные группы могут присутствовать на одном и том же углероде, или на разных углеродах, при условии получения устойчивой структуры.
Понятно, что специалист, владеющий обычными практическими навыками в данной области, может включить один или несколько атомов Si в катионные липиды по настоящему изобретению для обеспечения катионных липидов, которые являются химически стабильными и которые могут быть с легкостью синтезированы с использованием технологических приемов, известных в данной области, из легкодоступных исходных материалов.
В соединениях по формуле А атомы могут проявлять свой природный изотопный состав, или один или несколько атомов могут быть искусственно обогащенными определенным изотопом, имеющим то же самое атомное число, но атомную массу или атомное число, отличные от атомной массы или атомного числа, преимущественно встречающихся в природе. Настоящее изобретение предназначено для включения в себя всех подходящих изотопных вариантов соединений по формуле А. Например, различные изотопные формы водорода (Н), в том числе протий (1Н) и дейтерий (2Н). Протий представляет собой преобладающий изотоп водорода, встречающийся в природе. Обогащение дейтерия может обеспечить некоторые терапевтические преимущества, такие как увеличение времени полужизни in vivo, или снижение потребности в дозировках, или может обеспечить соединение, пригодное в качестве стандарта для описания характеристик биологических образцов. Изотопно-обогащенные соединения по формуле А могут быть получены без проведения излишних экспериментальных работ, используя общепринятые технологические приемы, хорошо известные специалистам в данной области, или используя процессы, аналогичные описанным в схемах и примерах, применяя соответствующие изотопно-обогащенные реагенты и/или промежуточные соединения.
Используемый здесь термин «алкил» означает насыщенный алифатический углеводород с неразветвленной цепью, циклический или разветвленный, имеющий определенное число атомов углерода.
Используемый здесь термин «алкенил» означает ненасыщенный алифатический углеводород с неразветвленной цепью, циклический или разветвленный, имеющий определенное число атомов углерода, в том числе, но не ограничиваясь этим, диеновые, триеновые и тетраеновые ненасыщенные алифатические углеводороды.
Примеры циклических «алкилов» или «алкенилов» включают в себя:
.
Используемый здесь термин «гетероциклил», или «гетероцикл», относится к 4-10-членному ароматическому или неароматическому гетероциклу, содержащему в себе от 1 до 4 гетероатомов, выбранных из группы, имеющей в своем составе О, N и S, и включает в себя бициклические группы. «Гетероциклил», таким образом, включает в себя следующее: бензоимидазолил, бензофуранил, бензофуразанил, бензопиразолил, бензотриазолил, бензотиофенил, бензоксазолил, карбазолил, карболинил, циннолинил, фуранил, имидазолил, индолинил, индолил, индолазинил, индазолил, изобензофуранил, изоиндолил, изохинолил, изотиазолил, изоксазолил, нафтпиридинил, оксадиазолил, оксазолил, оксазолин, изоксазолин, оксетанил, пиранил, пиразинил, пиразолил, пиридазинил, пиридопиридинил, пиридазинил, пиридил, пиримидил, пирролил, хиназолинил, хинолил, хиноксалинил, тетрагидропиранил, тетразолил, тетразолопиридил, тиадиазолил, триазолил, тиенил, триазолил, азетидинил, 1,4-диоксанил, гексагидроазепинил, пиперазинил, пиперидинил, пирролидинил, морфолинил, тиоморфолинил, дигидробензоимидазолил, дигидробензофуранил, дигидробензотиофенил, дигидробензоксазолил, дигидрофуранил, дигидроимидазолил, дигидроиндолил, дигидроизооксазолил, дигидроизотиазолил, дигидрооксадиазолил, дигидрооксазолил, дигидропиразинил, дигидропиразолил, дигидропиридинил, дигидропиримидинил, дигидропирролил, дигидрохинолинил, дигидротетразолил, дигидротиадиазолил, дигидротриазолил, дигидротиенил, дигидротриазолил, дигидроазетидинил, метилендиоксибензоил, тетрагидрофуранил, и тетрагидротиенил, и их N-оксиды, все из которых, необязательно, являются замещенными одним-тремя заместителями, выбранными из R".
Используемый здесь термин «полиамин» означает соединения, имеющие две или более аминогрупп. Примеры включают в себя путресцин, кадаверин, спермидин и спермин.
Используемый здесь термин «галоген» означает Br, Cl, F и I.
В одном варианте осуществления формулы А, R1 и R2 независимо выбраны из H и алкила (C1-C6), где указанный алкил, необязательно, замещенный одним-тремя заместителями, выбранными из R’, или R1 и R2 могут быть взяты вместе с азотом, к которому они присоединены, для формирования моноциклического гетероцикла с 4-7 членами, необязательно содержащего в себе, в дополнение к указанному азоту, один или два гетероатома, выбранных из N, O и S, указанный моноциклический гетероцикл, необязательно, является замещенным одним-тремя заместителями, выбранными из R’.
В одном варианте осуществления формулы А, R1 и R2 независимо выбраны из H, метила, этила и пропила, где указанный метил, этил и пропил, необязательно, являются замещенными с одним-тремя заместителями, выбранными из R’, или R1 и R2 могут быть взяты вместе с азотом, к которому они присоединены, для формирования моноциклического гетероцикла с 4-7 членами, необязательно содержащего в себе, в дополнение к указанному азоту, один или два гетероатома, выбранных из N, O и S, указанный моноциклический гетероцикл, необязательно, является замещенным одним-тремя заместителями, выбранными из R’.
В одном варианте осуществления формулы А, R1 и R2 независимо выбраны из H, метила, этила и пропила.
В одном варианте осуществления формулы А, R1 и R2, каждый, представляет собой метил.
В одном варианте осуществления формулы А, R3 независимо выбран из H и метила.
В одном варианте осуществления формулы А, R3 представляет собой H.
В одном варианте осуществления формулы А, R’ представляет собой R".
В одном варианте осуществления формулы А, R" независимо выбран из H, метила, этила и пропила, где указанный метил, этил и пропил, необязательно, являются замещенными одним или несколькими галогенами и OH.
В одном варианте осуществления формулы А, R" независимо выбран из H, метила, этила и пропила.
В одном варианте осуществления формулы А, n равен 0, 1, 2 или 3.
В одном варианте осуществления формулы А, n равен 0, 1 или 2.
В одном варианте осуществления формулы А, n равен 0, 1 или 2.
В одном варианте осуществления формулы А, n равен 0.
В одном варианте осуществления формулы А, n равен 2.
В одном варианте осуществления формулы А, L1 выбран из алкила C4-C24 и алкенила C4-C24, которые, необязательно, являются замещенными галогеном и OH.
В одном варианте осуществления формулы А, L1 выбран из алкила C4-C24 и алкенила C4-C24.
В одном варианте осуществления формулы А, L1 выбран из алкенила C4-C24.
В одном варианте осуществления формулы А, L1 выбран из алкенила C12-C24.
В одном варианте осуществления формулы А, L1 представляет собой алкенил C19.
В одном варианте осуществления формулы А, L1 представляет собой:
.
В одном варианте осуществления формулы А, L1 представляет собой:
.
В одном варианте осуществления формулы А, L2 выбран из алкила C3-C9 и алкенила C3-C9, которые, необязательно, являются замещенными галогеном и OH.
В одном варианте осуществления формулы А, L2 выбран из алкила C5-C9 и алкенила C5-C9, которые, необязательно, являются замещенными галогеном и OH.
В одном варианте осуществления формулы А, L2 выбран из алкила C7-C9 и алкенила C7-C9, которые, необязательно, являются замещенными галогеном и OH.
В одном варианте осуществления формулы А, L2 выбран из алкила C3-C9 и алкенила C3-C9.
В одном варианте осуществления формулы А, L2 выбран из алкила C5-C9 и алкенила C5-C9.
В одном варианте осуществления формулы А, L2 выбран из алкила C7-C9 и алкенила C7-C9.
В одном варианте осуществления формулы А, L2 представляет собой алкил C3-C9.
В одном варианте осуществления формулы А, L2 представляет собой алкил C5-C9.
В одном варианте осуществления формулы А, L2 представляет собой алкил C7-C9.
В одном варианте осуществления формулы А, L2 представляет собой алкил C9.
В одном варианте осуществления формулы А, L1 выбран из алкила C4-C24 и акленила C4-C24, где указанные алкил и алкенил, необязательно, являются замещенными одним или несколькими заместителями, выбранными из R’; и L2 выбран из алкила C3-C9 и алкенила C3-C9, указанные алкил и алкенил, необязательно, являются замещенными одним или несколькими заместителями, выбранными из R’.
В одном варианте осуществления формулы А, L1 выбран из алкенила C12-C24, указанный алкенил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’; и L2 выбран из алкила C5-C9, указанный алкил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’.
В одном варианте осуществления формулы А, L1 выбран из алкенила C19, указанный алкенил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’; и L2 выбран из алкила C7-C9, указанный алкил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’.
В одном варианте осуществления формулы А, L1 выбран из алкенила C19, указанный алкенил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’; и L2 выбран из алкила C9, указанный алкил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’.
В одном варианте осуществления формулы А, L1 выбран из алкенила C19 с неразветвленной цепью, указанный алкенил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’; и L2 выбран из алкила C9 с неразветвленной цепью, указанный алкил, необязательно, является замещенным одним или несколькими заместителями, выбранными из R’.
В одном варианте осуществления формулы А, «гетероциклил» представляет собой пирролидин, пиперидин, морфолин, имидазол или пеперазин.
В одном варианте осуществления формулы А, «моноциклический гетероциклил» представляет собой пирролидин, пиперидин, морфолин, имидазол или пеперазин.
В одном варианте осуществления формулы А, «полиамин» представляет собой путресцин, кадаверин, спермидин или спермин.
В одном варианте осуществления «алкил» представляет собой насыщенный алифатический углеводород с неразветвленной цепью, имеющий определенное число атомов углерода.
В одном варианте осуществления «алкенил» представляет собой ненасыщенный алифатический углеводород с неразветвленной цепью, имеющий определенное число атомов углерода.
В настоящее изобретение включена свободная форма катионных липидов по формуле А, а также их фармацевтически приемлемые соли и стереоизомеры. Некоторые из приведенных здесь в качестве примеров выделенных специфических катионных липидов представляют собой протонированные соли аминовых катионных липидов. Термин «свободная форма» относится к аминовым катионным липидам в несолевой форме. Охваченные фармацевтически приемлемые соли включают в себя не только приведенные в качестве примеров выделенные соли для определенных катионных липидов, описанных здесь, но также все типичные фармацевтически приемлемые соли свободной формы катионных липидов по формуле А. Свободная форма конкретной соли описанных катионных липидов может быть выделена с использованием технологических приемов, известных в данной области. Например, свободная форма может быть восстановлена в результате обработки данной соли подходящим разбавленным водным основным раствором, таким как разбавленный водный NaOH, карбонат калия, аммиак и бикарбонат натрия. Данные свободные формы могут отличаться от их соответствующих солевых форм, в некоторой степени, некоторыми физическими свойствами, такими, как растворимость в полярных растворителях, но кислые и основные соли в остальном являются эквивалентными их соответствующим свободным формам для целей данного изобретения.
Фармацевтически приемлемые соли данных катионных липидов могут быть синтезированы из катионных липидов по этому изобретению, которые содержат в себе основные или кислотные функциональные группы, используя общепринятые химические методы. В общих чертах соли основных катионных липидов получают либо с помощью ионообменной хроматографии, или в результате реакции свободного основания со стехиометрическими количествами, или с избытком необходимой солеобразующей неорганической или органической кислоты в подходящем растворителе, или различных комбинациях растворителей. Аналогичным образом, соли кислотных соединений формируются в результате реакций с соответствующим неорганическим или органическим основанием.
Таким образом, фармацевтически приемлемые соли катионных липидов по этому изобретению включают в себя традиционные нетоксичные соли катионных липидов по этому изобретению, полученные в результате реакции основных растворимых катионных липидов с неорганической или органической кислотой. Например, традиционные нетоксичные соли включают в себя те, которые получены из неорганических кислот, таких как соляная, бромистоводородная, серная, сульфаминовая, фосфорная, азотная и тому подобное, а также соли, которые получены из органических кислот, таких как уксусная, пропионовая, янтарная, гликолевая, стеариновая, молочная, оксиянтарная, винная, лимонная, аскорбиновая, пальмитиновая, малеиновая, гидроксималеиновая, фенилуксусная, глутаминовая, бензойная, салициловая, сульфаниловая, 2-ацетоксибензойная, фумаровая, толуолсульфоновая, метансульфоновая, этандисульфоновая, щавелевая, изетионовая, трифторуксусная (TFA) и тому подобное.
В случае, когда катионные липиды по настоящему изобретению являются кислотными, подходящие «фармацевтически приемлемые соли» означают соли, полученные из фармацевтически приемлемых нетоксичных оснований, в том числе неорганических оснований и органических оснований. Соли, полученные из неорганических оснований, включают в себя соли алюминия, аммиака, кальция, меди, трехвалентного железа, двухвалентного железа, лития, магния, трехвалентного марганца, двухвалентного марганца, калия, натрия, цинка и тому подобное. Особенно предпочтительными являются соли аммиака, кальция, магния, калия и натрия. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают в себя соли первичных, вторичных и третичных аминов, циклических аминов и основных ионообменных смол, таких как аргинин, бетаин кофеин, холин, N,N1-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин трипропиламин, трометамин и тому подобное.
Получение фармацевтически приемлемых солей описано выше и другие типичные фармацевтически приемлемые соли более подробно описаны у Berg et al, "Pharmaceutical Salts," J. Pharm. Sci, 1977: 66: 1-19.
Также следует отметить, что катионные липиды по настоящему изобретению представляют собой потенциально внутренние соли или цвиттерионы, поскольку в физиологических условиях депротеинированная кислотная функциональная группа в данном Соединении, например, карбоксильная группа, может быть анионной, и этот электронный заряд должен быть компенсирован внутренне относительно катионного заряда протеинированной или алкилированной основной функциональной группы, такой как четвертичный атом азота.
ПРИМЕРЫ
Представленные примеры предназначены для содействия в дальнейшем понимании данного изобретения. Конкретные используемые вещества, образцы и условия предназначены для дополнительной иллюстрации данного изобретения и не ограничивают его разумный диапазон. Реагенты, используемые при синтезе катионных липидов, являются либо коммерчески доступными, либо без труда готовятся специалистом, который обладает обычными навыками в данной области.
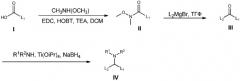
Синтез новых катионных липидов представляет собой линейный процесс, начинающийся с липидной кислоты (I). Связывание с N,О-диметил гидроксиламином приводит к образованию амида Вайнреба (Weinreb) II. Добавление реагента Гриньяра (Grignard) приводит к образованию кетона III. Опосредованное титаном восстановительное аминирование приводит к образованию конечных продуктов типа IV.
ОБЩАЯ СХЕМА 1
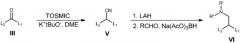
Синтез одноуглеродных допустимых катионных липидов V представляет собой линейный процесс, начинающийся с липидного кетона (III). Переход кетона в нитрил (V) осуществляется посредством обработки TOSMIC и трет-бутоксидом калия. Восстановление данного нитрила до первичного амина с последующим восстановительным аминированием обеспечивает конечные катионные липиды VI.
ОБЩАЯ СХЕМА 2
Синтез двухуглеродных допустимых катионных липидов IX представляет собой линейный процесс, начинающийся с липидного кетона (III). Переход данного кетона в α,β-ненасыщенный амид VII осуществляется в условиях реакции Петерсона. Сопряженное восстановление α,β-ненасыщенности осуществляется с использованием LS-Selectride для образования амида VIII. Восстановление данного амида с помощью алюмогидрида лития обеспечивает конечные катионные липида IX.
ОБЩАЯ СХЕМА 3
Циклопропил-содержащие липиды получены в соответствии с общей схемой 4. Ненасыщенные амиды Вайнреба II подвергают условиям циклопропанирования Симмонса-Смита для получения циклопропил-содержащих амидов Вайнреба X. Их доводят до конечных продуктов как показано в общих схемах 1-3.
ОБЩАЯ СХЕМА 4
Синтез аллиламиновых катионных липидов XVI представляет собой линейный процесс, начинающийся с альдегида XI. Добавление трет-бутилацетата приводит к образованию β-сложного гидроксиэфира XII. Преобразование данной гидроксильной функциональной группы во фтор-группу с последующей обработкой кислотой приводит к образованию β-фторзамещенной кислоты XIII. Преобразование данной кислоты в амид Вайнреба с последующим добавлением реагента Гриньяра приводит к образованию β-фтористого кетона XV. Восстановительное аминирование влечет за собой одновременное элиминирование для образования необходимого аллильного амина XVI.
ОБЩАЯ СХЕМА 5
20,23-нонакозадиен-10-амин, N,N-диметил-, (20Z,23Z) ( соединен ие 1)
11,14-эйкозадиеновую кислоту, (11Z,14Z)- (50 г, 162 ммоль), N,О-диметилгидроксиламин гидрохлорид (31,6 г, 324 ммоль), HOAt (44,1 г, 324 ммоль), Et3N (45,2 мл, 324 ммоль) и EDC (62,1 г, 324 ммоль) смешивали в DCM (810 мл) и перемешивали в течение ночи при температуре окружающей среды. Реакционную смесь затем отмывали 5×700 мл воды, затем отмывали 1×600 мл 1 M NaOH, высушивали с помощью сульфата натрия, фильтровали через целит и конденсировали до получения 53,06 г (93%) 11,14-эйкозадиенамида, N-метокси-N-метил-, (11Z,14Z) в виде очищенного золотистого масла. 1Н-ЯМР (400 МГц, CDCl3) δ 5,35 (м, 4H), 3,68 (с, 3H), 3,18 (с, 3H), 2,77 (м, 2H), 2,41 (т, J=7 Гц, 2H), 2,05 (м, 4H), 1,63 (м, 2H), 1,40-1,26 (м, 18H), 0,89 (т, J=7 Гц, 3H).
11,14-эйкозадиенамид, N-метокси-N-метил-, (11Z,14Z)- 1 (4 г, 11,38 ммоль) растворяли в сухом ТГФ (50,0 мл) в сосуде объемом 250 мл, затем 1 М нонилмагний бромид (22,76 мл, 22,76 ммоль) добавляли под азотом при температуре окружающей среды. Через 10 минут реакцию медленно подавляли с избытком насыщенного водного NH4Cl. Данную реакцию отмывали в делительной воронке с помощью гексана и воды, встряхивали, нижний водный слой удаляли, верхний слой высушивали с помощью сульфата натрия, фильтровали и конденсировали для получения неочищенного кетона в виде золотистого масла. К вышеуказанному неочищенному кетону добавляли диметиламин (2 M в ТГФ) (14,22 мл, 28,4 ммоль) с последующим добавлением Ti(O-i-Pr)4 (6,67 мл, 22,76 ммоль) и оставляли перемешиваться в течение ночи. На следующий день добавляли EtOH (50 мл), с последующим добавлением NaBH4 (0,646 г, 17,07 ммоль). После 5 мин перемешивания непосредственно вводили всю реакционную смесь в 40-г капиллярную кварцевую колонку, которая располагалась на одной линии с 330 г капиллярной кварцевой колонкой. Элюировали 10 мин 100% DCM, затем 30 мин 0-15% MeOH/DCM, собирали 20,23-нонакозадиен-10-амин, N,N-диметил-, (20Z,23Z) (1) (2,45 г, 5,47 ммоль, выход 48,1%) в виде бледно-золотистого масла. 1Н-ЯМР (400 МГц, CDCl3) δ 5,35 (м, 4H), 2,78 (м, 2H), 2,23 (м, 1H), 2,21 (с, 6H), 2,05 (м, 4H), 1,45-1,16 (м, 38H), 0,89 (м, 6H). HRMS рассчитано для C31H61N 448,4877, получено 448,4872.
Соединения 2-30 представляют собой новые катионные липиды и были получены в соответствии с общей схемой 1, представленной выше.
| Соединение | Структура | HRMS |
| 2 | рассчитано для C28H56N 406,4407, получено 406,4405 | |
| 3 | рассчитано для C27H54N 392,4251, получено 392,4250 | |
| 4 | рассчитано для C24H48N 350,3781, получено 350,3770 | |
| 5 | рассчитано для C23H46N 336,3625, получено 336,3613 | |
| 6 | рассчитано для C25H50N 364,3938, получено 364,3941 | |
| 7 | рассчитано для C26H52N 378,4094, получено 378,4081 | |
| 8 | рассчитано для C29H58N 420,4564, получено 420,4562 | |
| 9 | рассчитано для C26H52N 378,4094, получено 378,4089 | |
| 10 | рассчитано для C25H50N 364,3938, получено 364,3931 | |
| 11 | рассчитано для C30H60N 434,4720, получено 434,4717 | |
| 12 | рассчитано для C29H58N 420,4564, получено 420,4561 | |
| 13 | рассчитано для C28H56N 406,4407, получено 406,4404 |