Новые фосфатные соединения, способ их получения и фармацевтические композиции, содержащие их
Иллюстрации
Показать всеИзобретение относится к соединению формулы (I), его энантиомерам и фармацевтически приемлемым солям и композициям на их основе, которые могут применяться в онкологии:
где X и Y представляют собой С или N, но не могут быть одинаковыми, A1 и А2 вместе с атомами, несущими их, образуют гетероцикл Het, выбранный из 5,6,7,8-тетрагидроиндолизина или индолизина, или A1 и А2 представляют собой Н, (С1-С6)полигалогеналкил или (С1-С6)алкил, Т представляет собой Н, (С1-С6)алкил, необязательно замещенный одним-тремя атомами галогена, (C1-C4)алкил-NR1R2, или (С1-С4)алкил-OR6, R1 и R2 представляют собой Н или (С1-С6)алкил, или R1 и R2 с атомом азота, несущим их, образуют гетероциклоалкил, R3 представляет собой циклоалкил, гетероциклоалкил, арил или гетероарил, R4 представляет собой фенил, замещенный в пара-положении группой -ОРО(ОМ)(ОМ'), -ОРО(ОМ)(O-М1+), -OPO(O-M1+)(O-M2+), -ОРО(O-)(O-)М32+, -ОРО(ОМ)(O[CH2CH2O]nCH3), или -ОРО(O-М1+)(O[CH2CH2O]nCH3), где М и М' представляют собой Н, (С1-С6)алкил, (С2-С6)алкенил, (С2-С6)алкинил, циклоалкил или гетероциклоалкил из 5 или 6 членов, тогда как М1+, М2+ и М32+ представляют собой фармацевтически приемлемые катионы, n равен от 1 до 5, при этом атомы углерода предыдущих групп или их возможных заместителей могут быть дейтерированными, R5 представляет собой Н или галоген, (С1-С6)алкил или (C1-С6)алкокси, R6 представляет собой Н или (С1-С6)алкил, Ra, Rb, Rc и Rd представляет собой R7, галоген, (С1-С6)алкокси, гидрокси, NR7R7'-CO-(C0-C6)алкил-O-, или заместители пары (Rb,Rc) вместе с атомами углерода, несущими их, образуют кольцо из 5-7 членов с 1 или 2 гетероатомами, выбранными из О и S, при этом один или несколько атомов углерода кольца могут быть дейтерированными или замещенными 1-3 группами, выбранными из галогена и (С1-С6)алкила, R7 и R7' представляют собой H, (С1-С6)алкил, или R7 и R7' вместе с атомом азота, несущим их, образуют гетероцикл, состоящий из 5-7 членов, "арил" означает фенил, нафтил, бифенил или инденил, "гетероарил" означает моно- или бициклическую группу, состоящую из 5-10 членов c по меньшей мере одним ароматическим фрагментом и 1-4 гетероатомами, выбранными из O, S и N, "циклоалкил" означает моно- или бициклическую, неароматическую, карбоциклическую группу из 3-10 членов, "гетероциклоалкил" означает моно- или бициклическую, неароматическую, конденсированную или спирогруппу из 3-10 кольцевых членов с 1-3 гетероатомами, выбранными из О, S, SO, SO2 и N, причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, алкил, алкенил, алкинил и алкокси могут быть замещены посредством 1-3 групп, выбранных из (С1-С6)алкила, (С3-С6)спиро, (С1-С6)алкокси, (С1-С6)алкил-S-, гидрокси, оксо или N-оксида, нитро, циано, -COOR', -OCOR', NR'Rʺ, (С1-С6)полигалогеналкила, трифторметокси, (С1-С6)алкилсульфонила, галогена, арила, гетероарила, арилокси, арилтио, циклоалкила, гетероциклоалкила, необязательно замещенного одним или несколькими галогенами или алкилами, R' и Rʺ представляют собой Н или (C1-С6)алкил, Het группа может быть замещена 1-3 группами, выбранными из (C1-С6)алкила, гидрокси, (С1-С6)алкокси, NR1'R1ʺ и галогена, при этом R1' и R1ʺ принимают значения, определенные для групп R' и Rʺ. Предложены новые эффективные противоопухолевые агенты и эффективный способ их получения. 7 н. и 26 з.п. ф-лы, 25 пр., 11 табл.
Реферат
Настоящее изобретение относится к новым фосфатным соединениям, к способу их получения и к фармацевтическим композициям, содержащим их.
Соединения настоящего изобретения являются новыми и обладают чрезвычайно ценными фармакологическими и фармакокинетическими характеристиками для применения в области апоптоза и онкологии.
Апоптоз, или запрограммированная гибель клеток, является ключевым физиологическим процессом для эмбрионального развития и поддержания тканевого гомеостаза.
Гибель клеток по типу апоптоза вызывает морфологические изменения, такие как конденсация ядра, фрагментация ДНК, а также биохимический феномен, такой как активация каспаз, которые вызывают повреждение ключевых структурных компонентов клетки, вызывая, таким образом, ее разборку и смерть. Регуляция процесса апотоза является комплексной и задействует активацию или репрессию нескольких внутриклеточных путей передачи сигналов (Cory S. и др., Nature Review Cancer, 2002, 2, 647-656).
Дерегулирование апоптоза вовлечено в определенные патологии. Повышенный апоптоз связан с нейродегенеративными заболеваниями, такими как болезнь Паркинсона, болезнь Альцгеймера и ишемия. Наоборот, недостаточности осуществления апоптоза играют важную роль в развитии злокачественных новообразований и их резистентности к химиотерапии, при аутоиммунных заболеваниях, воспалительных заболеваниях и вирусных инфекциях. Следовательно, отсутствие апоптоза является одним из характерных фенотипических признаков злокачественного новообразования (Hanahan D. и др., Cell 2000, 100, 57-70).
Антиапоптозные белки семейства Bcl-2 связаны с многочисленными патологиями. Задействование белков семейства Bcl-2 описано для многочисленных видов злокачественных новообразований, таких как колоректальный рак, рак молочной железы, мелкоклеточный рак легкого, немелкоклеточный рак легкого, рак мочевого пузыря, рак яичников, рак предстательной железы, хронический лимфоидный лейкоз, фолликулярная лимфома, миелома, и т.д. Сверхэкспрессия антиапоптозных белков семейства Bcl-2 связана с онкогенезом, с устойчивостью к химиотерапии и с клиническим прогнозом пациентов, страдающих злокачественным новообразованием. Таким образом, существует терапевтическая потребность в соединениях, которые ингибируют антиапоптотическую активность белков семейства Bcl-2.
Помимо того, что соединения настоящего изобретения являются новыми, они обладают фармакологическими и фармакокинетическими свойствами, которые позволяют их применение при патологиях, в которые вовлечен дефект апоптоза, как, например, для лечения злокачественного новообразования, аутоиммунных заболеваний и заболеваний иммунной системы.
Более конкретно, настоящее изобретение относится к фосфатному соединению формулы (I):
в которой:
- X и Y представляют собой атом углерода или атом азота, при этом предполагается, что они не могут одновременно представлять собой два атома углерода или два атома азота,
- A1 и A2, вместе с атомами, несущими их, образуют необязательно замещенный, ароматический или неароматический гетероцикл Het, состоящий из 5, 6 или 7 кольцевых членов, который может содержать, в дополнение к азоту, представленному посредством X или Y, от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, при этом предполагается, что рассматриваемый азот может быть замещен группой, представляющей собой атом водорода, линейную или разветвленную (C1-C6) алкильную группу или группу -C(O)-O-Alk, в которой Alk означает линейную или разветвленную (C1-C6) алкильную группу,
или A1 и A2 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)полигалогеналкильную, линейную или разветвленную (C1-C6) алкильную группу или циклоалкил,
- T представляет собой атом водорода, линейную или разветвленную (C1-C6) алкильную группу, необязательно замещенную одним-тремя атомами галогена, группу (C1-C4)алкил-NR1R2, или группу (C1-C4)алкил-OR6,
- R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (C1-C6) алкильную группу,
или R1 и R2 с атомом азота, несущим их, образуют гетероциклоалкил,
- R3 представляет собой линейную или разветвленную (C1-C6) алкильную группу, линейную или разветвленную (C2-C6) алкенильную группу, линейную или разветвленную (C2-C6) алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(C1-C6) алкильную группу, где алкильный фрагмент является линейным или разветвленным, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода предыдущих групп, или их возможных заместителей, могут быть дейтерированными,
- R4 представляет собой арильную группу, гетероарильную группу, циклоалкильную группу или линейную или разветвленную (C1-C6) алкильную группу, при этом предполагается, что один или несколько атомов углерода предыдущих групп, или их возможных заместителей, могут быть дейтерированными,
- R5 представляет собой водород или атом галогена, линейную или разветвленную (C1-C6) алкильную группу, или линейную или разветвленную (C1-C6)алкокси группу,
- R6 представляет собой атом водорода или линейную или разветвленную (C1-C6) алкильную группу,
- Ra, Rb, Rc и Rd каждый независимо от других представляет собой R7, атом галогена, линейную или разветвленную (C1-C6) алкокси группу, гидрокси группу, линейную или разветвленную (C1-C6) полигалогеналкильную группу, трифторметокси группу, группу , нитро, R7-CO-(C0-C6)алкил-, R7-CO-NH-(С0-С6)алкил-, , , R7-SO2-NH-(C0-C6)алкил-, R7-NH-CO-NH-(C0-C6)алкил-, R7-O-CO-NH-(C0-C6)алкил-, гетероциклоалкильную группу, или заместители одной из пар (Ra,Rb), (Rb,Rc) или (Rc,Rd) вместе с атомами углерода, несущими их, образуют кольцо, состоящее из 5-7 кольцевых членов, которое может содержать от 1 до 2 гетероатомов, выбранных из кислорода и серы, при этом также предполагается, что один или несколько атомов углерода кольца, определенного выше, могут быть дейтерированными или замещенными 1-3 группами, выбранными из галогена и линейного или разветвленного (C1-C6)алкила,
- R7 и R7' независимо друг от друга представляют собой водород, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (С2-C6)алкенил, линейный или разветвленный (С2-C6)алкинил, арил или гетероарил, или R7 и R7' вместе с атомом азота, несущим их, образуют гетероцикл, состоящий из 5-7 кольцевых членов,
соединение формулы (I) является таким, что по меньшей мере один из атомов углерода, содержащихся в нем, замещен одной из следующих фосфатных групп: -ОРО(ОМ)(ОМ'), , , , -ОРО(ОМ)(O[CH2CH2O]nCH3), или , где М и М' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6) алкильную группу, линейную или разветвленную (С2-C6) алкенильную группу, линейную или разветвленную (С2-C6) алкинильную группу, циклоалкил или гетероциклоалкил, оба состоящие из 5 или 6 кольцевых членов, тогда как и независимо друг от друга представляют собой фармацевтически приемлемый однозарядный катион, и представляет собой фармацевтически приемлемый двухзарядный катион и n означает целое число от 1 до 5,
при этом предполагается, что:
- "арил" означает фенильную, нафтильную, бифенильную или инденильную группу,
- "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, имеющую по меньшей мере один ароматический фрагмент и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота (включая четвертичные атомы азота),
- "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов,
- "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, конденсированную или спиро группу, состоящую из 3-10 кольцевых членов и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, таким образом определенные, и группы алкил, алкенил, алкинил и алкокси могут быть замещены посредством 1-3 групп, выбранных из необязательно замещенного, линейного или разветвленного (C1-C6)алкила, (C3-C6)спиро, линейного или разветвленного, необязательно замещенного (C1-C6)алкокси, (C1-C6)алкил-S-, гидрокси, оксо (или N-оксида, в соответствующих случаях), нитро, циано, -COOR', -OCOR', NR'R", линейного или разветвленного (С1-C6)полигалогеналкила, трифторметокси, (C1-C6)алкилсульфонила, галогена, необязательно замещенного арила, гетероарила, арилокси, арилтио, циклоалкила, гетероциклоалкила, необязательно замещенного одним или несколькими атомами галогена или алкильными группами, при этом предполагается, что R' и R" независимо друг от друга представляют собой атом водорода или необязательно замещенную, линейную или разветвленную (С1-C6) алкильную группу,
причем Het группа, определенная в формуле (I), может быть замещена одной-тремя группами, выбранными из линейного или разветвленного (C1-C6)алкила, гидрокси, линейного или разветвленного (С1-C6)алкокси, и галогена, при этом предполагается, что R1' и R1'' принимают значения, определенные для групп R' и R", упомянутых выше,
к его энантиомерам и диастереоизомерам и к его солям присоединения с фармацевтически приемлемой кислотой или основанием.
Среди фармацевтически приемлемых кислот могут быть упомянуты, без какого-либо ограничения, соляная кислота, бромистоводородная кислота, серная кислота, фосфоновая кислота, уксусная кислота, трифторуксусная кислота, молочная кислота, пировиноградная кислота, малоновая кислота, янтарная кислота, глутаровая кислота, фумаровая кислота, винная кислота, малеиновая кислота, лимонная кислота, аскорбиновая кислота, щавелевая кислота, метансульфоновая кислота, камфорная кислота и т.д.
Среди фармацевтически приемлемых оснований могут быть упомянуты, без какого-либо ограничения, гидроксид натрия, гидроксид калия, триэтиламин, трет-бутиламин и т.д.
Предпочтительные соединения изобретения включают соединения формулы (I), в которой R4 представляет собой фенил, замещенный в пара-положении группой формулы -ОРО(ОМ)(ОМ'), , , , -ОРО(ОМ)(O[CH2CH2O]nCH3), или , где М и М' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-C6) алкильную группу, линейную или разветвленную (С2-C6) алкенильную группу, линейную или разветвленную (С2-C6) алкинильную группу, циклоалкил или гетероциклоалкил, оба состоящие из 5 или 6 кольцевых членов, тогда как и независимо друг от друга представляют собой фармацевтически приемлемый однозарядный катион, и представляет собой фармацевтически приемлемый двухзарядный катион и n означает целое число от 1 до 5, при этом предполагается, что фенильная группа необязательно может быть замещена одним или несколькими атомами галогенов.
Предпочтение отдают соединениям формулы (I), где R4 представляет собой фенильную или пиримидин-5-ильную группу, обе замещенные в пара-положении группой формулы , и еще более типично группой формулы -OPO(O-Na+)(O-Na+).
Предпочтительно, X представляет собой атом углерода и Y представляет собой атом азота. Еще более предпочтительно, группа:
представляет собой 5,6,7,8-тетрагидроиндолизин, индолизин или диметилированный пиррол.
Т предпочтительно представляет собой метальную, (морфолин-4-ил)метильную или 3-(морфолин-4-ил)пропильную группу.
В предпочтительных соединениях изобретения, Ra и Rd каждый представляет собой атом водорода и (Rb,Rc), вместе с атомами углерода, несущими их, образуют 1,3-диоксолановую группу или 1,4-диоксановую группу; или Ra, Rc и Rd каждый представляет собой атом водорода и Rb представляет собой водород или галоген.
В другом варианте осуществления изобретения, Ra и Rd каждый представляет собой атом водорода, Rb представляет собой атом галогена и Rc представляет собой метокси группу.
Альтернативно, Ra, Rb и Rd каждый предпочтительно представляет собой атом водорода и Rc представляет собой группу , и еще более предпочтительно Rc представляет собой 2-оксо-2-(пиперидин-1-ил)этокси группу.
Кроме того, R3 предпочтительно представляет собой группу, выбранную из фенила, 1H-индола, 1H-пирроло[2,3-6]пиридина, пиридина, 1H-пиразола, 1H-пиррола и 2,3-дигидро-1H-пирроло[2,3-b]пиридина, причем эти группы необязательно имеют один или несколько заместителей, выбранных из линейного или разветвленного (С1-C6)алкила (более предпочтительно метила), циано и тридейтерометила.
Среди предпочтительных соединений изобретения могут быть упомянуты:
-4-[{[3-(6-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}-1,3-бензодиоксол-5-ил)-5,6,7,8-тетрагидроиндолизин-1-ил]карбонил}(фенил)амино]фенил динатрийфосфат,
-4-[{[5-(5-хлор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}(пиридин-4-ил)амино]фенил динатрийфосфат,
-4-({[5-(5-хлор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}[1-(тридейтерометил)-1H-пиразол-4-ил]амино)фенил динатрийфосфат,
-4-[{[5-(5-хлор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}(5-циано-1,2-диметил-1H-пиррол-3-ил)амино]фенил динатрийфосфат,
-4-[{[5-(5-хлор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}(5-циано-1-метил-1H-пиррол-3-ил)амино]фенил динатрийфосфат,
-4-[{[5-(5-хлор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}(1-метил-1H-пиразол-4-ил)амино]фенил динатрийфосфат,
-4-[(5-циано-1,2-диметил-1H-пиррол-3-ил){[5-(5-фтор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}амино]фенил динатрийфосфат,
-4-[{[5-(5-фтор-2-{[(3S)-3-(морфолин-4-илметил)-3,4-дигидроизохинолин-2(1H)-ил]карбонил}фенил)-1,2-диметил-1H-пиррол-3-ил]карбонил}(1-метил-1H-пиразол-4-ил)амино]фенил динатрийфосфат,
их энантиомеры и диастереоизомеры и их соли присоединения с фармацевтически приемлемой кислотой или основанием.
Фармакокинетическое исследование фосфатных соединений формулы (I) показало, что они in vivo были превращены в соединения формулы (I'), отличающиеся тем, что фосфатная функция была метаболизирована в гидрокси функцию. Соответственно, соединения формулы (I) ведут себя в качестве пролекарств соединений формулы (I'), имеющих следующую формулу:
в которой:
- X и Y представляют собой атом углерода или атом азота, при этом предполагается, что они не могут одновременно представлять собой два атома углерода или два атома азота,
- A1 и A2, вместе с атомами, несущими их, образуют необязательно замещенный, ароматический или неароматический гетероцикл Het, состоящий из 5, 6 или 7 кольцевых членов, который может содержать, в дополнение к азоту, представленному посредством X или Y, от 1 до 3 гетероатомов, независимо выбранных из кислорода, серы и азота, при этом предполагается, что рассматриваемый азот может быть замещен группой, представляющей собой атом водорода, линейную или разветвленную (C1-C6) алкильную группу или группу -C(O)-O-Alk, в которой Alk означает линейную или разветвленную (C1-C6) алкильную группу,
или A1 и A2 независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-C6)полигалогеналкильную, линейную или разветвленную (C1-C6) алкильную группу или циклоалкил,
- T представляет собой атом водорода, линейную или разветвленную (C1-C6) алкильную группу, необязательно замещенную одним-тремя атомами галогена, группу (C1-C4)алкил-NR1R2, или группу (C1-C4)алкил-OR6,
- R1 и R2 независимо друг от друга представляют собой атом водорода или линейную или разветвленную (C1-C6) алкильную группу,
или R1 и R2 с атомом азота, несущим их, образуют гетероциклоалкил,
- R3 представляет собой линейную или разветвленную (C1-C6) алкильную группу, линейную или разветвленную (C2-C6) алкенильную группу, линейную или разветвленную (С2-C6) алкинильную группу, циклоалкильную группу, (C3-C10)циклоалкил-(C1-C6) алкильную группу, где алкильный фрагмент является линейным или разветвленным, гетероциклоалкильную группу, арильную группу или гетероарильную группу, при этом предполагается, что один или несколько атомов углерода предыдущих групп, или их возможных заместителей, могут быть дейтерированными,
- R4 представляет собой арильную группу, гетероарильную группу, циклоалкильную группу или линейную или разветвленную (C1-C6) алкильную группу, при этом предполагается, что один или несколько атомов углерода предыдущих групп, или их возможных заместителей, могут быть дейтерированными,
- R5 представляет собой водород или атом галогена, линейную или разветвленную (C1-C6) алкильную группу, или линейную или разветвленную (C1-C6) алкокси группу,
- R6 представляет собой атом водорода или линейную или разветвленную (C1-C6) алкильную группу,
- Ra, Rb, Rc и Rd каждый независимо от других представляет собой R7, атом галогена, линейную или разветвленную (C1-C6) алкокси группу, гидрокси группу, линейную или разветвленную (C1-C6) полигалогеналкильную группу, трифторметокси группу, группу , нитро, R7-CO-(C0-C6)алкил-, R7-CO-NH-(С0-С6)алкил-, , , R7-SO2-NH-(C0-C6)алкил-, R7-NH-CO-NH-(C0-C6)алкил-, R7-O-CO-NH-(C0-C6)алкил-, гетероциклоалкильную группу, или заместители одной из пар (Ra,Rb), (Rb,Rc) или (Rc,Rd) вместе с атомами углерода, несущими их, образуют кольцо, состоящее из 5-7 кольцевых членов, которое может содержать от 1 до 2 гетероатомов, выбранных из кислорода и серы, при этом также предполагается, что один или несколько атомов углерода кольца, определенного выше, могут быть дейтерированными или замещенными 1-3 группами, выбранными из галогена и линейного или разветвленного (C1-C6)алкила,
- R7 и независимо друг от друга представляют собой водород, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C2-C6)алкенил, линейный или разветвленный (C2-C6)алкинил, арил или гетероарил, или R7 и вместе с атомом азота, несущим их, образуют гетероцикл, состоящий из 5-7 кольцевых членов,
при этом предполагается, что:
- "арил" означает фенильную, нафтильную, бифенильную или инденильную группу,
- "гетероарил" означает любую моно- или бициклическую группу, состоящую из 5-10 кольцевых членов, имеющую по меньшей мере один ароматический фрагмент и содержащую от 1 до 4 гетероатомов, выбранных из кислорода, серы и азота (включая четвертичные атомы азота),
- "циклоалкил" означает любую моно- или бициклическую, неароматическую, карбоциклическую группу, содержащую от 3 до 10 кольцевых членов,
- "гетероциклоалкил" означает любую моно- или бициклическую, неароматическую, конденсированную или спиро группу, состоящую из 3-10 кольцевых членов и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы, SO, SO2 и азота,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, таким образом определенные, и группы алкил, алкенил, алкинил и алкокси могут быть замещены посредством 1-3 групп, выбранных из необязательно замещенного, линейного или разветвленного (C1-C6)алкила, (C3-C6)спиро, линейного или разветвленного, необязательно замещенного (C1-C6)алкокси, (C1-C6)алкил-S-, гидрокси, оксо (или N-оксида, в соответствующих случаях), нитро, циано, -COOR', -OCOR', NR'R", линейного или разветвленного (C1-C6)полигалогеналкила, трифторметокси, (C1-C6)алкилсульфонила, галогена, необязательно замещенного арила, гетероарила, арилокси, арилтио, циклоалкила, гетероциклоалкила, необязательно замещенного одним или несколькими атомами галогена или алкильными группами, при этом предполагается, что R' и R" независимо друг от друга представляют собой атом водорода или необязательно замещенную, линейную или разветвленную (C1-C6) алкильную группу,
причем Het группа, определенная в формуле (I'), может быть замещена одной - тремя группами, выбранными из линейного или разветвленного (C1-C6)алкила, гидрокси, линейного или разветвленного (C1-C6)алкокси, и галогена, при этом предполагается, что и принимают значения, определенные для групп R' и R", упомянутых выше,
их энантиомеров и диастереоизомеров и их солей присоединения с фармацевтически приемлемой кислотой или основанием.
Соединения формулы (I') обладают проапоптотическими свойствами и в результате этого имеют важное терапевтическое значение для лечения злокачественных новообразований, аутоиммунных заболеваний и заболеваний иммунной системы. В настоящем изобретении показано, что, путем введения фосфатных соединений формулы (I), in vivo воздействие соединений формулы (I') оптимизировалось. Фактически растворимость соединений формулы (I) является значительно большей, чем растворимость соединений формулы (I'). Следовательно, применение соединений формулы (I) для изготовления фармацевтических композиций с точки зрения галеновых препаратов особенно предпочтительно.
Изобретение относится также к способу получения соединений формулы (I), который отличается тем, что в качестве исходного вещества используют соединение формулы (II):
в которой Ra, Rb, Rc и Rd принимают значения, определенные для формулы (I'),
причем соединение формулы (II) подвергают реакции Хека, в водной или органической среде, в присутствии палладиевого катализатора, основания, фосфина и соединения формулы (III):
в которой группы A1, A2, X и Y принимают значения, определенные для формулы (I'), и Alk представляет собой линейный или разветвленный (C1-C6)алкил,
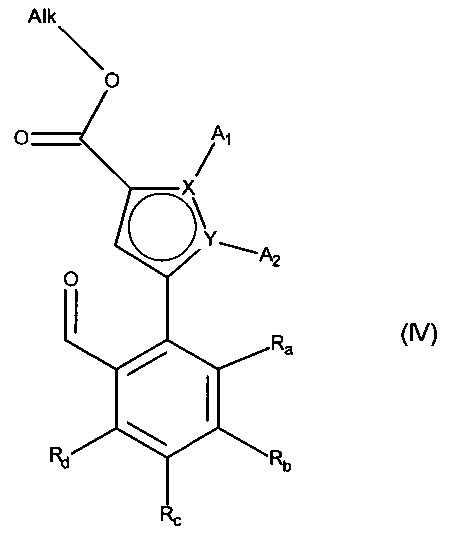
с получением соединения формулы (IV):
в которой A1, A2, X, Y, Ra, Rb, Rc и Rd принимают значения, определенные для формулы (I'), и Alk принимает значения, определенные выше,
альдегидную функцию соединения формулы (IV) окисляют до карбоновой кислоты с образованием соединения формулы (V):
в которой A1, A2, X, Y, Ra, Rb, Rc и Rd принимают значения, определенные для формулы (I'), и Alk принимает значения, определенные выше,
соединение формулы (V) затем подвергают пептидному сочетанию с соединением формулы (VI):
в которой T и R5 принимают значения, определенные для формулы (I'),
с получением соединения формулы (VII):
в которой A1, A2, X, Y, Ra, Rb, Rc, Rd, T и R5 принимают значения, определенные для формулы (I'), и Alk принимает значения, определенные выше,
сложноэфирную функцию соединения формулы (VII) гидролизуют с получением соответствующей карбоновой кислоты или карбоксилата, которую(-ый) можно превратить в производное по кислотной группе, такое как соответствующий ацилхлорид или ангидрид, перед сочетанием с амином NHR3R4, где R3 и R4 имеют те же значения, что и для формулы (I'), прежде чем подвергнуть действию пирофосфатного, фосфонатного или фосфорильного соединения в основных условиях, причем соединение, полученное таким образом, может быть необязательно гидролизовано или гидрогенолизировано с получением соединения формулы (I),
соединение формулы (I) может быть очищено в соответствии с обычными методами разделения, превращено, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на его изомеры в соответствии с обычными методами разделения,
при этом предполагается, что, в любое время, признанное подходящим в ходе описанного выше способа, определенные группы (гидрокси, амино…) реагентов или промежуточных соединений синтеза могут быть защищены и затем лишены защиты в соответствии с требованиями синтеза.
Соединения формул (II), (III), (VI) и амин NHR3R4 либо доступны для приобретения, либо могут быть получены специалистом в данной области техники с использованием обычных химических реакций, описанных в литературе.
Более конкретно, фосфатные соединения формулы (I) в соответствии с изобретением будут полезны для лечения хемо- или радиорезистентных злокачественных новообразований, а также при злокачественных заболеваниях крови и мелкоклеточном раке легкого.
Среди намеченных для лечения злокачественных заболеваний могут быть упомянуты, без какого-либо ограничения, рак мочевого пузыря, головного мозга, молочной железы и матки, хронические лимфоидные лейкозы, колоректальный рак, рак пищевода и печени, лимфобластные лейкозы, неходжкинские лимфомы, меланомы, злокачественные заболевания крови, миелы, рак яичников, немелкоклеточный рак легкого, рак предстательной железы и мелкоклеточный рак легкого. Среди неходжкинских лимфом, более предпочтительно, могут быть упомянуты фолликулярные лимфомы, лимфомы из клеток мантийной зоны, диффузные B-крупноклеточные лимфомы, мелкоклеточные лимфоцитарные лимфомы и B-клеточные лимфомы из клеток маргинальной зоны.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение формулы (I) в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
Среди фармацевтических композиций в соответствии с изобретением могут быть упомянуты особенно те, которые подходят для перорального, парентерального, назального, чрес- или транскожного, ректального, перлингвального, офтальмологического или респираторного введения, главным образом таблетки или драже, сублингвальные таблетки, саше, пакеты, капсулы, глоссеты, лепешки, суппозитории, кремы, мази, кожные гели, и питьевые или инъекционные ампулы.
Дозировка варьируется в зависимости от пола, возраста и веса пациента, пути введения, природы терапевтического показания, или каких-либо связанных лечений, и находится в диапазоне от 0.01 мг до 1 г в 24 часа за одно или несколько введений.
Кроме того, настоящее изобретение также относится к ассоциации соединения формулы (I) с противоопухолевым средством, выбранным из генотоксичных средств, митотических ядов, антиметаболитов, ингибиторов протеосом, ингибиторов киназ и антител, а также к фармацевтическим композициям, содержащим такой тип ассоциации, и к их применению для изготовления лекарственных средств для применения для лечения злокачественного новообразования.
Соединения настоящего изобретения также могут использоваться в ассоциации с радиотерапией для лечения злокачественного новообразования.
Следующие методики получения и примеры иллюстрируют изобретение, не ограничивая его каким-либо образом.
Методика получения 1: 6-[1-(Метоксикарбонил)-5,6,7,8-тетрагидро-3-индолизинил]-1,3-бензодиоксол-5-карбоновая кислота
Стадия A: 1-Формил-2-пиперидинкарбоновая кислота
К раствору 40 г рацемической смеси 2-пиперидинкарбоновой кислоты (0.310 ммоль) в 300 мл муравьиной кислоты, помещенному на баню с температурой 0°C, по каплям добавляют 200 мл (2.15 ммоль) уксусного ангидрида. Загрузочную порцию затем перемешивают при температуре окружающей среды в течение ночи. Затем, реакционную смесь охлаждают до 0°C, гидролизуют путем добавления 250 мл воды, и перемешивают в течение получаса при 0°C перед выполнением концентрирования досуха. Полученное таким образом масло переносят в 200 мл метанола и затем концентрируют досуха. Указанный в заголовке продукт получают в виде масла с выходом 98%. Его используют непосредственно, без очистки иным способом, на следующей стадии.
1Н ЯМР: δ (400 МГц; дмсо-d6; 300 K): 13.0 (m, 1H ОН); 8.0-8.05 (2s, 1Н альдегид); 4.9-4.5 (2d, 1Н α к N и СООН); 4.1-2.6 (m, 2Н α к N); 2.2-1.2 (m, 6Н пиперидин)
ИК: ν: -ОН: 2000-3000 см-1 кислота; ν:>С=0 1703 см-1 широкая полоса
Стадия B: Метил 5,6,7,8-тетрагидро-1-индолизинкарбоксилат
К раствору 10 г карбоновой кислоты, полученной на стадии A, (63.6 ммоль) в 65 мл дихлорэтана последовательно добавляют 13.4 г тозилхлорида (70.4 ммоль), 11.5 мл метил 2-хлоракрилата (113.5 ммоль) и затем, по каплям, 17.8 мл N,N,N-триэтиламина (127.2 ммоль). Реакционную смесь затем нагревают с обратным холодильником в течение 1 часа 30 минут. Ее затем доводят до температуры окружающей среды, и затем добавляют 5 мл метил 2-хлоракрилата (48.9 ммоль) и, по каплям, 9 мл N,N,N-триэтиламина (64 ммоль). Загрузочную порцию нагревают с обратным холодильником в течение ночи.
Реакционную смесь затем разбавляют метиленхлоридом, последовательно промывают 1М раствором HCl, насыщенным водным раствором NaHCO3 и затем соляным раствором до тех пор, пока не достигают нейтрального значения pH. Затем органическую фазу сушат над MgSO4, фильтруют, концентрируют досуха и очищают с помощью хроматографии на силикагеле (градиент гептан/AcOEt). Указанный в заголовке продукт получают в виде масла.
1Н ЯМР: δ (400 МГц; CDCl3; 300 K): 6.55-6.40 (d, 2Н тетрагидроиндолизин); 3.91 (t, 3Н сложный метиловый эфир); 3.78 (s, 3Н тетрагидроиндолизин); 3.08 (t, 2Н тетрагидроиндолизин); 1.95-1.85 (m, 4Н тетрагидроиндолизин)
ИК: ν:>C=O 1692 см-1 сложный эфир
Стадия C: Метил 3-(6-формил-1,3-бензодиоксол-5-ил)-5,6,7,8-тетрагидро-1-индолизинкарбоксилат
К раствору 6.4 г сложного эфира, полученного на стадии B, (35.7 ммоль) в 12 мл N,N-диметилацетамида последовательно добавляют 12.3 г 6-бром-1,3-бензодиоксол-5-карбальдегида (53.6 ммоль) и 7 г ацетата калия (71.4 ммоль), и затем загрузочную порцию перемешивают под аргоном в течение 20 минут. К ней затем добавляют 1.3 г палладиевого катализатора - дихлорбис(трифенилфосфин)палладия(II) (PdCl2(PPh3)2) (1.8 ммоль). Реакционную смесь затем нагревают при 130°C в течение одного часа перед добавлением к ней 139 мкл H2O. Нагревание продолжают, поддерживая такую же температуру в течение ночи. Температуре смеси позволяют вернуться к температуре окружающей среды и ее затем разбавляют с помощью AcOEt. Добавляют животный уголь (25 г на г продукта), и загрузочную порцию перемешивают при температуре окружающей среды в течение 1 часа и затем фильтруют. Затем органическую фазу промывают водой, сушат над сульфатом магния и концентрируют досуха. Полученный таким образом сырой продукт очищают с помощью хроматографии на силикагеле (градиент гептан/AcOEt). Указанный в заголовке продукт получают в виде масла.
1H ЯМР: δ:(400 МГц; дмсо-d6; 353 K): 9.65 (s, 1Н, Н альдегид); 7.3-7.15 (2s, 2Н, ароматические Н); 6.45 (s, 1H тетрагидроиндолизин); 6.20 (s, 2Н метилендиокси); 3.70 (s, 3Н сложный метиловый эфир); 3.5-4.0 (m, 2Н тетрагидроиндолизин); 3.05 (m, 2Н тетрагидроиндолизин); 1.85 (m, 4Н тетрагидроиндолизин)
ИК: ν:>C=O 1695 см-1 сложный эфир; ν:>C=O 1674 см-1
Стадия D: 6-[1-(Метоксикарбонил)-5,6,7,8-тетрагидро-3-индолизинил]-1,3-бензодиоксол-5-карбоновая кислота
Получают раствор, содержащий 3.37 г соединения, полученного на стадии C, (10.3 ммоль) в 9.3 мл ацетона и 8.8 мл (80.24 ммоль) 2-метил-2-бутена, и помещают его на баню с температурой 0°C. К нему по каплям добавляют 9.3 мл водного раствора, содержащего смесь 3.3 г хлорита натрия (NaClO2) (36.05 ммоль) и 3.6 г моногидрата дигидрофосфата натрия (NaH2PO4) (25.75 ммоль). Загрузочную порцию затем перемешивают при температуре окружающей среды в течение 7 часов. Реакционную смесь затем концентрируют для удаления ацетона. Полученное твердое вещество затем отфильтровывают, промывают водой и затем сушат при 40°C в вакууме в течение ночи. Указанный в заголовке продукт получают в виде твердого вещества, которое впоследствии используют без очистки иным способом.
1Н ЯМР: δ (400 МГц; дмсо-d6; 300 K): 12.10 (m, 1Н, Н карбоновая кислота); 7.40-6.88 (2s, 2Н, ароматические Н); 6.20 (s, 1Н, Н тетрагидроиндолизин); 6.18 (s, 2Н, Н метилендиокси); 3.70 (s, 3Н сложный метиловый эфир); 3.55 (t, 2Н тетрагидроиндолизин); 3.00 (t, 2Н тетрагидроиндолизин); 1.80 (m, 4Н, Н тетрагидроиндолизин)
ИК: ν: -ОН: 3000-2000 см-1 кислота; ν:>C=O 1686-1676 см-1 сложный эфир + кислота; ν:>C=C<1608 см-1
Методика получения 2: 2-[1-(Метоксикарбонил)-5,6,7,8-тетрагидро-3-индолизинил]бензойная кислота
Методика соответствует протоколу, описанному в методике получения 1, с заменой 6-бром-1,3-бензодиоксол-5-карбальдегида, используемого на стадии C, на 2-бромбензальдегид.
Методика получения 3: 6-[1-(Метоксикарбонил)-3-индолизинил]-1,3-бензодиоксол-5-карбоновая кислота
Стадия A: Бромид 1-(карбоксиметил)-1,2-дигидропиридиния
К раствору 16.2 мл пиридина (200 ммоль) в 120 мл этилацетата порциями добавляют 27.8 г (200 ммоль) бромуксусной кислоты. Загрузочную порцию затем перемешивают при температуре окружающей среды в течение ночи. Полученный таким образом осадок отфильтровывают и затем промывают холодным этилацетатом. После сушки, указанный в заголовке продукт получают в виде порошка, который непосредственно используют на следующей стадии.
1Н ЯМР: δ (400 МГц; дмсо-d6; 300 K): 9.15 (d, 2Н, ароматические Н, пиридин); 8.7 (t, 1Н, ароматический Н); 8.25 (t, 2Н, ароматический Н); 5.65 (s, 2Н, Н СН2СООН)
ИК: ν: C=O: 1732 см-1; -ОН кислота: 2800 см-1
Стадия B: Метил 1-индолизинкарбоксилат
К суспензии 6.55 г соли пиридиния, полученной на стадии A, (30 ммоль) в 240 мл толуола последовательно добавляют 16.7 мл метилакрилата (150 ммоль), 4.2 мл триэтиламина (30 ммоль) и затем, порциями, 20.9 г MnO2 (240 ммоль). Загрузочную порцию затем нагревают при 90°C в течение 3 часов. После охлаждения, реакц