Антитела, не содержащие fc-фрагмента, включающие два fab-фрагмента, и способы их применения
Иллюстрации
Показать всеГруппа изобретений относится к биотехнологии, в частности к биспецифическим антителам и их применению. Биспецифические антитела содержат два Fab фрагмента, причем первый Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении первого антигена, и второй Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении второго антигена, где произведен обмен вариабельными участками или константными участками между тяжелой и легкой цепями второго Fab фрагмента, причем биспецифическое антитело лишено Fc домена. Предложены также способ и клетка-хозяин для их получения, а также фармацевтическая композиция и иммуноконъюгат для лечения рака, содержащие указанные биспецифические антитела. Преимущество заявленных биспецифических антител состоит в пониженной агрегации фрагментов, повышенной стабильности и в повышении эффективности связывания с антигеном. Предлагаемые иммуноконъюгат и фармацевтическая композиция позволяют эффективно проводить терапию рака. 5 н. и 8 з.п. ф-лы, 23 ил., 2 табл., 9 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к биспецифическим антителам, содержащим по меньшей мере два Fab фрагмента, где первый Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении первого антигена, и второй Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении второго антигена, где произведен обмен вариабельными участками или константными участками между тяжелой и легкой цепями второго Fab и где биспецифическое антитело лишено Fc домена; способам их получения, фармацевтическим композициям, содержащим указанные антитела, и их применению.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Моноклональные антитела (mAbs) представляют собой все более важный класс терапевтических агентов. Кроме продуктов mAb, состоящих из полноразмерных форм IgG, были разработаны разнообразные форматы мультиспецифических рекомбинантных антител, например, тетравалентные биспецифические антитела, созданные путем слияния, например, антител в формате IgG и одноцепочечных доменов (см., например, Coloma, M.J., et al., Nature Biotech 15 (1997) 159-163; WO 2001/077342; и Morrison, S.L, Nature Biotech 25(2007) 1233-1234).
Разработали несколько других новых форматов антител, способных связывать два или более антигенов, у которых структура остова антитела (IgA, IgD, IgE, IgG или IgM) не сохраняется, такие как диа-, триа- или тетратела, миниантитела, и несколько одноцепочечных форматов (scFv, Bis-scFv), (Holliger, Р., et al., Nature Biotech 23 (2005) 1126-1136; Fischer, N., Leger, 0., Pathobiology 74 (2007) 3-14; Shen, J., et al., Journal of Immunological Methods 318 (2007) 65-74; Wu, С., et al., Nature Biotech. 25 (2007) 1290-1297).
Во всех этих форматах используются линкеры либо для объединения остова антитела (IgA, IgD, IgE, IgG или IgM) с другим связывающим белком (например, scFv), либо для объединения, например, двух Fab фрагментов или scFv (Fischer, N., Leger, 0-, Pathobiology 74 (2007) 3-14). Тандемные scFV представляют собой два фрагмента scFv, связанные при помощи дополнительного пептидного линкера, они также обозначаются (scFv)2. За счет сокращения длины пептидного линкера между вариабельными доменами были получены диатела. Добавление дополнительного пептидного линкера между двумя полипептидами позволяет получить т.н. одноцепочечные диатела. US 2007/0274985 относится к антителам, содержащим одноцепочечные Fab (scFab) фрагменты. Использование фрагментов антител в качестве терапевтических средств имеет как преимущества, так и недостатки по сравнению с полноразмерными моноклональными антителами: одно из преимуществ состоит в том, что они обладают меньшим размером и быстрее проникают в ткани и опухоли. Кроме того, предполагается, что малый размер фрагментов позволяет связываться с эпитопами, недоступными для полноразмерных моноклональных антител. С другой стороны, фрагменты демонстрируют короткое время полужизни в кровотоке человека, возможно вследствие почечного клиренса. Более короткое время полужизни может препятствовать достаточному накоплению терапевтического средства в целевом участке. Получение фрагментов антител является непростой задачей, поскольку фрагменты склонны к формированию агрегатов и могут быть менее стабильными по сравнению с полноразмерными моноклональными антителами. Кроме того, нежелательное образование пар между чужеродными тяжелыми и легкими цепями приводит к формированию неактивных антигенсвязывающих сайтов и/или других нефункциональных нежелательных побочных продуктов, что представляет собой наибольшую трудность при масштабном производстве и терапевтическом применении фрагментов антител. В частности, невозможно получить конструкции тандемных Fab (Tandem-Fab), в которых два или более Fab объединены друг с другом посредством одного линкера, вследствие произвольной ассоциации двух легких цепей, приводящей к образованию нежелательных неактивных побочных продуктов. Новый формат антител по изобретению позволяет преодолеть эти трудности. В данной заявке описывается новый формат биспецифического антитела, которое можно легко получить с высоким выходом благодаря снижению количества ошибочно спаренных побочных продуктов, и которое демонстрирует пониженную агрегацию по сравнению с фрагментами биспецифических антител, известными в области техники. Применение подхода, основанного на взаимном обмене участками между тяжелой и легкой цепями (кроссовера), способствует правильной ассоциации легких цепей без необходимости создания общей легкой цепи. Подход с использованием общей легкой цепи невозможно применить к существующим антителам. Кроме того, биспецифические антитела нового формата имеют более высокий молекулярную массу по сравнению со многими стандартными фрагментами биспецифических антител, что препятствует избыточному почечному клиренсу и приводит к увеличению времени полужизни in vivo. Биспецифические антитела нового формата являются полностью функциональными и обладают сравнимым или улучшенным связыванием и активностью по сравнению с соответствующими стандартными биспецифическими антителами.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к биспецифическим антителам, содержащим по меньшей мере два Fab фрагмента, где первый Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении первого антигена, и второй Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении второго антигена, где произведен обмен вариабельными участками или константными участками между легкой и тяжелой цепями второго Fab и где биспецифическое антитело лишено Fc домена. В одном воплощении первый и второй Fab фрагменты соединены при помощи пептидного линкера. Предпочтительно, указанный пептидный линкер представляет собой линкер (G4S)2.
В одном воплощении указанное антитело дополнительно содержит третий Fab фрагмент. В другом воплощении указанный третий Fab фрагмент содержит по меньшей мере один антигенсвязывающий сайт, специфический в отношении первого или второго антигена, предпочтительно в отношении первого антигена.
В одном воплощении третий Fab фрагмент связан с легкой цепью или тяжелой цепью первого Fab фрагмента. В другом воплощении третий Fab фрагмент связан с N или С-концом легкой цепи или тяжелой цепи второго Fab фрагмента. В одном воплощении третий Fab фрагмент связан с первым или вторым Fab фрагментом посредством пептидного линкера. Предпочтительно, указанный пептидный линкер представляет собой линкер (G4S)2.
Биспецифические антитела по изобретению являются по меньшей мере бивалентными и могут быть тривалентными или мультивалентными, например, тетравалентными. В одном воплощении указанные биспецифические антитела являются бивалентными (формат 1+1) и имеют по одному сайту связывания, направленному против первого и второго антигена, соответственно. В другом воплощении указанные биспецифические антитела являются тривалентными (формат 2+1), с двумя сайтами связывания, каждый из которых направлен против первого антигена, и одним сайтом связывания, направленным против второго антигена, что будет подробно описано в следующем разделе.
Второй объект настоящего изобретения относится к фармацевтической композиции, содержащей биспецифическое антитело по настоящему изобретению.
Третий объект настоящего изобретения относится к биспецифическому антителу по настоящему изобретению для лечения рака. В другом воплощении предложено применение биспецифического антитела в качестве лекарственного препарата. Предпочтительно, указанное применение направлено на лечение рака.
Следующие объекты изобретения относятся к последовательности нуклеиновой кислоты, содержащей последовательность, кодирующую тяжелую цепь- биспецифического антитела по настоящему изобретению, последовательности нуклеиновой кислоты содержащей последовательность, кодирующую легкую цепь биспецифического антитела по настоящему изобретению, экспрессирующему вектору, содержащему последовательность нуклеиновой кислоты по настоящему изобретению, и к прокариотической или эукариотической клетке-хозяину, содержащей вектор по настоящему изобретению. Кроме того, предложен способ получения антитела, включающий культивирование клетки-хозяина с получением антитела.
В следующем воплощении предложен иммуноконъюгат, содержащий биспецифическое антитело по изобретению и цитотоксический агент.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг.1: Схематическая иллюстрация приведенных в качестве примера форматов биспецифических антител по изобретению, а) молекула Fab-кpoccFab, расположенный на С-конце, b) молекула Fab-кpoccFab, расположенный на N-конце с) молекула (Fab)2-кpoccFab, расположенный на С-конце d) молекула (Fab)2-кpoccFab, расположенный на N-конце е) молекула Fab-кpoccFab-Fab.
Фиг.2: Анализ получения и очистки hu Fab(MCSP)-кpoccFab(CD3): ДСН-ПАГ: 4-12% Бис/Трис (NuPage [invitrogen]; окрашивание Кумасси): а) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)-кpoccFab(CD3) в невосстанавливающих условиях; b) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)-кpoccFab(CD3) в восстанавливающих условиях.
Фиг.3: Анализ получения и очистки Fab(MCSP)-кpoccFab(CD3). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 200 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца).
Фиг.4: Анализ получения и очистки hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3): ДСН-ПАГ: 4-12% Бис/Трис (NuPage [invitrogen]; окрашивание Кумасси): а) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) в невосстанавливающих условиях; b) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) в восстанавливающих условиях.
Фиг.5: Анализ получения и очистки hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 200 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца).
Фиг.6: Анализ получения и очистки hu Fab(MCSP)- кpoccFab(CD3) -Fab(MCSP). ДСН-ПАГ: 4-12% Бис/Трис (NuPage [invitrogen]; окрашивание Кумасси): а) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)- кpoccFab(CD3)-Fab(MCSP) в невосстанавливающих условиях; b) 1 - маркер Mark 12 (invitrogen), 2 - hu Fab(MCSP)-кpoccFab(CD3) -Fab(MCSP) в восстанавливающих условиях.
Фиг.7: Анализ получения и очистки hu Fab(MCSP)-кpoccFab(CD3)-Fab(MCSP). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 200 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца).
Фиг.8: Анализ получения и очистки кpoccFab мыши (CD3) -Fab(MCSP)-Fab(MCSP). ДСН-ПАГ: 4-12% Бис/Трис (NuPage [invitrogen]; окрашивание Кумасси): а) 1 - маркер Mark 12 (invitrogen), 2 - кpoccFab мыши (CD3)-Fab(MCSP)-Fab(MCSP) в невосстанавливающих условиях; b) 1 - маркер Mark 12 (invitrogen), 2 - кpoccFab мыши (CD3)-Fab(MCSP)-Fab(MCSP) в восстанавливающих условиях.
Фиг.9: Анализ получения и очистки кpoccFab мыши (CD3) -Fab(MCSP)-Fab(MCSP). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 200 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца).
Фиг.10: Цитолитическая активность в отношении опухолевых клеток MDA-МВ-435 (оцениваемая по высвобождению ЛДГ) при совместном культивировании с общей популяцией Т-клеток человека (соотношение эффекторные клетки:клетки-мишеней=5:1) и активация в течение 20 часов при помощи различных концентраций hu Fab(MCSP)-кpoccFab(CD3) (="Fab-кpoccFab"), hu Fab(MCSP)-кpoccFab(CD3)-Fab(MCSP) (="Fab-кpoccFab-Fab"), hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) (="(Fab)2-кpoccFab"), а также биспецифических молекул (scFv)2 (антиМСSР/антиhuCD3e) (="(scFv)2"). Конструкции, имеющие две валентности, направленные против MCSP, демонстрируют цитотоксическую активность сравнимую с конструкцией "(scFv)2", тогда как конструкция "Fab-кpoccFab", имеющая одну валентность связывания для MCSP, явно обладает меньшей эффективностью.
Фиг.11: Сравнение конструкций hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) (="(Fab)2-кpoccFab") и (scFv)2 (антиМСSР/антиhuCD3e) (="(scFv)2"). Показано высвобождение ЛДГ из опухолевых клеток MDA-MB-435 при совместном культивировании с общей популяцией Т-клеток человека (соотношение эффекторные клетки:клетки-мишени=5:1) и активации в течение 21 часа с использованием биспецифических конструкций и соответствующих IgG в различных концентрациях. Присутствие "(Fab)2-кpoccFab" индуцировало апоптоз клеток-мишеней по меньшей мере так же эффективно, как и присутствие молекул (scFv)2.
Фиг.12: Сравнение конструкций hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) (="(Fab)2-кpoccFab") и (scFv)2 (антиМСSР/антиhuCD3e) (="(scFv)2"). Показано высвобождение ЛДГ из опухолевых клеток меланомы человека MV-3 при совместном культивировании с человеческими МКПК (соотношение эффекторные клетки:клетки-мишени=10:1) и активации в течение 26 часов с использованием биспецифических конструкций и соответствующих IgG в различных концентрациях. Присутствие "(Fab)2-кpoccFab" индуцировало апоптоз клеток-мишеней по меньшей мере так же эффективно, как и присутствие молекул (scFv)2.
Фиг.13: Высвобождение ЛДГ из опухолевых клеток B16/F10-huMCSP Fluc2, клон 48, индуцированное активацией первичных Т-клеток мыши с использованием конструкции кpoccFab мыши (CD3)-Fab(MCSP)-Fab(MCSP) (=(Fab)2-кpoccFab), направленной против MCSP человека и CD3 мыши. Соотношение эффекторных клеток: клеток-мишеней составляло 5:1. Результаты теста анализировали после инкубации в течение 23,5 часов при 37°С, 5% CO2. Конструкция индуцирует зависимый от концентрации, опосредованный Т-клетками апоптоз клеток-мишеней, экспрессирующих MCSP человека.
Фиг.14: Высвобождение ЛДГ из опухолевых клеток B16/F10-huMCSP Fluc2, клон 48, индуцированное активацией первичных Т-клеток мыши с использованием конструкции кpoccFab мыши (CD3)-Fab(MCSP)-Fab(MCSP) (=(Fab)2-кpoccFab), направленной против MCSP человека и CD3 мыши, в концентрации 50 нМ. Соотношение эффекторных клеток: клеток-мишеней составляло 5:1. Результаты теста анализировали после инкубации в течение 23,5 часов при 37°С, 5% CO2. Конструкция индуцирует опосредованный Т-клетками апоптоз клеток-мишеней, экспрессирующих MCSP человека. При использовании конструкции в такой концентрации происходит только незначительная гиперактивация Т-клеток.
Фиг.15: Концентрации различных цитокинов, измеренные в супернатанте, после инкубации цельной крови с различными биспецифическими конструкциями CD3-MCSP (hu Fab(MCSP)-Fab(MCSP)-кpoccFab(CD3) (="(Fab)2-кpoccFab") и (scFv)2 (aHTHMCSP/антиhuCD3e) (="(scFv)2")) в концентрации 1 нМ в течение 24 часов в присутствии (А, В) или в отсутствие (С, D) опухолевых клеток Colo-38. В каждую лунку 96-луночного планшета помещали по 280 мкл цельной крови и добавляли по 30 000 клеток Colo-38, в соответствии с описанием. Основным цитокином, секретируемым при активации Т-клеток в присутствии опухолевых клеток Colo-38, был IL-6, затем следовал ИФН-гамма. Кроме того, при активации Т-клеток в присутствии клеток-мишеней также значительно повышался уровень гранзима В. В целом, конструкция "(scFv)2" повышала уровни ФНО и ИФН-гамма, а также гранзима В в присутствии клеток-мишеней (А и В) несколько более эффективно по сравнению с другими биспецифическими конструкциями.
При активации Т-клеток биспецифическими конструкциями в присутствии (или в отсутствие) клеток-мишеней не отмечалось выраженной секреции ТП2 цитокинов (IL-10 и IL-4). В этом тесте также наблюдалась незначительная секреция ИФН-гамма, индуцированная конструкцией "(Fab)2-кpoccFab" в отсутствие клеток-мишеней.
Фиг.16: Уровень поверхностной экспрессии позднего маркера активации CD25 в общей популяции Т-клеток мыши, выделенных из спленоцитов. Общую популяцию Т-клеток мыши инкубировали с конструкцией кpoccFab мыши (CD3)-Fab(MCSP)-Fab(MCSP) (=(Fab)2-кpoccFab) (биспецифической конструкцией, направленной против CD3 мыши и MCSP человека) в концентрации 50 нМ в присутствии или в отсутствие опухолевых клеток B16/F10-huMCSP Fluc2 клон 48, в соответствии с описанием (соотношение эффекторных клеток: клеток-мишеней 10:1). Показан уровень экспрессии позднего маркера активации CD25 на поверхности CD8+ Т-клеток через 70 часов. Повышение CD25 на поверхности CD8+ Т-клеток под воздействием конструкции (Fab)2-кpoccFab происходит только в присутствии клеток-мишеней. Референтные IgG, которые использовали в той же молярности, были не способны привести к повышению CD25.
Фиг.17: Анализ получения и очистки Fab(CD33)-кpoccFab (CD3). ДСН-ПАГ: а) 3-8% Трис/Ацетат (NuPage [invitrogen]; окрашивание Кумасси): а) 1 - маркер HiMark (invitrogen), 2 - Fab(CD33)-кpoccFab (CD3) в невосстанавливающих условиях; b) 4-12% Бис/Трис (NuPage [invitrogen]: 1 - маркер Mark 12 (invitrogen), 2 - Fab(CD33)-кpoccFab (CD3) в восстанавливающих условиях.
Фиг.18: Анализ получения и очистки Fab(CD33)-кpoccFab (CD3). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 200 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца).
Фиг.19: Цитолитическая активность в отношении опухолевых клеток MV-3 (оцениваемая по высвобождению ЛДГ) при совместном культивировании МКПК человека (соотношение эффекторные клетки: клетки-мишени=10:1) и активации в течение 24 часов с использованием биспецифических конструкций CD3-MCSP (hu Fab(MCSP)-кpoccFab(CD3); обозначенных "1+1 без Fc" и референтной молекулы (scFv)2 (антиМСSР/антиhuCD3e) (="(scFv)2")) в различных концентрациях. Конструкция "1+1 без Fc" индуцирует апоптоз клеток-мишеней MV-3 с рассчитанным значением ЕС50 25,4 пМоль, тогда как рассчитанное значение ЕС50 для референтной молекулы "(scFv)2" составляет 57 пМоль, что показывает чуть большую эффективность молекулы "1+1 без Fc" по показателю ЕС50.
Фиг.20: Активация CD4+ или CD8+Т-клеток, оцениваемая по повышению CD69 (А), соответствующему увеличению количества клеток, положительных по CD69 (В), в присутствии huMCSP-положительных опухолевых клеток MV-3 при совместном культивировании с МКПК человека (соотношение эффекторных клеток: клеток-мишеней=10:1), под воздействием биспецифических конструкций CD3-MCSP (hu Fab(MCSP)-кpoccFab(CD3); обозначенных "1+1 без Fc", и референтной молекулы (scFv)2 (антиМСSР/антиhuCD3e) (="(scFv)2"), соответственно) в течение ~24 часов. В целом, медианные значения CD69 выше у CD8+ Т-клеток по сравнению с CD4+ Т-клетками. Наблюдается четкое зависимое от концентрации повышение медианных значений CD69, а также процентного содержания положительных по CD69 клеток в случае обеих конструкций.
Фиг.21: Иллюстрация референтной молекулы (scFv)2.
Фиг.22: Анализ получения и очистки (scFv)2 (антиМСSР/антиhuCD3e). ДСН-ПАГ: 4-12% Бис/Трис (NuPage [invitrogen]; окрашивание Кумасси): 1 - маркер Mark 12 (invitrogen), 2 - (scFv)2 (антиМСSР/антиhuCD3e) в восстанавливающих условиях; 3 - (scFv)2 (антиМСSР/антиhuCD3e) в невосстанавливающих условиях.
Фиг.23: Анализ получения и очистки (scFv)2 (антиМСSР/антиhuCD3e). Аналитическая эксклюзионная хроматография, хроматограмма А280 (Superdex 75 10/300 GL [GE Healthcare]; 2 мМ MOPS pH 7,3, 150 мМ NaCl, 0,02% (масс./об) NaCl; инжектировали 50 мкг образца ((scFv)2 (антиМСSР/антиhuCD3e))).
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
I. Определения
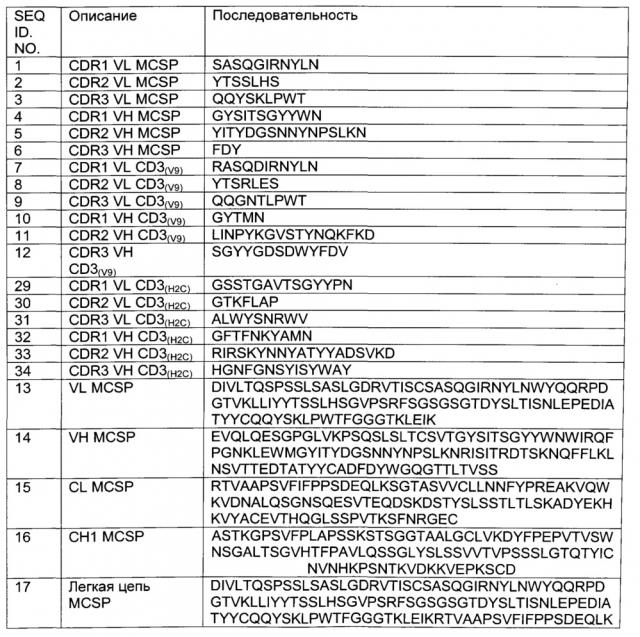
"Каркасные участки" или "FR" (от англ. "framework") обозначают остатки вариабельного домена, отличные от остатков гипервариабельного участка (HVR). FR вариабельного домена, как правило, состоит из 4 FR доменов: FR1, FR2, FR3 и FR4. Соответственно, последовательности HVR и FR в составе VH (или VL), как правило, располагаются в следующей последовательности: FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
"Акцепторные каркасные участки человеческого происхождения" в целях данного описания представляют собой каркасные участки, содержащие аминокислотную последовательность каркасного участка вариабельного домена легкой цепи (VL) или каркасные участки вариабельного домена тяжелой цепи (VH), полученные на основе каркасных участков иммуноглобулина человека или консенсусных каркасных участков человеческого происхождения, определение которым приведено ниже. Акцепторные каркасные последовательности, "полученные на основе" каркасной последовательности иммуноглобулина человека или консенсусных каркасных участков человека, могут содержать ту же аминокислотную последовательность или могут иметь измененную аминокислотную последовательность. В некоторых воплощениях число аминокислотных замен равно 10 или менее, 9 или менее, 8 или менее, 7 или менее, 6 или менее, 5 или менее, 4 или менее, 3 или менее, или 2 или менее. В некоторых воплощениях акцепторная последовательность каркасных участков VL идентична последовательности каркасных участков VL иммуноглобулина человека или консенсусной последовательности каркасных участков человеческого происхождения.
"Консенсусные каркасные участки человеческого происхождения" представляют собой каркасные участки, представляющие наиболее часто встречающиеся аминокислотные остатки в наборе последовательностей каркасных участков VL или VH иммуноглобулинов человека. Как правило, последовательности VL или VH иммуноглобулинов человека выбирают из подгруппы последовательностей вариабельных доменов. Как правило, подгруппа последовательностей представляет собой подгруппу согласно описанию Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols.1-3. В одном воплощении, подгруппой для VL является подгруппа каппа I, согласно Kabat et а1.,см выше. В одном воплощении, подгруппой для VH является подгруппа III, согласно Kabat et al., см выше.
Термин "гипервариабельный участок" или "HVR", используемый здесь, обозначает каждый из участков вариабельного домена антитела, имеющих гипервариабельную последовательность и/или формирующих петли определенной структуры ("гипервариабельные петли"). Как правило, нативные антитела, состоящие из четырех цепей, имеют 6 HVR; три в VH (Н1, Н2, Н3), и три в VL (L1, L2, L3). Как правило, HVR содержат аминокислотные остатки гипервариабельных петель и/или "участков определяющих комплементарность" (CDR), последние характеризуются наибольшей вариабельностью последовательности и/или задействованы в распознавании антигена. Приведенные в качестве примера гипервариабельные петли находятся между аминокислотными остатками 26-32 (L1), 50-52 (L2), 91-96 (L3), 26-32 (Н1), 53-55 (Н2) и 96-101 (Н3) (Chothia and Lesk, J. Mol. Biol. 196:901-917 (1987). Приведенные в качестве примера CDR (CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-Н2 и CDR-H3) находятся между аминокислотными остатками 24-34 в L1, 50-56 в L2, 89-97 в L3, 31-35 В в Н1, 50-65 в Н2 и 95-102 в Н3. (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991).) Термины гипервариабельные участки (HVR) и участки, определяющие комплементарность (CDR), здесь используются взаимозаменяемо для обозначения частей вариабельного участка, формирующих антигенсвязывающие участки. Эти конкретные участки были описаны в публикациях Kabat et al., U.S. Dept. of Health and Human Services, "Sequences of Proteins of Immunological Interest" (1983) и Chothia et al., J. Mol. Biol. 196:901-917 (1987), и при сравнении друг с другом данные определения включают перекрывающиеся группы аминокислотных остатков. Тем не менее, применение любого из определений для обозначения CDR антитела или его вариантов находится в рамках термина, используемого в настоящем документе. Соответствующие аминокислотные участки, содержащие CDR, согласно любой из вышеупомянутых ссылок, для сравнения представлены ниже в Таблице 1. Точные номера аминокислотных остатков, содержащих конкретные CDR, могут варьировать в зависимости от последовательности и размера CDR. Специалисты в данной области могут легко определить по указанной аминокислотной последовательности вариабельного участка антитела, какие аминокислотные остатки содержат конкретный CDR.
| Таблица 1. | |||
| Определения CDR1 | |||
| CDR | Kabat | Chothia | AbM2 |
| VH CDR1 | 31-35 | 26-32 | 26-35 |
| VH CDR2 | 50-65 | 52-58 | 50-58 |
| VH CDR3 | 95-102 | 95-102 | 95-102 |
| VL CDR1 | 24-34 | 26-32 | 24-34 |
| VL CDR2 | 50-56 | 50-52 | 50-56 |
| VL CDR3 | 89-97 | 91-96 | 89-97 |
| 1Нумерация всех определений CDR в Таблице 1 соответствует системе нумерации, разработанной Кабат и др. (см. ниже). | |||
| 2"AbM" с прописной буквой "b" согласно использованию в Таблице 1 обозначают CDR в соответствии с программой моделирования антител "AbM" Oxford Molecular. |
Kabat et al. также разработали систему нумерации для последовательностей вариабельных участков, которую можно применить для любого антитела. Любой специалист в данной области может однозначно "пронумеровать по системе Кабат" любую последовательность вариабельного участка, не основываясь на каких-либо экспериментальных данных помимо самой последовательности. В данном документе "нумерация согласно Кабат" относится к системе нумерации, разработанной Кабат и др., U.S. Dept. of Health and Human Services, "Sequence of Proteins of Immunological Interest" (1983). Если не указано иначе, ссылки на номера позиций конкретных аминокислотных остатков в вариабельном участке антитела указаны в соответствии с системой нумерации согласно Кабат.
Как правило, CDR содержат аминокислотные остатки, образующие гипервариабельные петли, за исключением CDR1 в составе VH. CDR также включают "остатки, определяющие специфичность" или "SDR," которые представляют собой остатки, контактирующие с антигеном. SDR находятся в составе участков CDR, обозначаемых "укороченными CDR", или a-CDR (от англ. abbreviated-CDRs). Приведенные в качестве примера a-CDR (a-CDR-L1, a-CDR-L2, a-CDR-L3, a-CDR-H1, a-CDR-H2 и a-CDR-Н3) образованы аминокислотными остатками в положениях 31-34 в L1, 50-55 в L2, 89-96 в L3, 31-35 В в Н1, 50-58 в Н2 и 95-102 в НЗ (см. Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008).) Если не указано иначе, остатки HVR и иные остатки вариабельного домена (например, остатки каркасного участка) здесь пронумерованы в соответствии с Kabat et аl., см. выше.
Термин "антитело" здесь используется в широком смысле и включает антитела с различной структурой, включая моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител, при условии, что они проявляют желаемую антигенсвязывающую активность, но не ограничивается ими. В частности, термин "антитело" также включает биспецифические антитела по изобретению, содержащие по меньшей мере два Fab фрагмента, но не имеющие Fc домена.
"Человеческое антитело" представляет собой антитело, имеющее аминокислотную последовательность, которая соответствует последовательности антитела, продуцируемого в организме или в клетках человека или полученного из источника, не относящегося к человеку, но задействующего репертуар антител человека или иные последовательности, кодирующие антитела человека. Данное определение человеческого антитела в частности исключает гуманизированные антитела, содержащие антигенсвязывающие остатки, не являющиеся человеческими.
Термин "рекомбинантное человеческое антитело" в данном документе включает все человеческие антитела, приготовленные, экспрессированные, созданные или выделенные с использованием рекомбинантных методов, такие как антитела, выделенные из клеток-хозяев, таких как клетки NSO или СНО, или из организма животного (например, мыши), трансгенного по генам человеческих иммуноглобулинов, или антитела, экспрессированные с использованием рекомбинантных векторов экспрессии, трансфецированных в клетку-хозяина. Такие рекомбинантные человеческие антитела имеют вариабельный и константный участки в перегруппированном виде. Рекомбинантные человеческие антитела согласно изобретению были подвергнуты соматической гипермутации in vivo. Таким образом, аминокислотные последовательности VH и VL доменов рекомбинантных антител представляют собой последовательности, которые получены на основе и близки последовательностям VH и VL зародышевой линии человека, но не могут существовать естественным образом в зародышевом наборе человеческих антител in vivo.
"Гуманизированное" антитело обозначает химерное антитело, содержащее аминокислотные остатки гипервариабельных участков, не являющихся человеческими, и аминокислотные остатки каркасных участков человеческого происхождения. В определенных воплощениях гуманизированное антитело содержит по существу все из по меньшей мере одного, а обычно двух вариабельных доменов, в которых все или по существу все гипервариабельные участки (например, CDR) соответствуют участкам антитела, не являющегося человеческим, и все или по существу все каркасные участки соответствуют участкам человеческого антитела. Гуманизированное антитело может содержать по меньшей мере часть константного участка антитела, полученного из антитела человека. "Гуманизированная форма" антитела, например, антитела не являющегося человеческим, обозначает антитело, прошедшее гуманизацию. Другие формы "гуманизированных антител", охватываемые настоящим изобретением, представляют собой такие, у которых константный участок был дополнительно модифицирован или изменен по сравнению с константным участком исходного антитела для получения свойств по изобретению, в частности, относящихся к связыванию C1q и/или связыванию Fc рецептора (FcR).
Термин "химерное" антитело обозначает антитело, в котором часть тяжелой и/или легкой цепи получена из конкретных источников или биологических видов, тогда как оставшаяся часть тяжелой и/или легкой цепи получена из другого источника или биологического вида, как правило полученное с использованием технологий рекомбинантной ДНК. Предпочтительными являются химерные антитела, содержащие мышиный вариабельный участок и человеческий константный участок. Другими предпочтительными формами "химерных антител", охватываемыми настоящим изобретением, являются те, у которых константный участок был модифицирован или изменен по сравнению с исходным антителом для получения свойств по изобретению, в частности, относящихся к связыванию C1q и/или связыванию Fc рецептора (FcR). Такие химерные антитела также обозначаются "антитела с переключенным классом". Химерные антитела являются продуктом экспрессии генов иммуноглобулинов, содержащих сегменты ДНК, кодирующие вариабельные участки иммуноглобулинов, и сегменты ДНК, кодирующие константные участки иммуноглобулинов. Способы получения химерных антител включают стандартные технологии рекомбинантной ДНК и трансфекции генов, хорошо известные в области техники. См., например, Morrison, S.L, et al., Proc. Natl. Acad. Sci. USA 81 (1984) 6851-6855; патенты США US 5,202,238 и 5,204,244.
Термин "моноклональное антитело" в данном документе используется для обозначения антитела, полученного из популяции по существу гомогенных антител, т.е. отдельные антитела, составляющие популяцию, идентичны и/или связывают один эпитоп, за исключением возможных вариантов антител, например, содержащих мутации, которые возникают естественным путем или в ходе получения препарата моноклонального антитела, при этом подобные варианты, как правило, присутствуют в минорных количествах. В противоположность препаратам поликлональных антител, обычно содержащим различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело в препарате моноклональных антител направлено против единственной детерминанты или антигена. Таким образом, определение "моноклональное" указывает на характер антитела, полученного из по существу гомогенной популяции антител, и не должно рассматриваться как необходимость получения антитела определенным способом. Например, моноклональные антитела, предназначенные для применения в соответствии с настоящим изобретением, могут быть произведены с помощью различных технологий, включая гибридомную технологию, технологию рекомбинантной ДНК, технологию фагового дисплея и технологии с использованием трансгенных животных, имеющих все локусы человеческих иммуноглобулинов или их часть, но не ограничиваясь ими; данные способы и другие приведенные в качестве примера способы производства моноклональных антител описаны в данном документе.
"Фрагмент антитела" обозначает молекулу, отличную от интактного антитела, содержащую часть интактного антитела, связывающую антиген, с которым связывается интактное антитело. Примеры фрагментов антитела включают Fv, Fab, Fab', Fab'-SH, F(ab')2, диатела, линейные антитела, молекулы одноцепочечных антител (например, scFv) и мультиспецифические антитела, образованные из фрагментов антител, но не ограничиваются ими. Антитела scFv описаны, например, Houston, J.S., Methods in Enzymol. 203 (1991) 46-96). Кроме того, фрагменты антител содержат одноцепочечные полипептиды, обладающие характеристиками VH домена, а именно способные объединяться вместе с VL доменом, или характеристиками VL домена, а именно способные объединяться вместе с VH доменом с образованием функционального антигенсвязывающего сайта и таким образом обеспечивающие антигенсвязывающие свойства полноразмерных антител.
В данном документе "Fab фрагмент" обозначает фрагмент антитела, содержащий фрагмент легкой цепи, содержащий VL домен и константный домен легкой цепи (CL), а также VH домен и первый константный домен (СН1) тяжелой цепи. Биспецифические антитела по изобретению содержат по меньшей мере два Fab фрагмента, причем произведен обмен вариабельными участками или константными участками между тяжелой и легкой цепями второго Fab фрагмента. Вследствие обмена вариабельными участками или константными участками указанный второй Fab фрагмент также обозначается "кpoccFab (crossFab) фрагмент" или "xFab фрагмент" или "кроссовер-Fab (crossover Fab) фрагмент". Возможны два различных варианта компоновки молекулы кроссовер-Fab в составе биспецифических антител по изобретению: с одной стороны, может происходить обмен вариабельными участками между тяжелой и легкой цепями Fab, т.е. молекула кроссовер-Fab содержит пептидную цепь, состоящую из вариабельного участка легкой цепи (VL) и константного участка тяжелой цепи (СН1), и пептидную цепь, состоящую из вариабельного участка тяжелой цепи (VH) и константного участка легкой цепи (CL). Такая молекула кроссовер-Fab также обозначается кpoccFab (vlvh). С другой стороны, когда происходит обмен константными участками между тяжелой и легкой цепями Fab, молекула кроссовер-Fab содержит пептидную цепь, состоящую из вариабельного участка тяжелой цепи (VH) и константного участка легкой цепи (CL), и пептидную цепь, состоящую из вариабельного участка легкой цепи (VL) и константного участка тяжелой цепи (СН1). Такая молекула кроссовер-Fab также обозначается кpoccFab(CLCH1).
В одном воплощении указанные Fab фрагменты соединены при помощи пептидного линкера. "Соединены" означает, что Fab фрагменты связаны посредством пептидных связей, либо напрямую, либо при помощи одного или более пептидных линкеров.
Термин "пептидный линкер", используемый в изобретении, обозначает пептид с аминокислотной последовательностью, которая предпочтительно имеет искусственное происхождение. Эти пептидные линкеры по изобретению используются для соединения одного из Fab фрагментов с С- или N-концом другого Fab фрагмента с образованием мультиспецифического антитела по изобретению. Предпочтительно, указанные пептидные линкеры являются пептидами с аминокислотной последовательностью длиной по меньшей мере 5 аминокислот, предпочтительно длиной от 5 до 100, более предпочтительно от 10 до 50 аминокислот. В одном воплощении указанный пептидный линкер представляет собой (GxS)n или (GxS)nGm, где G=глицин, S=серин, а (х=3, n=3, 4, 5 или 6, и m=0, 1, 2 или 3) или (х=4, n=2, 3, 4 или 5, и m=0, 1, 2 или 3), предпочтительно х=4 и n=2 или 3, более предпочтительно х=4, n=2. Кроме того, линкеры могут содержать (часть) шарнирный(ого) участок(ка) иммуноглобулина. В одном воплощении указанный пептидный линкер представляет собой (G4S)2 (SEQ ID: NO 28). Другими пептидными линкерами, подходящими для соединения Fab фрагментов, являются, например, (G4S)6-GG (SEQ ID NO:147) или (SG3)2-(SEG3)4-(SG3)-SC (SEQ ID NO:148) или EPKSC(D)-(G4S)2 (SEQ ID NO 145 и 146).
Термин "антигенсвязывающий домен" обозначает часть антигенсвязывающей молекулы, содержащую область, которая специфически связывается и является комплементарной целому антигену или его части. В случаях, когда антиген имеет большие размеры, антигенсвязывающая молекула может связывать только отдельную часть антигена, которая называется эпитопом. Антигенсвязывающий домен может быть образован, например, одним или несколькими вариабельными доменами антитела (также называемыми вариабельными участками антитела). Предпочтительно, антигенсвязывающий домен содержит вариабельный участок легкой цепи антитела (VL) и вариабельный участок тяжелой цепи антитела (VH).
Термин "вариабельный участок" или "вариабельный домен" обозначает домен легкой или тяжелой цепи антитела, задействованный в связывании антитела с антигеном. Вариабельные домены тяжелой и легкой цепей нативного антитела (VH и VL, соответственно), как правило, имеют схожую структуру, каждый домен содержит четыре консервативных каркасных участка (FR) и три гипервариабельных участка (HVR) (См., например, Kindt et al. Kuby Immunolo