Способ диагностики у детей функционального расстройства желудка и 12-перстной кишки, ассоциированного с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, техногенного происхождения
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к лабораторной диагностике. Для диагностики у детей функциональных расстройств желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, производят отбор пробы крови и устанавливают в ней содержание хрома, никеля, марганца и наличие хлороформа и тетрахлорметана. Выявляют нарушения функционального состояния вегетативной регуляции, биллиарного тракта, печени, желудка и 12-перстной кишки. Определяют в сыворотке крови уровень пепсиногена-1, пепсиногена-II, дофамина, серотонина, кортизола и тиреотропного гормона ТТГ. При повышении уровня пепсиногена-II на 20%, уровня кортизола на 10-15%, уровня ТТГ на 10% и снижении уровня пепсиногена-I на 15%, дофамина на 20%, серотонина на 15% диагностируют наличие функциональных расстройств желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца, хлороформа и тетрахлорметана, техногенного происхождения. Способ позволяет диагностировать у детей функциональные расстройства желудка и 12-перстной кишки, ассоциированные с воздействием хрома, никеля, марганца, хлороформа и тетрахлорметана, техногенного происхождения. 4 табл.
Реферат
Изобретение относится к области медицины, экологии, токсикологии, в частности, к способам лабораторной диагностики токсического действия хрома, никеля, марганца и хлорорганических соединений (далее - ХОС): хлороформа и тетрахлорметана, в виде проявления хронических воспалительно-дегенеративных заболеваний желудочно-кишечного тракта (далее - ХВДЗ ЖКТ), а именно: функциональные расстройства желудка и 12-перстной кишки (код согласно Международной классификации болезней 10-го пересмотра - МКБ-10: К-31.9) (1 уровень), у детей, проживающих в условиях техногенной нагрузки среды обитания.
Изобретение может быть использовано для выявления токсических функциональных расстройств желудка и 12-перстной кишки, ассоциированных с воздействием указанных металлов и ХОС при поступлении с атмосферным воздухом и питьевой водой, для последующего проведения в отношении таких детей определенно направленных лечебно-профилактических мероприятий.
По классическому определению функциональные расстройства желудка и 12-перстной кишки обусловлены нарушением регуляции между нервной системой кишечника и центральной нервной системой (http://mcpulse.ru/gastroenterologiya/funktsionalnye-narusheniya/129-funktsionalnye-rasstrojstva-zheludka-i-12-perstnoj-kishki).
Среда обитания промышленных городов характеризуется многосредовым загрязнением химическими веществами, в том числе, тяжелыми металлами (чаще возможен ингаляционный путь поступления металлов в организм ребенка), а также хлорорганическими соединениями (хлороформ и тетрахлорметан поступают в организм с питьевой водой).
Хронические воспалительные болезни ЖКТ - наиболее часто встречающиеся заболевания детского возраста. Выявляемость хронических заболеваний желудка и 12-перстной кишки у детей регионов РФ увеличилась за последние 5 лет на 48,2% и в структуре детской гастроэнтерологическая патология регистрируется у 100-150 на 1000 детей. Получены новые данные, указывающие, что патологический процесс у детей носит сочетанный характер поражения, распространяется с желудка на 12-перстную кишку. Особенностью хронических заболеваний ЖКТ у детей на современном этапе является высокая частота сочетанной патологии (70-80% случаев) с преобладанием дисфункциональных расстройств билиарного тракта, что является одним из факторов, влияющих на торпидность патологического процесса.
Одной из причин, определяющих рост и формирование особенностей течения хронических гастродуоденальных заболеваний, является воздействие опасных химических факторов среды обитания, прежде всего, металлов (хром, никель, марганец) и хлорорганических соединений. По статистическим данным в 2013-2014 г.г. марганец и его соединения относились к ведущим загрязнителями атмосферного воздуха, (превышающие ПДКс.с. в 5 и более раз), а никель и хром - к стабильно присутствующим на уровне 1,3-1,5 ПДКс.с. Среди основных загрязнителей питьевой воды особое внимание уделяется тригалометанам (хлороформ, тетрахлорметан и др.), стабильно регистрирующимся в 8-13% проб питьевой воды в концентрациях в 2-8 раза выше гигиенических нормативов. Опасность хронического воздействия загрязняющих веществ, указывающая на вероятность поражения органов ЖКТ, при многосредовом поступлении (с питьевой водой и атмосферным воздухом) для соединений хрома6+, марганца по суммарному индексу составляет от 1,41 до 3,65. А комплексное воздействие химических соединений (металлы и хлорорганические соединения) обуславливает возникновение дополнительных случаев заболеваний желудка и 12-перстной кишки на уровне 18% в год.
Действующие методы диагностики хронических воспалительно-дегенеративных заболеваний верхних отделов ЖКТ не учитывают влияния химических факторов риска на возникновение и течение заболевания, что ограничивает их возможности и не позволяет адекватно оценивать тяжесть процесса и вероятность его прогрессирования, развитие осложнений в старших возрастных группах и повышает риск инвалидизации. В связи с этим, является актуальным научное обоснование и разработка технологии ранней диагностики у детей с ХВДЗ ЖКТ, обусловленных воздействием опасных химических факторов.
Из уровня техники известен ряд технических решений, представляющих собой способы диагностики заболевания ЖКТ. Но большинство из них характеризует диагностику, наряду с заболеванием 12-перстной кишки, уже и наличие язвенной болезни, т.е. уже на стадии, вплотную переходящей в хронический гастродуоденит. И был установлен только один патент по диагностике функционального расстройства желудка у детей.
Так, известен способ диагностики стадий язвенной болезни желудка и 12-перстной кишки путем определения эпителиального индекса слизистой оболочки желудка, являющегося отношением количества всех эпителиальных клеток к количеству остальных клеток (Патент РФ №2098814). Основным недостатком этого метода является большая трудоемкость его (необходимо подсчитать все имеющиеся в наличии клетки в квадратном миллиметре среза слизистой оболочки желудка), а также невысокая специфичность, что определяется большим количеством разнообразных клеток, влияющих на величину ЭИ.
Известен способ диагностики язвенной болезни желудка и 12-перстной кишки путем определения в желудочном соке молекул средней массы (МСМ). Если величина содержания МСМ находится в пределах 0,82-1,42 единиц оптической плотности (ЕОП) на длине волны 254 нм и 0,8-1,52 на длине волны 280 нм, то по этому показателю судят о наличии язвенного дефекта слизистой оболочки и обострении заболевания (Патент РФ №2051388). Основными недостатками данного метода являются: невозможность на его основе дифференцировать все стадии язвенной болезни (обострение, неполную ремиссию и ремиссию), а также то, что он неприемлем в качестве скрининг-теста т.е. для быстрого обследования большого количества людей, что особенно важно в условиях поликлиники.
Из Патента РФ №2228525 известен способ диагностики стадий язвенной болезни желудка и 12-перстной кишки, который заключается в том, что в слюне обследуемых пациентов определяют величину содержания пептидов и при ее значении 0,882 единиц оптической плотности (ЕОП) и выше судят об обострении язвенной болезни; при ее значении в пределах 0,881-0,539 ЕОП - о стадии неполной ремиссии; при значении в пределах 0,538-0,359 ЕОП - о стадии стойкой ремиссии. Величина содержания пептидов менее 0,358 ЕОП свидетельствует о том, что больной не страдает язвенной болезнью. Его недостатком является то, что способ не учитывает содержание у пациента токсичных металлов и ХОС в биологических средах, повышенный уровень которых обуславливает повышение степени тяжести патологического процесса, а следовательно, предложенные критерии не будут адекватно отражать стадию течения язвенной болезни в условиях многосредового воздействия металлов и ХОС.
Согласно известному способу диагностики патологии желудочно-кишечного тракта больного (Патент РФ №2098819), производят забор крови, разведение ее и контрольного образца в физрастворе до эталонной концентрации эритроцитов, воздействие на пробы соляной кислотой с последующим определением в установленные промежутки времени значений оптической плотности исследуемой и контрольной проб, по которым делают вывод о процентной концентрации эритроцитов, разделяя их на характерные группы по стойкости к гемолитическому воздействию соляной кислоты: повышенно-, пониженно-, среднестойкие, и по ним судят о состоянии желудочно-кишечного тракта, до воздействия на пробы крови соляной кислотой производят инкубацию их с лектинами в дозах пороговой концентрации, не вызывающей агглютинации эритроцитов, и о состоянии желудочно-кишечного тракта больного судят следующим образом: увеличение процентной концентрации повышенно стойких эритроцитов указывает на ранние признаки язвенно-эрозивных повреждений слизистой оболочки, увеличение процентной концентрации пониженно стойких эритроцитов указывает на ремиссию заболевания.
Однако данный известный способ приемлем только при исследовании больного в стадии открытой язвы при высокой активности воспалительного процесса. Способ не дает представления о доклинических лабораторных признаках ухудшения состояния больного, не обладает диагностической значимостью для определения индивидуальной чувствительности больного к развитию язвенной болезни двенадцатиперстной кишки и его нельзя применять для определения групп риска развития язвенной болезни.
Из уровня техники (Патент РФ №2110797) известен способ диагностики нарушений функционального состояния желудка у детей раннего возраста, согласно которому проводят путем однократного забора желудочного содержимого и определения уровня связанной N-ацетилнейраминовой кислоты во фракции нерастворимой слизи. Если уровень N-ацетилнейраминовой кислоты 17,8 мкмоль/дм3 и ниже, диагностируют дуоденогастральной рефлюкс, указывающий на функциональное расстройство желудка. Его недостатком является то, что метод требует достаточно жестких показаний к проведению гастродуоденального зондирования, потенциально опасен по возможности распространения ротовирусных инфекций, не применим в качестве скрининг-теста.
При этом из уровня техники не были выявлены известные способы диагностики функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, техногенного происхождения, поэтому сделать выбор ближайшего аналога к заявляемому объекту не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в создании информативного и доказательного способа диагностики у детей функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца, хлороформа и тетрахлорметана, техногенного происхождения, позволяющего в последующем назначить адекватную терапию и предупредить развитие осложнений.
Указанный технический результат достигается предлагаемым Способом диагностики у детей функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, техногенного происхождения, заключающемся в том, что у ребенка производят отбор пробы крови и устанавливают в ней содержание хрома, никеля, марганца и наличие хлороформа и тетрахлорметана, и при повышенном содержании в крови указанных металлов, по сравнению с референтным уровнем, в 1,5-2,0 раза, а также при наличии в крови хлороформа и тетрахлорметана выше нижнего предела обнаружения, определяют состояние вегетативной регуляции; функциональное состояние билиарного тракта; ультразвуковое исследовании печени и моторной функции желудка и 12-перстной кишки, и далее, при наличии нарушения вегетативной регуляции, т.е. при наличии у ребенка ваготонического исходного вегетативного тонуса и гиперсимпатикотонической реактивности; при функциональном состоянии биллиарного тракта, характеризующемся спазмом сфинктеров Одди, Люткенса; при реактивном изменении печени и при нарушении моторной функции желудка и 12-перстной кишки по гиперкинетическому типу с наличием дуоденогастрального рефлюкса, осуществляют исследование путем определения в сыворотке крови ребенка следующих лабораторных показателей: уровень пепсиногена-I, пепсиногена-II, дофамина, серотонина, кортизола и тиреотропного гормона ТТГ, и при наличии следующих отклонений: превышение относительно физиологической возрастной нормы уровня пепсиногена-II на 20%; уровня кортизола на 10-15%; уровня ТТГ на 10%; и снижения уровня пепсиногена-I на 15%; дофамина на 20%; серотонина на 15%; диагностируют наличие функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца, хлороформа и тетрахлорметана, техногенного происхождения.
Следует указать, что заболеваемость детского населения (на примере территорий Пермского края) болезнями органов пищеварения (БОП) за последние 15 лет увеличилась в 3,4 раза и на 1 января 2014 г. составила , при этом ее прогнозный уровень к 2018 г. составил 190,0%.
Для понимания существа вопроса, следует пояснить, что проблема оценки влияния промышленного загрязнения окружающей среды на здоровье детского населения является актуальной для многих стран мира, в том числе и для России. Детская популяция представляет собой группу высокого риска, так как дети имеют ряд физиологических особенностей, характеризуются наличием критических периодов развития, большей чувствительностью к влиянию токсичных веществ.
При воздействии химических соединений в первую очередь, страдают неспецифические звенья защитных систем, в частности, иммунная и биохимическая системы, обеспечивающие поддержание гомеостаза. Комплекс биохимических реакций, направленных на метаболизм и трансформацию токсических соединений экзо-генного происхождения, определяет развитие адаптационно-компенсаторных процессов. Нарушение согласованности этапов биотрансформации, являясь одним из общих механизмов эндогенной интоксикации, способствует поддержанию воспаления и дисрегенерации при гастроэнтерологических заболеваниях.
Механизм повреждающего действия металлов: хрома, никеля, марганца, и ХОС является сложным и неоднозначным. Выделяют общие патоморфологические механизмы их реализации на клеточно-молекулярном уровнях: генотоксический, ферментотоксический и мембранотоксический. Мембранная концепция исходит из предпосылки, что металлы и ХОС обладают сильными прооксидантными свойствами. Развитие хронических заболеваний ЖКТ у детей сопровождается повреждением тканей вследствие избыточного образования в них активных форм кислорода, основным источником которых в гастродуоденальной зоне являются полиморфноядерные лейкоциты, инфильтрирующие слизистую оболочку желудка и 12-перстной кишки. Снижение активности системы антиоксидантной защиты способствует повышению активности свободнорадикальных процессов и усиленному образованию токсических продуктов, вызывающих мембранодеструктивный эффект и освобождение медиаторов воспаления. Перекисное окисление липидов катализируется ионами металлов с переходной валентностью (никель, хром, марганец и др.), что на фоне снижения антиокислительной защиты приводит к повышению уровня малонового диальдегида и снижению фракции восстановленного глутатиона и, в конечном итоге, приводит к мембранопатологическим процессам. Результатом мембрано- и ферментопатологического действия металлов является нарушение функции митохондрий, приводящее к снижению продукции макроэргов, падению активности АТФ-зависимых ферментных систем. Металлы являются сильными повреждающими агентами для эпителия тонкой кишки, вызывающими деградацию и хронический воспалительный процесс. Деструктивные изменения гастродуоденальных эпителиоцитов и нарушение процессов активного транспорта и энергообеспечения обуславливают нарушение инкреторной и секреторной функций желудка и 12-перстной кишки.
Благодаря тому, что в предлагаемом способе используют информацию о содержании хрома, никеля, марганца, хлороформа и тетрахлорметана в крови ребенка и заявляемые конкретные функциональные, инструментальные и лабораторные совокупные показатели, характеризующие специфическое техногенное происхождение функционального расстройства желудка и 12-перстной кишки, клиническая значимость которых доказана методом корреляционно-регрессионного анализа, обеспечивается дополнительная информационная связь изменений указанных лабораторных показателей с определенным, заявляемым превышением над референтным уровнем содержания в крови указанных металлов и ХОС, что делает предлагаемый способ точным и достоверным.
Кроме того, результаты испытаний показали, что для установления точного диагноза о возникновении функционального расстройства желудка и 12-перстной кишки, ассоциированной с внешнесредовым токсическим воздействием указанных металлов и ХОС техногенного происхождения, достаточно, чтобы у ребенка наблюдалось изменение указанных лабораторных показателей в следующих пределах: превышение относительно физиологической возрастной нормы уровня пепсиногена-II на 20%; уровня кортизола на 10-15%; уровня ТТГ на 10%; и снижения уровня пепсиногена-I на 15%; дофамина на 20%; серотонина на 15%, что было подтверждено параметрами модели.
Исследования показали, что достоверная корреляция между указанными лабораторными показателями и концентрацией хрома, никеля, марганца в крови достигается только при повышенном, по сравнению с референтным уровнем, содержанием в 1,5-2,0 раза, и при одновременном наличии в крови хлороформа и тетрахлорметана выше нижнего предела обнаружения (Предел обнаружения в химическом анализе - минимальное содержание определяемого вещества в пробе, сигнал от которого можно надежно отличить от фона, https://ru.wikipedia.org/wiki/).
При более низкой или более высокой концентрации указанных ксенобиотиков в пробе крови достоверная связь между этой концентрацией и лабораторными показателями в отношении функционального расстройства желудка и 12-перстной кишки не выявлена. Это, по-видимому, обусловлено тем, что указанные металлы при их содержании в крови ниже указанной цифры не оказывает повреждающее действие на ЖКТ, а при более высокой их концентрации будут происходить качественные изменения в аппарате ЖКТ, что приводит к появлению более тяжелой формы заболевания.
Переход к установлению указанных выше лабораторных показателей и их отклонению от физиологической нормы необходим только в том случае, если предварительно выявлено у ребенка наличие нарушения вегетативной регуляции, т.е. при наличии у ребенка ваготонического исходного вегетативного тонуса и гиперсимпатико-тонической реактивности; при функциональном состоянии билиарного тракта, характеризующемся спазмом сфинктеров Одди, Люткенса; при реактивном изменении печени и при нарушении моторной функции желудка и 12-перстной кишки по гиперкинетическому типу с наличием дуоденогастрального рефлюкса.
Это объясняется тем, что наличие нарушений в состоянии вегетативной регуляции; в функциональном состоянии билиарного тракта; в изменении печени и в моторной функции желудка и 12-перстной кишки, являются дополнительным маркером именно функционального расстройства желудка и 12-перстной кишки и указывает на ведущую роль в патогенезе патологического процесса повышенного содержания в крови хрома, никеля, марганца и указанных ХОС.
Таким образом, предлагаемый способ позволяет диагностировать с достаточной точностью функциональное расстройство желудка и 12-перстной кишки у детского населения, обусловленные токсическими эффектами воздействия указанных металлов и ХОС. Все это позволит повысить эффективность медикаментозного лечения и профилактики детей с точным диагнозом, обеспечить конкретное планирование санитарно-гигиенических мероприятий по предупреждению и устранению воздействия вредных химических веществ, обуславливающих экологически обусловленную патологию у детского населения.
Исходя из вышеизложенного, можно сделать вывод, что поставленный технический результат обеспечивается за счет совокупности всех операций предлагаемого способа, их последовательности и режимов его реализации.
При практической реализации предлагаемого способа осуществляют следующие операции в нижеуказанной последовательности:
1. Выбирают экологически неблагополучную территорию по высокой нагрузке химических факторов среды обитания. При этом указанную территорию выбирают в отношении детского населения в возрасте 8-12 лет, проживающего на этой территории, которая характеризуется:
- повышенным уровнем заболеваемости детей (выше регионального и/или среднероссийского) гастродуоденальной патологией (МКБ-10: К-31.9). Для формирования контингента детей, страдающих хроническими воспалительно-дегенеративными заболеваниями верхних отделов желудочно-кишечного тракта (ЖКТ) (МКБ-10: К-31.9), проводится ретроспектный анализ фактической заболеваемости по данным обращаемости за медицинской помощью. Выделяются группа детей в возрасте 8-12 лет (наиболее уязвимая возрастная группа по первичной манифестации исследуемых нозологических форм) с частотой обращаемости за медицинской помощью два и более раза в год;
- загрязнением атмосферного воздуха (на примере металлов) и воды хозяйственно-питьевого водоснабжения (на примере хлорорганических соединений) в концентрациях, превышающих гигиенические нормативы и определяющих основной вклад в формирование неприемлемого риска заболеваний ЖКТ; При этом исследование качества атмосферного воздуха и питьевой воды проводится согласно Постановлению правительства РФ от 02.02.2006 г. №60 «Положение о проведении социально-гигиенического мониторинга с изменениями от 04.09.2012 г.,
- наличием неприемлемого риска развития патологии (HI>1,0) верхних отделов ЖКТ, ассоциированной с аэрогенной экспозицией указанных металлов и пероральной экспозицией ХОС, дисфункция которых лежит в основе формирования функционального расстройства желудка и 12-перстной кишки. Оценка риска развития указанных заболеваний (МКБ-10: К-31.9) осуществляется по стандартизованной методике в соответствии с «Руководством по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду» (Р 2.1.10.1920-04);
2. Далее проводятся исследования, включающие комплекс традиционных клинических исследований (анализ наследственности, генетических и анамнестических данных, особенностей клинического течения, клинические признаки гастроинтестинального синдрома с гиперкинетическим вариантом моторных нарушений, билиарных дисфункций по гипокинетическому типу, диспепсического синдрома, астено-невротических расстройств с преобладанием парасимпатической симптоматики, признаков вариабельного иммунодефицита), с целью установления детей, страдающих заболеваниями верхних отделов ЖКТ (МКБ-10: К-31.9).
Этот диагноз ставится тогда, если выражены умеренно: клинические признаки гастроинтестинального синдрома с гиперкинетическим вариантом моторных нарушений; клинические признаки билиарных дисфункций по гипокинетическому типу и диспепсический синдром.
3. У каждого такого ребенка производят отбор пробы крови и устанавливают в ней содержание хрома, никеля, марганца и наличие хлороформа и тетрахлорметана.
4. При повышенном содержании в крови указанных металлов, по сравнению с референтным уровнем, в 1,5-2,0 раза, а также при наличии в крови хлороформа и тетрахлорметана выше нижнего предела определения, определяют состояние вегетативной регуляции; функциональное состояние билиарного тракта; ультразвуковое исследовании печени и моторной функции желудка и 12-перстной кишки.
5. Наличие у детей функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений (хлороформа и тетрахлорметана), диагностируют при отклонении относительно возрастной физиологической нормы следующих показателей (т.е. отклонения принимают в качестве диагностических критериев):
- нарушение вегетативной регуляции, т.е. наличие ваготонического исходного вегетативного тонуса и гиперсимпатикотонической реактивности;
- отклонение в функциональном состоянии билиарного тракта, характеризующемся спазмом сфинктеров Одди, Люткенса;
- наличие реактивного изменения печени;
- нарушение моторной функции желудка и 12-перстной кишки по гиперкинетическому типу с наличием дуоденогастрального рефлюкса;
- превышение относительно физиологической возрастной нормы уровня пепсиногена-II на 20%; уровня кортизола на 10-15%; уровня ТТГ на 10%;
- снижение уровня пепсиногена-I на 15%; дофамина на 20%; серотонина на 15%.
В качестве критериев оценки отклонений лабораторных показателей используются возрастные физиологические уровни, для содержания хрома, никеля, марганца - референтные уровни (Н. Тиц, 2003), для содержания ХОС - предел обнаружения в соответствии с методом определения ХОС в крови (МУК 4.1.2115-06 «Определение массовой концентрации хлороформа, 1,2-дихлорэтана, тетрахлорметана в биосредах (кровь) методом газохроматографического анализа равновесного пара»).
Основными методами исследований при реализации предлагаемого способа являлись:
- санитарно-гигиенические: сравнительный анализ мониторинговых наблюдений; пространственно-временной анализ в среде ГИС с использованием программы УПРЗА «Эколог», версия 3.0 и «Эколог-средние» - 15 моделей по 3 элементам на площадке из 65000 точек; расчет коэффициентов и индекса опасности для 5 компонентов (Руководство по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду: Руководство 2.1.10.1920-04.М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. 143 с.); эпидемиологические методы с использованием одномерного статистического анализа и построением трендовой модели с динамическим экспоненциальным сглаживанием (Четыркин Е.М. Статистические методы прогнозирования. М.: Статистика. 1977. 356 с.);
- диагностические: клинические, функциональные и инструментальные (кардиоинтервалография, электроэнцефалография, ультразвуковое исследование УЗИ); лабораторные (общеклинические - гематологические показатели; биохимические - показатели окислительно-антиоксидантных процессов (в сыворотке крови), ферментативной активности, обмена железа, воспалительных реакций (в сыворотке крови); иммуно-аллергологические - показатели клеточного, гуморального, специфического иммунитета; иммуноферментные - показатели обмена нейромедиаторов) (Медицинские лабораторные технологии и диагностика: справочник. Медицинские лабораторные технологии в 2-х томах / Под ред. А.И. Карпищенко. С-Пб: Интермедика, 2002. 408 с.);
- химико-аналитические методы исследования (газовая хроматография на газовом хроматографе Хроматэк-Кристалл-500, масс-спектрометрия с индуктивно связанной плазмой на масс-спектрометре Agilent 7500сх).
Для доказательства правомерности применяемых в предлагаемом способе диагностических критериев был использован корреляционный анализ между полученными функциональными и лабораторными показателями и содержанием хрома, никеля, марганца, хлороформа и тетрахлорметана в крови ребенка с использованием модели логистической регрессии, согласно которой рассчитывают вероятность негативного изменения маркера ответа организма (вышеуказанные лабораторные показатели) при воздействии на организм маркера экспозиции (указанных токсикантов). Выявление и оценку связи между изменением лабораторных показателей у детей и концентрацией указанных токсикантов в крови выполняется на основании расчета показателя отношения шансов (OR) и его доверительного интервала (ДИ). Критерием наличия связи «концентрация хрома, никеля, марганца, хлороформа и тетрахлорметана в крови - показатель ответа» является OR≥1. Обоснование маркеров ответа осуществляется на основании оценки параметров зависимости изменения показателя отношения шансов от концентрации этих металлов и ХОС в крови, описываемой регрессионной моделью в виде экспоненциальной функции. В качестве критерия для проверки статистических гипотез используется критерий Фишера (F). Различия считаются статистически значимыми при вероятности p≤0,05.
Пример конкретной реализации предлагаемого способа: 1. Способ был апробирован на экологически неблагоприятной территории г. Чусового Пермского края. Заболеваемость детского населения г.Чусовой болезнями органов пищеварения (далее - БОП) за последние 15 лет увеличилась с 69,84% до 241,52% и с 2005 г. И превышала среднекраевой в 1,2 раза.
Данные натурных наблюдений свидетельствуют о превышении гигиенических нормативов в атмосферном воздухе жилой застройки по марганцу, никелю, хрому на уровне 1,3-1,5 ПДКс.с. Расчетные концентрации загрязняющих веществ на участках селитебной территории составляют 1,8-2,2 ПДКс.с. В зонах экспозиции при этом находится около 1,5 тыс. детей.
Источниками питьевого водоснабжения населения г.Чусовой является вода поверхностных водоемов. Результаты мониторинговых наблюдений качества питьевой воды свидетельствуют о превышении гигиенических нормативов по содержанию преимущественно хлороформа в среднем до 2,5-2,8 ПДК (максимум до 5,3-7,3 ПДК) и тетрахлорметана - до 2,1 ПДК. Доля нестандартных проб составляет 52,5%-100%.
Расчет коэффициентов и индекса опасности при хронической многосредовой экспозиции с атмосферным воздухом и питьевой водой изучаемыми химическими факторами выявил недопустимый риск поражения центральной нервной системы (ЦНС) и гепато-билиарной системы, дисфункциональные нарушения которых инициируют развитие ХВДЗ ЖКТ, превышающий приемлемый уровень (HQ=1) в 27-44 раза по металлам и в 2,4 раза - по ХОС. Одновременное поступление данных загрязнений увеличивает риск поражения критических систем (HI=29-46). Долевой вклад металлов составляет 95%, ХОС - 5%.
2. Для обоснования у детей критериев диагностики функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, было проведено анамнестическое, клиническое, функциональное и лабораторное обследование. Группу наблюдения составили 350 человек в возрасте 8-12 лет с установленным ранее диагнозом заболевание верхних отделов ЖКТ (МКБ-10: К-31.9) вне обострения (47% мальчиков и 53% девочек), проживающих постоянно на выбранной территории Пермского края. Группу сравнения составили 250 детей в возрасте 8-12 лет (49% мальчиков и 51% девочек) с предварительным диагнозом заболевание верхних отделов ЖКТ (МКБ-10: К-31.9) в периоде ремиссии, проживающие в условиях санитарно-гигиенического благополучия.
При анализе медико-социальных анкет достоверных различий между группами по социальным показателям не выявлено.
3. В ходе химико-аналитического исследования у детей группы наблюдения установлено присутствие в крови хрома (0,0211±0,0030 - 0,0239±0,0012 мг/дм3), никеля (0,000075-0,0001 мг/дм3), марганца (0,019±0,005 г/дм3), в концентрациях, превышающих референтный уровень в 1,5-2,0 раза, и наличие хлороформа и тетрахлорметана выше нижнего предела определения (НПО), которые отсутствовали у детей сравниваемой группы (р=0,001-0,009). Данные о содержании токсикантов в крови обследованных детей приведены в таблице 1.
Выявление и оценка параметров зависимости «доза загрязняющего вещества - концентрация токсиканта в биосреде» позволили получить адекватные модели зависимости (критерий Фишера F≥3,96; p≤0,05) между суточной дозой металлов и указанными хлорорганических соединений и их концентрацией в крови, описываемые линейными уравнениями (F=17,54-1323,17; коэффициент детерминации R2=0,42-0,71; p=0,0001).
Проведенные исследования показали, что клинические проявления функционального расстройства желудка и 12-перстной кишки у детей группы наблюдения не соответствуют классическим представлениям: с увеличением уровня контаминации биосред снижается выраженность субъективной гастроэнтерологической симптоматики (отношение шансов OR=2,83-4,20; доверительный интервал DI=2,1-4,8), только у 5,88±1,19% детей группы наблюдения имело место сочетание шести и более патогномоничных гастроинтестинальных симптомов, а в группе сравнения такое сочетание отмечено у каждого пятого ребенка (OR=4,41; DI=0,8-5,2).
В клинической картине функционального расстройства желудка и 12-перстной кишки у детей группы наблюдения (p<0,0001) превалируют признаки эндогенной интоксикации (OR=2,89; DI=2,2-3,8), вегетативных дисфункций (OR=1,44; DI=1,2-2,5), поражения сердечно-сосудистой системы (OR=1,84; DI=1,3-2,9), пролиферации лимфоидной ткани (OR=2,16; DI=1,8-2,9).
В группе наблюдения комплекс симптомов, характеризующий поражение гепатобилиарной системы, регистрировался в 2 раза чаще (p≤0,05), чем в группе сравнения (OR=2,03), реактивные изменения печени - в 1,5 раза (OR=2,04; DI=1,3-3,0). В качестве триггеров возникновения функционального расстройства желудка и 12-перстной кишки у детей группы наблюдения чаще выступают внешнесредовые факторы (p≤0,003) относительно группы сравнения: проживание в центральных районах (OR=4,59; DI=3,8-5,6), близость от места жительства промышленных предприятий (OR=2,89; DI=2,2-3,7), отсутствие оздоравливающих мероприятий и полноценного отдыха (OR=3,99; DI=3,2-4,7).
4. Далее, с целью установления достоверности диагностики функционального расстройства желудка и 12-перстной кишки, ассоциированных с воздействием хрома, никеля, марганца и хлорорганических соединений: хлороформа и тетрахлорметана, техногенного происхождения, по предлагаемому способу, все дети проходили следующие обследования:
- состояния вегетативной регуляции;
- функциональное состояние билиарного тракта;
- ультразвуковое исследовании печени;
- моторной функции желудка и 12-перстной кишки;
и далее, при наличии нарушения вегетативной регуляции, т.е. при наличии у ребенка ваготонического исходного вегетативного тонуса и гиперсимпатикотонической реактивности; при функциональном состоянии билиарного тракта, характеризующемся спазмом сфинктеров Одди, Люткенса; при реактивном изменении печени и при нарушении моторной функции желудка и 12-перстной кишки по гиперкинетическому типу с наличием дуоденогастрального рефлюкса, осуществляют дополнительное обследование путем установления в сыворотке крови следующих лабораторных показателей: уровня пепсиногена-I, пепсиногена-II, дофамина, серотонина, кортизола и тиреотропного гормона (ТТГ). При выполнении условия: превышение относительно физиологической возрастной нормы уровня пепсиногена-II на 20%; уровня кортизола на 10-15%; уровня ТТГ на 10%; и снижение уровня пепсиногена-I на 15%; дофамина на 20%; серотонина на 15%, диагностируют у ребенка наличие функционального расстройства желудка и 12-перстной кишки, ассоциированное с воздействием хрома, никеля, марганца и хлорорганических соединений (хлороформа и тетрахлорметана) техногенного происхождения.
При проведении исследований в ходе УЗИ сканирования гастродуоденальной области регистрировалось наличие натощак в желудке умеренного количества жидкости, как признака гиперсекреции, в 3 раза чаще в группе наблюдения относительно группы сравнения (33% и 11% соответственно, р=0,003).
Физиологический вариант моторной функции желудка и 12-перстной кишки определялся у детей группы наблюдения в 2 раза реже (14%), чем в группе сравнения (28%, р=0,03). Доминирующим типом нарушений являлось наличие дуодено-гастрального рефлюкса, которое регистрировалось в группе наблюдения в 1,5 раза чаще (р=0,04), чем в группе сравнения (OR=1,41-1,52; DI=1,12-3,87). Ускорение прохождение содержимого из желудка в 12-перстной кишку установлено только у детей в группе наблюдения (р=0,03).
Установлены причинно-следственные связи повышенного содержания хрома, никеля, марганца, ХОС в крови с нарушениями моторной функции желудка и 12-перстной кишки (R2=0,25-0,52; F=46,5-119,18; р=0,01-0,001).
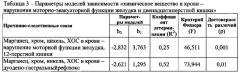
Данные о сравнительном анализе показателей моторно-эвакуаторной функции желудка и двенадцатиперстной кишки (по данным УЗИ) приведены в таблице 2; а данные о параметрах моделей зависимости «химическое вещество в крови - нарушения моторно-эвакуаторной функции желудка и двенадцатиперстной кишки» приведены в таблице 3.
Установлена связь между повышением содержания в крови тетрахлорметана, хлороформа и никеля с обнаружением желчи в желудке (R2=0,55-0,61, р=0,0002-0,004).
Оценка вегетативной реактивности показала, что у детей группы наблюдения симпатикотонический тип ответной реакции отмечался лишь в 25%, что в 1,2 раза реже, чем в группе сравнения (30%, OR=1,2; DI=1,1-1,7). Преобладающим типом реактивности являлся гиперсимпатикотонический вариант (62,5%), свидетельствующий о чрезмерном напряжении механизмов адаптации. В группе сравнения этот вариант встречался в 1,5 раза реже (OR=1,45; ДИ=1,16-3,11).
Преобладание гиперсимпатикотонической реактивности подтверждается и более высоким средним показателем отношения индексов напряжения (ИН2/ИН1), который составлял 3,43±1,11 у.е. и в 1,6 раза превышал аналогичный в группе сравнения (2,12±1,30 у.е.; р=0,011). Выявлены прямые достоверные связи между повышенным содержанием в крови марганца, хрома, никеля, ХОС и развитием исходной ваготонии и гиперсимпатикото