Способ подготовки пробы лекарственного растительного сырья для парофазного анализа
Иллюстрации
Показать всеИзобретение относится к газовой хроматографии и может быть использовано при подготовке пробы для парофазного анализа (ПФА) различного лекарственного сырья (ЛРС) в медицине, фармакологии, здравоохранении, пищевой, парфюмерной и других отраслях промышленности. Способ подготовки пробы лекарственного растительного сырья для парофазного анализа заключается в том, что фиксированное количество измельченного лекарственного растительного сырья помещают в герметичный стеклянный сосуд и выдерживают при определенной температуре. Затем равновесную паровую фазу отбирают с помощью стеклянного шприца и дозируют в испаритель газового хроматографа с пламенно-ионизационным детектором для анализа. Причем стеклянный шприц для исключения конденсации компонентов выдерживают при температуре пробы, которую определяют методом внутреннего стандарта по начальному участку постоянных значений зависимости отношения площади пиков анализируемых компонентов к площади пика стандартного наиболее летучего компонента пробы от температуры. Техническим результатом является повышение достоверного определения температуры пробы ЛРС для ПФА по начальному участку постоянных значений этой зависимости, а также обеспечение возможности исключения конденсации части компонентов на холодной поверхности стеклянного шприца. 2 ил., 1 табл.
Реферат
Изобретение относится к газовой хроматографии и может быть использовано при подготовке пробы для парофазного анализа (ПФА) различного лекарственного сырья (ЛРС) в медицине, фармакологии, здравоохранении, пищевой, парфюмерной и других отраслях промышленности.
Известно пробоотборное устройство ПФА, используемое для стандартизации ЛРС и фитопрепаратов на их основе, при котором фиксированное количество измельченного ЛРС или таблетки помещают в герметичный сосуд и выдерживают при температуре 100°С в течение 40 минут. После чего с помощью крана дозируют равновесную паровую фазу в испаритель хроматографа для анализа (см.: Арутюнов Ю.И., Онучак Л.А., Куркин В.А., Платонов И.А., Никитченко Н.В. Способ оценки подлинности лекарственного растительного сырья и устройство для его осуществления. Патент РФ №2452944 от 10 июня 2012 г. // Бюл. №16).
Известны также способы подготовки пробы различных ЛРС для ПФА при 100°С и времени выдержки 40 минут (см.: Хусаинова А.И., Куркин В.А., Онучак Л.А., Арутюнов Ю.И. Газохроматографическое исследование летучих компонентов сырья и препаратов пижмы обыкновенной. // Фармацевтические науки, №1 (7). 2015. С. 86 - 91, см. также: Павлова Л.В., Платонов И.А., Новикова Е.А., Никитченко Н.В. Хромато-масс-спектрометрический анализ эвкалипта прутовидного (Eucalipti viminalis Labill) с использованием различных способов пробоподготовки // Аналитика и контроль, 2013. Т. 17. №3. С. 304-313).
Однако в известных способах подготовки пробы ЛРС для ПФА температуру пробы 100°С выбирают по качественной оценке хроматограмм, полученных при разных температурах пробы. При этом число пиков на хроматограммах с повышением температуры пробы увеличивается и используемое при измерении методом внутренней нормализации относительное содержание летучих компонентов Аотнi, %, становится не достоверной характеристикой.
где Ai - площадь пика исследуемого i-го компонента пробы; - сумма площадей пиков всех летучих компонентов пробы; N - число пиков на хроматограмме.
Наиболее близким к изобретению по совокупности существенных признаков является способ пробоподготовки для ПФА плодов и препаратов расторопши пятнистой, при котором фиксированное количество измельченного ЛРС или таблеток помещают в герметичный стеклянный сосуд объемом 15 см3 и выдерживают при 100°С в течение 40-60 мин. Затем через резиновую мембрану с помощью шприца отбирают пробу паровой фазы и дозируют в испаритель газового хроматографа для анализа с использованием капиллярной колонки с пламенно-ионизационным детектором при линейном программировании температуры колонки. Из полученных хроматограмм рассчитывают индексы удерживания Ванден-Доола и Кратца и содержание каждого компонента методом внутренней нормализации (Aomн.i, %) (см.: Онучак Л.А., Арутюнов Ю.И., Платонов И.А, Куркин В.А., Никитченко Н.В. Газохроматографические характеристики летучих веществ в плодах и препаратах расторопши пятнистой (Silybum mazianum L.) // Журн. аналит. химии, 2012. Т. 67. №6. С. 619-624).
Недостатками известного способа являются отсутствие возможности достоверного выбора температуры пробы ЛРС для ПФА и возможная конденсация некоторых компонентов пробы на холодной поверхности шприца.
Задачей изобретения является исключение возможной конденсации анализируемых компонентов пробы в шприце и повышение достоверности при выборе температуры пробы ЛРС для ПФА.
Эта задача решается за счет того, что в способе подготовки пробы ЛРС для ПФА, при котором фиксированное количество измельченного ЛРС помещают в герметичный стеклянный сосуд и выдерживают при определенной температуре, равновесную паровую фазу отбирают с помощью стеклянного шприца и дозируют в испаритель газового хроматографа с пламенно-ионизационным детектором для анализа, причем стеклянный шприц для исключения конденсации компонентов выдерживают при температуре пробы, которую определяют методом внутреннего стандарта по начальному участку постоянных значений зависимости отношения площади анализируемых компонентов к площади стандартного наиболее летучего компонента пробы от температуры.
При решении поставленной задачи создается технический результат, заключающийся в следующем:
1. Уменьшаются потери некоторых летучих компонентов, извлекаемых из лекарственного растительного сырья, за счет исключения конденсации части этих компонентов на холодной поверхности стеклянного шприца.
2. Использование метода внутреннего стандарта в виде зависимости отношения площади анализируемого компонента к площади стандартного наиболее летучего компонента от температуры пробы обеспечило возможность более достоверного определения температуры пробы ЛРС для ПФА по начальному участку постоянных значений этой зависимости.
Пример конкретного выполнения способа
Измельченное ЛРС в количестве 3 г помещают в герметичный стеклянный сосуд и выдерживают при заданной температуре от 30 до 140°С в течение 40 минут. Для каждой температуры готовят свежую пробу ЛРС для повышения достоверности результатов анализа.
Равновесную паровую фазу (РПФ) отбирают из герметичного стеклянного сосуда через резиновую мембрану, покрытую тонкой пленкой фторопласта с помощью стеклянного шприца, нагретого до температуры пробы, для исключения конденсации компонентов РПФ.
Газохроматографический анализ РПФ проводили на хроматографе «Кристалл-5000.2» ЗАО СКБ «Хроматэк» с пламенно-ионизационным детектором с использованием капиллярной колонки с неполярной полидиметилсилоксановой неподвижной фазой (VF-1, 30 м ×0,32 мм, df=0,5 мкм) фирмы Varian (США). Газохроматографический эксперимент проводили в режиме линейного программирования температуры со скоростью 4°С/мин. Начальная температура 40°С, конечная - 180°С. Газ-носитель - водород, объемная скорость на выходе из колонки 1,0 см3/мин. Избыточное давление на входе колонки 36 кПа. Пробу РПФ дозировали стеклянным шприцем в испаритель с делением потока 1:50. Объем пробы 1,0 см3. Температура испарителя 200°С, температура детектора 200°С. На основании газохроматографического эксперимента рассчитывали следующие характеристики:
I. Индексы удерживания Ван-ден-Доола и Кратса летучих компонентов РПФ, (см.: Н. van den Dool, P.D. Kratz. A generalization of the retention index system including liner temperature programmed gas-liquid partition chromatography // J. of Chromatography, 1963. V. 11. №4. P. 463-471.
где tRj - время удерживания /-го исследуемого компонента; fRz и tRz+1 - время удерживания соседних гомологов н-алканов с числом углеродных атомов в молекулах z и z+1 соответственно, причем tRz+1>tRi>tRz.
2. Относительную площадь пиков методом внутреннего стандарта, в качестве которого используют наиболее летучий компонент РПФ.
где Ai - абсолютное значение площади пика исследуемого i-го компонента РПФ; Ast - абсолютное значение площади пика наиболее летучего компонента РПФ.
Необходимость использования метода внутреннего стандарта вместо метода внутренней нормализации вызвано тем, что при изменении температуры пробы количество анализируемых компонентов РПФ не остается постоянным и достоверность определения необходимой температуры подготовки пробы ЛРС для ПФА снижается.
Метод внутреннего стандарта обеспечивает возможность повысить достоверность, так как Ai и Ast всегда присутствуют в пробе РПФ при любых температурах пробоподготовки.
Рассмотрим механизм формирования измерительного сигнала в методе внутреннего стандарта.
где Ki и Kst - константы равновесного распределения i-го компонента и стандарта между их концентрациями (С) в растении, верхний индекс (Р) и паровой фазе (П). После преобразования уравнений (3) получим
где пропорционально отношению - измерительный сигнал метода внутреннего стандарта.
Из уравнения (4) следует, что будет иметь максимальное значение при низкой температуре пробы, так как Ki>>Kst.
По мере повышения температуры пробы характер изменения Ki, будет приближаться к Kst и при какой-то определенной температуре отношение - достигнет минимума. При этом с повышением температуры пробы пропорционально увеличиваются Ai и Ast, а их отношение остается постоянным.
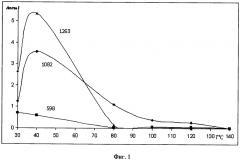
Пример 1. В качестве объекта исследования использовали воздушно-сухое сырье лекарственного растения пижма обыкновенная (Tanacetum Vulgare L.) производства ОАО «Красногорслексредства» (Россия, Московская обл., г. Красногорск). Газохроматографический анализ РПФ проводили для каждой из следующих температур подготовки пробы: 30, 40, 80, 100, 120, 140°С. Для определения индексов удерживания проводили дополнительный анализ смеси н-алканов от пентана до пентадекана включительно. Объем вводимой пробы 0,2 мкл. Из полученных хроматограмм рассчитывали индексы удерживания и и строили зависимость Аотн i=ƒ/(Тпробы). По начальному участку постоянных значений Аотн i определяли температуру пробоподготовки. В качестве примера на фиг. 1 (Зависимость относительной площади пика (Аотн i) от температуры пробы в термостате Т°С для РПФ пижмы обыкновенной) приведены такие зависимости для трех компонентов РПФ, элюирующихся в начале, середине и в конце анализа с индексами удерживания 598, 1082 и 1263. В качестве стандарта использовали наиболее летучий компонент с индексом удерживания 487. Из приведенных на фиг. 1 зависимостей видно, что температура подготовки пробы ЛРС для компонентов с индексом 598 составляет 80°С, 1082 - 100°С и 1263 - 90°С. Учитывая, что зависимость Аотн i=ƒ/(Тпробы) для большинства компонентов РПФ достигает постоянных значений при 100°С, то температура подготовки пробы лекарственного растения пижма для ПФА выбрана 100°С.
Пример 2. В качестве объекта исследования использовали ЛРС зверобоя продырявленного (Hypericum Perforatum L.) производства ОАО «Красногорслексредства» (Россия, Московская обл., г. Красногорск). Газохроматографический анализ РПФ проводили для каждой из следующих температур подготовки пробы: 60, 80, 100, 120 и 140°С. Методика проведения анализа описана в примере 1.
Из полученных хроматограмм рассчитывали и Аотн i и строили зависимости Аотн i от температуры пробоподготовки Тпробы.
В качестве примера на фиг. 2 (Зависимость относительной площади пика (Аотн i) от температуры пробы в термостате Т°С для РПФ зверобоя продырявленного) приведены зависимости Аотн i=ƒ/(Тпробы) для трех компонентов РПФ зверобоя с индексами удерживания 494, 783 и 1091. В качестве стандарта использовали летучий компонент с индексом удерживания 458. Из приведенных на фиг. 2 зависимостей выбрана температура пробоподготовки растений зверобой для ПФА, равная 85°С.
Пример 3. В этом примере приведены результаты экспериментального исследования влияния холодного стеклянного шприца на определение концентрации летучих компонентов РПФ лекарственного растения пижма обыкновенная (Tanacetum Vulgare L.). Концентрацию компонентов РПФ определяли методом внутренней нормализации по уравнению (1) как среднее значение из 10 последовательных анализов отдельно для холодного и нагретого до температуры пробы шприца. Условия газохроматографического анализа описаны в примере 1.
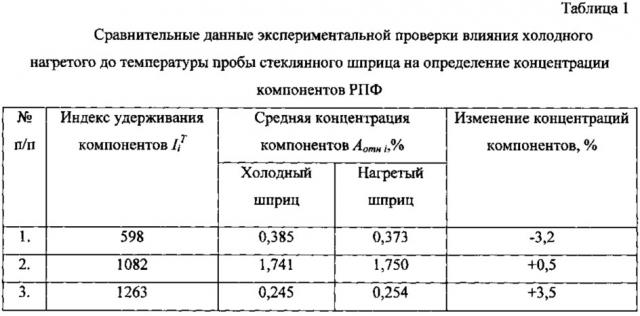
Результаты эксперимента сведены в табл. 1 «Сравнительные данные экспериментальной проверки влияния холодного и нагретого до температуры пробы стеклянного шприца на определение концентрации компонентов РПФ».
Из приведенных в табл.1 данных видно, что при дозировании РПФ в газовый хроматограф для анализа стеклянным шприцем, нагретым до температуры подготовки пробы, концентрация более тяжелых компонентов, например, с индексом удерживания 1263 увеличивается на 3,5%, а концентрация легких компонентов с индексом 598 уменьшается на 3,2% по сравнению с результатами анализа холодным шприцем. Это вызвано частичной конденсацией тяжелых компонентов РПФ на поверхности холодного шприца и измеренная концентрация тяжелых компонентов уменьшается, а концентрация легких компонентов РПФ, которые не конденсируются холодным шприцем, соответственно увеличивается с 0,373% до 0,385%.
Использование предлагаемого способа подготовки пробы лекарственного растительного сырья для парофазного анализа позволяет:
1. Проводить подготовку пробы различного лекарственного растительного сырья для парофазного анализа с повышенной достоверностью определения температуры пробы в различных отраслях промышленности.
2. Уменьшить потери при дозировании компонентов равновесной паровой фазы в испаритель хроматографа нагретым до температуры пробы стеклянным шприцем.
Способ подготовки пробы лекарственного растительного сырья для парофазного анализа, при котором фиксированное количество измельченного лекарственного растительного сырья помещают в герметичный стеклянный сосуд и выдерживают при определенной температуре, равновесную паровую фазу отбирают с помощью стеклянного шприца и дозируют в испаритель газового хроматографа с пламенно-ионизационным детектором для анализа, отличающийся тем, что стеклянный шприц для исключения конденсации компонентов выдерживают при температуре пробы, которую определяют методом внутреннего стандарта по начальному участку постоянных значений зависимости отношения площади пиков анализируемых компонентов к площади пика стандартного наиболее летучего компонента пробы от температуры.