7β-метил-3,17αβ-дисульфамоилокси-d-гомо-6-окса-эстра-1,3,5(10),8,14-пентаен в качестве ингибитора роста клеток рака молочной железы mcf-7
Иллюстрации
Показать всеИзобретение относится к 7β-метил-3,17αβ-дисульфамоилокси-D-гомо-6-окса-эстра-1,3,5(10),8,14-пентаену формулы
в качестве ингибитора роста клеток рака молочной железы МСF-7. Технический результат: получено новое соединение, которое может применяться при лечении рака молочной железы. 1 пр.
Реферат
Изобретение относится к синтезу 7β-Метил-3,17αβ-дисульфамоилокси-D-гомо-6-окса-эстра-1,3,5(10),8,14-пентаен в качестве ингибитора роста клеток рака молочной железы МСF-7 и предполагает возможность его применения в медицине.
Рак молочной железы женщин является одним из самых распространенных онкологических заболеваний [1], который часто бывает эстрогенозависимым [2]. Один из путей лечения таких заболеваний направлен на ингибирование образования свободных эстрогенов в опухоли, мишенями являются ароматаза, 17β-гидроксистероид дегидрогеназы и стероидная сульфатаза [3]. Модифицированные эстрогены с сульфаматной группой в ароматическом кольце могут одновременно ингибировать активность стероидной сульфатазы и ароматазы [4], стероидной сульфатазы и 17β-гидрок-систероид дегидрогеназы [5,6]. При взаимодействии сульфаматов эстрогенов со стероидной сульфатазой происходит необратимая дезактивация фермента с освобождением носителя сульфаматной группы [7]. Поэтому поиск новых сульфаматов проводят на основе стероидов, не имеющих гормональной активности [2].
Известно, что введение метильной группы в положение 7β эстрогенов с природным сочленением колец приводит к заметному снижению эстрогенного действия [8], однако синтез таких веществ технически сложен [8-10], поэтому их использование в качестве промежуточных соединений экономически не целесообразно. В дальнейшем исследование таких веществ было остановлено. Тем не менее, модифицированные стероиды с указанным заместителем представляют интерес для создания на их основе соединений с противоопухолевыми свойствами.
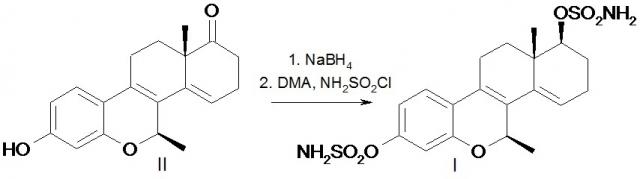
Целью изобретения является расширение группы веществ, блокирующих рост клеток рака молочной железы MCF-7. Поставленная цель достигается синтезом рацемического 7β-метил-3,17αβ-дисульфамоил-окси-D-гомо-6-окса-эстра-1,3,5(10),8,14-пентаена (I) из достаточно доступного соединения эстрапентаена (II) [11], что послужило основанием для предложенного пути синтеза.
Пример
7β-Метил-3,17αβ-дисульфамоилокси-D-гомо-6-окса-эстра-1,3,5(10),8,14-пентаен (I). К раствору 70 мг эстрапентаена (II) [10] в 3 мл тетрагидрофурана и 0.3 мл воды добавляют 15 мг борогидрида натрия, реакционную смесь перемешивают 3 ч при 20ºС, затем избыток борогидрида натрия разлагают, медленно прикапывая уксусную кислоту. Далее реакционную смесь выливают в 50 мл воды, продукты реакции экстрагируют 50 мл этилацетата, экстракт промывают равным объемом воды и сушат над сульфатом натрия. Растворитель удаляют на роторном испарителе, остаток растворяют в 2 мл диметилацетамида, раствор охлаждают смесью льда и соли, а затем в атмосфере аргона добавляют 80 мг сульфамоилхлорида. Раствор перемешивают 4 ч, после чего оставляют на 12 ч при 20°С, а затем выливают в 50 мл воды. Продукты реакции экстрагируют 50 мл этилацетата, экстракт промывают равным объемом насыщенного раствора хлористого натрия, сушат над сульфатом натрия. Растворитель удаляют на роторном испарителе, продукт реакции очищают флэш-хроматографией на силикагеле в элюирующей системе гексан-этилацетат 3:1-2.1. После кристаллизации из смеси гексан-этилацетат получают 67 мг (62%) целевого продукта (I), т.пл. > 185°С (разл.)
Спектр ЯМР 1Н (CD3CN, δ, м.д.): 7.30 д (1Н, J=8.5 Гц, Н1); 6.91 дд (1Н, J=8.5 Гц, J= 2.4 Гц, Н2), 6.79 д (1Н, J=1.8 Гц, Н4); 6.06 с (2H, C3-SO3NH2); 5.77 c (2H, C17-SO3NH2); 5.77 (1Н, Н15), 5.37 кв (1Н, J=6.4 Гц, Н7α); 4.45 дд (1H, J=12.4 Гц, J=4.1 Гц, H17аα); 2.61 (1H, H11β), 2.46 (1H, H11α), 2.41 (2H, H16); 2.19 (1H, Н17α); 2.17 (1Н, Н12β); 2.07 (1H, H17β); 1.51 ддд (J=12.6 Гц, 12.6 Гц, 5.8 Гц, H12α); 1.21 д (3Н, J=6.5 Гц, СН37β), 1.06 с (3Н, H18). Спектр ЯМР 13С (CD3CN, δ, м.д.): 152.3; 150.1 (C3, С5); 135.9 (C9); 123.9 (C1); 129.4; 123.0; 122.6 (C8, C10, С14); 120.9 (C15); 114.9, 110.4 (C2, C4); 86.6 (C17а); 70.4 (C7); 36.6 (C13); 31.9; 24.7; 23.3; 21.0 (C11, C12, C16, C17); 17.6; 16.7 (СН37β; C18). HRMS (ESI-TOF), ион [M+Na]+, [С19Н24N2О7S2Na]+: вычислено 479.0917, найдено 479.0925.
Спектры ЯМР 1Н снимали при 25°С на спектрометре DPX-300 фирмы Bruker с рабочей частотой 300,130 МГц, спектры ЯМР 13С – на том же приборе, рабочая частота 75.468 МГц.
Исследование влияния сульфамата (I) на рост клеток рака молочной железы проводили в условиях работы [12].
Клеточные культуры и условия культивирования.
Работа проведена на перевиваемой культуре клеток человека MCF-7 (аденокарцинома молочной железы). В качестве отрицательного контроля использовали нормальные кожные фибробласты человека (КФЧ) ранних пассажей. Клетки культивировали во флаконах Карреля в среде DMEM/F12 (Биолот) с добавлением 1% эмбриональной сыворотки крупного рогатого скота (Биолот), без антибиотиков, в 5% СО2 атмосфере, при 37ºС.
Оценка пролиферативной активности клеток.
Клетки высаживались на флаконы Карреля по 50×104 клеток на флакон.
Для изучения пролиферативной активности клеток в условиях подавления сульфатаз, через 24 часа после посева, культуральную среду заменяли на среду, содержащую ингибиторы сульфатаз до конечной концентрации 50 мкг/мл, после чего инкубировали данные опухолевые клеточные линии в течение различных промежутков времени (от 24 до 72 ч). Ингибитор растворяли в ДМСО. Конечная концентрация ДМСО в культуральной среде не превышала 0.5%. Для исключения цитотоксического действия ДМСО ставили контроль с добавлением ДМСО без ингибитора сульфатаз. Для исключения неспецифического губительного действия веществ использовали нормальные кожные фибробласты человека. Далее клетки снимали раствором версена-трипсина (Биолот), рассеивали на флаконы Карреля, содержащие новую полную культуральную среду. Подсчет клеток проводили в момент достижения необработанными контрольными клетками максимальной плотности клеток на единицу площади поверхности культурального флакона (монослой), при этом их количество определялось как 100%. Пролиферативную активность всех исследованных клеточных культур при воздействии ингибиторов сульфатаз определяли не менее трех раз.
Исследование влияние полученного сульфамата на рост перевиваемой культуры клеток человека MCF-7 (аденокарцинома молочной железы показало, что стероид (I) практически полностью блокирует рост опухолевых клеток при концентрации 20 мкг/мл, при этом он не влияет на рост кожных фибробластов человека, не имеющих рецепторов эстрогенов. Рост опухолевых клеток ингибируется в той же степени, что и под действием тамоксифена, применяемого в медицинской практике более 30 лет. Это весьма важно, поскольку сульфаматы и тамоксифен имеют разные механизмы действия.
Список источников
[1] Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012. Cancer J Clin. 2012. Vol. 62, pp.10-29.
[2] Yue W, Yager JD, Wang Ji-P, Jupe ER, Santen R.J. Estrogen receptor-depended and independent mechanisms of breast cancer carcinogenesis. Steroids. 2013. Vol. 78, N 2, pp. 161-170.
[3] Thomas M.P., Potter B.V.L. Estrogen O-sulfamates and their analogues: Clinical steroid sulfatase inhibitors with broad potential // J. Steroid Biochem. Mol. Biol. 2015. Vol. 153, pp. 160-169.
[4] Numazawa M, Tominaga T, Watari Y, Tada Y. Inhibition of estrone sulfatase by aromatase inhibitor-based estrogen 3-sulfamates. Steroids. 2006. Vol. 71, N5, pp. 371–379.
[5] Vicker N, Lowrence HRR, Allan GM, Bubert C, Fisher DSM, Purohit A, Reed MJ, Potter BVL. 17β-Hydroxysteroid dehydrogenase inhibitors. US patent 8003783 B2; 2011.
[6] Lowrence H.R., Vicker N., Alan G.M., Bubert C., Smith A., Mahon M.F., Tutil H.J., Fischer D.S., Purohit A., Reed M.J., Potter B.V.L. Preparation of steroid derivatives as inhibitors of 17β-hydroxy steroid dehydrogenase. U.S. Pat. Appl. US 2006 74060.
[7] Reed M.J., Purochit A., Woo L.W.L., Newman S.P., Potter B.V.L. Steroid sulfatase: molecular biology, regulation and inhibition. Endocrine Rev. 2005. Vol. 26, N 2, pp. 171-202.
[8] 7β-Alkyl-steroids. Pat. GB 1298974 A1.
[9] Eder U., Haffer G., Neef G., Sauer G., Seeger A., Wiechert R. Synthese des (+)-1,3-Dimethoxy-7β-methyl-1,3,5(10)-ӧstratrien-17-ones. Chem. Ber. 1977. Bd. 110, N 9, s. 3161-3167.
[10] 17-Difluoromethylene-estratrienes. US Pat. 6136800 (2000).
[11] Fidarov A.F., Vihma V., Morozkina S.N., Bogautdinov R.P., Shavva A.G., Tikkanen M.J. Synthesis and evaluation of new estrogen analogues. Antioxidant effect on low density lipoprotein. J. Steroid Biochem. Mol. Biol. 2015. Vol. 154, pp. 142-149.
[12] Морозкина С.Н., Дроздов А.С., Ковалев Р.А., Филатов М.В., Шавва А.Г. Рацемический 2,17β-дисульфамоилокси-3-метокси-8α-эстра-1,3,5(10)-триен в качестве ингибитора пролиферации опухолевых клеток МСF-7. Патент РФ 2562242 (2015).
7β-метил-3,17αβ-дисульфамоилокси-D-гомо-6-окса-эстра-1,3,5(10),8,14-пентаен формулы
в качестве ингибитора роста клеток рака молочной железы МСF-7.