Стенд для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему (варианты)
Иллюстрации
Показать всеГруппа изобретений относится к области медицины и может быть использована для изучения процесса накопления магнитных наночастиц в заданном участке сосудистой системы под воздействием внешнего магнитного поля. Стенд для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему содержит У-образную трубку, единичный конец которой расположен между магнитом и регистратором и соединен с накопительной емкостью, помпу, расходомер, а также датчик давления и элемент доставки наночастиц. Выход накопительной емкости соединен через помпу и расходомер с одним из раздвоенных концов У-образной трубки, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец У-образной трубки соединен также с датчиком давления и элементом доставки наночастиц. Элемент доставки наночастиц по первому варианту представляет собой шприц, а по второму варианту представляет собой электромагнитный зонд, соединенный с источником питания. Группа изобретений обеспечивает возможность исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему. 2 н. и 1 з.п. ф-лы, 7 ил., 1 табл., 1 пр.
Реферат
Изобретение относится к области медицины, в частности к экспериментальной медицине, и может быть использовано для изучения процесса накопления магнитных наночастиц в заданном участке сосудистой системы под воздействием внешнего магнитного поля.
Наночастицы с магнитными свойствами в последние годы активно изучаются и находят применение в медицинской визуализации, диагностике и терапии. Использование контрастных веществ на основе магнитных наночастиц (МНЧ) в магнитно-резонансной томографии позволяет визуализировать воспаление различной локализации в нервной системе, почках, кишечнике, легких, печени, костной и жировой тканях [Wu Y., Briley-Saebo K., Xie J. et al. Inflammatory bowel disease: MR- and SPECT/CT-based macrophage imaging for monitoring and evaluating disease activity in experimental mouse model-pilot study // Radiology. - 2014. - Vol. 271, №2. - P. 400-406; Luciani A., Dechoux S., Deveaux V. et al. Adipose tissue macrophages: MR tracking to monitor obesity-associated inflammation // Radiology. - 2012. - Vol. 263, №3. - P. 786-878]. Кроме того, МНЧ в экспериментальных исследованиях применяются в следующих областях: для направленной доставки противоопухолевых препаратов, направленной термочувствительной химиотерапии [Pradhan P., Giri J., Rieken F. et al. Targeted temperature sensitive magnetic liposomes for thermo-chemotherapy // J Control Release. - 2010. - Vol. 142, №1. - P. 108-129], магнитной фотодинамической терапии [Cinteza L.O., Ohulchanskyy T.Y., Sahoo Y. et al. Diacyllipid micelle-based nanocarrier for magnetically guided delivery of drugs in photodynamic therapy // Mol Pharm. - 2006. - Vol. 3, №4. - P. 415-437] и флуоресцентной визуализации [Yang L., Mao H., Cao Z. et al. Molecular imaging of pancreatic cancer in an animal model using targeted multifunctional nanoparticles // Gastroenterology. - 2009. - Vol. 136, №5 - P. 1514-1538].
Вопрос эффективности применения лекарственных препаратов противоишемического действия, иммобилизированных на поверхности магнитных наночастиц, в литературе представлен единичными статьями. В то же время магнитоуправляемая доставка лекарственных препаратов в зону ишемии потенциально может обеспечить увеличение терапевтического действия с одновременным уменьшением выраженности системных побочных эффектов [Galagudza М., Korolev D., Postnov V. et al. Passive targeting of ischemic-reperfused myocardium with adenosine-loaded silica nanoparticles // Int J Nanomedicine. - 2012. - №7. - P. 1671-1678]. В работе Zhang и соавт. [Zhang Y., Li W., Ou L. et al. Targeted delivery of human VEGF gene via complexes of magnetic nanoparticle-adenoviral vectors enhanced cardiac regeneration // PLoS One. - 2012. - Vol. 7, №7. - P. e39490] был продемонстрирован положительный эффект от использования магнитных наночастиц в качестве транспортера сосудистого эндотелиального фактора роста на модели лигирования коронарной артерии у крысы.
Для установления перспектив использования магнитных наночастиц в качестве транспортера лекарственных препаратов необходимо решить ряд задач, в частности выяснить оптимальную интенсивность магнитного поля для обеспечения накопления наночастиц в очаге ишемии, изучить биосовместимость наночастиц, а также изучить кардиопротективный эффект препаратов, иммобилизированных на поверхности наночастиц.
Однако изучение процесса магнитоуправляемой доставки правильнее начинать в модельных условиях in vitro. Для этого необходима разработка специализированного испытательного стенда, имитирующего участок системы кровообращения и позволяющего прилагать магнитное воздействие, а также осуществлять регистрацию накопления нанообъектов. Подобные задачи частично решались при конструировании систем вспомогательного кровообращения. Пик исследований в этой области пришелся на конец 70-х, начало 80-х годов прошлого века [Описание изобретения к авторскому свидетельству №685294. Стенд-имитатор системы кровообращения организма. / М.А. Локшин, Ю.Н. Гаврилов, В.И. Ковин, опубл. 15.09.79; Описание изобретения к авторскому свидетельству №936922. Стенд для моделирования системы кровообращения. / А.П. Осипов, В.М. Мордашев, В.А. Кремнев, Ю.М. Киселев, опубл. 23.06.82; Описание изобретения к авторскому свидетельству №939013. Устройство для моделирования гемодинамических явлений в системе кровообращения. / B.C. Бедненко, А.С. Нехаев, А.Н. Козлов, опубл. 30.06.82; Описание изобретения к авторскому свидетельству SU 1029961 А. Стенд для испытания искусственного сердца. / М.А. Локшин, В.И. Копин, В.Г. Северин, А.В. Врубель, В.А. Стасенков, опубл. 23.07.83].
Однако к недостаткам этих стендов следует отнести их ограниченные функциональные возможности.
Проведенные авторами патентные исследования не выявили прототип предлагаемого изобретения.
Задачей, на решение которой направлено заявляемое изобретение, является изучение процесса накопления магнитных наночастиц в заданном участке сосудистой системы под воздействием внешнего магнитного поля.
Данная задача решается за счет того, что в первом варианте конструкция стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему включает У-образную трубку, единичный конец которой, расположенный между магнитом и регистратором, соединен с накопительной емкостью, выход последней соединен через помпу и расходомер с одним из раздвоенных концов У-образной трубки, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец У-образной трубки соединен также с датчиком давления и элементом доставки наночастиц, представляющим собой шприц.
Данная задача решается также за счет того, что во втором варианте конструкция стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему включает У-образную трубку, единичный конец которой, расположенный между магнитом и регистратором, соединен с накопительной емкостью, выход последней соединен через помпу и расходомер с одним из раздвоенных концов У-образной трубки, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец трубки соединен также с датчиком давления, а в другой раздвоенный конец У-образной трубки помещен элемент доставки наночастиц, представляющий собой электромагнитный зонд, соединенный с источником питания.
Во втором варианте данная задача решается также за счет конструкции электромагнитного зонда, выполненного в форме соленоида с длиной, значительно превышающей его диаметр.
Техническим результатом, обеспечиваемым приведенной совокупностью признаков заявленной группы изобретений, является создание универсального стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему, сочетающего в себе модель участка системы кровообращения, систему приложения магнитного воздействия и систему наблюдения за процессом накопления наночастиц.
Изобретение поясняется чертежами, где:
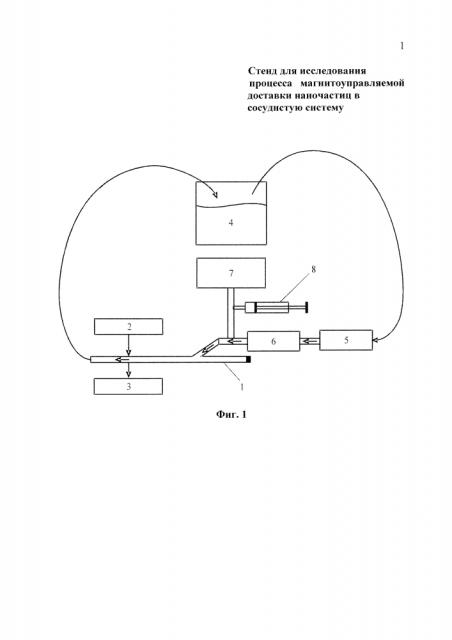
на фиг. 1 представлена блок-схема стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему (вариант 1);
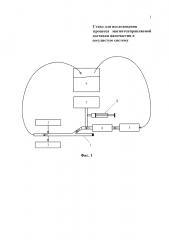
на фиг. 2 представлена блок-схема стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему (вариант 2);
на фиг. 3 представлена конструкция магнитного зонда (вариант 2);
на фиг. 4 - график зависимости объемного расхода модельной жидкости от мощности помпы;
на фиг. 5 - микрофотография нанопорошка магнетита;
на фиг. 6 - график магнитной восприимчивости магнитных наночастиц;
на фиг. 7 - накопление магнитных наночастиц в зоне движения модельной жидкости: А - фотография накопления магнитных наночастиц; Б - схематическое изображение топографии магнитного поля (распределение магнитной индукции в пространстве).
Конструкция стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему в первом варианте (фиг. 1) содержит: У-образную трубку 1, единичный конец которой, расположенный между магнитом 2 и регистратором 3, соединен с накопительной емкостью 4, выход последней соединен через помпу 5 и расходомер 6 с одним из раздвоенных концов У-образной трубки 1, упомянутый раздвоенный конец У-образной трубки 1 соединен также с датчиком давления 7 и элементом доставки наночастиц 8, представляющим собой шприц.
Конструкция стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему во втором варианте (фиг. 2) содержит: У-образную трубку 1, единичный конец которой, расположенный между магнитом 2 и регистратором 3, соединен с накопительной емкостью 4, выход последней соединен через помпу 5 и расходомер 6 с одним из раздвоенных концов У-образной трубки 1, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец У-образной трубки 1 соединен также с датчиком давления 7, а в другой раздвоенный конец У-образной трубки 1 помещен элемент доставки наночастиц 8, представляющий собой электромагнитный зонд, соединенный с источником питания 9.
У-образная трубка 1 (фиг. 1 и 2) может быть выполнена, например, из пирексного стекла.
В качестве регистратора 3 (фиг. 1 и 2) могут быть применены промышленная видеокамера или цифровой фотоаппарат. Возможно также применение флуоресцентных красителей в совокупности с соответствующими светофильтрами и источниками излучения.
Гидравлическая часть имитирующей системы кровообращения (фиг. 1 и 2) включает: накопительную емкость 4, представляющую собой ресивер, помпу 5, в качестве которой может быть использована, например, помпа от аппарата искусственной почки, и расходомер 6. Расход и давление в системе измеряются непосредственно перед входом в У-образную трубку.
В качестве элемента доставки наночастиц 8 по варианту 2 (фиг. 2) был спроектирован электромагнитный зонд в форме соленоида (фиг. 3) с длиной, значительно превосходящей диаметр, и обеспечивающий расчетную индукцию магнитного поля 6.55 мТл. Параметры электромагнитного зонда отражены в приведенной таблице.
Разработанная конструкция электромагнитного зонда позволяет изучить баланс сил магнитного удержания - турбулентного отрыва для различных режимов функционирования и выявить параметры гарантированного удержания для определенного вида МНЧ.
Предусмотрены два принципиально разных способа доставки МНЧ, соответственно и два разных элемента доставки. Первый вариант (фиг. 1) предусматривает введение суспензии наночастиц при помощи шприца 8 и последующее накопление в зоне действия магнитного поля, создаваемого магнитом 2, расположенным вдоль оси стеклянной трубки. Второй вариант (фиг. 2) предусматривает введение наночастиц, удерживаемых на электромагнитном зонде 8, непосредственно в У-образную трубку в зоне ее прямого прохода по оси. Питание электромагнитного зонда 8 осуществляется от источника питания постоянного тока 9.
Объемный расход модельной жидкости в зоне эксперимента может изменяться в диапазоне от 40 до 80 л/час, что соответствует задаваемой мощности от 10 до 100% (фиг. 4).
В качестве модельной жидкости использовали дистиллированную воду.
Работа стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему в первом варианте (фиг. 1) осуществляется следующим образом.
Модельная жидкость из накопительной емкости 4 при помощи помпы 5 подается в Y-образную трубку 1, куда при помощи шприца 8 вводится суспензия магнитных наночастиц. Удержание магнитных наночастиц в Y-образной трубке осуществляется при помощи магнита 2. Контроль процесса накопления магнитных наночастиц осуществляется регистратором 3. Измерение расхода модельной жидкости осуществляется при помощи расходомера 6, давления - датчика давления 7. Таким образом, можно имитировать магнитоуправляемую доставку лекарств, связанных с магнитными наночастицами, в локальные участки сосудистого русла. Примером таких участков могут служить конечности. В этом случае при доставке лекарственного вещества, например неотона (креотинфосфат, фосфокреатин) в конечности, можно осуществлять регенерацию мышечной ткани. В качестве магнита можно использовать смесевые магнитные термоэластопласты для изделий медицинского назначения [Кисель Л.О., Красовский В.Н.. Королев Д.В., Суворов К.А. Смесевые магнитные термоэластопласты (ТЭП) для изделий медицинского назначения // Каучук и резина. - 1999, №1. - С. 11-13].
Работа стенда для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему во втором варианте (фиг. 2) осуществляется следующим образом.
Модельная жидкость из накопительной емкости 4 при помощи помпы 5 подается в Y-образную трубку 1. Магнитные наночастицы вводятся внутрь Y-образной трубки при помощи электромагнита 8. Электромагнит питается от источника 9, позволяющего задавать различные значения силы тока и напряжения. Удержание магнитных наночастиц в Y-образной трубке, оторвавшихся от электромагнита 8, осуществляется при помощи магнита 2. Контроль процесса накопления магнитных наночастиц осуществляется регистратором 3. Измерение расхода модельной жидкости осуществляется при помощи расходомера 6, давления - датчика давления 7. Данная схема позволяет смоделировать процесс магнитоуправляемой доставки непосредственно в сосудистое русло при помощи средств доставки, аналогичных средствам доставки стентов, применяемых для стентирования коронарных артерий.
ПРИМЕР
Эксперимент по исследованию магнитоуправляемой доставки проводился для суспензии наночастиц магнетита размером 7-10 нм (фиг. 5) и удельной поверхностью, измеренной по упрощенному методу БЭТ на установке Клячко-Гурвича, 95 м2/г. Расчетная удельная поверхность наноматериала составляет 130 м2/г [Афонин М.В., Евреинова Н.В., Королев Д.В. и др. Исследование физических свойств и биодеградации наночастиц магнетита in vitro // Биотехносфера. - 2015. - №2(38). - С. 32-34]. Как видно из микрофотографии (фиг. 5), зародышеобразование будущих МНЧ начинается с образования гамма-окиси железа. Об этом свидетельствует ярко выраженная игольчатая форма наночастиц.
График магнитной восприимчивости, полученный на вибрационном магнитометре Lake Shore 7410 (Lake Shore Cryotronics Inc., USA) в воздушной среде при стандартной температуре, показан на фиг. 6. Отсутствие петли гистерезиса говорит о том, что исследованные образцы относятся к суперпарамагнетикам или к мягким ферромагнитным материалам с большой магнитной проницаемостью. Это совпадает с классическими представлениями о магнитных свойствах наноматериалов [Поздняков В.А. Физическое материаловедение наноструктурных материалов: Учеб. пособие. - М.: МГИУ, 2007. - 423 с.]. Варианты использования подобных МНЧ предложены авторами в Патенте на изобретение RU 2525430 C2. Носитель для лекарственных средств и биологически активных веществ для лечения и диагностики и способ его получения. / Королев Д.В., Афонин М.В., Галагудза М.М. и др., опубл. 10.08.2014, Бюл. №22.
Синтез наноматериала проводили следующим образом [Королев Д.В., Галагудза М.М., Афонин М.В. и др. Обоснование использования магнитных наночастиц для направленной доставки лекарственных препаратов в ишемизированную скелетную мышцу // Биотехносфера. - 2012. - 1(19). - С. 2-6]. К раствору, содержащему смесь сульфатов железа (II), железа (III) в мольном соотношении 2:1 и объемом 700 мл, при постоянном перемешивании со скоростью 4 мл/мин добавляли смесь 25% раствора гидроксида аммония и 1% раствора ацетата аммония. Таким образом, соотношение железа и ацетата аммония составляло 2:1:0,1. Синтез проводили до фиксации насыщенно черной окраски и установления значения pH=8-9. На следующий день полученный коллоидный продукт отделяли центрифугированием и промывали 4 раза дистиллированной водой. Для подготовки сухой пробы полученные МНЧ отфильтровывались и подвергались лиофильной сушке при температуре -48°C в течение 48 часов.
Коллоидный раствор наночастиц в физиологическом растворе имел концентрацию МНЧ 2 мг/мл и приготовлялся на ультразвуковом диспергаторе УЗД-2 в течение 5 минут.
Исследование магнитоуправляемой доставки проводилось на заявленном стенде по варианту 1. Суспензия наночастиц в количестве 5 мл концентрацией 2 мг/мл в физиологическом растворе вводилась при помощи шприца в течение 10 с, как показано на фиг. 1. Скорость прокачки модельной жидкости составляла 80 л/ч (100% мощности). В качестве модельной жидкости использовалась дистиллированная вода. Удержание наночастиц из потока жидкости осуществлялось при помощи постоянного магнитного поля неодимового магнита класса N35 размером 30×20×10 мм.
Эксперимент показал, что в течение 5 минут из потока циркулирующей модельной жидкости 100% МНЧ оседают в зоне приложения магнитного поля (фиг. 7А). Таким образом, за время эксперимента при данном расходе модельной жидкости в трубке накопилось 10 мг наночастиц магнитного материала. Преимущественное накопление МНЧ наблюдалось на концах постоянного магнита. Такое их поведение вполне объяснимо в сопоставлении с топографией магнитного поля постоянного магнита (фиг. 7Б).
Таким образом, предлагаемая группа изобретений позволяет изучать процесс магнитоуправляемой доставки МНЧ in vitro в зависимости от объемного расхода, солевого состава и вязкости модельной жидкости.
1. Стенд для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему, включающий У-образную трубку, единичный конец которой, расположенный между магнитом и регистратором, соединен с накопительной емкостью, выход последней соединен через помпу и расходомер с одним из раздвоенных концов У-образной трубки, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец У-образной трубки соединен также с датчиком давления и элементом доставки наночастиц, представляющим собой шприц.
2. Стенд для исследования процесса магнитоуправляемой доставки наночастиц в сосудистую систему, включающий У-образную трубку, единичный конец которой, расположенный между магнитом и регистратором, соединен с накопительной емкостью, выход последней соединен через помпу и расходомер с одним из раздвоенных концов У-образной трубки, образуя замкнутый контур, имитирующий систему кровообращения, причем упомянутый раздвоенный конец трубки соединен также с датчиком давления, а в другой раздвоенный конец У-образной трубки помещен элемент доставки наночастиц, представляющий собой электромагнитный зонд, соединенный с источником питания.
3. Стенд по п. 2, отличающийся тем, что электромагнитный зонд выполнен в форме соленоида с длиной, значительно превышающей его диаметр.