Устройство для выделения клеточных фракций из тканей человека и животных и способ его применения
Иллюстрации
Показать всеГруппа изобретений относится к области клеточной технологии. Предложено устройство для выделения стромально-васкулярной фракции из тканей человека и животных, способ выделения клеточных фракций с использованием данного устройства, стромально-васкулярная фракция жировой ткани для создания тканеинженерных конструкций и для использования в качестве клеточного аутотрансплантата, а также способ лечения, репарации или замещения ткани с использованием стромально-васкулярной фракции жировой ткани. Устройство включает герметичную емкость для обработки ткани с системой каналов и штуцеров-переходников. При этом емкость имеет конусообразную форму и разделена на две камеры системой микрофильтров. Одна камера емкости служит для обработки ткани, а другая для концентрирования клеток. Емкость также имеет каналы в толще стенки, где один из каналов выходит в первую камеру, а другой во вторую камеру. Способ включает декантацию, отмывку и ферментативную обработку липоаспирата, центрифугирование, фильтрацию через микрофильтры с последующим удалением примесей жира и стромальной ткани, а также вторичной отмывкой и концентрацией клеточной фракции. Изобретения обеспечивают контролируемое выделение стромально-васкулярной фракции жировой ткани, характеризующейся высокой выживаемостью клеток, отсутствием дебриса, остатков стромальной и жировой ткани и клеток циркулирующей крови, низкой концентрацией и активностью остаточных ферментов. 5 н. и 3 з.п. ф-лы, 7 ил., 1 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящая группа изобретений относится к медицинской биотехнологии и клеточной технологии и предназначена для выделения клеточных фракций из тканей человека и животных, а именно выделения стромально-васкулярной фракции жировой ткани.
УРОВЕНЬ ТЕХНИКИ
Подкожная жировая клетчатка является альтернативным костному мозгу источником стволовых и прогениторных клеток для регенеративной медицины. Основным преимуществом жировой ткани является малая инвазивность процедуры забора, минимальная болезненность, дискомфорт и риск для пациента. Жировая ткань обеспечивает значительно большее количество стволовых клеток по сравнению с костным мозгом. Костномозговой трансплантат содержит 0,006-0,06×106 стволовых клеток на 100 мл, а число жизнеспособных стволовых и прогениторных клеток во фракции жировой ткани составляет примерно 0,5×106 до 20×106 клеток на 100 мл ткани.
Гетерогенную фракцию жировой ткани, отделенную от стромы и адипоцитов с использованием коллагеназ, принято называть стромально-васкулярной фракцией. Стромально-васкулярная фракция характеризуется значительной неоднородностью и вариабельностью клеточного состава в зависимости от состояния донора, его возраста и места забора биологического материала. После сортировки из стромально-васкулярной фракции могут быть выделены популяции клеток: эндотелиальные и гладкомышечные клетки, перициты, фибробласты, тучные клетки и преадипоциты. Интерес представляют клетки регенераторной фракции, а именно комплекса стволовых и прогениторных клеток жировой ткани (adipose derived stem cells, ADSCs). ADSCs имеют значительный потенциал к дифференцировке в адипоциты, хондроциты и остеобласты, миоциты, нейрональные клетки, кардиомиоциты и гепатоциты.
Клиническое применение стромально-васкулярной фракции включает регенерацию мягких тканей и костей, косметические дефекты, хронические трофические и лучевые язвы, ожоги, болезнь Крона, рассеянный склероз, при реакции трансплантат против хозяина, при инфаркте миокарда и инсультах различного генеза. Основными преимуществами использования данного типа клеток является легкий доступ к источнику клеток, большое количество и высокий выход на единицу объема ткани, высокую мультипотентность, сравнимую эффективность и безопасность относительно мезенхимальных клеток костного мозга. Кроме того, процедура липоаспирации широко используется, стандартизована, проста в исполнении в условиях процедурного кабинета и может быть проведена в течение короткого времени - порядка 90 минут. Таким образом, клеточные фракции, выделенные из жировой ткани могут быть выгодно использованы для клинической практики, и в том числе, исключая стадию культивирования.
Известен способ выделения стволовых клеток из жировой ткани с использованием ручного метода (Zuk Р.А., Zhu М., Mizuno Н. et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng. 2001; 7(2): 211-28.). Данный метод основан на обработке липоаспирата 0,075% раствором коллагеназы I типа при температуре 37°С в течение 30 минут и последующим центрифугированием получившейся суспензии при 800 g. После центрифугирования суспензия клеток разделяется на две фракции: в верхнем слое - супернатанте находятся адипоциты, а в осадке - стромально-васкулярная фракция с примесью эритроцитов, которые удаляли во время инкубации в лизирующем растворе хлорида аммония. Недостатками данного метода являются высокие временные и организационные затраты, наличие «человеческого фактора», высокий риск нарушения стерильности процесса и контаминации биологического материала и конечного продукта.
Технологии выделения развиваются в сторону автоматизации процесса. Созданы автоматические и полуавтоматические системы выделения клеток.
Из предшествующего уровня техники известно устройство (System for processing lipoaspirate cells ЕР 1921133 A2, CYTORI THERAPEUTICS, INC (US), МПК A61K 31/436, опубл. 14.05.2008), представляющее собой замкнутую систему для обработки липоаспирата, полученного в ходе липосакции. Система подсоединяется непосредственно к липоаспирационной канюле. Включает вакуумный насос, контейнер для сбора липоаспирата, миксер для смешивания обработанного биоматериала с добавками и активаторами, систему из двух фильтров с порами разного диаметра. Первый фильтр разделяет липоаспират на 2 фракции, где одна фракция содержит популяцию клеток, включающую в себя стволовые клетки жировой ткани, а другая фракция содержит липиды, кровь, адипоциты и солевой раствор. При этом первый фильтр вращается и конструктивно делит емкость на две камеры, для соответствующих фракций, а второй фильтр концентрирует клеточную фракцию перед подачей в миксер. Проводящая магистраль позволяет извлечь конечную фракцию, не нарушая герметичности системы и направить ее в центрифугу, затем асептично извлечь полученную фракцию. Устройство позволяет вводить активаторы и добавки. Также система имеет встроенный контроллер температуры. Основным недостатком данного устройства является то, что на первом этапе обработки липоаспират фильтруется без обеспечения разрушения стромы ткани, которая фиксирует клетки стромально-васкулярной фракции и не позволяет им пройти через фильтр, снижая тем, самым концентрацию клеток в пермеате. Также недостатками системы являются магистрали большой протяженности и значительное количество примыканий, являющиеся средой для адгезии и потери целевых клеток.
Из предшествующего уровня техники известно устройство (Method and Apparatus for Separating a Material, US 20110251041 A1, BIOMET BIOLOGICS, LLC (US), МПК B04B 1/08, опубл. 13.10.2011), представляющее собой систему для сепарации многокомпонентного материала, по меньшей мере, на две фракции. Данное устройство представляет собой емкость, в виде полого цилиндра, разделенного клапаном на две неравные по объему части. Функцией клапана является разграничение фракций разной плотности. Система содержит отстойник в основании конструкции с наклонными стенками, отделенный клапаном от основного объема камеры. Клапан имеет коническую поверхность, включает в себя вставку, также имеющую коническую поверхность, между боковой стенкой и продольной осью цилиндра, коническая поверхность обращена углом вниз. Клапан содержит диск с отверстиями круглой формы и формы сектора. Клапан включает гибкую мембрану, активирующую его при возрастании гидравлического давления при центрифугировании, при повороте диска происходит сопоставление отверстий, обеспечивая, проницаемость клапана. Система укомплектована дополнительно измельчителем и вакуумным насосом, сообщающимся с разделительной камерой. При этом жировая ткань разделяется на три фракции. Первая фракция изолируется между клапаном и дном камеры и содержит клеточный материал. Вторая фракция изолируется между клапаном и верхним концом камеры и содержит жир. Третья фракция изолируется между компонентами клапана и включает туменесцентную жидкость. Основным недостатком данной системы является возможность заполнения фрагментами ткани элементов механического устройства, что влечет риск несрабатывания устройства, загрязнение конечной фракции компонентами исходного биоматериала. Обработка без обеспечения разрушения стромы ткани, которая фиксирует клетки стромально-васкулярной фракции и не позволяет им пройти через фильтр, снижая тем, самым концентрацию клеток в пермеате.
Из предшествующего уровня техники известно устройство (Regenerative cell extraction device WO 2013183797 A1, HURIMBIOCELL CO., LTD (KR), МПК C12M 1/10, опубл. 12.12.2013), представляющее собой емкость с дном конусовидной формы и вращающейся продольной осью, приводимой в движение от внешнего двигателя. На оси закрепляется изделие, состоящее из множества лепестков, которое оказывает непосредственное воздействие на липоаспират. Емкость снабжена патрубком для введения биоматериала и выделения тканевой фракции содержащей стволовые клетки. Недостатками данной системы является значительное механическое воздействие на клетки, что приводит к их разрушению и повреждению высвобожденными ферментами прочих клеток, загрязнение конечного продукта компонентами исходного липоаспирата, высокий риск микробиологической контаминации биоматериала за счет отсутствия асептических барьеров.
Из предшествующего уровня техники известно устройство (Device for separating adult stem cell US 20130344589 A1, HUMAN MED AG (DE), МПК C12M 1/00, опубл. 26.12.2013), представляющее собой систему, включающую контейнер для жировой ткани, снабженный устройством для подачи жидкости с целью отмывки биоматериала, смеси необходимых реагентов, попеременно с извлечением фракции содержащей стволовые клетки, клапаном для выравнивания давления, поршнем, вибратором, полупроницаемой мембраной имеющей электростатический заряд и клапаном, которые делят контейнер на 2 части, контроллером температуры. Одна из камер снабжена устройством для перемешивания исходного биоматериала с добавками, совершающего вращательные и/или маятниковые движения. Основным недостатком данного устройства является метод создания давления за счет поршня, что приводит высокой механической нагрузке на целевые клетки из-за продавливания через фильтр и краевого разрушения клеток в месте примыкания поршня к стенке цилиндра.
В качестве прототипа выбрано устройство для выделения стволовых клеток жировой ткани (System and methods for preparation of adipose-derived stem cells, US 20130012921 A1, PUSTILNIK FELIX, МПК A61M 37/00, опубл. 10.01.2013), представляющее собой конусовидную емкость, герметично закрытую крышкой, снабженную разъемами для введения и выведения биоматериала и жидкостей для его обработки, а также вспомогательную пробирку для концентрации, полученной стромально-васкулярной фракции. Недостатками данной системы являются наличие двух пробирок-емкостей, что увеличивает риск контаминации материала, его потери при перенесении между емкостями, влечет дополнительные требования к вспомогательному оборудованию. Кроме этого, в системе отсутствует разделение первичного липоаспирата на фракции, содержащие целевые клетки и побочные продукты обработки, загрязняющие конечный продукт.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Общей технической задачей настоящей группы изобретений является повышение эффективности и безопасности способа выделения клеток, расширение его функциональных возможностей и оптимизация процедуры выделения.
Общим техническим результатом предлагаемой группы изобретений является контролируемое выделение стромально-васкулярной фракции жировой ткани, характеризующейся высокой выживаемостью клеток, отсутствием дебриса, остатков стромальной и жировой ткани и клеток циркулирующей крови, низкой концентрацией и активностью остаточных ферментов.
Поставленная техническая задача достигается за счет наличия в устройстве двух камер, разделенных между собой системой микрофильтров с различным диаметром пор; наличия изолированных каналов в стенке системы; наличия клапанов на штуцерах-переходниках для ввода биологического материала, внесения реагентов и промывочного буфера, отбора дебриса и остатков стромы жировой ткани, отбора конечного продукта; использования антиадгезионной обработки внутренней поверхности устройства и использования для заливки и отбора биологического материала шприца луер-лок с удлиненным носиком и увеличенной ручкой поршня.
Предложенное устройство представляет собой замкнутую герметичную систему в виде прозрачной конусовидной емкости объемом 150-300 мл, с нанесенной внешней градуировкой по объему, системой каналов и штуцеров-переходников, имеющих разъемы типа «луер-лок», причем емкость разделена многослойным фильтром на две камеры - рабочая камера для обработки ткани и камера для концентрирования клеток, причем рабочая камера имеет объем 145-299 мл, а камера для концентрирования имеет объем 1-5 мл.
Система фильтров представляет собой комплекс, по крайней мере, из 2-х нейлоновых фильтров диаметром от 10 мкм для нижнего фильтра до 500 мкм для верхнего фильтра, разделенных полимерными прокладками и помещенными в полимерный корпус, имеющий на своей окружности рычаги и запирающий элемент для байонетного соединения с емкостью. Система фильтров устанавливается в емкость в силиконовую прокладку посредством байонетного соединения, для этого место соединения фильтра с емкостью имеет секторные пазы.
Конусообразная форма емкости для обработки ткани и разделение ее на две камеры системой микрофильтров с диаметром пор 10-500 мкм обеспечивает повышение эффективности, безопасности и экономичности способа выделения клеток.
Устройство имеет изолированные каналы, расположенные в боковых стенках емкости, причем вход каждого канала имеет углубления и секторальные пазы для байонетного соединения со штуцерами-переходниками.
Устройство имеет канал для введения биологического материала, заканчивающийся пазом-углублением в рабочей камере для обработки ткани.
Устройство имеет канал для введения реагентов и промывочных буферов, заканчивающийся пазом-углублением в рабочей камере для обработки ткани.
Устройство имеет канал для отбора супернатанта, содержащего клеточный дебрис, остатки необработанной стромальной и жировой ткани, заканчивающийся у места крепления фильтра в рабочей камере для обработки ткани.
Устройство имеет канал для отбора конечного продукта - стромально-васкулярной фракции жировой ткани, заканчивающийся у основания емкости в камере для концентрирования клеток.
Устройство может иметь дополнительные каналы для внесения или отбора компонентов, заканчивающихся в рабочей камере для обработки ткани и/или в камере для концентрирования клеток.
Устройство имеет бактериологический фильтр для выравнивания давления внутри системы.
Устройство имеет крышку, причем крышка по своей окружности имеет запирающие элементы и соединяется с емкостью через силиконовую прокладку посредством байонет соединения или резьбы.
Крышка устройства может иметь отверстия для каждого из каналов и бактериологического фильтра.
Крышка может соединяться с емкостью через силиконовую прокладку посредством стальных болтов, для этого емкость имеет соответствующие отверстия с резьбой.
Устройство имеет штуцеры-переходники для каждого из каналов. Каждый штуцер-переходник имеет обратный клапан. Каждый штуцер-переходник имеет резьбу типа «луер-лок» для соединения со шприцем. Каждый штуцер-переходник имеет навинчивающуюся крышку. Каждый штуцер-переходник имеет силиконовые прокладки для обеспечения герметичности при соединении с емкостью. Каждый штуцер-переходник имеет запирающий элемент для соединения с емкостью. Каждый штуцер-переходник соединяется с емкостью через крышку и силиконовую прокладку посредством байонетного соединения.
Устройство может иметь кожух-чехол, причем кожух-чехол соединяется с емкостью посредством байонет соединения или резьбы.
Устройство может иметь ножки в виде лопастей, являющиеся подставкой для емкости.
Устройство может иметь пазы для закрепления на бакет-роторе центрифуги. В этом случае устройство снабжают внутренней стальной арматурой по ходу пазов.
Внутреннюю поверхность устройства покрывают органосиликоновой и/или агарозной пленкой с целью придания поверхности гидрофобных и антиадгезивных свойств. Для этого стерильную и обезжиренную систему высушивают и обрабатывают внутренние поверхности системы и каналы 0,1-10% раствором полидиметилсилоксана в хлороформе и/или 0,1-5% раствором агарозы. Обработанную систему помещают на 1-5 часов в сушильный шкаф при температуре 100°С - 300°С.
Устройство может имеет шприц типа «луер-лок» (на чертежах не показано) объемом 50-200 мл с удлиненным носиком, завинчивающейся крышкой и увеличенной ручкой поршня для внесения биологического материала и отбора супернатанта и конечного продукта.
Все компоненты устройства, включая емкость, крышку, штуцеры-переходники, крышки штуцеров-переходников, корпус системы фильтров и прокладки системы фильтров изготавливаются из поликарбоната и/или полипропилена и/или полиэтилена и/или фторопласта. Прокладки и клапаны изготавливаются из силикона и/или резины.
Способ выделения стромально-васкулярной фракции жировой ткани из липоаспирата по настоящему изобретению включает следующие стадии:
- декантацию и отмывку липоаспирата от остатков крови, причем декантацию осуществляют в течение 10-30 минут, причем отмывку липоаспирата проводят физиологическим раствором и/или сбалансированным солевым раствором Хенкса и/или средой Игла в модификации Дульбеко при температуре 37°С, причем отмывку липоаспирата проводят 1-5 раз;
- ферментативную обработку липоаспирата смесью ферментов состоящую из коллагеназы I и/или коллагеназы II и/или термолизина и/или диспазы и/или трипсина, причем обработку проводят при 37°С в условиях термостата, причем обработку проводят при перемешивании на шейкере при 10-200 об./мин, причем обработку проводят в течение 30-60 минут;
- сепарирование стромально-васкулярной фракции от клеточного дебриса и остатков стромы жировой ткани, причем сепарирование осуществляют в условиях центрифугирования при 500-2000 g, причем центрифугирование проводят в течение 15-45 минут;
- удаление клеточного дебриса и остатков стромы жировой ткани;
- отмывку конечного продукта от остатков ферментов, причем отмывку проводят физиологическим раствором и/или сбалансированным солевым раствором Хенкса и/или средой Игла в модификации Дульбеко при температуре 37°С, причем отмывку конечного продукта проводят 1-5 раз;
- концентрирование стромально-васкулярной фракции, причем концентрирование осуществляют в условиях центрифугирования при 500-2000 g, причем центрифугирование проводят в течение 15-45 минут;
- причем все стадии способа осуществляют в устройстве по настоящему изобретению;
- причем внесение биологического материала и отбор биологического материала из устройства осуществляют с использованием шприца для внесения и отбора биологического материала.
Выделенная стромально-васкулярная фракция жировой ткани может применяться в биологии и медицине в качестве клеточного элемента для создания тканеинженерных конструкций на основе синтетических и природных материалов.
Выделенная стромально-васкулярная фракция жировой ткани может применяться в биологии и медицине для использования в качестве клеточного аутотрансплантата для замещения и регенерации дефектов твердых и мягких тканей, путем введения стромально-васкулярной фракции жировой ткани в твердые и/или мягкие ткани
Таким образом, биологическая ткань, помещенная в систему, отмывается от остатков циркулирующей крови; подвергается ферментативной обработке смесью коллагеназ I и II, термолизина, диспазы и трипсина, за счет чего происходит лизис стромальной ткани и выход стромально-васкулярной фракции в среду. На следующем этапе происходит разделение клеточного компонента и остатков стромальной и жировой ткани центрифугированием через систему фильтров с различным размером пор с последующей отмывкой клеточной фракции от остаточных ферментов и ее концентрирование. За счет обработки внутренней поверхности антиадгезивными средами остатки циркулирующей крови и клеточная фракция не прилипают к стенкам системы и полностью отмываются во время процедуры. За счет использования смеси ферментов происходит полный лизис стромальной ткани и выход стромально-васкулярной фракции в среду. За счет наличия системы фильтров с различным диаметром пор происходит оптимальное выделение клеточной фракции без примесей стромальной и жировой ткани. Наличие каналов ввода - вывода с выходами на разном уровне внутри стенки системы позволяет минимизировать общую площадь внутренней поверхности системы, что снижает риск адгезии клеток на поверхности трубок; позволяет контролируемо пристеночно вносить биологический материал и реактивы, что снижает физическое воздействие на биологический материал и повышает степень выживаемости клеток; позволяет полностью отбирать супернатант с остатками стромы жировой ткани, не затрагивая осадок; позволяет полностью отбирать осадок в виде стромально-васкулярной фракции жировой ткани. Наличие входных клапанов на каналах обеспечивает стерильность процессов происходящих внутри системы. Использование в качестве основного материала прозрачного пластика позволяет визуально контролировать процесс выделения клеток, внесение биологического материала и реактивов, отбор супернатанта с остатками стромальной и жировой ткани и отбор конечной стромально-васкулярной фракции. Наличие градуировки на поверхности системы позволяет визуально контролировать объем вносимого биологического материала и реактивов. Использование шприца с удлиненным носиком позволяет удобно вносить и отбирать биологический материал и реагенты без риска контаминации материала и пролива жидкостей вне системы.
Стромально-васкулярная фракция жировой ткани, выделенная с использованием заявленного изобретения может применяться для создания тканеинженерных конструкций на основе синтетических и природных материалов; для использования в качестве клеточного аутотрансплантата; в качестве способа лечения, репарации или замещения ткани, включающий введение стромально-васкулярной фракции жировой ткани в твердые и/или мягкие ткани.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
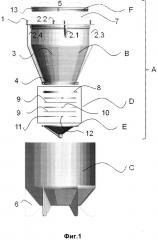
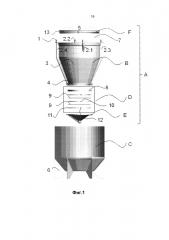
На Фиг. 1 - изображено устройство для выделения клеточных фракций из тканей человека и животных в развернутом виде.
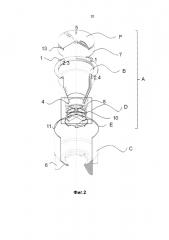
На Фиг. 2 - изображено устройство для выделения клеточных фракций из тканей человека и животных в развернутом виде в разрезе.
На Фиг. 3 - изображено устройство для выделения клеточных фракций из тканей человека и животных в собранном виде.
На Фиг. 4 - изображено устройство для выделения клеточных фракций из тканей человека и животных в собранном виде в разрезе.
На Фиг. 5 - изображено устройство для выделения клеточных фракций из тканей человека и животных (вид сверху).
На Фиг. 6 - изображен монослой клеток в культуре р0 (пассаж №1), 5-е сутки. Фазовый контраст (увеличение х10).
На Фиг. 7 - изображен монослой клеток в культуре р1 (пассаж №1), 5-е сутки. Фазовый контраст (увеличение х10).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Сущность изобретения поясняется чертежами, где на фиг 1 изображено устройство для выделения клеточных фракций из тканей человека и животных в развернутом виде; на фиг 2 изображено устройство в развернутом виде в разрезе; на фиг 3 изображено устройство в собранном виде; на фиг 4 изображено устройство в собранном виде в разрезе; на фиг 5 изображено устройство (вид сверху). На фиг. 6 приведена микрофотография монослоя клеток в культуре р0 (пассаж №1), 5-е сутки. Фазовый контраст. Увеличение х10; на фиг. 7 приведена микрофотография монослоя клеток в культуре р1 (пассаж №1), 5-е сутки. Фазовый контраст. Увеличение х10 (т. 1).
Устройство для выделения клеточных фракций из тканей человека и животных представляет собой замкнутую герметичную систему в виде прозрачной конусовидной емкости (А) с нанесенной внешней градуировкой по объему (3), совокупностью каналов (2.1, 2.2, 2.3, 2.4) и штуцеров-переходников (1), имеющих разъемы типа «луер-лок», закрепленную в прозрачный кожух-чехол (С) посредством байонетного соединения (4); причем емкость разделена системой микрофильтров (D) на две камеры - рабочая камера для обработки ткани (В) и камера для концентрирования клеток (Е).
Система микрофильтров представляет собой совокупность по крайней мере из двух нейлоновых микрофильтров (9), разделенных полимерными прокладками (10) и помещенными в полимерный корпус, содержащий верхнюю часть - силиконовую прокладку (8) и основание (11), имеющий на своей окружности рычаги и запирающий элемент (12) для соединения с камерой обработки ткани (В) и камерой для концентрирования клеток (Е). Система микрофильтров устанавливается в емкость в силиконовую прокладку (8). Устройство имеет изолированные каналы (2.1, 2.2, 2.3, 2.4), расположенные в боковых стенках емкости, причем вход каждого канала имеет углубления и секторальные пазы (на чертежах устройства отсутствует) для байонетного соединения со штуцерами-переходниками. Устройство имеет бактериологический фильтр (5) для выравнивания давления внутри системы. Устройство имеет крышку (F) по крайней мере с одним отверстием, причем крышка по своей окружности имеет запирающие элементы и соединяется с емкостью через силиконовую прокладку (7) посредством байонетного соединения или резьбы (13). Устройство имеет штуцеры-переходники (1) для каждого из каналов. Устройство имеет подставку-кожух (С) с ножками в виде лопастей (6).
ПРИМЕР ОСУЩЕСТВЛЕНИЯ СПОСОБА
Приведенный пример не предназначен для ограничения изобретения, а предложен исключительно в качестве иллюстрации.
В общем виде работа устройства представляет собой процесс постадийной отмывки и обработки жировой ткани протеолитическими ферментами с целью выделения стромально-васкулярной фракции, где жировую ткань - липоаспират вносят в устройство - герметичную емкость (А), а именно в камеру для обработки ткани (В) через канал (2.1), посредством соединения шприца с биологическим материалом со штуцером-переходником (1). Биологическая ткань отмывается от остатков крови в буферном растворе, внесенном через канал (2.2). Излишки жидкости удаляются из системы через канал (2.4). Биологическая ткань подвергается ферментативной обработке смесью протеолитических ферментов, внесенных через канал (2.2). Устройство подвергается центрифугированию при котором стромально-васкулярная фракция проходит через систему микрофильтров (D) в камеру для концентрирования клеток (Е). Излишки жидкости удаляются через канал (2.3), осадок отмывается от остатков ферментов буферным раствором. Конечная стромально-васкулярная фракция отбирается через канал (2.4).
Работу выполняли на 3 образцах липоаспирата, полученного в результате операции по липосакции. Липоаспират собирали в шприцы типа с замком «луер-лок» объемом 50 мл. Липоаспират в объеме 100 мл аккуратно по стенке вносили в систему в камеру для обработки ткани (В) через канал (2.1), посредством соединения шприца (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Вносили сбалансированный солевой раствор Хэнкса в объеме 100 мл через канал (2.2) посредством соединения шприца с буфером (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Систему помещали в термостатируемую при 37°С камеру с шейкером со скоростью вращения 100-150 об./мин на 15-20 минут для промывки биологического материала. Систему центрифугировали при 500 g в течение 10 мин. Не переворачивая систему, с помощью шприца аккуратно отбирали осадок через канал (2.4) в объеме 100 мл и плотно закрывали крышку. Повторяли цикл промывки три раза. Вносили смесь коллагеназы I, коллагеназы II, термолизина, диспазы и трипсина в общем объеме 10 мл через канал (2.2) посредством соединения шприца (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Вносили сбалансированный солевой раствор Хэнкса в объеме 90 мл через канал (2.2) посредством соединения шприца (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Систему помещали в термостатируемую при 37°С камеру с шейкером со скоростью вращения 100-150 об./мин на 45 минут для ферментативной обработки биологического материала. Систему центрифугировали при 1000 g в течение 30 мин. Не переворачивая систему, с помощью шприца аккуратно отбирали примеси жира, стромы, дебриса и остатков эритроцитов через канал (2.3) в объеме 190 мл, посредством соединения шприца (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Вносили сбалансированный солевой раствор Хэнкса в объеме 190 мл через канал (2.2) посредством соединения шприца (на рисунке не показан) со штуцером переходником (тип 1) и плотно закрывали крышку штуцера переходника. Систему центрифугировали при 1000 g в течение 5 мин. Процедуру промывки повторяли три раза. Не переворачивая систему, с помощью шприца аккуратно отбирали примеси жира, стромы и дебриса через канал (2.3) в объеме 190 мл и плотно закрывали крышку. С помощью шприца вносили 10 мл аутосыворотки пациента через канал (2.2). Систему помещали в термостатируемую при 37°С камеру с шейкером со скоростью вращения 100-150 об./мин на 5 минут для инактивации ферментов. Систему центрифугировали при 1000 g в течение 5 мин. Отбирали стромально-васкулярную фракцию через канал (2.4) в объеме 2 мл.
Полученную первичную культуру клеток стромально-васкулярной фракции характеризовали по жизнеспособности клеточных элементов и экспрессии поверхностных маркеров - CD90, CD105, CD73, CD34, CD11b, CD19, CD45, CD44 сразу после выделения, на первом и втором пассажах.
Были проанализированы не менее 100 000 событий для каждого образца. После обработки и центрифугирования клеточной суспензии согласно протоколу проводили анализ прямого (FSC) и бокового (SSC) светорассеяния в целях определения размеров изучаемых объектов и наличия внутриклеточных включений.
Выделенная фракция характеризуется «чистотой» событий и низким содержанием дублей и дебриса. По оптическим характеристикам были определены лимфоцитарно-моноцитарный гейт и целевая фракция клеток. Так, было показано, что на 47 264 события отдельные клетки составляли 92%, что в абсолютных величинах составляет 43 487 события; дубли (слипшиеся клетки) - 1,4%, а дебрис (остатки клеток в образце) и эритроциты лишь 6,2%. Из общего пула единичных событий лимфоцитарно-моноцитарный гейт составил 91,8%, а целевая фракция - 7,5%. В то же время, общая концентрация клеток стромально-васкулярной фракции в образце в пересчете на единицу объема составила 66000 клеток на 100 мкл.
Для выявления и анализа регенераторной фракции в выделенном образце использовали общепринятые маркеры зрелых стволовых клеток - CD90, CD73, CD105, CD44.
Результаты эксперимента показали, что выделенная фракция содержит до 20% CD 90 позитивных клеток, 0,24% CD105 позитивных клеток, не менее 0,01% CD44 позитивных клеток. Экспрессия эндоглина (CD 105) характерна для МСК после пассирования, однако данный маркер может экспрессироваться и на прогениторных клетках - «мезенхимоангиобластах». Таким образом, процентное содержание регенераторных клеток в выделенной стромально-васкулярной фракции составляет 0,5%.
Был проведен анализ жизнеспособности клеточной фракции, включающей подсчет клеток, находящихся в состоянии апоптоза и подсчет мертвых клеток. Исследование выполнено с использованием теста, основанного на использовании аннексина V (Annexin V меченый FITC), аффинного к фосфатидилсерину, который в процессе апоптоза локализуется на клеточной поверхности и формирует один из специфичных сигналов для распознавания апоптотических клеток. Результаты аннексинового теста показали, что в исследуемой фракции клеток 1,02% находится в состоянии апоптоза, 0,04% разрушенных и 98,94% живых клеток.
После пассирования клеток наблюдали стойкое увеличение экспрессии CD 90 и CD 105, что характерно для мезенхимальных стромаьных клеток в культуре. На пятые сутки каждого пассажа клетки достигали 100% конфлюэнтности (монослоя), что продемонстрировано на фиг. 3 и фиг. 4
Выше было описано устройство для выделения клеточных фракций из тканей человека и животных, содержащее герметичную емкость для обработки ткани с системой каналов и штуцеров-переходников, в котором, согласно изобретению, емкость для обработки ткани имеет конусообразную форму и разделена на две камеры системой микрофильтров с диаметром пор 10-500 мкм, герметично закрепленна байонетным соединением через силиконовую прокладку, причем одна камера служит для обработки ткани, а другая для концентрирования клеток, причем емкость покрыта с внутренней поверхности гидрофобным антиадгезивным покрытием, а для минимизации площади внутренней поверхности имеет каналы, расположенные в толще стенки емкости, причем один из каналов выходит в камеру обработки ткани, а другой в камеру концентрирования клеток, а с целью выравнивания давления имеет бактериологический фильтр.
Выше был также описан способ выделения клеточных фракций из тканей человека и животных с использованием предлагаемого устройства, который включает декантацию липоаспирата; деликатную отмывку липоаспирата в буферных растворах; ферментативную обработку с использованием смеси коллагеназ, термолизина, диспазы и трипсина при 37°С; центрифугирование при 500-2000 g и фильтрацию через микрофильтры с размером пор 10-300 мкм с последующим удалением примесей жира и стромальной ткани; вторичную отмывку и концентрацию клеточной фракции
Хотя настоящее изобретение было подробно описано на примерах вариантов, которые представляются предпочтительными, необходимо помнить, что эти примеры осуществления изобретения приведены только в целях иллюстрации изобретения. Данное описание не должно рассматриваться как ограничивающее объем изобретения, поскольку в этапы описанных способов и устройств специалистами в области медицинской биотехнологии и клеточной технологии и др. могут быть внесены изменения, направленные на то, чтобы адаптировать их к конкретным устройствам или ситуациям, и не выходящие за рамки прилагаемой формулы изобретения. Специалисту в данной области понятно, что в пределах сферы действия изобретения, которая определяется пунктами формулы изобретения, возможны различные варианты и модификации, включая эквивалентные решения.
ССЫЛКИ
1. System for processing lipoaspirate cells ЕР 1921133 A2
2. Method and Apparatus for Separating a Material US 20110251041 A1
3. Regenerative cell extraction device WO 2013183797 A1
4. Device for separating adult stem cell US 20130344589 A1
5. System and methods for preparation of adipose-derived stem cells, US 20130012921 A1, WO 2014011213 A1
1. Устройство для выделения стромально-васкулярной фракции из тканей человека и животных, содержащее герметичную емкость для обработки ткани с системой каналов и штуцеров-переходников, отличающееся тем, что емкость для обработки ткани имеет конусообразную форму и разделена на две камеры системой микрофильтров, представляющей собой по крайне мере два нейлоновых микрофильтра диаметром пор от 10 мкм для нижнего фильтра до 500 мкм для верхнего фильтра, разделенных полимерными прокладками, герметично закрепленна байонетным соединением через силиконовую прокладку, причем одна камера служит для обработки ткани, а другая для концентрирования клеток, причем емкость покрыта с внутренней поверхности гидрофобным антиадгезивным покрытием и имеет каналы, расположенные в толще стенки емкости, причем один из каналов выходит в камеру обработки ткани, а другой в камеру концентрирования клеток, при этом емкость также имеет бактериологический фильтр, выполненный с возможностью выравнивания давления внутри устройства.
2. Устройство по п. 1, отличающееся тем, что имеет ножки в виде лопастей в нижней части конуса.
3. Устройство по п. 1, отличающееся тем, что имеет пазы для закрепления на бакет-роторе центрифуги, причем устройство снабжено внутренней стальной арматурой по ходу пазов.
4. Устройство по п. 1, отличающееся тем, что имеет насосы для подачи жидкостей и отбора клеток.
5. Способ выделения клеточных фракций из тканей человека и животных с использованием устройства по любому из пп.1-4, включающий декантацию липоаспирата; деликатную отмывку липоаспирата в буферных растворах; ферментативную обработку липоаспирата с использованием смеси коллагеназ, термолизина, диспазы и трипсина при 37°С; центрифугирование при 500-2000 g и фильтрацию через микрофильтры с размером пор 10-500 мкм с последующим удалением примесей жира и стромальной ткани; вторичную отмывку и концентрацию клеточной фракции.
6. Стромально-васкулярная фракция жировой ткани, полученная с использованием устройства по п.1, для создания тканеинженерных конструкций на основе синтетических и природных материалов.
7. Стромально-васкулярная фракция жировой ткани, полученная с использованием устройства по п. 1, для использования в качестве клеточного аутотрансплантата.
8. Способ лечения, репарации или замещения ткани, включающий введение стромально-васкулярной фракции жировой ткани по п. 7 в твердые и/или мягкие ткани человека или животных.