Блок имплантата для реконструкции дефектной части кости и способ реконструкции дефектной части кости
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к челюстно-лицевой хирургии, и предназначена для использования при реконструкции дефектной части кости, в частности атрофированной части челюсти с последующей или одновременной имплантацией зуба. Блок имплантата для реконструкции дефектной части кости, включающий несущую часть из биосовместимого с костной тканью материала и полость, предназначенную для размещения биоматериала, выполнен по крайней мере из одного объемного элемента, способного к деформации и сплетению с образованием единой пространственной ячеистой конструкции в объеме планируемой реконструкции дефектной части кости. Предпочтительно его элемент выполнять из титана в виде спирали или объемной паутинки, обладающих возможностью пластической и/или упругой деформации, при этом возможно спираль выполнять цилиндрической, конической, бочкообразной или с торовой образующей, а паутинку с регулярной или нерегулярной структурой. В части способа реконструкции дефектной части кости, включающего создание в дефектной костной части рецепиентного ложа и формирование соответствующего объему планируемой реконструкции блока имплантата из биосовместимого с костной тканью материала, блок имплантата выполняют из набора способных к деформации и сплетенных между собой с образованием единой пространственной конструкции ячеистых объемных элементов в количестве не менее одного, и деформируют его путем фиксации к поверхности рецепиентного ложа в объеме планируемой реконструкции, предпочтительно блок имплантата окончательно формировать путем фиксации поверх него защитной мембраны, оптимально пространство в объеме блока имплантата заполнять остеоиндуктивным биоматериалом. Изобретения позволяют повысить технологичность и снизить инвазивность способа при одновременном обеспечении унификации и повышении функциональности блока имплантата. 2 н. и 13 з.п. ф-лы, 6 ил., 2 пр.
Реферат
Изобретение относится к медицине, преимущественно к челюстно-лицевой хирургии, и может быть использовано для реконструкции дефектной части кости, в частности атрофированной части челюсти с последующей или одновременной имплантацией (зуба).
Известен способ реконструкции атрофированной альвеолярной части нижней челюсти, заключающийся в использовании костного блока аутотрансплантата, состоящего из костных пластин и костной крошки, заполняющей пространство реконструкции, ограниченное костной пластиной и альвеолярной частью челюсти. Способ предусматривает фиксацию костных пластин с помощью внутрикостных шурупов к краю кости атрофированной альвеолярной части нижней челюсти. Костную пластину фиксируют параллельно краю кости атрофированной альвеолярной части челюсти [Khoury F. Happe A: Zur Diagnostik und Methodik von intraoralen Knochenentnahmen. Zzahnarztl Implantol 1999:15(3): 167-176].
Этот аналог имеет следующие недостатки:
- конструкция аналога не способна обеспечить стабильность объема костного блока на время формирования регенерата;
- способ фиксации костного блока, предложенный в аналоге, невозможен при выраженной в вертикальном направлении атрофии края кости альвеолярной части челюсти;
- не обеспечиваются условия для создания максимальной площади соприкосновения костного блока с костью реципиентного ложа края кости атрофированного альвеолярного отростка.
Наиболее близким к заявленному - прототипом - является способ реконструкции атрофированной альвеолярной части нижней челюсти, согласно которому формируют костный блок из двух параллельных костных пластин, фиксированных между собой и к поверхности рецепиентного ложа, а также костной крошки между ними таким образом, что одну костную пластину фиксируют непосредственно к поверхности рецепиентного ложа, перпендикулярно к краю кости альвеолярной части или телу нижней челюсти, а вторую - над ней, и пространство между костными пластинами заполняют костной крошкой, при этом расстояние между костными пластинами определяется объемом планируемой реконструкции.
Прототип характеризуется следующими преимуществами:
- при фиксации костной пластины непосредственно к поверхности рецепиентного ложа обеспечивается максимальная площадь соприкосновения костного блока с костью рецепиентного ложа атрофированного альвеолярного отростка, что в дальнейшем повышает качество регенерата;
- жесткая конструкция из двух костных пластин с костной крошкой между ними обеспечивает сохранение объема костного блока во время формирования регенерата;
- при выраженной в вертикальном направлении атрофии края кости альвеолярной части челюсти возможна фиксация костных пластин к телу нижней челюсти.
Таким образом, по сути, прототип представляет собой способ реконструкции дефектной части кости, включающий создание в дефектной костной части рецепиентного ложа и формирование соответствующего объему планируемой реконструкции блока имплантата, содержащего фиксированный к кости каркас из биосовместимого с костной тканью материала, заполненный биоматериалом.
К недостаткам прототипа следует отнести:
- невысокую функциональность (в части васкуляризации/реваскуляризации, остеокондуктивности, некоторых других параметров) блока имплантата в отличие от функциональности реконструируемой кости вследствие существенного различия их структуры;
- низкую технологичность способа, обусловленную уникальностью используемого блока имплантата;
- повышенную инвазивность, вызванную использованием донорских участков пациента для изготовления каркаса.
Задача изобретения - создание блока имплантата, имеющего максимально схожую структуру со структурой реконструируемой кости, и эффективного и технологичного способа реконструкции дефектной части кости без использования донорских участков пациента.
Достигаемый технический результат - повышение технологичности и снижение инвазивности способа при одновременном обеспечении унификации и повышении функциональности блока имплантата.
Поставленная задача решается, а заявленный технический результат достигается тем, что блок имплантата для реконструкции дефектной части кости, включающий несущую часть из биосовместимого с костной тканью материала и полость, предназначенную для размещения биоматериала, выполнен по крайней мере из одного объемного элемента, способного к деформации и сплетению с образованием единой пространственной ячеистой конструкции в объеме планируемой реконструкции дефектной части кости, предпочтительно его элемент выполнять из титана в виде спирали или объемной паутинки, обладающих возможностью пластической и/или упругой деформации, при этом возможно спираль выполнять цилиндрической, конической, бочкообразной или с торовой образующей, а паутинку с регулярной или нерегулярной структурой, в части способа реконструкции дефектной части кости, включающего создание в дефектной костной части рецепиентного ложа и формирование соответствующего объему планируемой реконструкции блока имплантата из биосовместимого с костной тканью материала, блок имплантата выполняют по крайней мере из одного объемного элемента, способного к деформации и сплетению с образованием единой пространственной ячеистой конструкции, и деформируют его путем фиксации к поверхности рецепиентного ложа в объеме планируемой реконструкции, предпочтительно блок имплантата окончательно формировать путем фиксации поверх него защитной мембраны, оптимально пространство в объеме блока имплантата заполнять остеоиндуктивным биоматериалом.
Изобретение поясняется иллюстрациями, где изображены:
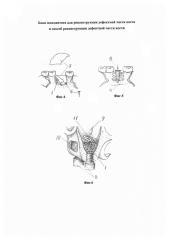
Фиг. 1 - примеры элементов блока имплантата;
Фиг. 2-5 - поэтапный пример реконструкции дефектной части кости;
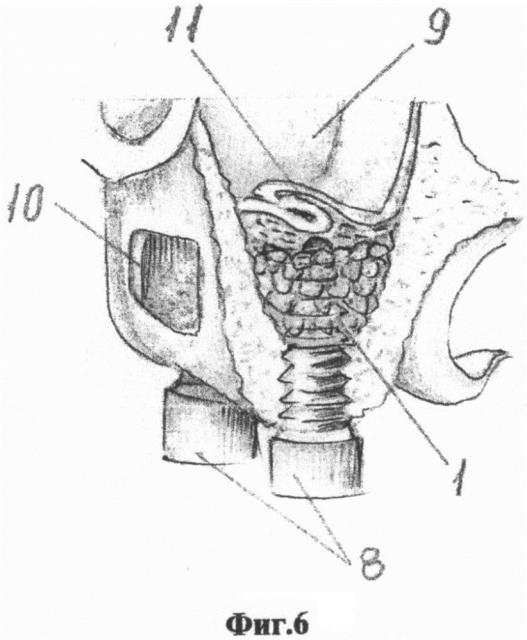
Фиг. 6 - пример открытого синус-лифтинга костной ткани в области гайморовых пазух через латеральное окно.
В соответствии с изобретением блок имплантата 1 выполнен в виде объемного элемента (на Фиг. 1 это: а) - объемная паутинка с регулярной структурой, б) - набор вплетенных друг в друга цилиндрических спиралей) с ячейками 2, предназначенными для заполнения биоматериалом 3 в процессе установки блока имплантата и/или регенерируемым телом реконструируемой кости 4 после установки блока имплантата. Исполнение блока имплантата может быть весьма разнообразным, однако, исходя из соображений технологичности, его удобнее выполнять из титановой (биосовместимой с костной тканью) проволоки по форме спирали или объемной паутинки. Возможно использование, например, тантала, но это более дорогостоящий и менее технологичный материал. Как показывает практика, толщина проволоки (в зависимости от вида реконструкции) может колебаться в широких пределах, однако основной диапазон можно выделить от 0,05 до 1 мм, что обусловлено, с меньшей стороны - способностью проволоки выполнять несущую функцию, а с большей стороны - возможностью деформации проволоки в процессе адаптации блока имплантата в рецепиентном ложе 5 в объеме реконструкции. Размер ячеек 2 определяется возможностью их беспрепятственного заполнения в объеме всего блока имплантата 1 биоматериалом 3, в зависимости от толщины проволоки можно выделить наиболее приемлемый диапазон от 0,1 до 2 мм. Блок имплантата 1 может быть выполнен как одноэлементным (например, по форме объемной паутинки, как это показано на Фиг. 1, а) так и двух - и более элементным, например, состоящим из нескольких ввитых друг в друга спиральных элементов (см. Фиг. 1, б). Элементы блока имплантата до стерилизации целесообразно подвергать специальной обработке. Для титана это двойное протравливание смесью HCL+H2SO4 при температуре 100°C, что обеспечивает выраженную пористость поверхности, что усиливает остеоинтегративные свойства поверхности, на которой может располагаться минерализованная матрица кости и покрываться выделенными из крови плазматическими белками, такими как фибропектин и витропектин. Титан (в достаточно чистом виде) имеет ценное качество биосовместимости - когда кость не реагирует на металл, как на инородное тело, а признает его иммунологически себе подобным. Липофильные свойства поверхности блока имплантата поддерживают связывание белков и последующее формирование временной фибриновой сети. Плотная сеть фибрина обеспечивает быстрое прилипание остеогенных клеток-остеобластов. Вследствие гидрофильности поверхности титанового блока имплантата обеспечивается адекватное кровоснабжение между костной тканью и остеогенными клетками, расположенными на поверхности титанового блока имплантата. Ускоренная вербовка остеобластов на поверхность титанового блока имплантата приводит к формированию костной ткани за 3-4 месяца. Таким образом остеокондуктивность и остеоиндуктивность заявленного блока имплантата близка к остеокондуктивности и остеоиндуктивности реконструируемой кости.
Заявленный способ реконструкции дефектной части кости с использованием вышеописанного блока имплантата реализуется следующим образом.
Осуществляют разрез мягких тканей и их отслойку от кости. Формируют рецепиентное ложе путем придания ему ровной и устойчивой формы и его перфорации для улучшения кровоснабжения реконструируемой области. Формируют подходящий блок имплантата 1 для реконструкции дефектной части кости, как это описано выше, и размещают его в рецепиентном ложе 5. Поскольку блок имплантата, что следует из его материала и формы, сжимаем/разжимаем практически в любом направлении, его форму, используя упруго-пластические свойства, подгоняют под необходимую конфигурацию и фиксируют к реципиентному ложе 5 фиксирующими винтами 6. Ячейки 2 блока имплантата 1 целесообразно заполнить остеоиндуктивным биоматериалом 3, который следует обильно пропитать кровью (при небольшом объеме реконструкции возможно не заполнять ячейки внешним биоматериалом, имея в виду, что они заполнятся регенирируемой костной тканью пациента). Затем блок имплантата 1 покрывают изолирующей мембраной 7 (резорбируемой или нерезорбируемой, в зависимости от вида операции), предназначенной для обеспечения направления регенерации реконструируемой области от реципиентного ложа (регенерируется костная ткань), а не от мягких тканей (когда регенерируется мягкая грануляционная ткань). Одновременно мембрана 7 может выполнять и формообразующую функцию, в этом случае ее следует в положении, когда она за счет натяжения придает блоку имплантата 1 окончательную форму, зафиксировать относительно кости, например, фиксирующими винтами 6. Через сформированный имплантат (в случае дентальной операции) в челюстную кость можно сразу инсталировать зубной имплант 8 (Фиг. 5). Аналогично возможно, например, осуществить открытый синус-лифтинг (субантральную аугментацию) костной ткани в области гайморовых пазух 9 через латеральное окно 10 для доступа к дну гайморовой пазухи, сохраняя целостность слизистой оболочки 11 гайморовой пазухи (Фиг. 6).
Примеры реализации способа реконструкции дефектной части кости.
Пример 1. Больная К., 47 лет. Диагноз: вторичная адентия верхней челюсти, концевой дефект справа, вертикальная атрофия альвеолярной части челюсти в области 13-14 зубов. Нет возможности из-за деффекта объема костной ткани устанавливать дентальный имплант без вертикальной аугменгтации. При планировании операции у пациентки получены следующие размеры деффекта альвелярного гребня: 24×1.4×2 мм. Исходя из этого подготовлен титановый блок из девяти вплетенных друг в друга цилиндрических спиралей диаметром 2 мм из титановой проводки толщиной 0,15 мм. Титановый блок по габаритам составил 26×1.6×2. Начало операции: проведена подготовка пациентки к операции - премедикация, антибиотикотерапия. Под инфильтрационным обезболиванием отслоен слизисто-надкостничный лоскут в области аугментации, подготовлено реципиентное ложе, кортикальная пластинка перфорирована по размеру дефекта кости, в области деффекта адаптирован сжатием в объеме реконструкции (деффекта альвелярного гребня) титановый блок и наглухо зафиксирован пятью титановыми винтами 2×8 мм. Ячейки блока заполнены биоматериалом (Bio oss), сверху блок накрыт резорбируемой мембраной, которая в свою очередь тоже зафиксирована шовной нитью №4 к блоку. Блок дополнительно пропитали кровью пациентки с линкомицином. В связи с нехваткой мягких тканей был проведен расщепленный метод. Лоскуты уложили на место и зафиксировали без натяжения шовным материалом №3. Пациентка была отпущена домой со стандартными послеоперационными рекомендациями. Через 12 дней сняты швы. Пациентка чуствует себя удовлетворительно, сохраняется небольшая отечность и гиперемия. На 3 месяц после оперативного вмешательства мембрана рассосалась и ячейки титанового блока заполнились молодой костью, таким образом регенерация прошла без видимых осложнений. Винты были отвинчены на месте фиксации блока. Произведен второй этап - инсталляция дентальных имплантов (2 шт. ) через реконструированный участок (имплантат). Первичная стабильность показала 25 Н/см2, что является показателем, практически соответствующим показателю собственной кости пациента.
Пример 2. Пациентка Л., 50 лет, диагноз - частичная вторичная адентия верхней челюсти слева, включенный дефект. Отсутствуют 25, 26 зубы. Планируется дентальная имплантация в области 25, 26 зубов. После изучения 3D компьютерной томографии выявлено, что высота костного гребня составила 4.6 мм. Рекомендована субантральная аугментация с одноэтапным имплантированием. Архитектоника кости в области имплантации четвертого типа, т.е. в основном рыхлая губчатая кость. Рекомендовано применение титанового блока, который будет фиксироваться со стороны дна гайморовой пазухи зубными имплантами (Фиг. 6). После отслойки слизисто-надкостничного лоскута и формирования латерального окна, аккуратно отслоив слизистую оболочку гайморовой пазухи без разрывов, и затем отодвинув ее так, чтобы освободить площадку для будущего блока имплантата и дентальных имплантов в области дна гайморовой пазухи на запланированных местах имплантации. До установки имплантов и формирования имплантационного ложа, на будущем блоке обозначены условные отверстия, тем самым рассчитав расстояния между двумя имплантами, путем натяжения проволок, т.к. блок имеет сетчатую структуру и легко адаптируется, сохраняя целостность, а поверхность импланта имеет агрессивную резьбу и коническую форму, что позволяет импланту самонакручиваться через сетчатую структуру блока и надежно схватываться с проволочным каркасом и стабильно фиксироваться на поверхности титанового блока, тем самым достигать надежную первичную стабильность импланта внутри кости. Костной фрезой сформировано имплантационное ложе меньшего размера, чем диаметр дентальных имплантов, по направлению к гайморовой пазухе. Затем титановый блок имплантата, надежно удерживая инструментом, уложили на дно гайморовой пазухи так, чтобы условные отверствия совпадали с имплантационными ложами. Через имплантационные лунки вкрутили импланты так, чтобы они вошли в условные отверстия титанового блока. Имплант, проходя через блок имплантата, осуществляет натяжение блока на себя, вкручиваясь в сетчатую поверхность блока, тем самым нет необходимости дополнительной фиксации блока к кости. Далее те зоны уже импланта и блока, которые располагаются открыто в гайморовой пазухе, заполняем сухим остеопластическим материалом (Bio oss), пропитывая его кровью пациента вместе с линкомицином. Изолирующую мембрана не была использована в области блока, мембраной было изолировано латеральное окно. Слизисто-надкостничный лоскут уложен на место, рана ушита. Применив титановый блок при субантральной аугментации с одномоментной имлантацией в области 25,26 зубов и связав блок с имплантами, достигнута надежная первичная стабильность имплантов, по сути замещена отсутствующая часть плотной кортикальной пластинки, поскольку титановый блок и имплантат однородны, по отношению к кости инертны и толерантны, и составили единую целостность и замену отсутствующей части плотной кости (кортикальной пластины). На дому назначено: щадящая диета, воздержание от перелетов, нагрузок, тепловых процедур в течение 2-3 недель, ротовые ванночки (0.05% раствором хлоргексидина, бетадина), антибиотики (аммоксиклав 625 мг по 1 таблетке 2 раза в день до еды 5-7 дней), линекс по 2 капсулы 3 раза в день 8-10 дней, кальцийсодержащие препараты (остеогенон 40 таблеток по 1 таблетке 2 раза вдень 20 дней), биопарокс в нос 2-3 раза 8-10 дней. Снятие швов проводилось на десятый день, состояние стабильное, рана заживает первичным натяжением, незначительная гиперемия раневой поверхности, болезненность при пальпации по переходной складке. Полная стабилизация (выздоровление) наблюдалась на 23 день после операции.
Таким образом вышесказанное свидетельствует о том, что поставленная задача изобретения - создание блока имплантата, имеющего максимально схожую структуру со структурой реконструируемой кости, и эффективного и технологичного способа реконструкции дефектной части кости без использования донорских участков пациента - решена, и заявленный технический результат - повышение технологичности и снижение инвазивности способа при одновременном обеспечении унификации и повышении функциональности блока имплантата - достигнут.
Анализ заявленного технического решения на соответствие условиям патентоспособности показал, что указанные в независимых пунктах формулы изобретения признаки являются существенными и взаимосвязаны между собой с образованием устойчивой совокупности неизвестной на дату приоритета из уровня техники необходимых признаков, достаточной для получения требуемого синергетического (сверхсуммарного) технического результата.
Таким образом, вышеизложенные сведения свидетельствуют о выполнении при использовании заявленного технического решения следующей совокупности условий:
- объект, воплощающий заявленное техническое решение, при его осуществлении относится к медицине, преимущественно к челюстно-лицевой хирургии, и может быть использовано для реконструкции дефектной части кости, в частности, атрофированной части челюсти с последующей или одновременной имплантацией (зуба);
- для заявленного объекта в том виде, как он охарактеризован в независимом пункте нижеизложенной формулы, подтверждена возможность его осуществления с помощью вышеописанных в заявке или известных из уровня техники на дату приоритета средств и методов;
- объект, воплощающий заявленное техническое решение, при его осуществлении способен обеспечить достижение усматриваемого заявителем технического результата.
Следовательно, заявленный объект соответствует требованиям условий патентоспособности «новизна», «изобретательский уровень» и «промышленная применимость» по действующему законодательству.
1. Блок имплантата для реконструкции дефектной части кости, включающий несущую часть из биосовместимого с костной тканью материала и полость, предназначенную для размещения биоматериала, отличающийся тем, что он выполнен по крайней мере из одного объемного элемента, способного к деформации и сплетению с образованием единой пространственной ячеистой конструкции в объеме планируемой реконструкции дефектной части кости.
2. Блок имплантата для реконструкции дефектной части кости по п. 1, отличающийся тем, что его элемент выполнен из титана.
3. Блок имплантата для реконструкции дефектной части кости по п. 1, отличающийся тем, что его элемент выполнен в виде спирали.
4. Блок имплантата для реконструкции дефектной части кости по п. 1, отличающийся тем, что его элемент выполнен в виде объемной паутинки.
5. Блок имплантата для реконструкции дефектной части кости по п. 1, отличающийся тем, что его элемент выполнен с возможностью пластической деформации.
6. Блок имплантата для реконструкции дефектной части кости по п. 1, отличающийся тем, что его элемент выполнен с возможностью упругой деформации.
7. Блок имплантата для реконструкции дефектной части кости по п. 3, отличающийся тем, что его элемент выполнен в виде цилиндрической спирали.
8. Блок имплантата для реконструкции дефектной части кости по п. 3, отличающийся тем, что его элемент выполнен в виде конической спирали.
9. Блок имплантата для реконструкции дефектной части кости по п. 3, отличающийся тем, что его элемент выполнен в виде бочкообразной спирали.
10. Блок имплантата для реконструкции дефектной части кости по п. 3, отличающийся тем, что его элемент выполнен в виде спирали с торовой образующей.
11. Блок имплантата для реконструкции дефектной части кости по п. 4, отличающийся тем, что его элемент выполнен в виде объемной паутинки с регулярной структурой.
12. Блок имплантата для реконструкции дефектной части кости по п. 4, отличающийся тем, что его элемент выполнен в виде объемной паутинки с нерегулярной структурой.
13. Способ реконструкции дефектной части кости, включающий создание в дефектной костной части рецепиентного ложа и формирование соответствующего объему планируемой реконструкции блока имплантата из биосовместимого с костной тканью материала, отличающийся тем, что блок имплантата выполняют по крайней мере из одного объемного элемента, способного к деформации и сплетению с образованием единой пространственной ячеистой конструкции, и деформируют его путем фиксации к поверхности рецепиентного ложа в объеме планируемой реконструкции.
14. Способ реконструкции дефектной части кости по п. 13, отличающийся тем, что блок имплантата окончательно формируют путем фиксации поверх него защитной мембраны.
15. Способ реконструкции дефектной части кости по п. 13, отличающийся тем, что пространство в объеме блока имплантата заполняют остеоиндуктивным биоматериалом.