Средство, обладающее антимикробным, репаративным и ранозаживляющим действием
Иллюстрации
Показать всеИзобретение относится к средству, обладающему антимикробным, репаративным и ранозаживляющим действием. Указанное средство включает экстракт сухой из побегов рододендрона золотистого с содержанием суммы простых фенолов и фенологликозидов не менее 28%, полученный путем экстракции сырья с размером частиц 2-3 мм водой очищенной при соотношении сырья и экстрагента 1:10, время экстракции при первом контакте фаз 2 ч, втором - 1,5 ч, третьем - 1 ч, при перемешивании сырья и температуре 60±5°С. Изобретение обладает выраженной антимикробной, репаративной и ранозаживляющей активностью. 1 з.п. ф-лы, 1 ил., 11 табл., 1 пр.
Реферат
Описание изобретения
Изобретение относится к химико-фармацевтической промышленности, а именно к созданию средства, обладающего антимикробным, репаративным и ранозаживляющим действием. Средство содержит следующие ингредиенты: экстракт сухой рододендрона золотистого, эмульгатор Т-2, вазелин, воду очищенную. Средство расширяет ассортимент ранозаживляющих средств растительного происхождения, обладает антимикробным, репаративным и ранозаживляющим действием.
Изобретение относится к области медицины, фармации, фармакогнозии, к лекарственным средствам, обладающим выраженным ранозаживляющим действием.
В лечении гнойно-воспалительных заболеваний и сепсиса большое значение имеет борьба с возбудителями заболеваний. Считается общепризнанным, что чистую линейную рану следует защищать от инфекции, так как заживление инфицированной раны протекает медленнее.
Снижение эффективности антибиотикотерапии, интенсивный рост количества послеоперационных осложнений ран, развитие аллергических реакций на лекарственные препараты, содержащие антибиотики, обусловливают необходимость создания новых эффективных лекарственных средств для лечения инфекционно-воспалительных заболеваний кожи и раневого процесса. Одним из путей решения данной проблемы является использование препаратов растительного происхождения, которые малотоксичны, не вызывают аллергических реакций и обладают малыми побочными эффектами.
Известно «Ранозаживляющее средство», представляющее собой мазь, содержащую экстракт сухой сфагнового мха, димексид и полиэтиленгликоль [патент РФ 2396972, А61К 36/902. Авторы: Дмитрук С.Е., Бабешина Л.Г., Дмитрук B.C.].
Известно «Средство, обладающее противовоспалительным, антисептическим и регенераторным действием», представляющее собой эмульсию, содержащую спиртовые экстракты ромашки и календулы, алюминия гидрооксид, ксероформ, метилурацил. Указанное средство наносят тонким слоем на пораженные участки 1-2 раза в течение 7-10 дней. При этом не выявлено никаких побочных явлений, эмульсия ускоренно заживляет раны различной этиологии [патент РФ 2159113, А61К А61Р. Авторы: Гурбанова Ш.И., Гурбанов В.В.].
Известно «Лекарственное средство, обладающее регенерирующим и ранозаживляющим действием», содержащее ферментный препарат панкреатин, метилурацил и полиэтиленоксид. Данная мазь активно воздействует на раневую микрофлору, стимулирует процессы роста и созревания грануляционной ткани и повышает скорость эпителизации [патент РФ 2191574, А61К 31/00, А61Р 17/02. Авторы: Полунина Е.Е., Новоселова Е.А., Яфаров И.Ш.].
Известно «Средство, обладающее противовоспалительным и регенерирующим действием». Средство содержит экстракт хвойной зелени, очищенную живицу кедра (сосны, ели, пихты, лиственницы), мумие, прополис, эфирное масло пихты и растительное масло. Данное средство рекомендуют для наружного применения в медицине и ветеринарии [патент РФ 2418600, А61К 36/15, А61К 35/64, А61К 37/08. Авторы: Шило О.Ю., Коханова Е.В.].
Наиболее близким является «Лечебно-профилактическое средство, обладающее ранозаживляющим и антимикробным действием» [патент РФ 2153349, А61К 35/78. Авторы: Башура А.Г., Глушко С.Н.]. Средство состоит из жидкого (густого или сухого) экстракта из листьев ореха грецкого, полученного с использованием 35-45% спирта этилового. Указанное средство проявляет выраженную антимикробную активность к широкому кругу грамположительных и грамотрицательных тест-микроорганизмов {Bacillus subtilis, Pseudomonas aeruginosa, грибы рода Candida).
Цель изобретения - разработка растительного средства, обладающего антимикробным, репаративным и ранозаживляющим действием.
Технический результат изобретения - расширение ассортимента лекарственных средств растительного происхождения, обладающих антимикробным, репаративным и ранозаживляющим действием, за счет использования экстракта сухого из побегов рододендрона золотистого; повышение фармакологической активности средства достигается за счет увеличения выхода биологически активных веществ из сырья.
Технический результат достигается тем, что побеги рододендрона золотистого экстрагируют водой очищенной методом дробной мацерации в три ступени в динамических условиях; сушку извлечения проводят в распылительной сушилке; готовят мазь, содержащую следующие ингредиенты: экстракта сухого рододендрона золотистого (ЭСРЗ) - 10,0 г, вазелина - 54,0 г, воды очищенной - 27,0 г, эмульгатора Т-2 - 9,0 г.
Рододендрон золотистый {Rhododendron aureum Georgi.) семейства вересковых (Ericaceae), представляет собой кустарник до 50 см высотой с толстыми кожистыми листьями. Растет в темно-хвойных лесах лесного пояса и на влажных каменистых склонах высокогорного пояса в горах Восточного Саяна, на Алтае. Имеются достаточные сырьевые ресурсы этого растения. Надземные органы содержат дубильных веществ 17%, простые фенольные соединения - рододендрин, рододендрол, 5-метокси-1,3-гидроксибензол, флавоноиды - кверцетин, гиперазид [4, 5, 6, 8].
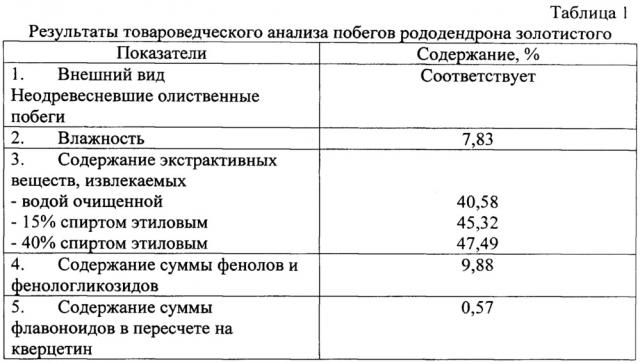
Условия экстракции побегов рододендрона золотистого подобраны экспериментально и приведены в таблицах 1-7.
Новым является то, что в качестве экстрагента применяется вода очищенная, степень измельчения сырья - 2,0-3,0 мм, соотношение сырья - экстрагента - 1:10 на всех трех ступенях экстракции.
Новым является и повышение эффективности процесса экстракции в результате введения температурного фактора (60±5°С) и гидродинамических условий.
Новым является то, что экспериментально установленная продолжительность ступеней экстракции - 2 ч, 1,5 ч, 1 ч обеспечивает сокращение трудозатрат (в известном способе - 24 ч, 6 ч, 6 ч). При этом эффективность предложенного способа экстракции составляет: по экстрактивным веществам - 84,7%, по сумме фенолов и фенологликозидов - 98,768, по сумме флавоноидов - 96,20% (табл. 8).
Новым является введение в мазевую основу ЭСРЗ в количестве 10%.
При получении экстракта сухого из побегов рододендрона золотистого по известному способу при экстрагировании 45% спиртом этиловым эффективность процесса экстракции по экстрактивным веществам составила только 80,7%, по сумме фенольных соединений - 86,4%, по сумме флавоноидов - 96,40% (табл. 8).
Количественное содержание суммы фенолов и фенологликозидов определяли спектрофотометрическим методом.
Около 0,3 г (точная навеска) экстракта сухого помещают в мерную колбу емкостью 200 мл, прибавляют 150 мл воды очищенной и нагревают на водяной бане до полного растворения, охлаждают и доводят водой до метки. Берут из колбы 25 мл и переносят в мерную колбу на 100 мл. К полученному раствору прибавляют 1 мл 8% раствора свинца ацетата основного и нагревают на плитке, поддерживая слабое кипение в течение 10 мин (до полного формирования осадка). Затем прибавляют 5 мл 10% раствора натрия сульфата (для удаления избытка ионов свинца). Далее колбу охлаждают до комнатной температуры в течение 1 часа и доводят объем раствора до метки, перемешивают и фильтруют через двойной бумажный фильтр в сухую колбу. Первые 10-15 мл фильтрата отбрасывают.
Измеряют оптическую плотность полученного раствора на спектрофотометре при длине волны 276 нм в кювете с толщиной слоя 1 см. В качестве раствора сравнения используют воду очищенную. Содержание суммы фенолов и фенологликозидов в пересчете на рододендрин, в процентах вычисляют по формуле:
,
где
D - оптическая плотность исследуемого раствора;
47,2 - удельный показатель поглощения рододендрина (Е 1%1см);
m - масса сухого экстракта, в г;
W - потеря в массе при высушивании экстракта, в %.
Содержание суммы флавоноидов определяли методом дифференциальной УФ-спектрофотометрии по ГФ XI [1, 2]. В ЭСРЗ содержится суммы фенолов и фенологликозидов 25,35-29,22%; суммы флавоноидов 1,47-1,62%; содержание влаги 2,92-4,61%. В ЭСРЗ должно быть суммы фенолов и фенологликозидов не менее 28% (табл. 7).
Новым является то, что в качестве лекарственной формы предлагается использование мази с содержанием 10% экстракта сухого рододендрона золотистого.
Пример. Описание технологического процесса получения экстракта сухого:
1 стадия. В экстрактор помещают 1 кг побегов рододендрона золотистого с размером частиц от 2-3 мм, заливают 10 л воды очищенной. Нагревают до 60±5°С и перемешивают в течение всего времени экстракции - 2 ч. Извлечение фильтруют на друк-фильтре, замеряют объем слитого извлечения (V1=6,7 л). Шрот с фильтра возвращают в экстрактор.
2 стадия. В экстрактор со шротом, оставшимся после первого извлечения, заливают в объеме, равном объему слитого извлечения на первой стадии (6,7 л). Экстракцию проводят 1,5 ч при указанных выше условиях. Фильтруют, замеряют объем слитого извлечения (V2=6,5 л). Шрот с фильтра возвращают в экстрактор.
3 стадия. В экстрактор со шротом, оставшимся после второго извлечения, заливают воду очищенную в объеме 6,5 л. Экстракцию проводят 1 ч при тех же условиях. Фильтруют, замеряют объем слитого извлечения (V3=6,3 л).
4 стадия. Объединяют извлечения V1+V2+V3 = 6,7 л + 6,5 л + 6,3 л и получают 19,5 л извлечения.
Далее извлечение отстаивают при температуре +10°С в течение 3 суток, фильтруют через друк-фильтр. Фильтрат подают в вакуум-распылительную сушилку до остаточной влажности экстракта сухого не более 5,0%.
5 стадия. Отработанный шрот выбрасывают.
Описание технологического процесса получения мази [7]:
1. В емкости 1 (выпарительная чашка) на водяной бане расплавляют (80°С) эмульгатор Т-2 9,0 г, вазелин 54,0 г (60°С), быстро переносят в микроизмельчитель и перемешивают 2 минуты.
2. В емкости 2 (подставка) растворяют 10,0 г ЭСРЗ в 27 мл воды очищенной горячей (60°С).
3. Полученный водный раствор экстракта сухого вводят в расплавленную основу и гомогенизируют на микроизмельчителе тканей 3 минуты.
Количественное содержание суммы фенолов и фенологликозидов в мази определяли спектрофотометрическим методом.
Около 1,0 г (точная навеска) мази помещают в колбу объемом 200 мл, прибавляют 20 мл воды очищенной, нагревают на водяной бане, охлаждают под струей холодной воды (не взбалтывая), фильтруют через бумажный фильтр в мерную колбу объемом 100 мл. Операцию повторяют 3 раза. К полученному раствору прибавляют 1 мл 8% раствора основного ацетата свинца и нагревают на плитке, поддерживая слабое кипение в течение 10 мин (до полного формирования осадка). Затем добавляют 5 мл 10% раствора натрия сульфата (для удаления избытка ионов свинца). Далее колбу охлаждают до комнатной температуры в течение 1 часа и доводят объем раствора до метки, перемешивают и фильтруют через двойной бумажный фильтр в сухую колбу. Первые 10-15 мл фильтрата отбрасывают.
Измеряют оптическую плотность полученного раствора на спектрофотометре при длине волны 276 нм в кювете с толщиной слоя 1 см. Раствор сравнения готовят по методике, указанной выше, из навески мази, приготовленной без экстракта сухого.
Содержание суммы фенолов и фенологликозидов в пересчете на рододендрин в мази с РЗЭС в процентах (X) вычисляют по формуле:
;
где
D - оптическая плотность исследуемого раствора;
47,2 - удельный показатель поглощения рододендрина (Е 1%1см);
m - масса мази, в г.
Количественное содержание суммы фенолов и фенологликозидов в мази составляет 2,52-2,65%.
Антимикробную активность экстракта сухого и мази изучали на 12 штаммах грамположительных и грамотрицательных микроорганизмов на плотной питательной среде методом «лунок». Об активности препаратов судили по величине диаметра стерильной зоны, приняв следующие обозначения: 10 мм - «+», 10-15 мм - «++», 15-20 мм - «+++», 25-30 мм - «++++». Экстракт сухой и мазь проявляют антимикробную активность в отношении Bacillus subtilis, Staphylococcus aureus, Pseudomonas aeruginosa, Salmonella typhymurium (табл. 9).
Ранозаживляющее действие было изучено на модели инфицированной раны, вызванной введением лабораторного штамма Staphylococcus aureus. Опыты проведены на 30 белых крысах, весом 200-230 г, обоего пола линии Wistar, содержащихся в стандартных условиях вивария. Животных содержали в стандартных условиях в соответствии с правилами, утвержденными МЗ СССР 06.07.1973 г., и в соответствии с директивой Совета ЕС от 24.11.1986 г. по вопросам защиты животных, используемых для экспериментальных и других научных целей. Животные получали стандартный пищевой рацион (ПК-120-1).
Исследование ранозаживляющего действия мази с ЭСРЗ проводили в сравнении с мазью «Календула» 10% (регистрационный номер 79/301/5), которая применяется при лечении ожогов, незаживающих ран и свищей. Мазь «Календула» обладает противовоспалительным, противомикробным и репаративным действием [3].
После анестезии тиопенталом-натрия и подготовки кожи крысам на спине параллельно позвоночнику наносили линейную рану до мышечного слоя длиной 3 см. Затем в раны вносили по 0,2 мл взвеси, длительно пассировавшегося на питательных средах лабораторного штамма Staphylococcus aureus, содержащей в 1 мл 109 микробных тел (концентрация определялась по стандарту мутности). После этого раны ушивались адаптационными швами шелком №2.
Животные были разделены на 3 группы по 10 крыс в каждой:
1 группа (контроль) - крысы с полнослойной кожной раной, инфицированной штаммами St.aureus, рана заживала естественным путем;
2 группа (опытная) - крысы с полнослойной кожной раной, инфицированной штаммами St. aureus, получавшие лечение мазью с ЭСРЗ 10%;
3 группа (сравнения) - крысы с полнослойной кожной раной, инфицированной штаммами St. aureus, получавшими лечение мазью «Календула» 10%.
Наличие местного гнойного процесса оценивали на 3, 7 и 14 сутки. Контрольные временные точки определялись тем, что рана приобретает признаки острого воспаления через 72 часа.
Особое внимание уделялось признакам воспаления со стороны раны - гиперемия, пастозность краев, состояние швов, отделяемое из раны (преимущественное гнойное).
Животных выводили из опыта на 14 сутки после внутрибрюшинного введения летальной дозы тиопентала-натрия.
Для ранотензиометрического и гистологического исследования в поперечном направлении из иссеченных ран забирали полоски ткани шириной 0,5 см. Исследование биомеханических свойств заживающей раны производили путем определения прочности сращения ее краев в граммах. С этой целью использовали универсальный прибор для механических и термомеханических испытаний полимерных волокон и пленок модели УМИВ-3 (Россия).
Для гистологического исследования ткани из ран срезы препаратов, фиксированных в формалине, окрашивали гематоксилином и пикрофуксином.
Статистическую обработку полученных данных проводили с помощью программы «Statistica 6,0», предназначенной для оценки результатов медицинских и биологических наблюдений, с вычислением средней арифметической (М), среднеквадратического отклонения (σ), средней ошибки средней арифметической (m), коэффициента достоверности (t), показателя вероятности (р).
Статистическую обработку данных проводили с использованием стандартной программы обработки данных MS Excel.
Результаты исследований свидетельствуют, что на 3-и сутки эксперимента у крыс контрольной группы отмечались гиперемия и пастозность краев раны, обильное гнойное отделяемое с неприятным запахом (около 3 мл), признаки интоксикации (адинамия, жажда, плохой аппетит). Дно раны влажное, гиперемированное, с наложениями фибрина. У крыс опытной группы и группы сравнения указанные явления отмечались у 80% животных - слабая гиперемия и отечность краев раны, небольшое количество гнойного отделяемого без характерного запаха, слабые признаки интоксикации. При этом размер ран у крыс контрольной, опытной и группы сравнения длиной 2,5 см, шириной 0,1 см, со швами.
На 7 сутки эксперимента у животных контрольной группы и группы сравнения сохранялись клинические признаки гнойного воспаления, однако отек и количество гнойного отделяемого из-под сформировавшегося струпа уменьшились. У крыс опытной группы отмечалось незначительное мокнутие ран без запаха. Микробиологические исследования показали отсутствие золотистого стафиллококка в отделяемом из раны. Размер ран у крыс 1-й группы длиной 2,5 см, шириной 0,4 см (диастаз краев раны), у крыс 2-й и 3-й групп - 2.5 см, шириной 0,1 см (диастаза краев нет). При этом у всех групп дно раны очищено и представлено грануляционной тканью.
На 14 сутки эксперимента у крыс 2-й и 3-й групп раны полностью эпителизировались, в то время как в 1-й группе оставались 10% животных с менее выраженной эпитализацией и частичным сохранением струпа. В целом заживление раневого дефекта у всех групп животных в виде рубца.
Результаты исследований свидетельствуют, что мазь с СЭРЗ увеличивает прочность послеоперационного рубца на 14 сутки в 4,1 раза в сравнении с контрольной группой. При этом препарат сравнения мазь «Календула» увеличивал прочность послеоперационного рубца на 14 сутки в 3,6 раза в сравнении с контрольной группой (табл. 10). Мазь с ЭСРЗ превосходит мазь «Календула» на 12,9% по прочности образующегося послеоперационного рубца (рис. 1).
Таким образом, в результате проведенных исследований было установлено, что ранозаживляющее действие мази с СЭРЗ не уступает препарату сравнения - мази с экстрактом календулы.
1. Государственная Фармакопея СССР: вып. 1. Общие методы анализа / МЗ СССР. - 11-е изд., доп. - М.: Медицина, 1987. - 336 с.
2. Государственная Фармакопея СССР: Вып. 2. Общие методы анализа. Лекарственное растительное сырье / МЗ СССР. - 11-е издание, доп. - М.: Медицина, 1990. - 400 с.
3. Государственный реестр лекарственных средств 2014 г. / http://grls.rosminzdrav.ru/grls.aspx.
4. Количественное определение биологически активных компонентов растения Rhododendron aureum Georgi методом ВЭЖХ // Химико-фармацевтический журнал. - 2000. - Т. 34, №12. - С. 30-32.
5. Мирович В.М. Ресурсная характеристика видов рододендронов на территории Иркутской области и западной части республики Бурятия / В.М. Мирович, Г.М. Федосеева, Г.И. Бочарова // Разработка, исследование и маркетинг новой фармацевтической продукции: Сб. научных трудов. Вып. 64. - Пятигорск, 2009. - С. 85-87.
6. Сырчина А.И. Компонентный состав фенольных соединений Rhododendron aureum G. / А.И. Сырчина [и др.] // Растительные ресурсы. - 2000. - Т. 36, вып. 3. - С. 52-55.
7. Фармацевтическая технология. Технология лекарственных форм: учебник / И.И. Краснюк, Г.В. Михайлова, Т.В. Денисова, В.И. Скляренко; под ред. И.И. Краснюка, Г.В. Михайловой. - М.: ГЭОТАР - Медиа, 2011. - 656 с.
8. Флора Центральной Сибири / под ред. Малышева Л.И., Пешковой Г.А. - Новосибирск, 1979. - 1046 с.
1. Средство, обладающее антимикробным, репаративным и ранозаживляющим действием, на основе растительного экстракта, отличающееся тем, что оно содержит экстракт сухой из побегов рододендрона золотистого с содержанием суммы простых фенолов и фенологликозидов не менее 28%, полученный путем экстракции сырья с размером частиц 2-3 мм водой очищенной при соотношении сырья и экстрагента 1:10, время экстракции при первом контакте фаз 2 ч, втором - 1,5 ч, третьем - 1 ч, при перемешивании сырья и температуре 60±5°С.
2. Средство по п.1, отличающееся тем, что оно содержит экстракт сухой рододендрона золотистого, вазелин, эмульгатор Т-2 при следующих соотношениях, мас. %:
экстракт сухой рододендрона золотистого 10,
вазелин 54,
эмульгатор Т-2 9,
вода очищенная 27.