Способ повышения летучести комплексов лантаноидов
Иллюстрации
Показать всеИзобретение относится к способу повышения летучести комплексов лантаноидов. Способ включает получение бета-дикетонатных комплексов лантаноидов и их обработку кислородсодержащими органическими соединениями. В качестве кислородсодержащего органического соединения используются кислородсодержащие фторорганические соединения из класса полифторированных эфиров этиленгликоля общей формулы RF1O(CH2CH2O)RF2, полифторированных эфиров диэтиленгликоля общей формулы RF1O(CH2CH2O)2RF2 или из класса полифторированных формалей общей формулы RF1O(CH2)ORF2, где RF1, RF2 - полифторированные углеводородные радикалы общей формулы H(CF2-CF2)mCH2, где m=1-4. Изобретение позволяет повысить летучесть соединений лантаноидов и снизить температуру испарения соединений лантаноидов до 50-80°С. 4 з.п. ф-лы, 1 табл., 3 пр.
Реферат
Предлагаемое изобретение относится к технологиям, основанным на использовании летучих соединений лантаноидов (лантаноиды - 15 элементов с атомными номерами 57-71). Летучие соединения лантаноидов могут быть использованы в технологиях химического осаждения из газовой фазы при нанесении покрытий со специальными свойствами, при легировании полупроводников и синтезе сверхпроводниковых материалов, при разделении сложных смесей металлов и их глубокой очистке от примесей.
Свойство летучести, то есть сравнительно высокое давление паров (10-1000 Па) при температурах до 200°С, является принципиально важным для возможности технической реализации подобных газофазных процессов [Y.К. Gun'ko, F.Т. Edelmann, Organolanthanides in Materials Science, Comments on Inorganic Chemistry, Volume 19, Issue 3, 1997, p. 153-184]. Повышение летучести, т.е. концентрации соединения лантаноида в газовой фазе, приводит к повышению скорости массопереноса и, следовательно, к повышению производительности процесса. Одновременно, более летучие соединения можно испарять при более низкой температуре, что позволяет упростить аппаратурное оформление процесса. В промышленности в качестве летучих соединений лантаноидов наиболее часто используют бета-дикетонаты лантаноидов общей формулы (R1COCHCOCR2)3Ln, где R1, R2 - алкильный радикал, Ln - атом лантаноида. Бета-дикетонаты лантаноидов сочетают устойчивость на воздухе, простоту синтеза и заметную летучесть при температурах 150-200°С [К. Binnemans, Rare-Earth beta-Diketonates, Handbook on the Physics and Chemistry of Rare-Earth, Vol. 25, 2005, p. 111-247].
Давление паров наиболее летучих индивидуальных бета-дикетонатов лантаноидов: трис-1,1,1,5,5,5-гексафторпентан-2,4-дионатов (гексафторацетилацетонатов, HFA) - R1=R2=CF3, трис-2,2,6,6,-тетраметил-3,5-гептадионатов (дипивалоилметанатов, TMHD) - R1=R2=C(CH3)3) достигает практически приемлемых значений ~10-100 Па только при температурах ~175-200°С [К. Binnemans, Rare-Earth beta-Diketonates, Handbook on the Physics and Chemistry of Rare-Earth, Vol. 25, 2005, p. 111-247; Yu.B. Zwverev, S.C. Chesnokova, Vysokochistye veschestva. V. 1, 1996, p. 75-78]. Для повышения летучести бета-дикетонатов лантаноидов, и снижения тем самым температуры испарения и повышения скорости процессов предложены методы, основанные на обработке бета-дикетонов фосфорорганическими основаниями [US 5698022 A, Lanthanide phosphorus precursor compositions for MOCVD of lanthanide phosphorus oxide films, Dec. 16, 1997] и алкильными эфирами моно-, ди-, три- и т.д. этиленгликолей [US Patent Application Publication 2010/034719 A1, Novel Lanthanide Beta-Diketonate Precursors For Lanthanide Thin Film Deposition, Feb. 11]. Основным недостатком этих способов является невозможность достижения заметной летучести (более 10 Па) соединений лантаноидов при температурах ниже 150°С.
Наиболее близким к предлагаемому способу является способ, описанный в патенте [US 5837321 A, Volatile organic lanthanide compounds and methods for the preparation of lanthanide-containing layered materials from these compounds, Nov. 17, 1998], который выбран нами в качестве прототипа. Согласно данному способу предварительно синтезированные бета-дикетонаты лантаноидов обрабатываются в среде органического растворителя соединением, выбранным из классов кислород или азот содержащих органических соединений (нейтральных донорных лигандов) таких, как алкильные эфиры гликолей, фосфиноксиды, пиридиноксиды, полиамины и т.д., растворитель отгоняется в вакууме, а полученная в остатке композиция используется в качестве летучего соединения лантаноида. Полученные композиции имеют давление паров на уровне 10 Па при температурах 120-140°С.
Недостатком данного способа является сравнительно небольшое повышение летучести (температуру испарения не удается снизить ниже практически удобного уровня 100°С) и образование при испарении композиции значительного количества нелетучего остатка (до 5%) вследствие разложения. Практические неудобства создает также необходимость применения органического растворителя на стадии получения композиции.
Задачей изобретения является повышение летучести комплексов лантаноидов и уменьшение потерь при испарении.
Поставленная задача, а именно, увеличение летучести комплексов лантаноидов (т.е. увеличение давления паров) и уменьшение потерь при испарении за счет разложения, решается добавлением к бета-дикетонату лантаноида кислород содержащего фторорганического соединения из класса полифторированных эфиров этиленгликоля общей формулы RF1O(CH2CH2O)RF2, полифторированных эфиров диэтиленгликоля общей формулы общей формулы RF1O(CH2CH2O)2RF2 или из класса полифторированных формалей общей формулы RF1O(CH2)ORF2, где RF1, RF2 - полифторированные углеводородные радикалы общей формулы H(CF2-CF2)mCH2, где m=1-4. При этом, полифторированные углеводородные радикалы RF1, RF2 в составе фторорганического соединения могут быть как одинаковыми (RF1=RF2), так и различными (RF1≠RF2). Также, обработку бета-дикетоната можно проводить смесью из перечисленных фторорганических соединений, при содержании компонентов в смеси от 0 до 100%.
Кислород содержащие фторорганические соединения, обеспечивающие повышение летучести комплексов лантаноидов согласно данного изобретения, имеют, следовательно, следующие общие формулы:
1. H(CF2-CF2)m1CH2O(CH2CH2O)CH2(CF2-CF2)m2H, где m1, m2 = 1-3 в случае полифторированных эфиров этиленгликоля;
2. H(CF2-CF2)m1CH2O(CH2CH2O)2CH2(CF2-CF2)m2H, где m1, m2 = 1-3 в случае полифторированных эфиров диэтиленгликоля;
3. H(CF2-CF2)m1CH2O(CH2)OCH2(CF2-CF2)m2H, где m1, m2 = 1-3 в случае полифторированных формалей.
Сущность предложенного способа увеличения летучести соединений лантаноидов заключается, таким образом, в обработке бета-дикетонатов лантаноидов кислород содержащими фторорганическими соединениями указанных общих формул 1, 2 или 3 вместо известного способа обработки бета-дикетонатов лантаноидов циклическими, ациклическими эфирами, эфирами гликолей или полиэфирами. При этом обработку осуществляют при перемешивании в течение 0,1-100 часов при температуре 20-100°С.
В качестве бета-дикетонатов лантаноидов могут применяться соединения общей формулы (R1COCHCOCR2)3Ln, где Ln - лантаноид - элемент с атомным номером 57-71, где R1, R2 - линейный или разветвленный алкильный радикал общей формулы CkX2k+1, где X - водород или фтор: Х=Н, F, а k=1-4. Например, используют в качестве бета-дикетоната трис-1,1,1,5,5,5-гексафторпентан-2,4-дионат неодима (Ln=Nd, R1=R2=CkX2k+1, где X=F а k=1).
Кислородсодержащие фторорганические соединения, обеспечивающие повышение летучести комплексов лантаноидов, синтезируют из доступных в промышленных количествах спиртов - теломеров общей формулы H(CF2CF2)xCH2OH, где х=1-3 [Промышленные фторорганические продукты. Справочник. Б.Н. Максимов, В.Г. Барабанов, И.Л. Серушкин и др., Л.: Химия, 1990, 554 с]. Синтез полифторированных эфиров этиленгликоля и диэтиленгликоля (общие формулы 1 и 2) осуществляют взаимодействием полифторированных спиртов H(CF2-CF2)1-3CH2OH с хлорексом (2,2-дихлордиэтиловым эфиром) в щелочной среде [Патент SU 424855, Способ получения моно- или диполифтор- алкиловых эфиров гликолей. Заявлено 18.04.72, опубликовано 25.04.74, А.И. Крылов, Л.Ш. Вахлакова, Т.М. Петрова и др., Журн. ВХО им. Менделеева, т. 22, №4, с. 469-470, 1977]. Синтез полифторированных формалей H(CF2-CF2)m1CH2O(CH2)OCH2(CF2-CF2)m2H осуществляют конденсацией указанных спиртов с формальдегидом в присутствии серной кислоты [M.E. Hill, R.J. Shipp, US patent 3526667 A, Process for acetal preparation, 15.02.1962].
Бета-дикетонаты лантаноидов синтезируют по общепринятым методикам [R.C. Mehrotra, R. Bohra, D.P. Gaur, Metal β-diketonates and Allied Derivatives, Chapter 2, Academic Press, Inc., New York, NY, 1978, 383 р.]. Трис-ацетилацетонаты и их алкильные производные общей формулы (R1COCHCOCR2)3Ln, где R1, R2 - линейный или разветвленный алкильный радикал общей формулы CkX2k+1, где X - водород, а k=1-4 получают в растворе вода - этанол (1:1) из нитратов лантаноидов и этанольного раствора натриевой соли соответствующего дикетона [К J. Eisentraut and R.Е. Sievers, Volatile Rare-Earth Chelates of 2,2,6,6-tetramethylheptane-3,5-dione, Inorganic Syntheses, Volume XI, Edited by William L. Jolly, 1968, p. 94-98]. Фтор замещенные бета-дикетонаты общей формулы (R1COCHCOCR2)3Ln, где Ln - лантаноид - элемент с атомным номером 57-71, где R1, R2 - линейный или разветвленный фторалкильный радикал общей формулы CkX2k+1, где X -фтор, а k=1-4 получают экстракционным способом, исходя из водного раствора хлорида лантаноида и эфирного раствора соответствующего дикетона в присутствии гидроксида аммония [M.F. Richardson, W.F. Wagner and D.E. Sands. Rare-earth trishexafluoroacetylacetonates and related compounds, J. of Inorganic and Nuclear Chemistry, V. 30,1. 5, P. 1275-1289].
Технический результат изобретения заключается в повышении летучести соединений лантаноидов и снижения потерь вещества при испарении. В сравнении с прототипом достигается также упрощение процедуры получения конечного летучего соединения, так как исключается применение органического растворителя.
Предлагаемые примеры иллюстрируют возможности применения способа.
Пример 1 (по прототипу, Example 21, US5837321 A, Volatile organic lanthanide compounds and methods for the preparation of lanthanide-containing layered materials from these compounds, Nov. 17, 1998). Для повышения летучести бета-дикетоната ербия используют обработку трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er 4-третбутилпиридин-N-оксидом (нейтральным донорным лигандом).
Трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er синтезируют обработкой раствора 10 ммоль нитрата ербия гексагидрата Er(NO3)3⋅6H2O в смеси 25 мл воды и 25 мл этанола раствором 30 ммоль 2,2,6,6,-тетраметил-3,5-гептадиона в 50 мл этанола в присутствии 30 ммоль гидроокиси натрия. Образец полученного бета-дикетоната очищают сублимацией при 200°С и ~10 Па. Полученный образец (TMHD)3Er (2,53 г) перемешивают в среде толуола (20 мл) с 4-третбутилпиридин-N-оксидом (0,53 г) в течении 1 часа. Затем толуол удаляют в вакууме и остаток перекристаллизовывают из гексана (10 мл). Получают 1,751 г кристаллов с температурой плавления 105-109°С. Вещество сублимируется при ~10 Па при температуре 120°С. Потери при испарении за счет разложения составляют 1,1-1,8%.
Пример 2. Согласно данному изобретению для повышения летучести соединения ербия используют обработку трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er кислород содержащим фторорганическим соединением - полифторированным формаль общей формулы H(CF2-CF2)2CH2OCH2OCH2(CF2-CF2)2H - 1,1,2,2,3,3,4,4,10,10,11,11,12,12,13,13-гексадекафтор-6,8-диоксатридеканом.
Трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er синтезируют аналогично выше приведенной методики [К J. Eisentraut and R.Е. Sievers, Volatile Rare-Earth Chelates of 2,2,6,6-tetramethylheptane-3,5-dione, Inorganic Syntheses, Volume XI, Edited by William L. Jolly, 1968, p. 94-98]. Температура плавления полученного вещества 168-171°С.
Кислород содержащее фторорганическое соединение общей формулы H(CF2-CF2)2CH2OCH2OCH2(CF2-CF2)2H - 1,1,2,2,3,3,4,4,10,10,11,11,12,12,13,13-гексадекафтор-6,8-диоксатридекан (формаль 22) получают конденсацией спирта H(CF2-CF2)2CH2OH 2,2,3,3,4,4,5,5-октафторпентанола-1 с формалином в присутствии серной кислоты [M.E. Hill, RJ. Shipp, US patent 3526667A, Process for acetal preparation, 15.02.1962] с последующей очисткой вакуумной ректификацией при 105-109°С/1060 Па (d420=1,6662 г/см3).
Способ согласно данного изобретения повышение летучести бета-дикетоната ербия осуществляют путем перемешивания трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er (13,3 г, 17,7 ммоль) и 8,5 г формаля Ф22 (1,1,2,2,3,3,4,4,10,10,11,11,12,12,13,13-гексадекафтор-6,8-диоксатридекана) при 50-60°С в вакууме (~10 Па) в течении 0,5 часа. Получают густую жидкость розового цвета с плотностью 1,72 г/см3. Температура начала кристаллизации - 30-35°С.
Полученный продукт сублимируется без остатка при ~100 Па при температуре 60-70°С. Давление паров, измеренное методом потока (аргон - газ носитель, ферроцен -внутренний стандарт) составляет при 75°С 130±10 Па.
Сравнение характеристик:
Индивидуальный трис-2,2,6,6,-тетраметил-3,5-гептадионата ербия (TMHD)3Er плавится при 168-171°С и сублимируется в вакууме при ~200°С;
Продукт, полученный по прототипу обработкой (TMHD)3Er 4-третбутилпиридин-N-оксидом плавится при 105-109°С и сублимируется в вакууме при 120-150°С;
Продукт, получаемый согласно данного изобретения обработкой (TMHD)3Er кислород содержащим фторорганическим соединением формаль Ф22, имеет температуру начала кристаллизации 30-35°С и сублимируется в вакууме при 50-60°С.
Пример 3. Согласно данному изобретению для повышения летучести соединения неодима используют обработку трис-1,1,1,6,6,6-гексафторпентан-2,4-дионата неодима (HFA)3Nd кислород содержащим фторорганическим соединением - полифторированным эфиром диэтиленгликоля общей формулы H(CF2-CF2)CH2O(CH2CH2O)2CH2(CF2-CF2)H - ди-1,1,3-тригидротетрафторпропиловым эфиром диэтиленгликоля.
Синтез трис-1,1,1,6,6,6-гексафторпентан-2,4-дионата неодима (HFA)3Nd осуществляют экстракционным способом [M.F. Richardson, W.F. Wagner and D.E. Sands. Rare-earth trishexafluoroacetylacetonates and related compounds, J. of Inorganic and Nuclear Chemistry, V. 30, I. 5, P. 1275-1289]. Для этого готовят раствор 1,1,1,6,6,6-гексафторпентан-2,4-дионата аммония растворением 29 г (~0,12 моля) дигидрата 1,1,1,6,6,6-гексафторпентан-2,4-диона и 8,25 мл гидроокиси аммония (~0,12 моля) в 200 мл диэтилового эфира. Полученный раствор перемешивается с 40 мл 1М раствора хлорида неодима NdCl3 в течении 30 минут при комнатной температуре. Органический слой отделяется, промывается 20 мл воды, сушится сульфатом натрия и упаривается в вакууме. Полученный маслянистый остаток перекристаллизовывается из гексана и сушится в вакууме. Получают ~20 г трис-1,1,1,6,6,6-гексафторпентан-2,4-дионата неодима гидрата в виде фиолетовых кристаллов с температурой плавления - 120-125°С.
Синтез ди-1,1,3-тригидротетрафторпропилового эфира диэтиленгликоля проводят взаимодействием 50 мл (74 г, 0,56 моль) 1,1,3-тригидротетрафторпропилового спирта и 22,4 г (0,4 моль) гидрата окиси калия при температуре 70-80°С с последующей обработкой 23,5 мл (29 г, 0,2 моля) хлорексом (2,2-дихлордиэтиловым эфиром) при 100°С при перемешивании в течении 2 часов [Патент SU 424855, Способ получения моно- или диполифтор- алкиловых эфиров гликолей. Заявлено 18.04.72, опубликовано 25.04.74]. Полученную смесь нейтрализуют соляной кислотой, органический слой отделяют, промывают водой, сушат и перегоняют в вакууме (~1300 Па). Отбирают фракцию при 134-135°С и 1330 Па. Получают 11 мл (15,5 г) ди-1,1,3-тригидротетрафторпропилового эфира диэтиленгликоля H(CF2-CF2)CH2O(CH2CH2O)2CH2(CF2-CF2)H. Плотность d420=l,36.
Для повышения летучести соединения неодима осуществляют обработку трис-1,1,1,6,6,6-гексафторпентан-2,4-дионата неодима (HFA)3Nd (20 г) ди-1,1,3-тригидротетрафторпропиловым эфиром диэтиленгликоля (8,75 г) путем перемешивания компонентов при 50-60°С в вакууме (~10 Па) в течении 2 часов. Получают густую жидкость красно-сиреневого цвета с плотностью 1,63 г/см3 и температурой кристаллизации ~25°С. Полученный материал перегоняется в вакууме при 90°С и давлении 130 Па.
Сравнение характеристик:
Индивидуальный трис-1,1,1,6,6,6-гексафторпентан-2,4-дионата неодима (HFA)3Nd плавится при 120-125°С и медленно сублимируется в высоком вакууме (~1 Па) при температуре ~120°С с разложением. Масса нелетучего остатка составляет 30-50%;
Продукт, полученный по прототипу обработкой (HFA)3Nd диметиловым эфиром этиленгликоля, плавится при 62-66°С и сублимируется в вакууме (~1 Па) при 75-80°С;
Продукт, получаемый согласно данного изобретения обработкой (HFA)3Nd кислород содержащим фторорганическим соединением - ди-1,1,3-тригидротетрафторпропиловым эфиром диэтиленгликоля сублимируется в вакууме при 80°С и давлении 130 Па. Таким образом, он имеет летучесть примерно в 100 раз выше, чем согласно прототипа.
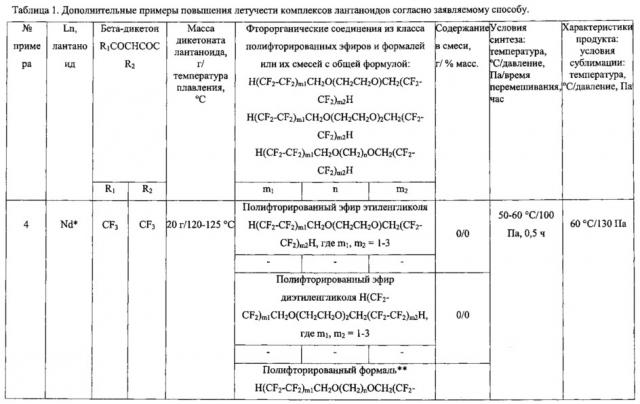
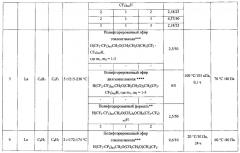
Дополнительные примеры повышения летучести комплексов лантаноидов согласно заявленному способу представлены в таблице 1.
Приведенные примеры подтверждают, что по сравнению со способом прототипом предложенное техническое решение имеет следующие основные преимущества:
а) Обеспечивает повышение летучести бета-дикетонатов лантаноидов от 10 до 100 раз. Температура испарения соединений лантаноидов снижается с 120-150°С до 50-80°С;
б) Исключает образование нелетучего остатка при испарении вещества;
в) Способ согласно заявляемому изобретению базируется на использовании дешевых, промышленно производимых продуктов и не требует применения органических растворителей.
Повышение летучести комплекса в присутствии фторированных соединений является неожиданным техническим эффектом. Аналоги этих соединений, например, фреоны, полифторированные спирта и т.д. - не оказывают заметного влияния на летучесть соединений лантаноидов.
1. Способ повышения летучести комплексов лантаноидов, включающий получение бета-дикетонатных комплексов лантаноидов и их обработку кислородсодержащими органическими соединениями, отличающийся тем, что в качестве кислородсодержащего органического соединения используются кислородсодержащие фторорганические соединения из класса полифторированных эфиров этиленгликоля общей формулы RF1O(CH2CH2O)RF2, полифторированных эфиров диэтиленгликоля общей формулы RF1O(CH2CH2O)2RF2 или из класса полифторированных формалей общей формулы RF1O(CH2)ORF2, где RF1, RF2 - полифторированные углеводородные радикалы общей формулы H(CF2-CF2)mCH2, где m=1-4.
2. Способ по п.1, отличающийся тем, что полифторированные углеводородные радикалы RF1, RF2 в составе фторорганического соединения могут быть как одинаковыми (RF1=RF2), так и различными (RF1≠RF2).
3. Способ по п.1, отличающийся тем, что в качестве кислородсодержащего фторорганического соединения используется смесь из перечисленных фторорганических соединений: полифторированных эфиров этиленгликоля общей формулы RF1O(CH2CH2O)RF2, полифторированных эфиров диэтиленгликоля общей формулы общей формулы RF1O(CH2CH2O)2RF2 или из класса полифторированных формалей общей формулы RF1O(CH2)ORF2 при содержании компонентов в смеси от 0 до 100%.
4. Способ по п.1, отличающийся тем, что в качестве бета-дикетонатов лантаноидов могут применяться соединения общей формулы (R1COCHCOCR2)3Ln, где L - лантаноид - элемент с атомным номером 57-71, где R1, R2 - линейный или разветвленный алкильный радикал общей формулы CkX2k+1, где X - водород или фтор: X=H, F, а k=1-4.
5. Способ по п.1, отличающийся тем, что обработку бета-дикетонатных комплексов лантаноидов полифторированными эфирами этиленгликоля, полифторированными эфирами диэтиленгликоля или полифторированными формалями или их смесью осуществляют при перемешивании в течение 0,1-100 часов при температуре 20-100°C.