Электрохимический способ получения наноразмерных порошков интерметаллидов гольмия и никеля в галогенидных расплавах
Иллюстрации
Показать всеИзобретение относится к электрохимическому получению наноразмерных порошков интерметаллидов гольмия и никеля, которые могут быть использованы в качестве катализаторов в химической и нефтехимической промышленности, в водородной энергетике для обратимого сорбирования водорода, а также для создания магнитных материалов. Проводят электролиз расплавленной смеси, содержащей хлорид калия, хлорид натрия, хлорид гольмия (III) и хлорид никеля (II), в кварцевой ячейке на вольфрамовом электроде при температуре 973 К и плотности тока 0,5÷1,9 A/см2. Обеспечивается снижение температуры проведения электролиза и получение наноразмерных порошков интерметаллидов гольмия и никеля. 6 ил., 3 табл., 5 пр.
Реферат
Изобретение относится к электрохимическому получению ультрадисперсных порошков интерметаллидов гольмия и никеля в галогенидных расплавах и может быть использовано в качестве катализаторов в химической и нефтехимической промышленности, в водородной энергетике для обратимого сорбирования водорода, а также для создания магнитных материалов.
Известен способ получения интерметаллидов гольмия и никеля путем диффузионного насыщения никелевого электрода ионами гольмия в расплаве в KCl-HoCl3 [Qiqin Y. Electrochemistry of deposition of rare earth metals and their alloys in molten salts. Proceedings of 6th International Symposium on Molten Salt Chemisry and Technology. Shanghai, China, Okt. 2001, p. 383-390].
Известен также способ получения, Su YZ, Yang QQ, Liu GK. Electroreduction of Ho3+ on nickel catode in molten KCI-HoCl3 // J. Rare Eartns, 2000. - V. 18. - N 1. P. 34-38] при температуре 1093°C.
Недостатком приведенных аналогов является высокая температура процесса, а также невозможность получения наноразмерных порошков, т.к. данным способом получают только диффузионные покрытия.
Наиболее близким к заявляемому техническому решению по технической сущности и достигаемому техническому результату является способ получения интерметаллидов гольмия и никеля диффузионным насыщением металлического никеля гольмием в расплаве KCl-NaCl (Самоделкина О.В. Восстановление хлоридов празеодима, неодима, тербия и гольмия в ионных расплавах: Дис. … канд. хим. наук: 02.00.05. Екатеринбург, 2004, 127 с. РГБ ОД, 61: 04-2/562). Этим способом можно получить только диффузионные покрытия.
Сущность диффузионного насыщения электроположительного металла электроотрицательным РЗМ из расплава заключается в следующем: электроположительный металл (никель) находится в расплаве соли щелочного металла с добавкой соли РЗМ (HoCl3) в контакте с металлическим щелочным металлом. При этом создается короткозамкнутый гальванический элемент, в котором натрий является анодом, а никель - катодом. Насыщение проводилось в температурном интервале 1073-1173 K в течение 20 минут.
Недостатком прототипа является невозможность получения ультрадисперсных порошков интерметаллидов гольмия и никеля. Также недостатком данного способа является ограничение скорости протекания процесса диффузии гольмия на поверхность металлического никеля.
Задачей изобретения является получение наноразмерных порошков интерметаллидов гольмия и никеля в галогенидных расплавах, снижение температуры проведения электролиза и снижение энергозатрат.
Поставленная задача решена следующим образом.
Электрохимический высокотемпературный синтез интерметаллидов гольмия и никеля в гальваностатическом режиме проводят в расплаве KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %:
HoCl3 - 0,5-3,0;
NiCl2 - 0,5-2,5;
остальное эквимольная смесь KCl и NaCl.
Электролиз проводят в высокотемпературной кварцевой ячейке в атмосфере инертного газа - аргона при температуре 973 K. Катодом служил вольфрамовый стержень высокой чистоты диаметром 3 мм. Анодом и одновременно контейнером для расплава служил стеклоуглеродный тигель.
Электрохимический синтез интерметаллидов гольмия и никеля проводят в гальваностатическом режиме в расплаве KCl-NaCl-HoCl3-NiCl2 следующим образом: вначале подготавливают используемые соли. Хлориды кали и натрия перекристаллизовывают, тщательно сушат в процессе вакуумирования при ступенчатом нагревании до 573-423 K и переплавляют при температурах плавления этих солей. Затем проводят сушку хлорида никеля в атмосфере четыреххлористого углерода, постепенно увеличивая температуру до 673 К. Источником ионов гольмия является безводный хлорид гольмия (III) (99,99%). Источником никеля служит безводный хлорид никеля (II). Взвешивания безводных хлоридов проводят в перчаточном боксе MbraunLabStar.
Далее проводят электролиз расплавленной смеси KCl-NaCl, содержащей хлорид гольмия (III) - 0,5÷3,0 мол. % и хлорид никеля (II) - 0,5÷2,5 мол. % при плотности тока 0,5÷1,9 A/см2.
На вольфрамовом электроде образуется металло-солевая «груша» (фиг. 1).
Выщелачивание катодного осадка осуществляют в горячей дистиллированной воде, что позволяет отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушат в вакуумном сушильном шкафу при температурах 373-423 К.
В зависимости от состава электролизной ванны и параметров электролиза образуется смесь фаз металлического никеля, гольмия и интерметаллидов HoNi, HoNi5, HoNi3.
На фиг. 2 представлена рентгенограмма продукта гальваностатического электролиза (фазовый состав катодного осадка), полученная из расплава KCl-NaCl-HoCl3-NiCl2 на вольфрамовом электроде. C (HoCl3)=2,5 мол. %, С(NiCl2)=0,5 мол. %. ik=1,2 A/см2. T=973 K. S=2,43 см2. Стандартные линии: 1 - HoNi, 2 - HoNi5, 3 - HoNi3.
Для определения оптимальных концентраций HoCl3 и NiCl2 необходимо учитывать, что вначале происходит выделение более электроположительного компонента - никеля.
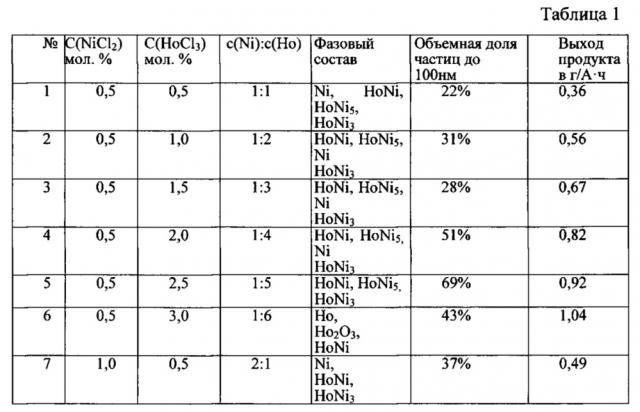
Электрохимическое восстановление ионов гольмия начинается по мере выработки хлорида никеля. Оптимальная концентрация хлорида никеля составляет порядка 0,5 мол. %. При более высоких концентрациях хлорида никеля осадок содержит металлический никель. Изучена зависимость состава катодных осадков от содержания хлорида никеля, хлорида гольмия и их соотношения в расплаве KCl-NaCl (1:1) (таблица 1).
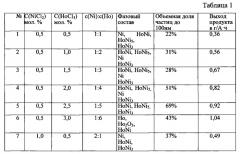
В таблице 1 представлена зависимость фазового состава и размера частиц продуктов гальваностатического электролиза от состава электролизной ванны KCl-NaCl-HoCl3-NiCl2. Продолжительность электролиза 60 мин. T=973 K, S=2,43 см2, i=1,2 A/см2.
Содержание интерметаллидов увеличивается как при увеличении концентрации хлорида гольмия в расплаве, так и при увеличении соотношения концентраций хлоридов гольмия и никеля (фиг. 3). Когда соотношение концентраций [HoCl3]:[NiCl2]=1:1, в катодном осадке превалирует фаза металлического никеля. С увеличением этого соотношения доля металлического никеля уменьшается, а содержание интерметаллидов HoNi, HoNi3, HoNi5 возрастает. При условии [HoCl3]:[NiCl2] больше 5 в катодном осадке фаза металлического никеля не обнаруживается, а образуется смесь фаз интерметаллидов. Причем фаза с большим содержанием гольмия превалирует.
На фиг. 3 представлена зависимость состава продуктов гальваностатического электролиза от соотношения компонентов электролизной ванны KCl-NaCl-HoCl3-NiCl2: 1 - HoNi, 2 - HoNi5, 3 - HoNi3, 4 - Ni.
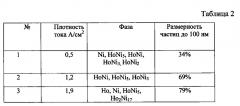
Была проведена серия экспериментов в гальваностатическом режиме при различных начальных плотностях тока (0,5÷2,0) А/см2 в электролизной ванне оптимального состава KCl-NaCl-NiCl2 (0,5 мол. %)-HoCl3 (2,5 мол. %) (таблица 2).
При начальной плотности тока 0,5 A/см2 в катодном осадке превалирует фаза металлического никеля и фазы интерметаллидов с большим содержанием никеля. С увеличением начальной плотности тока содержание никеля в катодном осадке уменьшается, а содержание гольмия возрастает.
При начальной плотности тока 1,2 A/см2 фаза металлического никеля в катодном осадке отсутствует, а из фаз интерметаллидов в большем количестве содержатся фазы с большим содержанием гольмия.
При еще большей плотности тока (~2,0 A/см2) в катодном осадке уже появляется фаза металлического гольмия.
В таблице 2 представлена зависимость фазового состава и размера частиц продуктов гальваностатического электролиза в расплаве KCl-NaCl-HoCl3-NiCl2 от плотности тока. Продолжительность электролиза 60 мин. С(HoCl3)=2,5 мол. %, С(NiCl2)=0,5 мол. %.
В таблице 3 представлена зависимость фазового состава продуктов гальваностатического электролиза в расплаве KCl-NaCl-HoCl3-NiCl2 от температуры проведения синтеза. Продолжительность электролиза 60 мин. С(HoCl3)=2,5 мол. %, С(NiCl2)=0,5 мол. %
На фиг. 4 представлен результат дисперсионного анализа порошков интерметаллидов гольмия и никеля, полученных гальваностатическим электролизом расплава (KCl-NaCl)эвт.-HoCl3-NiCl2 в соотношении 5:1 при плотности тока 1,2 А/см2 и температуре 973 K.
Проведено изучение структуры, морфологии и элементного состава полученных образцов (количественный и качественный) на сканирующем растровом электронном микроскопе VEGA3 LMH. Полученные снимки подтверждают процесс совместного электровыделения гольмия и никеля (фиг. 5, 6).
На фиг. 5 представлена карта образца, полученная на сканирующем растровом электронном микроскопе VEGA3 TESCAN. Фазовый состав: HoNi, HoNi5, HoNi3.
На фиг. 6 показано фото продукта гальваностатического электролиза (KCl-NaCl-HoCl3-NiCl2), полученное на сканирующем растровом электронном микроскопе VEGA3 TESCAN.
Пример 1
Высокотемпературный электрохимический синтез интерметаллидов гольмия и никеля осуществляют в расплавленной смеси KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %: HoCl3 - 0,5; NiCl2 - 0,5; остальное эквимольная смесь KCl и NaCl.
Катодом служит вольфрамовый стержень диаметром 3 мм, площадью 2,43 см2. Анодом и одновременно контейнером при гальваностатическом режиме электролиза служит стеклоуглеродный тигель. Электролиз проводился при температуре 973 K. Начальная плотность катодного тока 1,2 A/см2. Продолжительность электролиза 60 мин, после чего выливается расплав и извлекают упавшую на алундовую подложку металло-солевую «грушу». Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушили в вакуумном сушильном шкафу при температурах 373-423 K. По данным рентгенофазового анализа катодный осадок состоит из интерметаллидов Ni, HoNi, HoNi5, HoNi3. По данным анализа гранулометрического состава объемная доля частиц целевого продукта до 100 нм составляет 22%.
Пример 2
Высокотемпературный электрохимический синтез интерметаллидов гольмия и никеля осуществляют в расплавленной смеси KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %: HoCl3 - 2,5; NiCl2 - 0,5; остальное эквимольная смесь KCl и NaCl.
Катодом служит вольфрамовый стержень диаметром 3 мм, площадью 2,43 см2. Анодом и одновременно контейнером при гальваностатическом режиме электролиза служит стеклоуглеродный тигель. Электролиз проводился при температуре 973 K. Начальная плотность катодного тока 1,2 A/см2. Продолжительность электролиза 60 мин, после чего выливается расплав и извлекают упавшую на алундовую подложку металло-солевую «грушу». Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушили в вакуумном сушильном шкафу при температурах 373-423 K. По данным рентгенофазового анализа катодный осадок состоит из интерметаллидов HoNi, HoNi5, HoNi3. По данным анализа гранулометрического состава объемная доля частиц целевого продукта до 100 нм составляет 69%.
Пример 3
Высокотемпературный электрохимический синтез интерметаллидов гольмия и никеля осуществляют в расплавленной смеси KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %: HoCl3 - 2,5; NiCl2 - 0,5; остальное эквимольная смесь KCl и NaCl.
Катодом служил вольфрамовый стержень диаметром 3 мм, площадью 2,43 см2. Анодом и одновременно контейнером при гальваностатическом режиме электролиза служил стеклоуглеродный тигель. Электролиз проводился при температуре 973 K. Начальная плотность катодного тока 0,5 A/см2. Продолжительность электролиза 60 мин, после чего выливается расплав и извлекают упавшую на алундовую подложку металло-солевую «грушу». Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушили в вакуумном сушильном шкафу при температурах 373-423 К. По данным рентгенофазового анализа катодный осадок состоит из Ni, HoNi5, HoNi, HoNi3, HoNi2. По данным анализа гранулометрического состава объемная доля частиц целевого продукта до 100 нм составляет 34%.
Пример 4
Высокотемпературный электрохимический синтез интерметаллидов гольмия и никеля осуществляют в расплавленной смеси KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %: HoCl3 - 2,5; NiCl2 - 0,5; остальное эквимольная смесь KCl и NaCl.
Катодом служил вольфрамовый стержень диаметром 3 мм, площадью 2,43 см2. Анодом и одновременно контейнером при гальваностатическом режиме электролиза служил стеклоуглеродный тигель. Электролиз проводился при температуре 973 K. Начальная плотность катодного тока 1,9 A/см2. Продолжительность электролиза 60 мин, после чего выливается расплав и извлекают упавшую на алундовую подложку металло-солевую «грушу». Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушили в вакуумном сушильном шкафу при температурах 373-423 K. По данным рентгенофазового анализа катодный осадок состоит из Ho, Ni, HoNi5, Ho2Ni17. По данным анализа гранулометрического состава объемная доля частиц целевого продукта до 100 нм составляет 79%.
Пример 5
Высокотемпературный электрохимический синтез интерметаллидов гольмия и никеля осуществляют в расплавленной смеси KCl-NaCl-HoCl3-NiCl2 при следующем соотношении компонентов, мол. %: HoCl3 - 2,5; NiCl2 - 0,5; остальное эквимольная смесь KCl и NaCl.
Катодом служил вольфрамовый стержень диаметром 3 мм, площадью 2,43 см2. Анодом и одновременно контейнером при гальваностатическом режиме электролиза служил стеклоуглеродный тигель. Электролиз проводился при температуре 1073 K. Начальная плотность катодного тока 1,2 А/см2. Продолжительность электролиза 60 мин, после чего выливается расплав и извлекают упавшую на алундовую подложку металло-солевую «грушу». Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде осадок сушили в вакуумном сушильном шкафу при температурах 373-423 K. По данным рентгенофазового анализа катодный осадок состоит из HoNi, HoNi2. Анализ гранулометрического состава показал, что при температуре 1073 K не образуются наноразмерные порошки интерметаллидов гольмия и никеля.
Технический результат: получение наноразмерных порошков интерметаллидов гольмия и никеля из расплава KCl-NaCl-HoCl3-NiCl2 на вольфрамовом электроде.
Способ электрохимического получения наноразмерных порошков интерметаллидов гольмия и никеля, включающий электролиз расплавленной смеси, содержащей хлорид калия, хлорид натрия и хлорид гольмия (III), в атмосфере очищенного и осушенного аргона в высокотемпературной кварцевой ячейке, отличающийся тем, что расплавленная смесь хлорида калия, хлорида натрия и хлорида гольмия (III) дополнительно содержит хлорид никеля (II), при следующем соотношении компонентов, мол.%:
| HoCl3 | 0,5÷3,0 |
| NiCl2 | 0,5÷2,5 |
| эквимольная смесь KCl и NaCl | остальное |
при этом электролиз проводят при температуре 973 K и плотности тока от 0,5 до 1,9 А/см2 с использованием вольфрамового электрода.