Набор реагентов для выявления днк chlamydia trachomatis и его применение
Иллюстрации
Показать всеНастоящая группа изобретений относится к медицине. Предложен набор реагентов для выявления Chlamydia trachomatis в образце, включающий два олигонуклеотидных праймера для полимеразной цепной реакции (ПЦР), и применение указанного набора для выявления ДНК Chlamydia trachomatis в образце. Предложенный набор включает первый олигонуклеотидный праймер с последовательностью SEQ ID NO:2, и второй олигонуклеотидный праймер с последовательностью SEQ ID NO:3, а также, при необходимости, включает олигонуклеотидный зонд, термостабильную ДНК-полимеразу, буферный раствор для ПЦР, дезоксинуклеозидтрифосфаты. Набор позволяет эффективно выявлять клинически значимые штаммы/генотипы/серовары урогенитального биовара Chlamydia trachomatis с помощью единственной мишени ПЦР при использовании двух олигонуклеотидных праймеров, позволяющих получить продукт амплификации, который имеет размер, входящий в диапазон 70-110 пар нуклеотидов, и обеспечивающих амплификацию фрагмента ДНК Chlamydia trachomatis, лежащего внутри участка критической плазмиды Chlamydia trachomatis с последовательностью SEQ ID NO:1. Группа изобретений может быть использована в лабораторной диагностике Chlamydia trachomatis. 2 н. и 7 з.п. ф-лы, 5 табл., 2 пр.
Реферат
Область техники
Группа изобретений относится к медицине, более конкретно к лабораторной диагностике и может быть использована для выявления ДНК Chlamydia trachomatis в биологических образцах.
Уровень техники
Chlamydia trachomatis - облигатный внутриклеточный бактериальный патоген человека. Инфекция Chlamydia trachomatis (хламидиоз) является самой распространенной бактериальной инфекцией, передаваемой половым путем, инфицируя ежегодно свыше 90 миллионов человек [Lanjouw Ε. et al. European guideline for the management of Chlamydia trachomatis infections, 2010].
В настоящее время в пределах вида Chlamydia trachomatis выделяют 3 биовара и множество сероваров и генотипов: биовар трахома (серовары А-С), урогенитальный биовар (серовары D-K) и биовар венерическая лимфогранулема (ЛГВ, серовары L1-L3) [Lanjouw Ε. et al. European guideline for the management of Chlamydia trachomatis infections, 2010]. Представители урогенитального биовара Chlamydia trachomatis могут являться причиной воспалительных заболеваний урогенитального тракта у мужчин и женщин, таких как уретриты, цервициты, эпидидимиты. Однако до 90% случаев урогенитального хламидиоза у женщин и более 50% случаев урогенитального хламидиоза у мужчин имеют бессимптомное течение [Lanjouw Ε. et al. European guideline for the management of Chlamydia trachomatis infections, 2010]. Инфекции, протекающие бессимптомно, часто остаются не диагностированными и, следовательно, пациентам не назначается адекватная терапия в течение длительного периода времени. В отсутствие лечения хламидийная инфекция приводит к таким серьезным последствиям, как воспалительные заболевания органов малого таза у женщин, патология беременности, мужское и женское бесплодие, пневмония и конъюнктивит у новорожденных [Lanjouw Ε. et al. European guideline for the management of Chlamydia trachomatis infections, 2010; Jaton K. et al. A novel real-time PCR to detect Chlamydia trachomatis in first-void urine or genital swabs. J Med Microbiol. 2006 Dec; 55(Pt 12): 1667-1674].
В связи с затрудненной клинической диагностикой трудно переоценить важность надежной и эффективной лабораторной диагностики хламидийной инфекции.
Традиционные методы лабораторной диагностики бактериальных инфекций - бактериоскопический (микроскопический), бактериологический (культуральный) и иммунологический (серологический) - в настоящее время утратили свое доминирующее положение для диагностики Chlamydia trachomatis в развитых странах. Европейское руководство 2010 года по ведению больных с инфекциями, вызванными Chlamydia trachomatis, признает основными методами диагностики современные молекулярно-биологические методы, основанные на амплификации нуклеиновых кислот (МАНК) [Lanjouw Ε. et al. European guideline for the management of Chlamydia trachomatis infections, 2010]. Наибольшее распространение среди МАНК получил метод полимеразной цепной реакции (ПЦР).
Существует большое количество «in house» («домашних») и серийно выпускаемых (коммерческих) наборов реагентов (тест-систем) для выявления ДНК Chlamydia trachomatis методом полимеразной цепной реакции. Наборы различаются генами-мишенями для ПЦР, способами детекции продуктов амплификации, размерами продуктов амплификации, количеством одновременно выявляемых патогенов - от одного до семи [Gimenes F. et al. Sensitive simultaneous detection of seven sexually transmitted agents in semen by multiplex-PCR and of HPV by single PCR. PLoS One. 2014 Jun 12; 9(6): e98862. doi: 10.1371/journal.pone.0098862. eCollection 2014].
Известен набор реагентов для обнаружения ДНК Chlamydia trachomatis методом полимеразной цепной реакции ПОЛИМИК-ХЛ производства ООО НПФ «ЛИТЕХ» [Регистрационное удостоверение №ФСР 2007/00382 от 16.07.2007]. Детекция продуктов амплификации осуществляется методом гель-электрофореза.
Известны наборы реагентов для выявления ДНК Chlamydia trachomatis методом полимеразной цепной реакции ХЛАМИ-ГЕН производства ООО «НПО ДНК-Технология» [Регистрационное удостоверение №ФСР 2008/03890 от 26.04.2010]. Наборы производятся в трех модификациях, различающихся способами детекции продуктов амплификации: детекция методом гель-электрофореза, флуоресцентная детекция по конечной точке и флуоресцентная детекция в режиме реального времени.
В исследовании, посвященном сравнительной оценке тест-систем отечественного производства для выявления ДНК Chlamydia trachomatis, сообщается, что в наборе реагентов производства ООО НПФ «ЛИТЕХ» в качестве мишени для ПЦР используется криптическая плазмида, а в наборах реагентов производства ООО «НПО ДНК-Технология» в зависимости от способа детекции используются различные мишени: в наборе с детекцией методом гель-электрофореза в качестве мишени используется криптическая плазмида, а в наборе с флуоресцентной детекцией по конечной точке и в режиме реального времени используется ген 16S rRNA [Shipitsyna Ε. et al. First evaluation of six nucleic acid amplification tests widely used in the diagnosis of Chlamydia trachomatis in Russia. J Eur Acad Dermatol Venereol. 2009 Mar; 23(3): 268-276]. Однако более детальная информация, касающаяся конкретных фрагментов мишеней, размеров продуктов амплификации, нуклеотидных последовательностей используемых в наборах олигонуклеотидных праймеров и зондов, по сведениям авторов настоящих изобретений, не опубликована в общедоступных источниках информации.
На российском рынке присутствуют наборы реагентов (тест-системы) производства компании Roche Molecular Systems, Inc. серии COBAS® AMPLICOR: для выявления ДНК одного патогена - Набор реагентов для детекции ДНК Хламидии Трахоматис (Cobas Amplicor Chlamydia trachomatis Detection kit), для одновременного выявления двух патогенов - Набор реагентов для амплификации Хламидии Трахоматис и Нейссерии Гонореи (Amplicor CT/IMG Amplification kit) [Регистрационное удостоверение №ФСЗ 2011/09814 25.05.2011]. В наборах реализован принцип флуоресцентной детекции по конечной точке с использованием флуоресцентного интеркалирующего красителя SYBR GREEN. В данных наборах в качестве мишени для выявления Chlamydia trachomatis используется криптическая плазмида, и более конкретно фрагмент плазмиды в открытой рамке считывания ORF1 [ЕР 0420260 В1, ЕР 0630971 В1, ЕР 0875583 В1].
Данные тест-системы были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration) и были рекомендованы ВОЗ в качестве референсных тест-систем при валидации новых и модифицированных тест-систем [ПРОТОКОЛЫ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ ИНФЕКЦИИ ВЫЗВАННОЙ CHLAMYDIA TRACHOMATIS, (УРОГЕНИТАЛЬНОЙ ХЛАМИДИЙНОЙ ИНФЕКЦИИ) В РОССИЙСКОЙ ФЕДЕРАЦИИ (проект), www.cnikvi.ru/files/xlamidioz.doc], что свидетельствует об их надежности. Однако в 2007 году были обнаружены новые мутантные штаммы Chlamydia trachomatis (nvCT), содержащие делецию размером 377 пар нуклеотидов именно в том фрагменте ORF1 криптической плазмиды, который является мишенью полимеразной цепной реакции в данных диагностических наборах [Ripa Т. and Nilsson Р.Α. A Chlamydia trachomatis strain with a 377-bp deletion in the cryptic plasmid causing false-negative nucleic acid amplification tests. Sex Transm Dis. 2007 May; 34(5): 255-256]. Новые мутантные штаммы получили название «шведский вариант» по месту их обнаружения. Невозможность обнаружения данных штаммов наборами серии COBAS® AMPLICOR и другими наборами со сходной мишенью привело к тысячам ложноотрицательных результатов в диагностике хламидийной инфекции, что, вероятно, способствовало распространению мутантных штаммов [Steensels D. et al. Towards multitarget testing in molecular microbiology. Int J Microbiol. 2013; 2013:121057. doi: 10.1155/2013/121057. Epub 2013 Nov 25. Review].
Одним из путей решения проблемы «ухода» новых «шведских вариантов» Chlamydia trachomatis от обнаружения является введение дополнительной мишени для ПЦР в рамках одной тест-системы. Так, усовершенствованный набор реагентов для выявления Chlamydia trachomatis COBAS® TaqMan® CT Test, v2.0 [Регистрационное удостоверение №ФСЗ 2010/07038] компании Roche Molecular Systems, Inc. содержит реагенты для амплификации и детекции в режиме реального времени двух мишеней Chlamydia trachomatis: помимо вышеупомянутого фрагмента криптической плазмиды, также хромосомного гена оmр-1, кодирующего основной белок внешней мембраны (МОМР). Такой подход, несомненно, повышает надежность выявления Chlamydia trachomatis (снижает количество ложноотрицательных результатов), однако усложняет и удорожает анализ, повышая требования к лабораторному оборудованию (а именно к числу каналов детекции прибора). Кроме того, данный подход - увеличение количества мишеней для выявления одного патогена - снижает возможности одновременного выявления нескольких патогенов в одной пробирке на имеющемся в лаборатории оборудовании, что не вполне отвечает современным потребностям лабораторной диагностики урогенитальных заболеваний, часто протекающих по типу микст-инфекций.
Сущность группы изобретений.
Задачами настоящей группы изобретений являются: разработка и валидация набора реагентов, позволяющего выявлять все клинически значимые штаммы/генотипы/серовары урогенитального биовара Chlamydia trachomatis (в том числе nvCT) с помощью единственной мишени полимеразной цепной реакции, с возможностью как самостоятельного использования для выявления ДНК одного патогена - Chlamydia trachomatis, так и в составе мультиплексного набора для выявления ДНК нескольких патогенов, с возможностью количественного определения ДНК Chlamydia trachomatis; расширение арсенала тест-систем для выявления ДНК Chlamydia trachomatis.
В рамках настоящих изобретений в качестве мишени для полимеразной цепной реакции была выбрана криптическая плазмида Chlamydia trachomatis. Плазмида мультикопийна, то есть содержится в количестве 4-8 копий на клетку, что повышает аналитическую чувствительность тест-систем с данной мишенью по сравнению с тест-системами с однокопийными хромосомными мишенями. Кроме того, последовательность криптической плазмиды высококонсервативна: вариабельность среди представителей различных сероваров внутри одного биовара составляет менее 1% [Comanducci м. et al. Diversity of the Chlamydia trachomatis common plasmid in biovars with different pathogenicity. Plasmid. 1990 Mar; 23(2): 149-154], что делает эту мишень подходящей для выявления всех клинически значимых сероваров урогенитального биовара Chlamydia trachomatis при условии выбора фрагмента для амплификации с учетом данных о положении делеции в криптической плазмиде nvCT.
На основании анализа «выравниваний» нуклеотидных последовательностей криптических плазмид Chlamydia trachomatis из GenBank и имеющихся литературных данных о положении делеции в криптической плазмиде nvCT («шведских вариантов» Chlamydia trachomatis) был определен высококонсервативный участок внутри открытой рамки считывания 8 (ORF8) криптической плазмиды, имеющий последовательность SEQ ID NO:1, в качестве оптимальной «площадки» для дизайна олигонуклеотидных праймеров для специфической амплификации фрагмента ДНК внутри этой «площадки».
Помимо участка для дизайна олигонуклеотидных праймеров для специфической амплификации фрагмента ДНК криптической плазмиды Chlamydia trachomatis в рамках настоящих изобретений экспериментальным путем был определен оптимальный размер этого фрагмента (продукта амплификации) - от 70 до 110 пар нуклеотидов. Оказалось, что амплификация фрагментов такого размера обладает минимальной восприимчивостью как к примесям-ингибиторам ПЦР, так и к конкуренции со стороны других ПЦР мишеней. Последнее в свою очередь расширяет возможности мультиплексирования ПЦР, то есть одновременного выявления двух и более патогенов в одной реакции (в одной пробирке).
Таким образом поставленные задачи решены созданием набора реагентов для выявления ДНК Chlamydia trachomatis в образце методом полимеразной цепной реакции, включающего по меньшей мере два олигонуклеотидных праймера для полимеразной цепной реакции, отличающего тем, что указанные два олигонуклеотидных праймера обеспечивают специфическую амплификацию фрагмента ДНК Chlamydia trachomatis, лежащего внутри участка криптической плазмиды Chlamydia trachomatis последовательности SEQ ID NO:1, причем размер фрагмента составляет от 70 до 110 пар нуклеотидов.
В частном случае выполнения набор по изобретению характеризуется тем, что один олигонуклеотидный праймер имеет последовательность, гомологичную по меньшей мере на 80% последовательности SEQ ID NO:2, второй олигонуклеотидный праймер имеет последовательность, гомологичную по меньшей мере на 80% последовательности SEQ ID NO:3.
В частном случае выполнения набор по изобретению характеризуется тем, что один олигонуклеотидный праймер имеет последовательность SEQ ID NO:2, второй олигонуклеотидный праймер имеет последовательность SEQ ID NO:3.
В частном случае выполнения набор по изобретению характеризуется тем, что дополнительно содержит олигонуклеотидный зонд для детекции фрагмента ДНК Chlamydia trachomatis в режиме реального времени, где указанный зонд на 5'-конце содержит флуоресцентный краситель, на 3'-конце содержит гаситель флуоресценции.
В частном случае выполнения набор по изобретению характеризуется тем, что флуоресцентный краситель выбран из группы: JOE, FAM, R6G, ROX, Су5, Су5.5, HEX.
В частном случае выполнения набор по изобретению характеризуется тем, что гаситель флуоресценции выбран из группы: BHQ1, BHQ2, BHQ3, RTQ.
В частном случае выполнения набор по изобретению характеризуется тем, что олигонуклеотидный зонд имеет последовательность, гомологичную по меньшей мере на 80% последовательности SEQ ID NO:4.
В частном случае выполнения набор по изобретению характеризуется тем, что олигонуклеотидный зонд имеет последовательность SEQ ID NO:4.
В частном случае выполнения набор по изобретению характеризуется тем, что олигонуклеотидный зонд представляет собой
В частном случае выполнения набор по изобретению характеризуется тем, что олигонуклеотидный зонд представляет собой
В частном случае выполнения набор по изобретению характеризуется тем, что дополнительно содержит термостабильную ДНК-полимеразу, буферный раствор для ПЦР, дезоксинуклеозидтрифосфаты.
В частном случае выполнения набор по изобретению характеризуется тем, что дополнительно содержит по меньшей мере один калибратор для количественной оценки содержания ДНК Chlamydia trachomatis в образце, содержащий известные концентрации фрагмента ДНК Chlamydia trachomatis, используемого для выявления ДНК Chlamydia trachomatis.
В частном случае выполнения набор по изобретению характеризуется тем, что дополнительно содержит реагенты для выявления в образце методом мультиплексной полимеразной цепной реакции ДНК по меньшей мере одного дополнительного микроорганизма, выбранного из группы: Neisseria gonorrhoeae, Trichomonas vaginalis, Mycoplasma genitalium.
В частном случае выполнения набор по изобретению характеризуется тем, что биологический образец для проведения исследования выбран из группы: мазок из влагалища, моча, семенная жидкость, соскоб из уретры, соскоб из цервикального канала.
Объем притязаний включает также применение вышеописанных наборов реагентов для выявления ДНК Chlamydia trachomatis в биологических образцах.
Группа изобретений позволяет с высокой чувствительностью и специфичностью выявлять все клинически значимые штаммы/генотипы/серовары урогенитального биовара Chlamydia trachomatis (в том числе nvCT) с помощью единственной мишени полимеразной цепной реакции. В частном случае выполнения группа изобретений позволяет определять ДНК Chlamydia trachomatis в количественном формате, что может быть полезно для уточнения диагноза при сомнительных/дискордантных результатах анализа. Кроме того, уровень бактериальной нагрузки может иметь патогенетическое и прогностическое значение и оказывать влияние на выбор тактики этиотропной терапии. В частном случае выполнения группа изобретений позволяет выявлять одновременно несколько возбудителей инфекций, передаваемых половым путем, что может быть полезно для диагностики часто встречающихся микст-инфекций урогенитального тракта.
Сведения, подтверждающие возможность осуществления группы изобретений
Пример 1. Выявление (качественное определение) ДНК Chlamydia trachomatis в биологических образцах.
В исследование были включены 127 пациентов мужского пола с жалобами на наличие зуда/жжения в области половых органов и/или дизурии. От каждого пациента получали по два биологических образца - соскоба из уретры. Взятые у пациентов уретральные образцы помещали в 1 мл сахарозо-фосфатного буфера. Первый образец исследовали методом полимеразной цепной реакции с использованием двух референсных наборов реагентов для выявления ДНК Chlamydia trachomatis - COBAS® AMPLICOR (Roche Molecular Systems, Inc., США) и Light-Mix 480 HT (TIB MOLBIOL, Германия). Второй образец исследовали методом полимеразной цепной реакции с использованием набора реагентов по изобретению. Далее проводилось сопоставление результатов, полученных тремя наборами реагентов для выявления ДНК Chlamydia trachomatis.
Исследование образцов с использованием двух референсных наборов реагентов.
Выделение ДНК из биологических образцов проводили с использованием набора реагентов MagNa Pure LC DNA Isolation kit I (Roche Molecular Biochemicals, Германия) в соответствии с инструкцией производителя. Объем элюции составил 100 мкл, далее образец разводили в 2 раза, добавляя еще 100 мкл буфера. Для амплификации ДНК методом полимеразной цепной реакции использовали 50 мкл полученного элюата. Постановку полимеразной цепной реакции и интерпретацию результатов исследования осуществляли в соответствии с инструкциями производителя.
Исследование образцов с использованием набора реагентов по изобретению.
Выделение ДНК из биологических образцов проводили с использованием набора реагентов ДНК-Сорб-АМ (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, кат. №102-22). До выделения ДНК в пробирки вносили по 10 мкл препарата внутреннего контрольного образца (ВКО). Для амплификации ДНК методом полимеразной цепной реакции использовали 10 мкл полученного элюата (объем полученного элюата после экстракции составлял 100 мкл).
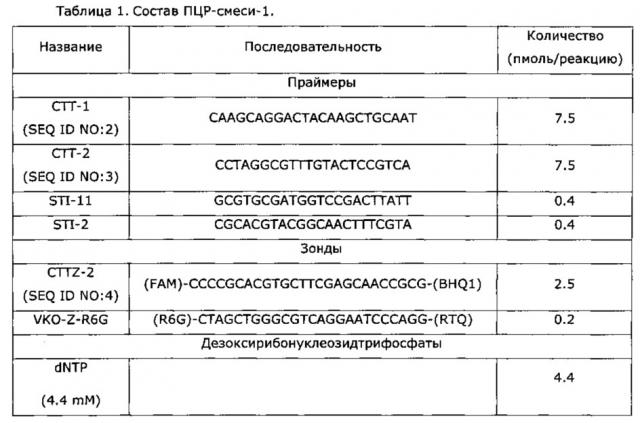
Реакционную смесь для полимеразной цепной реакции готовили следующим образом. Сначала готовили ПЦР-смесь-1, содержащую олигонуклеотидные праймеры, олигонуклеотидные зонды для детекции и дезоксирибонуклеозидтрифосфаты в буфере ТЕ. Состав ПЦР-смеси-1 приведен в таблице 1.
Затем в каждую реакционную пробирку вносили по 10 мкл ПЦР-смеси-1, по 5 мкл ПЦР-смеси-2 red (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, кат. №863), содержащей Taq-полимеразу, и по 10 мкл элюата, полученного при выделении ДНК из биологических образцов.
Амплификацию проводили на приборе «Rotor-Gene Q» (QIAGEN, Германия).
Полученные данные - кривые накопления флуоресцентного сигнала по двум каналам - анализировались с помощью программного обеспечения прибора «Rotor-Gene Q». Сигнал, свидетельствующий о накоплении продукта амплификации фрагмента ДНК Chlamydia trachomatis, детектировался по каналу Green, ДНК ВКО детектировался по каналу Yellow. Результаты интерпретировались на основании наличия (или отсутствия) пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, что определяет наличие (или отсутствие) для данной пробы ДНК значения порогового цикла «Ct» в соответствующей графе в таблице результатов.
Результаты интерпретировались следующим образом:
- ДНК Chlamydia trachomatis обнаружена, если для данной пробы в таблице результатов по каналу Green определено значение порогового цикла Ct. При этом кривая флуоресценции данной пробы должна пересекать пороговую линию на участке характерного экспоненциального подъема флуоресценции.
- ДНК Chlamydia trachomatis не обнаружена, если для данной пробы в таблице результатов по каналу Green не определено (отсутствует) значение порогового цикла Ct (кривая флуоресценции не пересекает пороговую линию), а в таблице результатов по каналу Yellow определено значение порогового цикла Ct, не превышающее 33.
- Результат анализа невалидный, если для данной пробы не определено (отсутствует) или превышает 33 значение порогового цикла Ct по каналу для детекции Yellow и не определено (отсутствует) значение порогового цикла Ct по каналу Green.
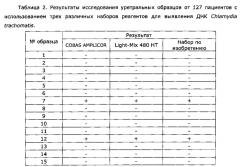
Результаты исследования уретральных образцов от 127 пациентов приведены в таблице 2.
Было получено 100%-ное совпадение при тестировании набора по изобретению относительно двух референсных наборов реагентов. Таким образом, диагностическая чувствительность, диагностическая специфичность, прогностическое значение положительного результата и прогностическое значение отрицательного результата набора по изобретению составили 100%.
Также было продемонстрировано, что набор по изобретению позволяет достоверно выявлять наличие ДНК Chlamydia trachomatis в биологических образцах методом мультиплексной полимеразной цепной реакции одновременно с выявлением ДНК других возбудителей инфекций, передаваемых половым путем: Neisseria gonorrhoeae, Trichomonas vaginalis, Mycoplasma genitalium.
Пример 2. Количественное определение ДНК Chlamydia trachomatis в биологических образцах.
Проводили исследование биологических образцов, описанных в примере 1, с использованием дополнительного набора реагентов для выявления ДНК Chlamydia trachomatis ХЛАМИ-ГЕН (ООО «НПО ДНК-Технология», Россия).
Результаты исследования уретральных образцов от 127 пациентов приведены в таблице 3. При анализе результатов исследования выявлен дискордантный образец №84.
Далее все образцы, в которых была выявлена ДНК Chlamydia trachomatis, исследовали методом количественной полимеразной цепной реакции с применением набора по изобретению.
Количественное определение ДНК микроорганизма основывается на существовании линейной зависимости между циклом начала увеличения флуоресценции образца (пороговый цикл, Cycle threshold, Ct) и исходной концентрацией ДНК-мишени. Для реализации количественного определения в реакции амплификации параллельно используются ДНК-калибраторы - образцы с известной концентрацией ДНК Chlamydia trachomatis. По результатам амплификации ДНК-калибраторов выстраивается калибровочная прямая, по которой происходит определение концентрации ДНК Chlamydia trachomatis в образцах.
Калибраторы (К1 и К2) готовили путем разведения стандартного образца производства (СОП) №86 Chlamydia trachomatis ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, содержащего фрагмент криптической плазмиды Chlamydia trachomatis, клонированный по сайтам EcoRI в плечи фага λ - λgt10. Для разведения исходного СОП используется ДНК-буфер с poly(A). Конечная концентрация для калибратора К1 составляет 1*106 ГЭ/мл; для калибратора К2 - 1*104 ГЭ/мл.
Амплификацию проводили на приборе «Rotor-Gene Q» (QIAGEN, Германия). Значения пороговых циклов калибраторов и исследуемых образцов анализировались программой автоматического учета результатов. В соответствии с этими значениями автоматически была построена калибровочная прямая и рассчитаны концентрации ДНК Chlamydia trachomatis в исследованных уретральных образцах от 16 пациентов (таблица 4).
Установлено, что в дискордантном образце концентрация ДНК Chlamydia trachomatis самая низкая из всех исследованных образцов и составляет 6,52Е+02 ГЭ/мл. Данная концентрация ДНК С.trachomatis лежит ниже границы аналитической чувствительности набора реагентов ХЛАМИ-ГЕН, что и объясняет получение отрицательного результата при исследовании с использованием этого набора.
Количественное определение ДНК Chlamydia trachomatis может быть полезно для различных клинико-лабораторных и научно-исследовательских целей, таких как уточнение диагноза при сомнительных/дискордантных результатах анализа, определении чувствительности различных методов диагностики, мониторинга эффективности терапии. Наконец, количественное определение возбудителя может иметь большое значение в выборе тактики этиотропной терапии, поскольку существуют основания полагать [Horner P. The case for further treatment studies of uncomplicated genital Chlamydia trachomatis infection. Sex Transm Infect. 2006 Aug; 82(4): 340-343], что рецидив хламидийной инфекции, не связанный с повторным инфицированием после проведенной антибактериальной терапии, вызван развитием гетеротипической устойчивости в результате высокой бактериальной нагрузки до начала лечения.
1. Набор реагентов для выявления ДНК Chlamydia trachomatis в образце, включающий по меньшей мере два олигонуклеотидных праймера для полимеразной цепной реакции и, при необходимости, олигонуклеотидный зонд, термостабильную ДНК-полимеразу, буферный раствор для ПЦР, дезоксинуклеозидтрифосфаты, отличающийся тем, что первый олигонуклеотидный праймер имеет нуклеотидную последовательность SEQ ID NO: 2, второй олигонуклеотидный праймер имеет нуклеотидную последовательность SEQ ID NO: 3.
2. Набор реагентов по п. 1, характеризующийся тем, что олигонуклеотидный зонд представляет собой олигонуклеотидный зонд для детекции ДНК Chlamydia trachomatis в режиме реального времени, где указанный зонд на 5'-конце содержит флуоресцентный краситель, на 3'-конце содержит гаситель флуоресценции.
3. Набор реагентов по п. 2, характеризующийся тем, что указанный флуоресцентный краситель выбран из группы: JOE, FAM, R6G, ROX, Су5, Су5.5, HEX.
4. Набор реагентов по п. 2, характеризующийся тем, что указанный гаситель флуоресценции выбран из группы: BHQ1, BHQ2, BHQ3, RTQ.
5. Набор реагентов по п. 2, характеризующийся тем, что указанный олигонуклеотидный зонд имеет последовательность SEQ ID NO: 4.
6. Набор реагентов по п. 2, характеризующийся тем, что указанный олигонуклеотидный зонд представляет собой (FAM)-CCCCGCACGTGCTTCGAGCAACCGCG-(BHQ1).
7. Набор реагентов по п. 2, характеризующийся тем, что указанный олигонуклеотидный зонд представляет собой (JOE)-CCCCGCACGTGCTTCGAGCAACCGCG-(BHQ1).
8. Набор реагентов по п. 1, характеризующийся тем, что указанный образец выбран из группы: мазок из влагалища, моча, семенная жидкость, соскоб из уретры, соскоб из цервикального канала.
9. Применение набора реагентов по любому из пп. 1-8 для выявления ДНК Chlamydia trachomatis в образце методом полимеразной цепной реакции.