Способ ранней диагностики заболеваний путем оптического измерения физических характеристик нативной биологической жидкости
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к лабораторной диагностике, и может быть использовано для исследования физических характеристик нативной биологической жидкости (НБЖ). Для этого через ее анализируемый образец, помещенный в прозрачную кювету, пропускают зондирующий лазерный луч оптического диапазона (ЗЛОД), измеряют характеристики рассеяния ЗЛОД на микро- и наночастицах (МЧ и НЧ) НБЖ с помощью одного матричного фотоприемника (МФП) для получения информации о характеристиках малоуглового динамического рассеяния указанного луча МЧ и по меньшей мере одного одноэлементного фотоприемника (ОЭФП), расположенного в диапазоне углов 30°…150° для получения информации о характеристиках излучения, рассеянного НЧ. Результаты измерений направляют в компьютер для математической обработки (МО). После изучения полученных результатов МО на образец НБЖ оказывают внешнее воздействие, вызывающее изменение флуктуационных характеристик рассеянной мощности, уточняющих или дополняющих после повторных оптических измерений ранее полученные характеристики. Изобретение обеспечивает повышение диагностической информативности исследования характеристик и состояния субмикронных частиц при оптическом анализе методом динамического рассеяния на указанных частицах лазерного излучения в образце нативной биологической жидкости. 3 з.п. ф-лы, 5 ил., 5 пр.
Реферат
Область использования
Изобретение относится к области медицины и может быть использовано для измерения физических характеристик нативных биологических жидкостей с целью ранней диагностики социально значимых заболеваний, а также для оценки эффективности проводимого лечения.
Уровень техники
Необходимым условием жизнедеятельности многоклеточного организма являются межклеточные взаимосвязи, позволяющие скоординировать общие биохимические процессы. Для осуществления такой координации, дающей возможность сообществу клеток контролировать поведение ее частей, требуются механизмы, которые позволяют обмениваться комплексной информацией на расстоянии. Сигналы передаются с помощью гормонов, цитокинов и хемокинов, факторов роста, нейромедиаторов, метаболитов, ионов (Медицинские термины / http://dic.academic.ru/ [1]). Как недавно выяснилось, есть еще один способ переноса информации между клетками - внеклеточные везикулы, выделяемые клетками в окружающую среду и разносимые кровотоком по всему организму. (Что такое везикулы / http://narod-medicina.ru/wp-content/uploads/2011/02/vezikuly.jpg/ [2]). Внеклеточные везикулы являются в настоящее время предметом интенсивного исследования, так как они присутствуют во всех органах и играют важнейшую роль во многих биологических процессах как физиологических, так и паталогических. Внеклеточные везикулы найдены в различных биологических жидкостях, в том числе в плазме крови, моче, слюне, амниотической жидкости, грудном молоке и жидкости, накапливающейся при плевральном асците. В 2013 году работы по изучению везикулярного транспорта были удостоены Нобелевской премии: (http://www.nobelprize.org/nobel_prizes/medicine/laureates/2013/med_image_press_eng.pdf] [3]). Отсутствие подходящих методов для их обнаружения и анализа оказывает существенное ограничение на развитие этих исследований.
Стремительное развитие современных методов медицинской диагностики и биоанализа основано прежде всего на достижениях молекулярной диагностики и генной инженерии. Известно, что развитие патологических процессов в организме человека сопровождается изменениями ряда молекулярных параметров в клетках и тканях, а также в важнейшей из биологических жидкостей - в крови (http://www.bibliotekar.ru/med-4/67.htm [4]). Кроме того, в крови непрерывно протекают иммунологические реакции, связанные с процессами агрегации иммунных комплексов. В последние годы достоверно установлено, что при патологических ситуациях в крови сильно увеличивается количество циркулирующих крупных субмикронных комплексов, в первую очередь, внеклеточных везикул, а их вид и состав различны в зависимости от вида патологии. В настоящее время для ранней диагностики онкологических заболеваний используется достаточно сложная и дорогостоящая лабораторная аппаратура типа ЯМР- и ЭПР-томографов, которая не может быть использована для массового профилактического обследования населения (скрининга) и не может выявлять проблему на ранней стадии, когда опухоль заметного размера еще не образовалась. Размеры микронных частиц обычно определяют с помощью оптических микроскопов и дифрактометров, а наночастиц - в большинстве случаев с помощью электронных или сканирующих зондовых микроскопов. Однако, стоимость электронных микроскопов высокого разрешения весьма велика (от 500 тысяч долларов США и более). Кроме того, они сложны в применении и принципиально непригодны для исследования частиц, которые существуют только в жидкой фазе (например, многих наноструктурированных лекарственных препаратов и биологических жидкостей). С поправкой на несколько меньшую цену сказанное относится и к сканирующим зондовым микроскопам. Ввиду принципиальной невозможности оперативного проведения измерений и сложности пробоподготовки, использование таких приборов в медицинской практике является очень сложной задачей.
Указанных недостатков лишены широко применяемые и совершенствуемые иммуноферментные методы диагностики. Инструментальной основой этого направления являются физические методы детектирования и реализующие их устройства, основанные на использовании современной оптики. Сюда можно отнести методы динамической спектроскопии рассеяния лазерного излучения, проточной цитометрии, фотоколориметрии и др.
В настоящее время основным источником информации о наличии крупных субмикронных комплексов, таких как внеклеточные везикулы, и об их свойствах в биологических жидкостях является проточная цитометрия (http://www.dakocytornation.ru/dako.html [5]). Упрощенно работа лазерного цитофлюориметра сводится к следующему. Суспензию клеток помешают в контейнер для образца и под давлением через фильтр подают по соединительной трубке к протоковому элементу. Клетки и внеклеточные везикулы идут одна за другой и в проточной ячейке пересекают лазерный пучок, тем самым ослабляя прохождение луча, рассеивая его, или, если клетки были окрашены флюорохромами, вызывая эффект флюоресценции. Использование интенсивных лазеров в сочетании с высокочувствительными фотоприемниками позволяет идентифицировать субмикронные частицы в проточном режиме. Нижний диапазон размеров измеряемых частиц зависит от их показателя преломления. У частиц биологического происхождения, показатель преломления мало отличается от показателя преломления воды, в которой они находятся. Данное обстоятельство затрудняет определение размеров этих биологических частиц менее 300-400 нм классическим методом, основанным на анализе интенсивности рассеянного излучения. Кроме того, недостатком данного метода является высокая стоимость проточного цитофлюориметра и многоступенчатость подготовки образцов к исследованию, что приводит к искажению результатов. Сложная пробоподготовка приводит к неспособности цитометра работать с нативной биологической жидкостью, что существенно ограничивает его возможности.
Широкое распространение в последние годы получила также оптическая диагностика размеров микрочастиц, основанная на спектроскопии динамического (квазиупругого) рассеяния света. Она уже в значительной степени развита экспериментально и используется как вариант спектроскопии высокого разрешения. Приборы, работающие на этом принципе, выпускаются несколькими производителями (Malvern - Zetasizer Nano ZS, Photocor - Photocor Complex, Particle Sizing Systems - Nicomp). Методы определения размеров дисперсных частиц на основе регистрации динамического рассеяния света основаны на идентификации частиц по эффективному коэффициенту диффузии, а заключения об их размерах строятся на основе моделей, связывающих коэффициент диффузии частиц с их эффективным размером. Методы, основанные на светорассеянии, позволяют измерять характеристики биологических объектов непосредственно в жидкой среде, не требуя сложной подготовки проб.
Известен, в частности, способ диагностики онкологических заболеваний, включающий исследование слабого водного раствора нативной плазмы или нативной сыворотки крови пациента методом лазерной корреляционной спектроскопии (RU 2132635, A61B 5/00,1999 [6]). Данный известный способ основан на экспериментальной оценке ряда характеристических параметров спектральной функции динамического рассеяния света в слабых растворах анализируемой биологической жидкости. Количественный фракционный состав плазмы и сыворотки крови, а также характер межмолекулярного взаимодействия, определяющие молекулярную динамику в анализируемом растворе, находятся в сильной зависимости от системы гомеостаза, функциональное состояние которой непосредственно связано с физиологическим состоянием основных биосистем. Поэтому любые изменения физиологического состояния организма, тем более патологические процессы, сопровождаются изменениями указанных выше физических параметров плазмы и сыворотки крови, что влечет за собой соответствующие изменения структуры молекулярной динамики в анализируемом растворе.
Известен также способ диагностики онкологических заболеваний, включающий последовательное исследование двух слабых водных растворов плазмы крови пациента методом лазерной корреляционной спектроскопии с соответствующим добавлением в приготовленные растворы дополнительных компонентов - щелочи и кислоты (RU 2276786, G01N 33/48, 2005 [7]). Согласно этому способу для каждого упомянутого раствора определяют амплитуды флуктуаций интенсивности светорассеяния в полосе частот 1-180 Гц.
Названные изобретения [6, 7] указали путь использования динамического рассеяния света в нативных биологических жидкостях для построения методов диагностики паталогических процессов в организме. Однако данными способами могут быть исследованы только некоторые ограниченные динамические характеристики флуктуаций рассеянного излучения в узком диапазоне частот (1-180) Гц. Как показали дальнейшие исследования, для обеспечения надежной диагностики этого явно недостаточно.
Прототипом данного изобретения может служить способ исследования физических характеристик нативной биологической жидкости, заключающийся в том, что через ее анализируемый образец, помещенный внутри прозрачной кюветы, пропускают зондирующий лазерный луч в оптическом диапазоне частот электромагнитных колебаний, измеряют характеристики динамического рассеяния указанного луча на содержащихся в указанном образце микро- и наночастицах с помощью одного матричного фотоприемника для получения информации о характеристиках малоуглового рассеяния указанного луча микрочастицами, и по меньшей мере одного одноэлементного фотоприемника, расположенного под углом 30°-150° к исходному направлению указанного луча для получения информации о характеристиках его излучения, рассеянного наночастицами, с последующей математической обработкой результатов измерений в компьютере путем совместного решения интегральных уравнений обратной задачи рассеяния (RU 2012145430 А, 10.05.2014, формула [8]).
Под «малоугловым рассеянием» принято понимать рассеяние электромагнитных волн частицами, размер которых соизмерим или больше длины волны зондирующего электромагнитного излучения (статья «Малоугловое рассеяние» в физической энциклопедии, 1988 г./ http://dic.academic.ru/dic.nsf/enc_physics/3830/%D0%9C%D0%90%D0%9B%D0%9E%D0%A3%D0%93%D0%9B%D0%9E%D0%92%D0%9E%D0%95 [9]). Из того же источника информации [9] следует, что с уменьшением диаметра частицы углы отклонения направления рассеянного излучения от первоначального должны увеличиваться и при значительном уменьшении D (для лазерного излучения светового диапазона - частицы субмикронного размера) выйти за приделы малоуглового рассеивания.
Способ согласно [8] обеспечивает получение подробной информации о размерах и характере распределения в анализируемом образце частиц субмикронного размера (микро- и наночастиц). Применительно к биологическим жидкостям такими частицами являются белки, липопротеины, а также внеклеточные везикулы. Однако информация о размерах взвешенных в биологической жидкости субмикронных частицах не всегда достаточна для надежного диагностирования наличия и характера исследуемого заболевания. В частности, характерные распределения микро- и наночастиц, выявленное в анализируемой биологической жидкости, для разных патологий могут перекрываться и/или иметь сезонные и возрастные изменения, которые снижают эффективность диагностирования, основанного на исследовании оптических характеристик динамического рассеяния лазерного луча согласно прототипу [8]. В связи с этим при первичных измерениях динамического рассеяния света в образце исследуемой биологической жидкости частиц с микро- и наноразмерами, характерных для надежного диагностирования искомого заболевания может оказаться слишком мало. Различные патологии могут сопровождаться появлением внеклеточных везикул близких размеров, которые методом динамического рассеяния не различаются. В то же время состав названных везикул различен и, поэтому, они могут по-разному агломерировать или разрушаться под действием внешних факторов, что легко различимо в изменении характера рассеяния.
Раскрытие изобретения
Задачей изобретения является повышение надежности ранней диагностики социально опасных заболеваний, а техническим результатом - повышение диагностической информативности исследования характеристик и состояния субмикронных частиц при оптическом анализе методом динамического рассеяния на указанных частицах лазерного излучения в образце нативной биологической жидкости. Решение указанной задачи путем достижения указанного технического результата обеспечивается тем, что при осуществлении способа исследования физических характеристик нативной биологической жидкости, заключающийся в том, что через ее анализируемый образец, помещенный внутри прозрачной кюветы, пропускают зондирующий лазерный луч в оптическом диапазоне частот электромагнитных колебаний, измеряют характеристики динамического рассеяния указанного луча на содержащихся в указанном образце микро- и наночастицах с помощью одного матричного фотоприемника для получения информации о характеристиках малоуглового рассеяния указанного луча микрочастицами, и по меньшей мере одного одноэлементного фотоприемника, расположенного под углом 30°-150° к исходному направлению указанного луча для получения информации о характеристиках его излучения, рассеянного наночастицами, с последующей математической обработкой результатов измерений в компьютере путем совместного решения интегральных уравнений обратной задачи рассеяния,
согласно патентуемому изобретению,
после изучения полученных результатов математической обработки данных указанных оптических измерений на тот же образец оказывают внешнее воздействие, вызывающее изменение флуктуационных характеристик рассеянной мощности, после чего проводят повторно математический анализ полученных результатов исследования указанного образца биологической жидкости.
При этом для осуществления указанного внешнего воздействия: в образец анализируемой биологической жидкости могут быть введены антигены, способные связывать большое количество антител с укрупнением подлежащих исследованию микрообъектов;
в образец анализируемой биологической жидкости могут быть введены растворы солей, кислот или щелочей, в концентрациях, приводящих к выпадению в осадок содержащихся в анализируемой жидкости заряженных биологических объектов, при переходе раствора через изоэлектрическую точку;
образец анализируемой биологической жидкости может быть нагрет до температуры диссоциации содержащихся в ней агломератов.
Причинно-следственная связь между совокупностью существенных признаков изобретения и указанным техническим результатом состоит в том, что внешнее воздействие, вызывающее изменение флуктуационных характеристик рассеянной мощности, уточняющих или дополняющих характеристики, полученные на основе первоначальных оптических измерений динамического рассеяния лазерного луча на содержащихся в образце анализируемой жидкости частицах субмикронного размера, позволяет обнаружить этим же методом дополнительную важную информацию о наличии или отсутствии у пациента факторов опасного заболевания. Дело в том, что при первичных измерениях характеристик динамического рассеяния света в образце исследуемой биологической жидкости на частицах с микро- и наноразмерами, характерных распределений по размерам для надежного диагностирования искомого заболевания может оказаться слишком мало. Вместе с тем не исключено, что характерные изменения размеров появляются под действием внешних факторов описанных ранее, что легко различимо в изменении характера рассеяния.
Внешнее воздействие, таким образом, должно быть направлено на то, чтобы соответственно укрупнить или уменьшить размеры указанных характерных для диагностирования заболевания частиц до требуемого диапазона.
Следует отметить, что сильной стороной данного подхода является использование для целей диагностики нативного образца, не претерпевающего изменений в процессе первичных оптических измерений, в связи с чем, он после изменения флуктуационных характеристик рассеянной мощности может быть исследован тем же методом повторно.
Краткое описание фигур чертежа
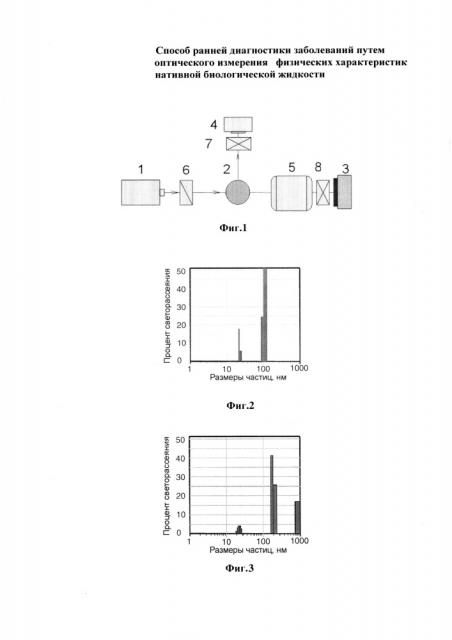
На фиг. 1 изображена принципиальная схема устройства для осуществления способа согласно изобретению; на фиг. 2 приведена полученная при осуществлении способа [8] диаграмма распределения концентраций наночастиц плазмы крови здорового человека; на фиг. 3 - то же для пациента с сердечнососудистой патологией; на фиг. 4 - гистограмма вируса гепатита А в культуральной жидкости; на фиг. 5 - гистограммы: А - иттербиевый комплекс 2,4-диметоксигематопорфирина; Б - гистограмма бычьего сывороточного альбумина; В - гистограмма комплекса 2,4-диметоксигематопорфирина с бычьим сывороточным альбумином через 55 минут после сливания растворов, Г - то же через 24 часа.
Перечень позиций фиг. 1 чертежа
1 - зондирующий лазер оптического диапазона частот электромагнитных колебаний; 2 - рабочая кювета с образцом анализируемой биологической жидкости; 3 - матричный фотоприемник; 4 - одноэлементный фотоприемник; 5 - объектив для сбора излучения малоуглового рассеяния лазерного луча; 6 - устройство поворота плоскости поляризации излучения; 7, 8 - поляризаторы излучения.
Осуществление изобретения
Способ исследования физических характеристик нативной биологической жидкости согласно изобретению реализуют с помощью устройства, схематически изображенного на (фиг. 1). Устройство содержит работающий в оптическом диапазоне частот электромагнитных колебаний зондирующий лазер 1 с оптическим трактом (не показан) транспортировки лазерного луча. На пути последнего установлена прозрачная рабочая кювета 2 с образцом анализируемой нативной биологической жидкости. В области рассеяния указанного лазерного луча на содержащихся в образце биологической жидкости микро- и наночастицах установлены в данном примере один матричный фотоприемник и один одноэлементный фотоприемник 4. При этом матричный фотоприемник 3 для получения информации о характеристиках малоуглового рассеяния (в диапазоне не более 10°) лазерного луча микрочастицами установлен без отклонения от исходного направления указанного лазерного луча в фокальной плоскости объектива 5, расположенного на пути этой части рассеянного излучения, а одноэлементный фотоприемник 4 - в диапазоне углов 30°…150° (в данном примере - под 90°) для получения информации о характеристиках его излучения, рассеянного наночастицами. Каждый из указанных фотоприемников 3, 4 снабжен узлом предварительной обработки вырабатываемых ими сигналов (не показаны), предназначенным для выделения полезного сигнала из шумов, его усиления и подготовки для последующей передачи в компьютер или микропроцессор. В компьютере (не показан) производится последующая математическая обработка сигналов с получением требуемого результата. Объектив 5 одновременно может служить и для наблюдения процесса диффузии относительно крупных биообъектов. На пути луча зондирующего лазера 1 перед прозрачной кюветой 2 может быть установлено устройство 6 поворота плоскости поляризации излучения, а перед каждым из фотоприемников 3, 4 установлен поляризатор соответственно 7, 8 для выделения вертикальной или горизонтальной составляющей поляризации рассеянного излучения. Использование поляризаторов (как и в прототипе) позволяет учитывать при математической обработке результатов деполяризованную компоненту рассеянного излучения. Объектив 5 может содержать пространственный фильтр (не показан) для уменьшения влияния прямого излучения.
Способ определения физических характеристик нашивных биологических жидкостей согласно изобретению осуществляется следующим образом. Зондирующий луч лазера 1 мощностью (1…100) мВт, генерируемый в оптическом диапазоне частот электромагнитных колебаний, пропускают через прозрачную рабочую кювету 2 с исследуемой нативной биологической жидкостью. Большая часть лазерного луча при проходе через анализируемую жидкость не рассеивается или подвергается малоугловому рассеянию микрочастицами на углы в диапазоне не более 10°. Это рассеянное излучение регистрируется матричным фотоприемником 3. Малая часть лазерного луча, рассеявшись наночастицами на углы в диапазоне 30°…150°, попадает на одноэлементный фотоприемник 4. В зависимости от разрешенного направления поляризации, задаваемого с помощью устройства 6 поворота плоскости поляризации и поляризаторов 7, 8, расположенных перед фотоприемниками 3, 4 на их чувствительные элементы попадает рассеянное излучение с вертикальной или горизонтальной поляризацией. Биения оптического сигнала, попадающего в одноэлементный фотоприемник 4, преобразуются во флуктуации фототока. Далее эти флуктуирующие электрические сигналы математически обрабатываются в компьютере, а в пикселях матрицы фотоприемника 3 формируются сигналы, характеризующие малоугловую диаграмму рассеянного излучения. Промежуточные результаты получаются после совместного решения соответствующей программой компьютера интегральных уравнений обратной задачи рассеяния. Анализируя полученные промежуточные результаты, оператор или компьютерная программа принимает решение об их достаточности или необходимости использования дополнительного внешнего воздействия, вызывающего изменение флуктуационных характеристик рассеянной мощности анализируемой биологической жидкости, уточняющих или дополняющих характеристики, полученные на основе первоначальных измерений.
В частности, в образец анализируемой биологической жидкости могут быть введены антигены, способные связывать большое количество антител с укрупнением подлежащих исследованию микрообъектов.
Указанное внешнее воздействие может быть также осуществлено путем введения в образец анализируемой биологической жидкости растворов солей, кислот или щелочей, в концентрациях, приводящих к переходу через изоэлектрическую точку содержащихся в анализируемой биологической жидкости заряженных белково-липидных комплексов.
Данный способ внешнего воздействия основан на следующих свойствах биологической жидкости. В молекулах белков имеются свободные карбоксильные и аминные группы, способные диссоциировать как кислоты и как основания являясь, таким образом, амфотерными электролитами. В щелочном растворе подавляется диссоциация аминных групп, молекулы белков заряжаются отрицательно и ведут себя как анионы. В кислой среде, в результате подавления диссоциации карбоксильных групп, белки заряжаются положительно, то есть становятся катионами. При определенной кислотности раствора, которая получила название изоэлектрической точки, в молекуле белка устанавливается равенство положительных и отрицательных зарядов, она становится электронейтральной. Положение изоэлектрической точки зависит от содержания и природы основных и кислых групп в молекуле белка. У большинства растительных белков изоэлектрическая точка находится в слабокислой среде. В изоэлектрической точке белок обладает наименьшей растворимостью и легко выпадает в осадок при воздействиях, снижающих гидратацию его молекул (при добавлении органических растворителей или солей). При этом молекулы белка слипаются, образуя более крупные частицы, и выпадают из раствора в виде осадка. Это позволяет более отчетливо выявить их свойства при повторном исследовании характеристик рассеяния лазерного луча, прошедшего рабочую кювету 2.
На экране монитора компьютера представляются итоговые результаты в удобном для пользователя виде, например, в виде графиков или таблиц, содержащих размеры и концентрации частиц в анализируемой биологической жидкости, а также информацию о содержании в ней белков или липидов.
Двухвалентность антител обеспечивает возможность соединения неограниченного числа антигенных частиц в конгломераты. При различном числе антигенных детерминант на молекуле антигена характер структуры конгломератов комплекса антиген - антитело может быть разным. При избытке антигена или антител крупные конгломераты вообще не возникают вследствие заполнения реагирующих участков молекул избыточным количеством второго компонента.
В силу ранее описанной специфики метода динамического рассеяния света, появление крупных частиц на фоне более мелких может быть измерено с высокой чувствительностью и точностью другими методами недостижимой. Более того, временная динамика такого изменения и характер конечного распределения могут быть очень информативными для выработки заключений о количестве и специфике исследуемых микроорганизмов или других биологических объектов.
Пример 1
Для уточнения промежуточных результатов после просвечивания образца биологической жидкости лазерным лучом на предмет выявления специфической патологии, связанной с бактериальным или вирусным воздействием на организм, вводили сорбент, содержащий иммобилизированные антигены, способные связывать большое количество антител. Это приводило к появлению в биологической жидкости укрупняющихся объектов, легко обнаруживаемых при повторном просвечивании образца лазерным лучом первоначальным методом. В силу ранее описанной специфики метода динамического рассеяния света, появление крупных частиц на фоне более мелких может быть измерено с высокой чувствительностью и точностью, другими методами недостижимыми. Используя антигены, связывающие антитела с различной специфичностью, таким методом можно проверять белки на наличие или отсутствие у них определенных генетических маркеров или определенных структурных субъединиц.
Пример 2
При исследовании по методу прототипа сыворотки крови онкологического больного были получены промежуточные результаты в виде кривой распределения концентраций наночастиц. После предварительного измерения образец был разделен на несколько частей, каждая из которых подвергалась процедуре титрования щелочью с одновременным наблюдением путем повторного просвечивания образца лазерным лучом за характером изменения распределения концентраций наночастиц. При приближении значения ионной силы раствора к изоэлектрической точке начиналось интенсивное укрупнение субмикронных объектов, которое сопровождалось даже видимым на глаз помутнением образца. Такие процессы наблюдались для разных исходных образцов, однако характер агломерации и необходимые для этого количества добавляемых реактивов оказались различными при различных патологиях. На современном этапе для строгого сопоставления полученных результатов с характером заболевания недостаточно знаний. В то же время было установлено, что сыворотка крови здорового человека обладает большей буферной силой и поэтому более устойчива к воздействию щелочью и кислотой, чем аналогичная сыворотка всех обследованных нами больных пациентов.
Пример 3
Было проведено диагностическое исследование на предмет раннего выявления у пациента сердечно-сосудистой патологии. Предварительно через образец анализируемой нативной биологической жидкости (плазмы крови), помещенный в прозрачную рабочую кювету 2 (фиг. 1) пропустили зондирующий луч от лазера 1, работающего в оптическом диапазоне электромагнитных колебаний. С помощью матричного и одноэлементного фотоприемников соответственно 3 и 4 и не показанных на чертеже средств математической обработки измеренных сигналов рассеяния лазерного луча были получены промежуточные результаты в виде кривой распределения концентраций наночастиц по размерам (фиг. 3). При сравнении этих результатов с аналогичными характеристиками образца плазмы крови здорового человека (фиг. 2) видна существенная разница, которую можно объяснить предполагаемой начальной стадией сердечно-сосудистого заболевания. Однако такой вывод казался недостаточно убедительным на фоне других возможных патологий, могущих привести к аналогичному результату. В связи с этим было решено нагреть образец примерно до 50°С, что привело к выявленному при повторном просвечивании образца лазерным лучом распаду крупных образований (около 1 мкм). Подобные крупные образования при наличии онкологии распадаются при существенно более высоких температурах, что свидетельствовало в пользу предварительного вывода.
Пример 4
Для уточнения промежуточных результатов после просвечивания образца биологической жидкости лазерным лучом на предмет выявления специфической патологии, связанной с бактериальным или вирусным воздействием на организм, в образец вводили антигены, иммобилизированные на латексные частицы, для выявления антител характеризующих вирусы. При последующем просвечивании образца лазерным лучом исследовались динамические характеристики конечного распределения размеров названных латексных частиц, связанные с процессом агломерации на латексах биологических объектов, присутствующих в исследуемой биологической жидкости. В отличие от классических иммунологических методов при таком исследовании достигается существенно более высокая чувствительность. Помимо этого, появляется возможность получения функциональной зависимости протекания процесса агглютинации во времени, что позволяет получить значения постоянных скорости протекающих реакций и тем самым расширить диагностические возможности исследования анализируемого образца.
Пример 5
Для уточнения промежуточных результатов после просвечивания образца биологической жидкости лазерным лучом на предмет выявления специфической патологии, связанной с бактериальным или вирусным воздействием на организм, в раствор вводили биологический препарат, содержащий антитоксины (антитела против токсинов), которые, соединяясь с соответствующими токсичными веществами, нейтрализуют их. Количество токсина определялось титрованием с одновременной регистрацией характера изменения во времени процесса рассеяния лазерного луча на образующихся в исследуемой жидкости агрегатах. Распределение размеров и концентраций, устанавливающееся между отдельными циклами титрования, может быть использовано для разработки частных методик исследования биологических жидкостей. Получение подобной информации другими известными нам методами невозможно.
Промышленная применимость
Исследования, направленные на выяснение состава внеклеточных везикул и их функциональной активности, сдерживаются сложностью составов биологических жидкостей. Способ для их обнаружения и анализа согласно предлагаемому изобретению открывает широкие перспективы для диагностики и сопровождения соответствующего лечения практически любых заболеваний.
Формула и описание изобретения изложены достаточно ясно для его практической реализации специалистами в области создания современного диагностического медицинского оборудования.
1. Способ исследования физических характеристик нативной биологической жидкости, заключающийся в том, что через ее анализируемый образец, помещенный внутри прозрачной кюветы, пропускают зондирующий лазерный луч в оптическом диапазоне частот электромагнитных колебаний, измеряют характеристики динамического рассеяния указанного луча на содержащихся в указанном образце микро- и наночастицах с помощью одного матричного фотоприемника для получения информации о характеристиках малоуглового рассеяния указанного луча микрочастицами и по меньшей мере одного одноэлементного фотоприемника, расположенного под углом 30°-150° к исходному направлению указанного луча для получения информации о характеристиках его излучения, рассеянного наночастицами, с последующей математической обработкой результатов измерений в компьютере путем совместного решения интегральных уравнений обратной задачи рассеяния, отличающийся тем, что после изучения полученных результатов математической обработки данных указанных оптических измерений на тот же образец оказывают внешнее воздействие, вызывающее изменение флуктуационных характеристик рассеянной мощности, после чего проводят повторно математический анализ полученных результатов исследования указанного образца биологической жидкости.
2. Способ по п. 1, отличающийся тем, что для осуществления указанного внешнего воздействия в образец анализируемой биологической жидкости вводят антигены, способные связывать большое количество антител с укрупнением подлежащих исследованию микрообъектов.
3. Способ по п. 1, отличающийся тем, что для осуществления указанного внешнего воздействия в образец анализируемой биологической жидкости вводят растворы солей, кислот или щелочей в концентрациях, приводящих к выпадению в осадок содержащихся в анализируемой жидкости заряженных биологических объектов при переходе раствора через изоэлектрическую точку.
4. Способ по п. 1, отличающийся тем, что для осуществления указанного внешнего воздействия образец анализируемой биологической жидкости нагревают до температуры диссоциации содержащихся в ней агломератов.