Лечение заболеваний, связанных с геном сиалидазы 4 (neu4), путем ингибирования природного антисмыслового транскрипта гена neu4
Иллюстрации
Показать всеГруппа изобретений относится к области биотехнологии. Представлены способы повышения экспрессии гена сиалидазы 4 (NEU4) с использованием олигонуклеотида, который специфически связывается с природным антисмысловым полинуклеотидом для гена NEU4. Представлен олигонуклеотид длиной от 10 до 30 нк, который специфически связывается с природным антисмысловым полинуклеотидом для гена NEU4. Также представлена фармацевтическая композиция, содержащая эффективное количество указанного олигонуклеотида. Группа изобретений позволяет повышать экспрессию гена NEU4, что применимо для лечения или предотвращения заболеваний, ассоциированных с геном NEU4 и/или по меньшей мере одним продуктом, кодируемым указанным геном. 6 н. и 30 з.п. ф-лы, 1 ил., 1 табл., 2 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ
[0001] Данная заявка испрашивает приоритет на основании предварительной заявки на патент США №61/390216, поданной 6 октября 2010 года, полное содержание которой включено в настоящее описание посредством ссылки.
[0002] Варианты реализации настоящего изобретения включают олигонуклеотиды, модулирующие экспрессию и/или функцию гена NEU4 и связанных с ним молекул.
УРОВЕНЬ ТЕХНИКИ
[0003] Гибридизация ДНК-РНК и РНК-РНК важна для многих аспектов функционирования нуклеиновых кислот, включая репликацию ДНК, транскрипцию и трансляцию. Гибридизация также играет главную роль во множестве технологий, которые позволяют либо обнаруживать конкретную нуклеиновую кислоту, либо изменять ее экспрессию. Антисмысловые нуклеотиды, например, нарушают экспрессию генов за счет гибридизации с РНК-мишенью, тем самым препятствуя сплайсингу РНК, транскрипции, трансляции и репликации. Антисмысловая ДНК обладает дополнительной особенностью, заключающейся в том, что гибриды ДНК-РНК выступают в качестве субстрата для ферментативного расщепления рибонуклеазой Н, активность которой присутствует в большинстве типов клеток. Антисмысловые молекулы могут быть доставлены в клетки, как в случае олигодезоксинуклеотидов (ОДН), или они могут представлять собой продукты экспрессии эндогенных генов в виде молекул РНК. Недавно Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) одобрило антисмысловое лекарственное средство, Витравен (VITRAVENE™) (для лечения цитомегаловирусного ретинита), что свидетельствует о возможности применения антисмыслового лекарственного средства в терапевтических целях.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Настоящее краткое описание предлагает краткое описание настоящего изобретения с той целью, чтобы вкратце обозначить предмет и сущность настоящего изобретения. Краткое описание представляют с пониманием того, что его не следует применять для толкования или ограничения объема или смыслового содержания формулы изобретения.
[0005] В одном варианте реализации согласно изобретению предложены способы для ингибирования действия природного антисмыслового транскрипта путем применения антисмыслового олигонуклеотида (олигонуклеотидов), нацеленного на любую область природного антисмыслового транскрипта, приводящего к увеличению экспрессии соответствующего смыслового гена. Авторы настоящей заявки также предполагают, что ингибирование природного антисмыслового транскрипта может быть достигнуто с помощью малых интерферирующих РНК (ммРНК), рибозимов и малых молекул, рассматриваемых в рамках настоящего изобретения.
[0006] Согласно одному варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида NEU4 в биологических системах, включая, но неограничиваясь перечисленными, клетки или ткани пациента in vivo или in vitro, включающий осуществление контакта указанной биологической системы или указанных клеток или тканей с антисмысловым олигонуклеотидом длиной примерно от 5 примерно до 30 нуклеотидов, при этом последовательность указанного олигонуклеотида по меньшей мере на 50% идентична последовательности обратного комплемента полинуклеотида, содержащего от 5 до 30 последовательных нуклеотидов в пределах нуклеотидов 1-2119 последовательности SEQ ID NO: 2, или в пределах нуклеотидов 1-1245 последовательности SEQ ID NO: 3, или 1-490 последовательности SEQ ID NO: 4, или 1-527 последовательности SEQ ID NO: 5, или 1-946 последовательности SEQ ID NO: 6, или 1-703 последовательности SEQ ID NO: 7, с обеспечением тем самым модулирования функции и/или экспрессии полинуклеотида NEU4 в указанных биологических системах, включая указанные клетки или ткани пациента in vivo или in vitro.
[0007] В одном варианте реализации олигонуклеотид нацелен на природную антисмысловую последовательность для полинуклеотидов NEU4, присутствующих в биологической системе, например, на нуклеотиды, указанные в последовательности, соответствующей SEQ ID NOS: 2-7, и любые их варианты, аллели, гомологи, мутанты, производные, фрагменты и последовательности, которые представляют собой их комплемент. Примеры антисмысловых олигонуклеотидов указаны в виде последовательностей, соответствующих SEQ ID NOS: 8-11.
[0008] Согласно другому варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида NEU4 в клетках или тканях пациента in vivo или in vitro, включающий осуществление контакта указанных клеток или тканей с антисмысловым олигонуклеотидом длиной от 5 до 30 нуклеотидов, при этом последовательность указанного олигонуклеотида по меньшей мере на 50% идентична последовательности обратного комплемента антисмысловой последовательности для полинуклеотида NEU4; с обеспечением тем самым модулирования функции и/или экспрессии полинуклеотида NEU4 в клетках или тканях пациента in vivo или in vitro.
[0009] Согласно другому варианту реализации предложен способ модулирования функции и/или экспрессии полинуклеотида NEU4 в клетках или тканях пациента in vivo или in vitro, включающий осуществление контакта указанных клеток или тканей с антисмысловым олигонуклеотидом длиной от 5 до 30 нуклеотидов, при этом последовательность указанного олигонуклеотида по меньшей мере на 50% идентична последовательности антисмыслового олигонуклеотида для антисмыслового полинуклеотида гена NEU4; с обеспечением тем самым модулирования функции и/или экспрессии полинуклеотида NEU4 в клетках или тканях пациента in vivo или in vitro.
[0010] Согласно другому варианту реализации изобретение включает способ модулирования функции и/или экспрессии полинуклеотида NEU4 в биологической системе, включающий осуществление контакта указанной биологической системы с по меньшей мере одним антисмысловым олигонуклеотидом, который нацелен на область природного антисмыслового транскрипта полинуклеотида NEU4; что приводит к модулированию функции и/или экспрессии полинуклеотида NEU4 в указанной биологической системе.
[0011] Согласно другому варианту реализации изобретение включает способ модулирования функции и/или экспрессии полинуклеотида NEU4 в биологической системе, включающий осуществление контакта указанной биологической системы с по меньшей мере одним антисмысловым олигонуклеотидом, который нацелен на область природного антисмыслового транскрипта полинуклеотида NEU4; что приводит к модулированию функции и/или экспрессии полинуклеотида NEU4 в указанной биологической системе.
[0012] В одном варианте реализации изобретение включает способ повышения функции и/или экспрессии полинуклеотида NEU4 в биологической системе, который соответствует SEQ ID NO. 1, включающий осуществление контакта указанной биологической системы с по меньшей мере одним антисмысловым олигонуклеотидом, который нацелен на область природного антисмыслового транскрипта полинуклеотида NEU4; что приводит к повышению функции и/или экспрессии указанного полинуклеотида NEU4 или экспрессии его продуктов.
[0013] Согласно другому варианту реализации изобретение включает способ повышения функции и/или экспрессии полинуклеотида NEU4 в биологической системе, который соответствует SEQ ID NO. 1, включающий осуществление контакта указанной биологической системы с по меньшей мере одним антисмысловым олигонуклеотидом, который нацелен на область природного антисмыслового транскрипта указанного полинуклеотида NEU4; что приводит к повышению функции и/или экспрессии указанного полинуклеотида NEU4 или экспрессии его продуктов, где природные антисмысловые транскрипты выбраны из SEQ ID NOS. 2-7.
[0014] Согласно другому варианту реализации изобретение включает способ повышения функции и/или экспрессии полинуклеотида NEU4 в биологической системе, который соответствует SEQ ID NO. 1, включающий осуществление контакта указанной биологической системы с по меньшей мере одним антисмысловым олигонуклеотидом, который нацелен на область природного антисмыслового транскрипта указанного полинуклеотида NEU4; что приводит к повышению функции и/или экспрессии указанного полинуклеотида NEU4 или экспрессии его продуктов, где природные антисмысловые транскрипты выбраны из SEQ ID NOS. 2-7, и где антисмысловые олигонуклеотиды выбраны по меньшей мере из одной SEQ ID NOS. 8-11.
[0015] В одном варианте реализации композиция содержит один или более антисмысловых олигонуклеотидов, которые связываются со смысловыми и/или антисмысловыми полинуклеотидами гена NEU4.
[0016] В одном варианте реализации олигонуклеотиды содержат один или более модифицированных или замещенных нуклеотидов.
[0017] В одном варианте реализации олигонуклеотиды содержат одну или более модифицированных связей.
[0018] В еще одном варианте реализации модифицированные нуклеотиды содержат модифицированные основания, включая молекулы фосфотиоатных, метилфосфонатных производных нуклеиновых кислот, пептидо-нуклеиновых кислот, 2'-O-метил-, фтор- или углерод-, метилен- или других закрытых нуклеиновых кислот (ЗНК; locked nucleic acids, LNA). Предпочтительно, модифицированные нуклеотиды представляют собой молекулы закрытых нуклеиновых кислот, включая ЗНК с α-L-рибо-конфигурацией (α-L-3HK).
[0019] В одном варианте реализации олигонуклеотиды вводят пациенту подкожно, внутримышечно, внутривенно или интраперитонеально.
[0020] В одном варианте реализации олигонуклеотиды вводят в составе фармацевтической композиции. Схема лечения включает по меньшей мере однократное введение антисмысловых соединений пациенту; однако, это лечение может быть модифицировано до введения многократных доз в течение некоторого периода времени. Лечение может быть объединено с одним или более другими типами терапии.
[0021] В одном варианте реализации олигонуклеотиды инкапсулированы в липосому или присоединены к молекуле-носителю (например, холестерину, ТАТ-пептиду).
[0022] Другие аспекты описаны ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
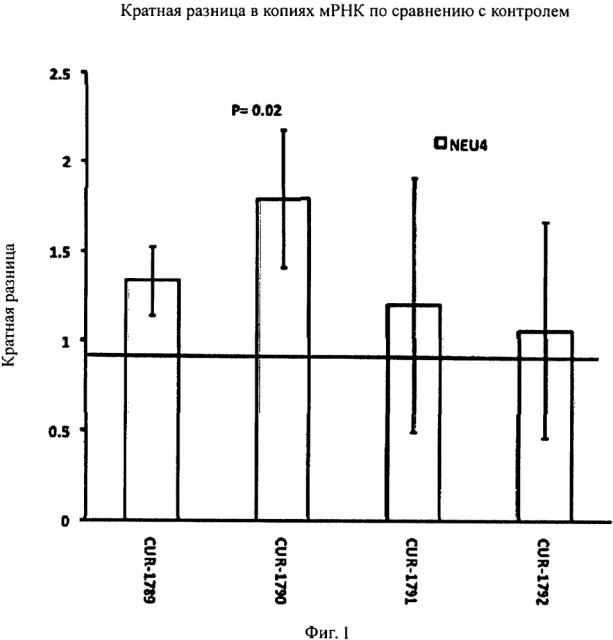
[0023] На Фигуре 1 представлены результаты полимеразной цепной реакции (ПЦР) в режиме реального времени, которые показывают кратное изменение + стандартное отклонение для мРНК гена NEU4 после обработки клеток HepG2 фосфоротиоатными олигонуклеотидами, введенными с применением липофектамина 2000, по сравнению с контролем. Результаты ПНР в режиме реального времени показывают, что уровни мРНК гена NEU4 в клетках HepG2 значимо повышаются через 48 часов после обработки одним из антисмысловых олигонуклеотидов NEU4 антисмысловым олигонуклеотидом Hs.678184. Столбцы диаграммы, обозначенные как CUR-1789-CUR-1792, соответствуют образцам, обработанным олигонуклеотидами, соответствующими SEQ ID NOS: 8-11, соответственно.
[0024] Описание Перечня последовательностей - SEQ ID NO: 1: сиалидаза 4 человека (NEU4), транскриптный вариант 3, мРНК (номер последовательности в базе данных NCBI (Национального центра биотехнологической информации США): NM_001167600); SEQ ID NO: 2: Природная антисмысловая последовательность (HS.678184) для гена NEU4; SEQIDNO:3: Природная антисмысловая последовательность (ВС038567) для гена NEU4; SEQ ID NO: 4: Природная антисмысловая последовательность (CR747539) для гена NEU4; SEQIDNO:5: Природная антисмысловая последовательность (BF527387) для гена NEU4; SEQ ID NO: 6: Природная антисмысловая последовательность (BF528789) для гена NEU4; SEQ ID NO: 7: Природная антисмысловая последовательность (BG913694) для гена NEU4, и SEQ ID NOS: 8-11: Антисмысловые олигонуклеотиды. Символ ʺ*ʺ обозначает фосфотиоатную связь.
ПОДРОБНОЕ ОПИСАНИЕ
[0025] Некоторые аспекты изобретения описаны ниже со ссылкой на примеры применения для иллюстрации. Следует понимать, что многочисленные конкретные детали, связи и способы приведены с целью обеспечения полного понимания изобретения. Однако специалист в данной области техники без труда обнаружит, что изобретение может быть применено на практике без одной или более конкретных деталей или с другими способами. Настоящее изобретение не ограничивается упорядочиванием действий или событий, так как некоторые действия могут быть осуществлены в разном порядке и/или одновременно с другими действиями или событиями. Кроме того, не все проиллюстрированные действия или события требуются для реализации методологии в соответствии с настоящим изобретением.
[0026] Все гены, названия генов и продукты генов, описанные в настоящей заявке, соответствуют гомологам из организмов любых видов, для которых применимы композиции и способы, предложенные в настоящей заявке. Таким образом, данные термины включают, но без ограничения, гены и генные продукты из организмов людей и мышей. Понимают, что, когда предложен ген или продукт гена из организма конкретного вида, этот элемент изобретения представлен исключительно в качестве примера, и его не следует истолковывать как ограничение, если контекст, в котором он появляется, ясно не указывает на обратное. Соответственно, например, гены, описанные в настоящей заявке, которые в некоторых вариантах реализации относятся к нуклеотидным и аминокислотным последовательностям млекопитающих, охватывают гомологичные и/или ортологичные гены и продукты генов из организмов других животных, включая, но без ограничения, других млекопитающих, рыб, земноводных, пресмыкающихся и птиц. В одном варианте реализации гены или нуклеотидные последовательности представляют собой гены или последовательности человека.
Определения
[0027] Терминология, применяемая в настоящей заявке, служит исключительно для описания конкретных вариантов реализации и не ограничивает изобретение. В настоящей заявке неопределенная и определенная формы единственного числа также включают множественные формы, если контекст ясно не предписывает иное. Кроме того, в той мере, в какой термины ʺвключающийʺ, ʺвключаетʺ, ʺимеющийʺ, ʺимеетʺ, ʺсʺ или их варианты применяют в подробном описании и/или формуле изобретения, такие термины подразумевают включение в себя подобно термину ʺсодержащийʺ.
[0028] Термин ʺпримерноʺ или ʺприблизительноʺ обозначает нахождение внутри диапазона приемлемой погрешности для конкретной величины, определенного специалистом в данной области техники, который будет зависеть отчасти от того, каким образом величину измеряют или определяют, т.е. от ограничений измерительной системы. Например, термин ʺпримерноʺ может означать, что величина находится в пределах 1 или более чем 1 стандартного отклонения, как показывает практика в данной области техники. Альтернативно, термин ʺпримерноʺ может означать диапазон погрешности, составляющий вплоть до 20%, предпочтительно вплоть до 10%, более предпочтительно вплоть до 5% и еще более предпочтительно вплоть до 1% от заданной величины. Альтернативно, применительно к биологическим системам или процессам, термин может означать нахождение в пределах порядка величины, предпочтительно в пределах пятикратного значения и более предпочтительно двукратного значения величины. В тех случаях, когда в заявке и формуле изобретения приведены конкретные значения, то, если не указано иное, следует предполагать термин ʺпримерноʺ, обозначающий нахождение внутри диапазона приемлемой погрешности для конкретной величины.
[0029] В настоящей заявке термин ʺмРНКʺ обозначает известный на настоящий момент мРНК-транскрипт(ы) гена-мишени и любые дополнительные транскрипты, происхождение которых может быть объяснено.
[0030] С помощью терминов ʺантисмысловые олигонуклеотидыʺ или ʺантисмысловое соединениеʺ обозначают молекулу РНК или ДНК, которая связывается с другой РНК или ДНК (РНК-, ДНК-мишенью). Например, если антисмысловое соединение представляет собой олигорибонуклеотид, оно связывается с другой РНК-мишенью за счет РНК-РНК-взаимодействий и изменяет активность РНК-мишени. Антисмысловой олигонуклеотид может увеличивать или подавлять экспрессию и/или функцию конкретного полинуклеотида. Определение включает любую чужеродную молекулу ДНК или РНК, подходящую с терапевтической, диагностической или другой точки зрения. Такие молекулы включают, например, молекулы антисмысловых ДНК или РНК, молекулы интерферирующих РНК (РНКи), микроРНК, ложных РНК, ммРНК, ферментативные РНК, РНК, применяемые в исправляющей терапии, и РНК, имеющие свойства агонистов и антагонистов, антисмысловые олигомерные соединения, антисмысловые олигонуклеотиды, олигонуклеотиды внешней направляющей последовательности (external guide sequence, EGS), сплайс-варианты, праймеры, зонды и другие олигомерные соединения, которые гибридизуются с по меньшей мере частью нуклеиновой кислоты-мишени. В связи с этим данные соединения могут быть введены в форме одноцепочечных, двухцепочечных, частично одноцепочечных или кольцевых олигомерных соединений.
[0031] В контексте настоящего изобретения термин ʺолигонуклеотидʺ относится к олигомеру или полимеру рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или их миметикам. Термин ʺолигонуклеотидʺ также включает линейные или кольцевые олигомеры природных и/или модифицированных мономеров или связей, включая дезоксирибонуклеозиды, рибонуклеозиды, их замещенные и альфа-аномерные формы, пептидо-нуклеиновые кислоты (ПНК), закрытые нуклеиновые кислоты (ЗНК; locked nucleic acids, LNA), фосфотиоатные, метилфосфонатные производные и т.п. Олигонуклеотиды способны к специфичному связыванию с полинуклеотидом-мишенью за счет регулярных взаимодействий между мономерными звеньями, такими как Уотсон-Криковский тип спаривания оснований, Хугстиновский или обратный Хугстиновский типы спаривания оснований и т.п.
[0032] Олигонуклеотид может быть ʺхимернымʺ, то есть составленным из разных областей. В контексте настоящего изобретения ʺхимерныеʺ соединения представляют собой олигонуклеотиды, которые содержат две или более химически отличные области, например, область (области) ДНК, область (области) РНК, область (области) ПНК и т.д. Каждая химически отличная область состоит из по меньшей мере одной мономерной единицы, т.е. нуклеотида в случае олигонуклеотидного соединения. Эти олигонуклеотиды, как правило, содержат по меньшей мере одну область, в которой олигонуклеотид модифицирован с целью проявления одного или более желаемых свойств. Желаемые свойства олигонуклеотида включают, но без ограничения, например, повышенную устойчивость к деградации нуклеазами, повышенное клеточное поглощение и/или повышенную способность к связыванию с нуклеиновой кислотой-мишенью. Разные области олигонуклеотида могут, таким образом, обладать разными свойствами. Химерные олигонуклеотиды согласно настоящему изобретению могут быть получены в виде смешанных структур из двух или более олигонуклеотидов, модифицированных олигонуклеотидов, олигонуклеозидов и/или аналогов олигонуклеотидов, описанных выше.
[0033] Олигонуклеотид может быть составлен из областей, которые могут быть соединены в ʺрядʺ, то есть когда мономеры соединены последовательно, как в нативной ДНК, или соединены посредством спейсеров. Спейсеры формируют ковалентный ʺмостикʺ между областями и имеют в предпочтительных случаях длину, не превышающую примерно 100 углеродных атомов. Спейсеры могут иметь разные функциональные характеристики, например, нести положительный или отрицательный заряд, обладать свойствами специфичного связывания нуклеиновых кислот (интеркаляторы, вещества, связывающиеся с бороздками, токсины, флуорофоры и т.д.), быть липофильными, индуцировать образование специфических вторичных структур, как, например, аланинсодержащие пептиды, которые индуцируют образование альфа-спиралей.
[0034] В настоящей заявке термины ʺген NEU4ʺ и ʺсиалидаза 4ʺ включают все члены семейства, мутанты, аллели, фрагменты, виды, кодирующие и некодирующие последовательности, смысловые и антисмысловые полинуклеотидные цепи и т.д.
[0035] В настоящей заявке слова LP5125, MGC102757, MGC18222, N-ацетил-альфа-нейраминидаза 4 и сиалидаза 4 рассматривают как имеющие одно и то же значение в литературе и применяют взаимозаменяемо в настоящей заявке.
[0036] В настоящей заявке термин ʺолигонуклеотид, специфичный кʺ или ʺолигонуклеотид, нацеленный наʺ относится к олигонуклеотиду, содержащему последовательность, (i) способную образовывать стабильный комплекс с частью гена-мишени или (ii) способную образовывать стабильный дуплекс с частью мРНК-транскрипта гена-мишени. Стабильность комплексов и дуплексов может быть определена посредством теоретических расчетов и/или анализов in vitro. Типовые анализы для определения стабильности гибридизационных комплексов и дуплексов описаны в Примерах ниже.
[0037] В настоящей заявке термин ʺнуклеиновая кислота-мишеньʺ охватывает ДНК, РНК (содержащую пре-мРНК и мРНК), транскрибируемую с такой ДНК, и также кДНК, получаемую на матрице такой РНК, кодирующие, некодирующие последовательности, смысловые или антисмысловые полинуклеотиды. Специфичная гибридизация олигомерного соединения с его нуклеиновой кислотой-мишенью препятствует нормальной функции нуклеиновой кислоты. Это модулирование функции нуклеиновой кислоты-мишени с помощью соединений, которые специфично гибридизуются с последней, в общем случае называют ʺантисенс-технологиейʺ. Затрагиваемые функции ДНК включают, например, репликацию и транскрипцию. Затрагиваемые функции РНК включают все жизненно важные функции, такие как, например, транслокация РНК к месту трансляции белков, трансляция белков на матрице РНК, сплайсинг РНК с образованием одного или более видов мРНК и каталитическая активность, которая может присутствовать у РНК или которой РНК может способствовать. Суммарный эффект такого препятствия функции нуклеиновой кислоты-мишени заключается в модулировании экспрессии кодируемого продукта или олигонуклеотидов.
[0038] РНК-интерференция ʺРНКиʺ опосредована молекулами двухцепочечной РНК (дцРНК), которые имеют последовательности, гомологичные их нуклеотидным последовательностям-ʺмишенямʺ. В некоторых вариантах реализации настоящего изобретения посредники представляют собой дуплексы ʺмалых интерферирующихʺ РНК (ммРНК) длиной 5-25 нуклеотидов. ммРНК образуются в результате разрезания дцРНК ферментом-РНКазой, известным как Дайсер (Dicer). Дуплексные продукты ммРНК включаются в состав мультибелкового комплекса, называемого RISC (индуцируемый РНК комплекс сайленсинга). Без привязки к какой-либо конкретной теории, комплекс RISC, как полагают, нацелен на нуклеиновую кислоту-мишень (на роль которой подходит мРНК), при этом дуплекс ммРНК взаимодействует с мРНК за счет комплементарности их последовательностей, вызывая расщепление мРНК каталитическим путем. Малые интерферирующие РНК, которые могут быть применены согласно настоящему изобретению, могут быть синтезированы и применены в соответствии со способами, которые хорошо известны в данной области техники и которые будут хорошо знакомы специалисту в данной области техники. Малые интерферирующие РНК для применения в соответствии со способами согласно настоящему изобретению подходящим образом содержат от примерно 1 до примерно 50 нуклеотидов (нт). В примерах неограничивающих вариантов реализации ммРНК могут содержать от примерно 5 до примерно 40 нт, от примерно 5 до примерно 30 нт, от примерно 10 до примерно 30 нт, от примерно 15 до примерно 25 нт или примерно 20-25 нуклеотидов.
[0039] Отбор подходящих олигонуклеотидов упрощается при применении компьютерных программ, которые автоматически выравнивают нуклеотидные последовательности и отмечают идентичные или гомологичные области. Такие программы применяют для сравнения нуклеотидных последовательностей, полученных, например, в результате поиска в базах данных, таких как GenBank, или посредством секвенирования ПЦР-продуктов. Сравнение нуклеотидных последовательностей из организмов ряда видов позволяет отобрать нуклеотидные последовательности, которые обнаруживают подходящую степень идентичности между видами. В случае генов, которые не были просеквенированы, проводят блотгинги по Саузерну с целью определения степени идентичности между генами вида-мишени и других видов. Путем проведения блоттингов по Саузерну при различных степенях строгости условий гибридизации, как хорошо известно в данной области техники, можно получить приблизительную меру идентичности. Эти процедуры позволяют осуществить отбор олигонуклеотидов, которые показывают высокую степень комплементарности нуклеотидным последовательностям-мишеням субъекта, подлежащего контролю, и меньшую степень комплементарности соответствующим нуклеотидным последовательностям других видов. Специалист в данной области техники обнаружит, что существует значительная свобода выбора подходящих областей генов для применения согласно настоящему изобретению.
[0040] С помощью термина ʺферментативная РНКʺ обозначают молекулу РНК, обладающую ферментативной активностью (Cech, (1988) J. American. Med. Assoc. 260, 3030-3035). Ферментативные нуклеиновые кислоты (рибозимы) действуют за счет, во-первых, связывания с РНК-мишенью. Такое связывание происходит через участок ферментативной нуклеиновой кислоты, связывающий РНК-мишень, который находится в непосредственной близости к ферментативному участку молекулы, катализирующему расщепление РНК-мишени. Таким образом, ферментативная нуклеиновая кислота сперва распознает и далее связывает РНК-мишень за счет спаривания оснований и, как только происходит связывание с нужным сайтом, проявляет ферментативную активность, разрезая РНК-мишень.
[0041] С помощью термина ʺложная РНКʺ обозначают молекулу РНК, которая имитирует природный связывающий домен для лиганда. Ложная РНК, таким образом, конкурирует с природной связывающей мишенью за связывание конкретного лиганда. Например, было показано, что сверхэкспрессия РНК-элемента трансактивационного ответа (TAR) ВИЧ может действовать как ʺложнаяʺ и эффективно связывает белок tat (транскрипционный трансактиватор) ВИЧ, таким образом препятствуя связыванию этого белка с последовательностями TAR, кодируемыми РНК ВИЧ. Подразумевают, что приведенная информация представляет собой конкретный пример. Специалисты в данной области техники обнаружат, что это всего лишь один пример, и другие варианты реализации могут быть легко разработаны с применением методик, общеизвестных в данной области техники.
[0042] В настоящей заявке термин ʺмономерыʺ, как правило, обозначает мономеры, соединенные посредством фосфодиэфирных связей или их аналогов с образованием олигонуклеотидов, размеры которых изменяются в пределах от нескольких мономерных единиц, например, от примерно 3-4, до примерно нескольких сотен мономерных единиц. Аналоги фосфодиэфирных связей включают: фосфотиоатные, фосфодитиоатные, метилфосфонатные, фосфоселеноатные, фосфорамидатные связи и т.п., как более подробно описано ниже.
[0043] Термин ʺнуклеотидʺ распространяется на встречающиеся в природе нуклеотиды, а также не встречающиеся в природе нуклеотиды. Специалисту в данной области техники должно быть ясно, что различные нуклеотиды, которые ранее считали ʺне встречающимися в природеʺ, были впоследствии найдены в природе. Таким образом, термин ʺнуклеотидыʺ включает не только известные молекулы, содержащие пуриновые и пиримидиновые гетероциклы, но также и их гетероциклические аналоги и таутомеры. Иллюстративные примеры других типов нуклеотидов представляют собой молекулы, содержащие аденин, гуанин, тимин, цитозин, урацил, пурин, ксантин, диаминопурин, 8-оксо-N6-метиладенин, 7-деазаксантин, 7-деазагуанин, N4,N4-этаноцитозин, N6,N6-этано-2,6-диаминопурин, 5-метилцитозин, 5-(C3-C6)-алкинилцитозин, 5-фторурацил, 5-бромурацил, псевдоизоцитозин, 2-гидрокси-5-метил-4-триазолпиридин, изоцитозин, изогуанин, инозин и ʺне встречающиеся в природеʺ нуклеотиды, описанные в публикации Benner et al, Патент США №5432272. Термин ʺнуклеотидʺ распространяется на каждый и все из этих примеров, а также их аналоги и таутомеры. Особенно интересными нуклеотидами являются те из них, которые содержат аденин, гуанин, тимин, цитозин и урацил, которые рассматривают как встречающиеся в природе нуклеотиды, относительно терапевтического и диагностического применения у людей. Нуклеотиды содержат природные 2'-дезокси- и 2'-гидроксисахара, например, описанные в Romberg and Baker, DNA Replication, 2 nd Ed. (Freeman, San Francisco, 1992), a также их аналоги.
[0044] Термин ʺаналогиʺ в применении к нуклеотид ам включает синтетические нуклеотиды, содержащие модифицированные основания и/или модифицированные сахара (см., например, аналоги, описанные, в основном, в Scheit, Nucleotide Analogs, John Wiley, New York, 1980; Freier & Altmann, (1997) Nucl. Acid. Res., 25 (22), 4429-4443, Toulme, J.J., (2001) Nature Biotechnology 19: 17-18; Manoharan M., (1999) Biochemica et Biophysica Acta 1489: 117-139; Freier S.M, (1997) Nucleic Acid Research, 25: 4429-4443, Uhlman, E., (2000) Drug Discovery & Development, 3: 203-213, Herdewin R, (2000) Antisense & Nucleic Acid Drug Dev., 10: 297-310); 2'-O, 3'-C-соединенные [3.2.0]бициклоарабинонуклеозиды. Такие аналоги включают синтетические нуклеотиды, направленные на усиление связывающих свойств, например, стабильности дуплексов или триплексов, специфичности и т.п.
[0045] В настоящей заявке термин ʺгибридизацияʺ обозначает спаривание практически комплементарных цепей олигомерных соединений. Один механизм спаривания задействует образование водородных связей, которые могут представлять собой Уотсон-Криковские, Хугстиновские или обратные Хугстиновские водородные связи между комплементарными основаниями нуклеозидов или нуклеотидов (нуклеотидами) цепей олигомерных соединений. Например, аденин и тимин являются комплементарными нуклеотидами, которые спариваются за счет образования водородных связей. Гибридизация может происходить при различных условиях.
[0046] Антисмысловое соединение является ʺспособным к специфичной гибридизацииʺ, если связывание указанного соединения с нуклеиновой кислотой-мишенью нарушает нормальное функционирование нуклеиновой кислоты-мишени, приводя к модулированию функции и/или активности, и степень комплементарности достаточна, чтобы избежать неспецифичного связывания указанного антисмыслового соединения с нуклеотидными последовательностями, не являющимися мишенями, в условиях, при которых необходимо специфичное связывание, т.е. в физиологических условиях в случае in vivo методик анализа или терапевтического воздействия и в условиях, при которых проводится анализ, в случае исследований in vitro.
[0047] В настоящей заявке фраза ʺстрогие условия гибридизацииʺ или ʺстрогие условияʺ относится к условиям, при которых соединение согласно изобретению будет гибридизоваться со своей последовательностью-мишенью, но с минимальным количеством других последовательностей. Строгие условия зависят от последовательности и будут различаться в разных обстоятельствах, и, в контексте настоящего изобретения, ʺстрогие условияʺ, при которых олигомерные соединения гибридизуются с последовательностью-мишенью, определяются природой и составом олигомерных соединений и видами анализов, посредством которых их исследуют. В общем случае, строгие условия гибридизации включают низкие концентрации (<0,15М) солей, содержащих неорганические катионы, такие как Na+ или К+ (т.е. низкую ионную силу), температуру выше точки, расположенной на 20°C-25°C ниже Тпл комплекса олигомерное соединение: последовательность-мишень, и присутствие денатурантов, таких как формамид, диметилформамид, диметилсульфоксид или детергент додецилсульфат натрия (ДСН). Например, скорость гибридизации снижается на 1,1% на каждый добавленный 1% формамида. Примером условий гибридизации с высокой степенью строгости является гибридизация с применением 0,1Х буфера хлорид натрия-цитрат натрия (SSC, стандартный цитратно-солевой)/0,1% (масс/об.) ДСН при 60°С в течение 30 минут.
[0048] В настоящей заявке термин ʺкомплементарныйʺ относится к способности точного спаривания между двумя нуклеотидами или одной или двумя олигомерными цепями. Например, если нуклеиновое основание в определенном положении цепи антисмыслового соединения способно к образованию водородных связей с нуклеиновым основанием в определенном положении цепи нуклеиновой кислоты-мишени, причем, указанная нуклеиновая кислота-мишень представляет собой молекулу ДНК, РНК или олигонуклеотида, то положение, в котором происходит образование водородных связей между олигонуклеотидом и нуклеиновой кислотой-мишенью, считают комплементарным положением. Олигомерное соединение и дополнительная молекула ДНК, РНК или олигонуклеотида комплементарны друг другу, когда достаточное число комплементарных положений в каждой молекуле заняты нуклеотидами, способными образовывать водородные связи друг с другом. Таким образом, термины ʺспецифично гибридизующийсяʺ и ʺкомплементарныйʺ применяют для обозначения достаточной степени точного спаривания, или комплементарности, в пределах достаточного числа нуклеотидов, так что между олигомерным соединением и нуклеиновой кислотой-мишенью происходит стабильное и специфичное связывание.
[0049] Как понимают специалисты в данной области техники, последовательность олигомерного соединения не обязательно должна быть на 100% комплементарна последовательности его нуклеиновой кислоты-мишени для того, чтобы соединение было способно к специфичной гибридизации. Кроме того, олигонуклеотид может гибридизоваться поверх одного или более сегментов, так что промежуточные или соседние сегменты оказываются не вовлеченными в процесс гибридизации (например, петлевая структура, отсутствие комплементарности или шпилечная структура). Олигомерные соединения согласно настоящему изобретению содержат последовательность, комплементарную на по меньшей мере примерно 70%, или по меньшей мере примерно 75%, или по меньшей мере примерно 80%, или по меньшей мере примерно 85%, или по меньшей мере примерно 90%, или по меньшей мере примерно 95%, или по меньшей мере примерно 99% области-мишени в пределах нуклеотидной последовательности-мишени, на которую эти соединения нацелены. Например, антисмысловое соединение, в котором 18 из 20 нуклеотидов антисмыслового соединения комплементарны области-мишени и, следовательно, специфично гибридизовались бы с ним, характеризовалось бы 90% комплементарностью. В данном примере остальные некомплементарные нуклеотиды могут располагаться в кластерах комплементарных нуклеотидов или чередоваться с комплементарными нуклеотидами и не обязательно должны примыкать друг к другу или к комплементарным нуклеотидам. По этой причине антисмысловое соединение длиной 18 нуклеотидов, содержащее 4 (четыре) некомплементарных нуклеотида, которые фланкированы двумя областями, полностью комплементарными нуклеиновой кислоте-мишени, в целом характеризовалось бы 77,8% комплементарностью с нуклеиновой кислотой-мишенью и попадало бы, таким образом, в рамки настоящего изобретения. Процент комплементарности антисмыслового соединения с областью нуклеиновой кислоты-мишени может быть определен обычным способом с применением программ BLAST (средства поиска основного локального выравнивания) и программ PowerBLAST, известных в данной области техники. Процент гомологии, идентичности последовательностей или комплементарности может быть определен с помощью, например, программы Gap (Wisconsin Sequence Analysis Package, Version 8 for Unix, Genetics Computer Group, University Research Park, Madison Wis.) с применением параметров, установленных по умолчанию, которая использует алгоритм Смита-Ватермана (Adv. Appl. MtfA., (1981) 2, 482-489).
[0050] В настоящей заявке термин ʺтемпература плавления (Тпл)ʺ относится к температуре, в условиях определенной ионной силы, pH и концентрации нуклеиновой кислоты, при которой 50% олигонуклеотидов, комплементарных последовательности-мишени, гибридизуются с последовательностью-мишенью в состоянии равновесия. Как правило, строгие условия гибридизации будут отличаться тем, что концентрация соли составляет по меньшей мере примерно от 0,01 до 1,0 М концентрации ионов Na (или других солей) при pH, равном 7,0-8,3, и температура равна по меньшей мере примерно 30°C для коротких олигонуклеотидов (например, длиной от 10 до 50 нуклеотидов). Строгие условия могут также быть достигнуты путем добавления дестабилизирующих агентов, таких как формамид.
[0051] В настоящей заявке термин ʺмодулированиеʺ обозначает либо увеличение (стимулирование), либо ослабление (ингибирование) экспрессии гена.
[0052] Термин ʺвариантʺ, применительно к последовательности полинуклеотида, может охватывать последовательность полинуклеотида, относящегося к гену дикого типа. Это определение может также включать, например, ʺаллельныеʺ, ʺсплайс-ʺ, ʺвидовыеʺ или ʺполиморфныеʺ варианты. Сплайс-вариант может быть в значительной степени идентичным исходной молекуле, но будет в общем случае содержать большее или мень