Способ получения сульфидированного лигнина и его использование в качестве сорбента для соединений тяжелых металлов
Иллюстрации
Показать всеИзобретение относится к области промышленной экологии и касается вопроса утилизации отхода лесохимии – лигнина - и использования материала, полученного на его основе, в качестве сорбента для очистки сточных вод от соединений тяжелых металлов. Лигнин предварительно подвергают хлорированию хлорной водой. Полученный хлорлигнин, содержащий не более 14,1% хлора, вводят во взаимодействие с полисульфидом щелочного металла, который получен в водном растворе гидразингидрата. Осуществляют процесс поликонденсации при температуре 40°С и мольном соотношении хлора к сере=1:1. Полученный продукт имеет величину сорбции для никеля до 360 мг/г, для цинка до 423 мг/г, для кадмия до 462 мг/г, для ртути до 467 мг/г, для меди 411 мг/г, для кобальта до 323 мг/г, для свинца до 376 мг/г. 2 н.п. ф-лы, 3 пр.
Реферат
Изобретение относится к области промышленной экологии и конкретно касается вопроса утилизации многотоннажного отхода лесохимии – лигнина - и получения на его основе сорбента для очистки сточных вод от соединений токсичных тяжелых металлов.
На лесохимических предприятиях (целлюлозно-бумажных и гидролизных) основную часть отходов составляет лигнин - разветвленный природный полимер нерегулярного строения, утилизация которого является важной экологической проблемой [1, 2]. Одно из основных направлений переработки лигнинов заключается в реализации их сорбционных свойств - их использование для производства сорбентов. Высокоэффективные сорбенты - активные угли могут быть получены путем карбонизации непосредственно лигнина или продуктов его незначительной переработки [2]. Однако карбонизация является высокоэнергозатратным процессом. Кроме того, из-за существенного газовыделения при карбонизации выход активированного угля обычно не высок. Известен способ получения сорбента с использованием непосредственно лигнина, в присутствии которого осуществляют поликонденсацию 1,2,3-трихлорпропана с полисульфидом натрия и тиомочевинной при температуре 60°С [3]. Частицы лигнина в этом процессе выступают, по-видимому, в роли центров поликонденсации и обеспечивают нужную дисперсность получаемого сорбента. Серосодержащий сорбент для очистки сточных вод от соединений тяжелых металлов получен реакцией полисульфида натрия, хлорорганических отходов и хлорированного лигнина в водном растворе гидразина [4]. Процесс поликонденсации проводят при температуре 40-45°С. Однако хлорлигнин для получения сорбента составляет только ~50% от массы используемых мономеров для поликонденсации. Остальные 50% представляют собой отходы производства эпихлоргидрина. С одной стороны, это позволяет утилизировать хлорорганические отходы, однако, с другой стороны, состав отходов может варьировать в очень широких пределах [5], вследствие чего трудно обеспечить необходимое соотношение полисульфида натрия и хлорсодержащих мономеров.
Одним из возможных путей переработки хлорированного лигнина является получение из него серосодержащего (сульфидированного) лигнина [6] (прототип)1 (1 Термин «серосодержащий лигнин» правильнее заменить на «сульфидированный лигнин», т.к. к серосодержащему лигнину могут быть отнесены лигносульфонаты и некоторые другие производные лигнина. А введение серы с использованием полисульфидов щелочных металлов или аммония способствует введению именно полисульфидных фрагментов, и такой лигнин лучше называть «сульфидированным».), который представляет собой твердый продукт, рекомендованный ранее для использования в качестве противозадирной присадки в смазочных композициях для тяжелонагруженных узлов трения [7]. В методе-прототипе лигнин, хлорированный электрохимическим методом, обрабатывают серосодержащим соединением (полисульфиды щелочных, щелочноземельных металлов или аммония) в водной среде при комнатной температуре (диапазон температуры 15-40°С) в течение 3-30 мин. Хлорирование гидролизного лигнина в среде соляной кислоты в бездиафрагменном электролизе с графитовыми электродами (плотность тока 10 А/дм2; концентрация HCl 20%, содержание лигнина 150 г/л) дает продукт, с максимальным содержанием хлора 30%, однако только 15-17% хлора является реакционноспособным и замещается на серу. В зависимости от используемого полисульфида и соотношения реагентов содержание серы в полученном полисульфиде составляет 21-30%, а содержание остаточного хлора 13,5-16,7%. Наличие сорбционных свойств для полученного продукта не отмечено. Кроме того, в способе-прототипе использован хлорлигнин с высоким (30%) содержанием хлора. Возможно это обусловлено тем, что при электрохимическом хлорировании хлор прежде всего встает в ароматическое ядро [8]. Как известно [9], нуклеофильное замещение неактивированного хлора в ароматическом кольце происходит с большим трудом. Поэтому малые количества хлора в хлорлигнине авторами [6] не использованы.
Целью предлагаемого технического решения является получения сульфидированного лигнина с существенно меньшим содержанием остаточного хлора, что обеспечивает возможность его использования в качестве сорбента для очистки сточных вод от соединений тяжелых металлов.
Поставленная цель достигается использованием для получения сульфидированного лигнина хлорлигнина, который был получен хлорированием лигнина газообразным хлором в водной среде (хлорной водой). Очевидно, в этих условиях хлор прежде всего вступает в боковые цепи макромолекулы лигнина и только в избытке хлорирующего реагента происходит хлорирование ароматических колец [9].
Для осуществления сульфидирования использован полисульфид щелочного металла (натрия или калия), получаемый из элементной серы в водном растворе в присутствии гидразингидрата и щелочи (NaOH или KOH) [10]:
4S+4МОН+N2H4*H2O→2M2S2+5H2O+N2
М=Na, K.
Дисульфиды натрия или калия образуются при мольном соотношении S:MOH=1:1. Полученный раствор без выделения дисульфидов в свободном соотношении использован в дальнейшей реакции с хлорлигнином. Для получения сульфидированного лигнина был использован хлорлигнин с содержанием хлора 2,6; 5,7; 7,1 и 14,1%. Количество дисульфида щелочного металла для осуществления синтеза берется исходя из соотношения M2S2:Cl=1:2, то есть на два атома хлора берется 1 моль M2S2. Таким образом, в предлагаемом методе использованы стехиометрические соотношения S:Cl. Процесс осуществляется в воде, в которую в соотношении 1:20 (гидразингидрат : вода) по массе вводится гидразингидрат. Растворение серы осуществляют при температуре 60-65°С в течение 2 часов, а реакцию с хлорлигнином проводят при температуре 40°С в течение 2,5 часов.
Несмотря не то что процесс сульфидирования протекает с участием твердой фазы (хлорлигнина) степень замещения хлора очень высокая. Возможно это может быть обусловлено тем, что известно использование раствора серы в щелочном гидразингидрате в качестве композиции для получения целлюлозы [11], т.е. система щелочь-гидразингидрат-сера способна расщеплять макромолекулы лигнина. Варку целлюлозы осуществляют при максимальной температуре 170°С. Предлагаемые нами условия сульфидирования гораздо мягче, тем не менее частично может идти расщепление молекул лигнина. Дальнейшее участие атомов хлора в поликонденсации приводит к обратной сшивке осколков.
В результате поликонденсации получен порошок коричневого цвета, который был исследован на способность адсорбировать тяжелые металлы (Ni, Cd, Pb, Hg, Cu, Co, Zn) из водных растворов.
Способ получения сульфидированного лигнина и его использование в качестве сорбента для извлечения соединений тяжелых металлов из водных растворов иллюстрируется следующими примерами.
Пример 1. В смеси 20 мл воды и 1 г гидразингидрата растворяют 0,42 г (0,00732 моль) KOH. В полученный раствор вводят 0,23 г (0,00732 моль) порошкообразной серы. Смесь перемешивают 2 часа при температуре 60-65°С, температуру снижают до 40°С и при перемешивании вводят 10 г хлорлигнина (содержание хлора 2,6%). Перемешивание продолжают 2,5 часа. Продукт отфильтровывают, промывают водой и сушат, выход 9,1 г (91%). Коричневый порошок, содержание серы 2,42%, Cl - отсутствует.
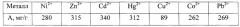
Сорбционное извлечение металлов из водных растворов осуществлено путем встряхивания навески сухого сорбента (0,5 г) с 50 мл водного раствора соли металла, концентрация 5 г/л (проводилось исследование максимально возможной эффективности сорбентов). Величину сорбции рассчитывали, как указано в работе [4], конечную концентрацию металлов в растворе определяли фотоколориметрически. В таблице представлены данные по величине сорбции.
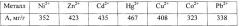
Пример 2. В условиях примера 1, но при растворении 0,64 г (0,0161 моль) NaOH, введении в раствор 0, 51 г (0,0161 моль) серы и использовании 10 г хлорлигнина, содержащего 5,7% хлора. Получено 9,3 г (93%) продукта, содержащего 5,48% серы и следовые количество хлора. Данные по величине сорбции ионов металлов представлены в таблице.
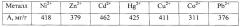
Пример 3. В условиях примера 1, но при растворении 1,14 г (0,02 моля) КОН, введении в раствор 0,64 г (0,02 моля) серы и использовании 10 г хлорлигнина, содержащего 7,1% хлора. Получено 9,2 г (92%) продукта, содержащего 7,0% серы и ~ 0,5% остаточного хлора. Данные по величине сорбции:
Пример 4. В условиях примера 1, но при растворении 1,6 г (0,04 моля) NaOH, введении в раствор 1,28 г (0,04 моля) серы и использовании 10 г хлорлигнина, содержащего 14,1% хлора, получено 9,3 г (93%) продукта, содержащего 12,5% серы и 2,3% остаточного хлора. Сорбционная активность (мг/г): Ni - 360; Zn - 290; Cd - 418; Hg2+ - 437.
Таким образом, в данном техническом решении предлагается способ получения сульфидированного лигнина, содержащего до 12,5% серы. Продукт может быть использован в качестве сорбента для извлечения соединений тяжелых металлов из сточных вод металлоперерабатывающих предприятий.
Литература
1. Чудаков М.И. Промышленное использование лигнина, 1983, 212 с.
2. Хитрин К.С, Фукс С.Л., Хитрин С.В., Казненко С.А., Метелева Д.С. Направление и методы утилизации лигнинов. Российский химический журнал. 2011, т. 55, №1, с. 38-44.
3. Малькина А.Г., Соколянская Л.В., Цыханский В.Д., Татаринова А.А., Гусаров А.В., Хамтаев В.А., Фомина Е.Ю. Новые высокоэффективные сорбенты на основе лигнина. Химия в интересах устойчивого развития, 1996, т. 4, №3, с. 307-311.
4. Патент №2558896 RU.
5. Силинская Я.Н., Томин В.П., Катульский Ю.Н., Корчевий Н.А. Анализ хлорорганических производств ОАО «Усольехимпром». Сборник научных трудов Ангарской государственной технической академии «Наука, технология, образование», Ангарск, 2000, часть 2, с. 89-93.
6. Авт.свид. СССР №933669 (1982) (прототип).
7. Патент №2552997 RU.
8. Химическая энциклопедия. Т. 2. Изд. «Советская энциклопедия». М, 1990, 591 с.
9. Патент №2439138 RU (2009).
10. Корчевий Н.А., Турчанинова Л.П., Дерягина Э.Н., Воронков М.Г. // Журнал общей химии. 1989. Т. 59, вып. 8. С. 1785-1787.
11. Патент №2104353 RU (1998).
1. Способ получения сульфидированного лигнина, включающий взаимодействие лигнина с хлорной водой с получением хлорированного лигнина, содержащего не более 14,1% хлора в хлорлигнине, получение раствора полисульфида щелочного металла путем взаимодействия при перемешивании серы и щелочи в водном растворе гидразингидрата при массовом соотношении гидразингидрата к воде, равном 1:20, мольном соотношении серы к щелочи, равном 1:1, и температуре 60-65°С, введение упомянутого хлорированного лигнина в полученный раствор полисульфида щелочного металла из расчета мольного соотношения хлора к сере, равного 1:1, проведение реакции поликонденсации при 40°С, фильтрование, промывку и сушку целевого продукта.
2. Использование сульфидированного лигнина, полученного по п. 1, в качестве сорбента для извлечения соединений тяжелых металлов из водных растворов.