Никелевый катализатор гидрирования аренов
Иллюстрации
Показать всеИзобретение относится к области каталитической химии, а именно разработке никелевого катализатора гидрирования аренов в наноразмерных системах, которое может быть использовано в химической промышленности, в частности при производстве циклогексана, циклогексанола, циклогесиламина и других продуктов гидрирования. Изобретение относится к катализатору гидрирования, содержащему соединение никеля(II) и восстановитель, при этом в качестве исходного соединения никеля(II) используют безводный бис(ацетилацетонат)никеля(II), а в качестве восстановителя - диэтилэтоксиалюминий (AlEt2(OEt)) при следующем мольном соотношении компонентов: [Ni(acac)2]:[AlEt2(OEt)]=1:(2÷10). Технический результат заключается в разработке никелевого катализатора, обладающего высокой каталитической активностью. 7 табл., 36 пр.
Реферат
Предлагаемое изобретение относится к области каталитической химии, а именно разработке никелевого катализатора гидрирования аренов в наноразмерных системах, которое может быть использовано в химической промышленности, в частности при производстве циклогексана, циклогексанола, циклогесиламина и других продуктов гидрирования.
Было установлено, что около 25% всех химических процессов приходится на долю стадий каталитического гидрирования или это составляет приблизительно 8% от всего мирового внутреннего валового продукта [, D. Albani, N. Almora-Barrios, N. , J. , ChemCatChem 8 (2015) 21-33]. Поскольку гидрирование - это наиболее часто используемая прикладная реакция получения химических веществ, то она же и самая широко исследуемая реакция в катализе. Но несмотря на многочисленные исследования до настоящего времени не удалось найти способ получения катализаторов, которые бы отличались простотой в приготовлении, высокой производительностью и стабильностью в условиях гидрирования аренов. Большинство известных на данный момент катализаторов гидрирования аренов - это гетерогенные системы, отличающиеся довольно жесткими условиями проведения процесса, небольшой производительностью и применением сложных и дорогостоящих технологических установок, позволяющих осуществлять всесторонний контроль над процессом гидрирования.
Известен катализатор гидрирования бензола до циклогексана [Robert М. Suggitt, 3,796,764, 1972], протекающего в две стадии. На первой стадии в качестве катализатора используются металлы группы железа, чаще никель, нанесенные на оксиды алюминия, кремния, магния, циркония, чаще алюминия. Никель может присутствовать в количестве 30-45 вес.%. На второй стадии в качестве катализатора используются благородные металлы, такие как платина, на алюминиевой подложке (предпочтительнее на γ-Al подложке), в количестве 0,01-2 вес.% Pt, Р=23-54 атм, Т=280-370°C. Кроме того, для достижения максимальной конверсии по бензолу в систему добавляют щелочной металл или его оксид в количестве 0,1-2 вес.%. Авторы отмечают, что добавление бензола ко второй реакционной зоне (с платиной) должно контролироваться таким образом, чтобы температура этой зоны не превышала 344°C.
К недостаткам катализатора такого типа можно отнести технически сложно осуществляемый контроль над потоком бензола в реакторе, высокую цену, обусловленную использованием благородных металлов, в частности платины. Кроме того, следует учитывать и сложную конструкцию реактора с последовательно расположенными реакционными зонами, а многокомпонентный состав сразу двух используемых катализаторов требует многостадийности процесса, что значительно усложняет процесс приготовления всей каталитической системы в целом.
Известен катализатор селективного неполного гидрирования ароматических соединений [Gerhard P. Nowack, 3912787, 1974] на основе водной дисперсии твердого рутениевого катализатора, модифицированного некоторыми количествами переходного металла (М), в условиях нейтральной или кислой среды. Рутений может быть использован в виде порошка, коллоидной дисперсии или нанесен на подложку. В качестве переходного металла предпочтительнее использовать Cr, Mo, W, Mn, Fe, Со и Ni в количестве M/Ru=0.1-1 (моль М)/(моль Ru) (М=Cr, Mo, W, Mn, Fe, Со или Ni). Температура проведения гидрирования должна колебаться в пределах 148-204°C, давление - 6-136 атм.
Недостатком такого катализатора являются высокая стоимость рутения и низкая селективность по циклогексану (не превышает 40%), а многокомпонентный состав увеличивает количество стадий процесса приготовления каталитической системы.
Известен способ получения циклогексана в ходе жидкофазного гидрирования бензола. В качестве катализатора используется система, состоящая из двух компонентов, первый компонент - это элемент(ы) VIII группы периодической таблицы (например, сочетание 60-85 мол.% Ni, 14-37 мол.% Cu и 1-6 мол.% Cr), второй - другой элемент VIII группы, обладающий более высокими каталитическими свойствами, нанесенный на оксид алюминия, кремния или титана (преимущественно 10-80 вес.% Ni, нанесенного на алюминиевую подложку), при Т=40-300°C и таком давлении, чтобы при выбранной температуре бензол оставался жидкостью (преимущественно 34-272 атм).
Недостатком данной каталитической системы являются высокие требования к качеству используемого водорода (рекомендуется криогенная методика дополнительной очистки) и относительно жесткие условия проведения гидрирования (высокое давление и температура). Кроме того, катализатор представляет собой сложную двухкомпонентную систему, каждый компонент которой, в свою очередь, отличается сложным составом и многостадийностью процесса приготовления.
С другой стороны, известны примеры микрогетерогенных или наноразмерных катализаторов гидрирования аренов. Такие катализаторы характеризуются высокой активность и/или производительностью, которые достигаются в относительно мягких условиях. С другой стороны, наноразмерные катализаторы отличаются очень низкой воспроизводимостью результатов и часто сложны в приготовлении, а также содержат в своем составе благородные металлы, что значительно влияет на их стоимость.
Известен высокоэффективный наногетерогенный Ru катализатор [Adv. Synth. Catal. 2007, 349, 2326-2330], инкапсулированный в полимерную оболочку, Т=20°C, Р=30 атм. Активность данного катализатора в гидрировании аренов достигает 1.67-10 мин-1, в зависимости от природы стабилизатора и гидрируемого арена.
К недостаткам данной системы можно отнести многостадийность процесса получения катализатора, что значительно увеличивает стоимость готового катализатора, а также быструю дезактивацию и низкую воспроизводимость результатов в процессах гидрирования аренов.
Известен наноразмерный платиновый катализатор гидрирования толуола и бензола [Journal of Catalysis, 2012, 292, 64-72], инкапсулированный в поливинилпирролидоновые или полиамидоаминовые дендримеры и нанесенный на SBA-15 мезапористый кремний, Т=343°C, Р=1 атм. Активность такого катализатора зависит от размера частиц Pt и достигает максимума 0.084±0.017 с-1 в гидрировании бензола (при 2.4 нм диаметре частиц) и 0.128±0.026 с-1 в гидрировании толуола (диаметр частиц составляет 3.1 нм). При использовании частиц платины большего или меньшего размера наблюдается резкое снижение числа оборотов (TOF) катализатора в гидрировании обоих субстратов. Несомненно, данные факт можно отнести к недостаткам рассматриваемой каталитической системы наравне с низкой активностью, сложностью процесса приготовления и стоимостью готового катализатора.
Известен высокоэффективный наноразмерный биметаллический RuyNix/C катализатор гидрирования бензола до циклогексана [Applied Catalysis A: General, 2015, 499, 124-132], Т=60°C, Р=52 атм. Активность такого катализатора зависит от отношения Ru/Ni и достигает максимума 400 мин-1 для Ru0.56Ni0.44/C.
Существенным недостатком такого катализатора является то, что высокая каталитическая активность проявляется лишь для узкого значения отношений Ru/Ni, например, если отношение Ru/Ni выше или ниже 0.56/0.44, то каталитическая активность гидрирования бензола резко снижается. К недостаткам рассматриваемого катализатора также можно отнести сложную и многостадийную процедуру приготовления и высокую стоимость готового катализатора.
Наиболее близким к изобретению с точки зрения состава катализатора, условий формирования катализатора и целей использования катализатора (гидрирования) является высокоэффективный никелевый катализатор гидрогенизации алкенов и способ его получения, описанный в патенте [№2565673, RU от 20.10.2015 (Бюл. №29. МПК B01J 21/02; B01J 23/755; B01J 31/12; С07С 5/02)], а именно Ni(acac)2⋅xH2O - AlEt3, температура гидрирования 30°C, . Никелевый катализатор гидрирования получают восстановлением кристаллогидрата бис(ацетилацетоната) никеля (Ni(acac)2⋅xH2O, где х=0.01-3.0) триэтилалюминием (AlEt3) с использованием модифицирующей добавки кетонов (ацетилацетон асасН, ацетофенон C8H8O и ацетона СН3С(О)СН3) и эфиров (С2Н5ОС2Н5) при следующем мольном соотношении реагентов: [Ni(асас)2]/[H2O]/[AlEt3]/[модификатор]=1:0.01-3:1÷10:1÷100. Оптимальные условия формирования никелевого катализатора следующие: [Ni(асас)2]/[Н2О]/[AlEt3]=1:0.5:5. Соотношение [модификатор] : [AlEt3] зависит от природы модификатора, для наиболее эффективного промотора - ацетона оно равно 2.5 ([ацетон]/[AlEt3]=2.5). Начальная активность полученного таким способом катализатора достигает 46 мин-1 в гидрировании стирола в мягких условиях (Т=30°C, ), однако полученный катализатор не активен в гидрировании аренов в указанных условиях гидрирования. Идентичных предлагаемому изобретению и по составу катализатора, и по способу формирования катализатора, и по возможностям практического применения катализатора (гидрирование) в просмотренных источниках найдено не было.
Задачей настоящего изобретения является разработка никелевого катализатора, обладающего высокой каталитической активностью и воспроизводимостью в широком интервале отношений Al/Ni в условиях гидрирования аренов (Т=80-120°C, Р=15-20 бар).
Поставленная цель достигается тем, что для формирования высокоактивного и воспроизводимого катализатора гидрирования аренов в качестве исходного соединения никеля используется бис(ацетилацетонат)никеля(II), в качестве восстановителя - диэтилэтоксиалюминий при следующем мольном соотношении реагентов: [Ni(acac)2] : [AlEt2(OEt)]=1:(2÷10). Формирование катализатора происходит непосредственно в среде гидрируемого арена.
Поскольку в литературе не было обнаружено каких-либо данных о влиянии заявленного отличительного признака на достигаемый результат, данное техническое решение, по мнению заявителя, соответствует критерию «изобретательский уровень».
Формирование высокоэффективного никелевого катализатора гидрирования аренов заключается в следующем.
К раствору безводного Ni(асас)2 в обезвоженном арене (содержание воды по Фишеру не превышает 1 ммоль/л) при комнатной температуре в токе водорода добавляют раствор AlEt2(OEt) в гексане. При введении AlEt2(OEt) цвет раствора меняется от зеленого до темно-коричневого. Полученную реакционную смесь переносят в токе водорода в стальной автоклав, снабженный механической мешалкой, пробоотборником, манометром, термостатом и линией подачи водорода. Автоклав герметизируют, реакцию проводят при непрерывном перемешивании, Т=80-120°C и .
Условия формирования никелевого катализатора гидрирования бензола для достижения оптимальных количественных характеристик следующие: отношение [Ni(асас)2] : [AlEt2(OEt)]=1:(2÷10) (табл. 2). Производительность катализатора не оценивалась, поскольку технические возможности автоклава позволяли проводить гидрирование в течение не более трех часов.
Количественные характеристики полученного таким способом катализатора определяются следующими параметрами:
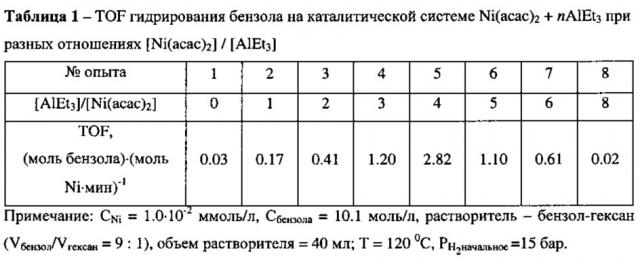
1) природой восстановителя и отношением Red/Ni (Red=AlEt3, AlEt2(OEt)) (табл. 1 и табл. 2). TOF достигает максимума при использовании в качестве восстановителя AlEt3, но высокая активность проявляется лишь в очень узком интервале отношений компонентов (Al/Ni=4, TOF=2.82 мин-1), что является существенным недостатком системы на основе Ni(асас)2 - AlEt3. Для систем на основе Ni(acac)2 - AlEt2(OEt) при Al/Ni=2÷10 активность практически остается постоянной (TOF=1.10 мин-1), то есть концентрация алюминийорганического вещества на стадии формирования катализатора практически не влияет на активность каталитической системы в указанном интервале отношений Al/Ni;
2) температурой проведения процесса (табл. 3), TOF достигает максимума при Т=120°C;
3) давлением, при котором проводится процесс (табл. 4). Оптимальное давление соответствует 15-20 бар, поскольку выше этого давления значение отношения TOF/P снижается;
4) концентрацией исходного никелевого комплекса (табл. 5). TOF достигает максимума при (0.5-1.0)⋅10-2 ммоль/л Ni(асас)2. Оптимальной, на наш взгляд, концентрацией является 1.0⋅10-2 ммоль/л, так как компоненты системы, взятые в таких количествах, менее подвержены отравляющему действию воды, которая может остаться на стенках автоклава, а также неизменно присутствует в растворителях и водороде. С другой стороны, использование более высоких концентраций (больше 1.0⋅10-2 ммоль/л) не позволяет полностью растворить исходный Ni(acac)2;
5) концентрацией гидрируемого арена. TOF достигает максимума при Cбензола ~10.1 моль/л (табл. 6).
6) природой гидрируемого арена (табл. 7).
Преимуществом описанного никелевого катализатора является высокая каталитическая активность и воспроизводимость в широком интервале отношений Al/Ni в гидрировании аренов при [Ni(асас)2] : [AlEt2(OEt)] = 1:(2÷10), Т=80-120°C и .
Пример 1: Раствор, состоящий из 0.1028 г (4⋅10-4 моль) Ni(acac)2 в 36 мл бензола и 4 мл гексана, помещают в заранее прокаленный и заполненный водородом автоклав, снабженный механической мешалкой, пробоотборником, манометром, термостатом и линией подачи водорода. Гидрирование проводят при Т=120°C и . Пробы отбирают после каждого падения давления от 15 до 10 бар. Контроль за протеканием процесса осуществляют по падению давления водорода на манометре и анализом проб методами ГЖХ (хроматограф «Хроматэк-Кристалл 5000.2» («Хроматэк», Россия), снабженный пламенно-ионизационным детектором, с применением капиллярной колонки HP Carbowax 20 М (длина 30 м, диаметр 0,53 мм), и масс-спектрометрии (масс-спектрометр GCMS-QP-2010, Shimadzu, Япония)). Гидрирование бензола характеризуется низким числом оборотов 0.03 мин-1 (табл. 1).
Пример 2-8: К раствору 0.1028 г (4⋅10-4 моль) Ni(acac)2 в 36 мл бензола, помещенному в отвакуумированный заполненный водородом сосуд Шленка, добавляют соответствующее количество AlEt3 в гексане так, чтобы отношение бензол/гексан составляло 36/4, и перемешивают реакционную смесь в течение 5 мин при комнатной температуре. Далее реакционный раствор переносят в заранее прокаленный и заполненный водородом автоклав, снабженный механической мешалкой, пробоотборником, манометром, термостатом и линией подачи водорода. Гидрирование проводят при Т=120°C и. Пробы отбирают после каждого падения давления от 15 до 10 бар. Контроль за протеканием процесса осуществляют по падению давления водорода на манометре и анализом проб методами ГЖХ (хроматограф «Хроматэк-Кристалл 5000.2» («Хроматэк», Россия), снабженный пламенно-ионизационным детектором, с применением капиллярной колонки HP Carbowax 20 М (длина 30 м, диаметр 0,53 мм), и масс-спектрометрии (масс-спектрометр GCMS-QP-2010, Shimadzu, Япония)). Гидрирование бензола характеризуется высоким числом оборотов при отношении Al/Ni=4 (табл. 1). По данным трансмиссионной электронной микроскопии (ТЭМ) средний размер частиц изменяется в интервале 1.2-2.26 нм.
Пример 9-15: К раствору 0.1028 г (4⋅10-4 моль) Ni(асас)2 в 36 мл бензола, помещенному в отвакуумированный заполненный водородом сосуд Шленка, добавляют соответствующее количество AlEt2(OEt) в гексане так, чтобы отношение бензол/гексан составляло 36/4, и перемешивают реакционную смесь в течение 5 мин при комнатной температуре. Далее реакционный раствор переносят в заранее прокаленный и заполненный водородом автоклав, снабженный механической мешалкой, пробоотборником, манометром, термостатом и линией подачи водорода. Гидрирование проводят при Т=120°C и . Пробы отбирают после каждого падения давления от 15 до 10 бар. Контроль за протеканием процесса осуществляют по падению давления водорода на манометре и анализом проб методами ГЖХ (хроматограф «Хроматэк-Кристалл 5000.2» («Хроматэк», Россия), снабженный пламенно-ионизационным детектором, с применением капиллярной колонки HP Carbowax 20М (длина 30 м, диаметр 0,53 мм), и масс-спектрометрии (масс-спектрометр GCMS-QP-2010, Shimadzu, Япония)). Гидрирование бензола характеризуется высоким числом оборотов и, кроме того, при отношении Al/Ni=2÷10 значения TOF остаются практически одинаковыми (табл. 2). По данным ТЭМ средний размер частиц изменяется в интервале 1.5-13.0 нм.
Пример 16-18: Данные примеры иллюстрируют влияние температуры на активность системы Ni(acac)2 + 5 AlEt2(OEt) в гидрировании бензола (табл. 3). Процедура проведения опытов аналогична примерам 9-15.
Пример 19-23: Данные примеры иллюстрируют влияние давления на активность системы Ni(асас)2 + 5 AlEt2(OEt) в гидрировании бензола (табл. 4). Процедура проведения опытов аналогична примерам 9-15.
Пример 24-27: Данные примеры иллюстрируют влияние концентрации исходного никелевого комплекса на активность системы Ni(асас)2 +5 AlEt2(OEt) в гидрировании бензола (табл. 5). Процедура проведения опытов аналогична примерам 9-15.
Пример 28-31: Данные примеры иллюстрируют влияние исходной концентрации арена на активность и производительность системы Ni(асас)2 +5 AlEt2(OEt) в гидрировании бензола (табл. 6). Процедура проведения опытов аналогична примерам 9-15.
Пример 32-36: Данные примеры иллюстрируют влияние природы арена на активность и производительность системы Ni(асас)2 +5 AlEt2(OEt) в гидрировании различных аренов (табл. 7). Процедура проведения опытов аналогична примерам 9-15.
Катализатор гидрирования, содержащий соединение никеля(II) и восстановитель, отличающийся тем, что в качестве исходного соединения никеля(II) используют безводный бис(ацетилацетонат)никеля(II), а в качестве восстановителя - диэтилэтоксиалюминий (AlEt2(OEt)) при следующем мольном соотношении компонентов: [Ni(acac)2]:[AlEt2(OEt)]=1:(2÷10).