Устройство для непрерывного неинвазивного измерения кровяного давления
Иллюстрации
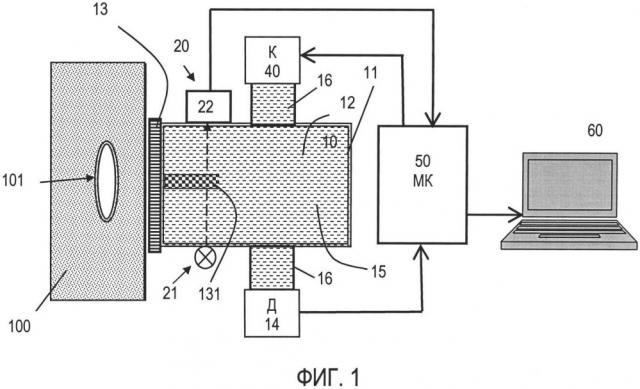
Показать всеИзобретение относится к медицинской технике. Устройство для непрерывного неинвазивного измерения кровяного давления содержит установленный в корпусе (11) аппликатор (10), выполненный в виде заполненной жидкостью (15) полости (12) с гибкой мембраной (13) для обеспечения механического контакта с тканями пациента (100) непосредственно над лучевой артерией (101) и связанный с полостью преобразователь (14) давления жидкости в электрический сигнал. Также устройство содержит средство для регулирования состояния мембраны в процессе измерения на основе контура управления и блок управления (50) на основе микроконтроллера. Контур управления содержит связанные между собой оптический датчик (20) положения мембраны (13), блок формирования давления жидкости (55) и сообщенный с полостью аппликатора компрессор (40). Блок управления (50) связан с компьютером (60) и выполнен с возможностью вычисления параметров и регистрации артериального давления. Средство регулирования состояния мембраны (13) выполнено с возможностью поддержания исходного плоского состояния мембраны (13), соответствующего нулевой разности давлений снаружи и внутри полости (12) при отсутствии механического контакта мембраны (13) с телом пациента (100). Блок управления (50) выполнен с возможностью прогнозирования параметров сигнала последующей пульсовой волны на основе значения локального периода сигнала за предшествующий промежуток времени, рассчитываемого по автокорреляционной функции (АКФ), и содержит сформированные программными средствами модуль вычисления кровяного давления, модуль вычисления АКФ, модуль вычисления локального периода, модуль формирования прогноза параметров последующей пульсовой волны, а также блок формирования давления жидкости в полости. Достигается повышение точности и достоверности определения кровяного давления за счет прогнозирования сигнала последующей пульсовой волны, формируемого с помощью величины локального периода, найденного по АКФ значений сигнала за предшествующий промежуток времени. 5 з.п. ф-лы, 4 ил.
Реферат
Изобретение относится к медицинской технике и предназначено для непрерывного контроля кровяного давления.
Известно большое число разработок в области неинвазивного непрерывного измерения кровяного давления (АД), и проблема их усовершенствования является актуальной (см., например, Non-invasive continuous blood pressure monitoring: a review of current applications. Chung E, Chen G, Alexander B, Cannesson M. / Front Med. 2013 Mar; 7(1):91-101. Epub 2013 Jan 23). Для большинства решений использован метод объемной компенсации, основанный на идее "разгрузки стенок сосудов", т.к. предполагается, что в "разгруженном" состоянии давление внутри сосудов равно давлению вне их. Давление регулируется таким образом, чтобы поддерживать объем крови постоянным во времени, равным объему, который при калибровке выбран как "разгружающий" сосуды. В других решениях датчик прижимает артерию к лучевой кости настолько, чтобы в достаточной степени ее сжать, сделать контакт с ее стенкой плоским, но не пережать до окклюзии. Затем через стенки сосуда с помощью тензодатчиков бокового давления регистрируются пульсовые изменения АД. Величина давления, необходимая для того, чтобы уплощить стенки артерии, но не закрыть ее, известна как "рабочее усилие прижима" и рассчитывается по достаточно сложному алгоритму, который включает в себя предварительные оценки систолического, диастолического и пульсового давлений.
Описано устройство для непрерывного неинвазивного измерения давления (RU 2140187 С1, Медвэйв, Инк. (US), 27.10.1999). Содержит средство для приложения изменяемого прижимающего давления к чувствительному средству, средство для вычисления кровяного давления на основании воспринятых пульсовых колебаний давления внутри нижерасположенной артерии и средство для нейтрализации сил, создаваемых тканью вблизи нижерасположенной артерии, с одновременным обеспечением соответствия участку тела пациента. Датчик, имеющий чувствительную поверхность для восприятия кровяного давления в нижерасположенной артерии пациента, содержит преобразователь, боковую стенку, гибкую диафрагму и текучую соединительную среду. Боковая стенка расположена на некотором расстоянии от преобразователя и поддерживает его над нижерасположенной артерией. Текучая среда соединяет между собой чувствительную поверхность преобразователя и гибкую диафрагму и передает пульсовые колебания кровяного давления от гибкой диафрагмы к чувствительной поверхности преобразователя.
Недостаток устройства состоит в том, что подстройка изменяемого прижимающего давления к чувствительному средству осуществляется для относительно медленного выравнивания среднего давления в артерии и не отслеживает разгрузку стенок артерии в течение всего цикла, что приведет к искажению передаваемых жидкой средой пульсаций давления.
Наиболее близким к патентуемому устройству является устройство неинвазивного мониторинга АД субъекта (US 5848970, Voss, et al., 15.12.1998 - прототип). Неинвазивный мониторинг АД субъекта осуществляется посредством камеры с жидкостью, в котором гибкая мембрана, установленная внутри, прижимает покрывающие артерию ткани с достаточной силой, чтобы сжать артерию. Система сервоуправления оптимизирует степень сжатия артерии, которое происходит при величине среднего трансмурального давления около нуля, путем модуляции объема жидкости внутри камеры и отмечая результирующий эффект от давления в камере. Так как различные эффекты давления проявляются в соответствии с частотой сжатия артерии, то может быть получен соответствующий управляющий сигнал, что обеспечивает оптимальное среднее давление на мембране. Система сервоуправления относительно быстро регулирует подачу и слив жидкости из камеры таким образом, чтобы компенсировать изменения давления внутри артерии. Это сводит к минимуму колебания эффективного диаметра артерии, в результате чего давление в заполненной жидкостью камере близко следует за фактическим сигналом артериального пульса. Конструктивно устройство (fig. 6) содержит аппликатор для приема пульсовых колебаний давления крови, выполненный в виде заполненной жидкостью полости с гибкой мембраной для механического контакта с артерией пациента, преобразователь давления жидкости в электрический сигнал, помещенный в указанной полости. Средство для регулирования положения мембраны включает оптический датчик положения мембраны, блок формирования давления жидкости и компрессор, сообщенный с полостью аппликатора, микроконтроллер для вычисления параметров и регистрации и компьютер.
Анализ показывает, что принцип работы этого устройства ограничивается только эффектом зависимости трансмуральной передачи давления из артерии во внешнюю ткань от величины напряжения/разгрузки этой артерии, и концепция измерения строится только на основе этого эффекта. Заявителем проведены детальные эксперименты по зондированию стенок артерии сигналами переменного давления разной частоты по схеме, практически совпадающей с обсуждаемой в прототипе - патенте US 5848970, однако при этом не обнаружен эффект, который авторами положен в основу измерений. Однако даже если допустить возможность зависимости микроскопических изменений трансмуральной передачи давления от величины напряжения/разгрузки артерий, то система автоматического контроля объема, находящаяся в петле обратной связи, не будет в состоянии обеспечить все те функции, которые подразумеваются при их измерении.
Настоящее изобретение направлено на повышение точности и достоверности непрерывного измерения кровяного давления.
Патентуемое устройство для непрерывного неинвазивного измерения кровяного давления содержит установленный в корпусе аппликатор, выполненный в виде заполненной жидкостью полости с гибкой мембраной для обеспечения механического контакта с тканями пациента, преобразователь давления жидкости в электрический сигнал, связанный с полостью. Средство для регулирования состояния мембраны в процессе измерения на основе контура управления включает связанные между собой оптический датчик положения мембраны, блок формирования давления жидкости и компрессор, сообщенный с полостью аппликатора, а также блок управления на основе микроконтроллера для вычисления параметров и регистрации АД, связанный с компьютером.
Отличие состоит в том, что средство для регулирования состояния мембраны в процессе измерения выполнено с возможностью поддержания исходного плоского, без прогиба, состояния мембраны, соответствующего нулевой разности давлений снаружи и внутри полости при отсутствии механического контакта мембраны с телом пациента. Блок управления выполнен с возможностью прогнозирования значений сигнала последующей пульсовой волны на основе значения локального периода сигнала за предшествующий промежуток времени, рассчитываемого по автокорреляционной функции (АКФ), и содержит сформированные программными средствами модуль вычисления кровяного давления, модуль вычисления АКФ, модуль вычисления локального периода, модуль формирования прогноза параметров последующей пульсовой волны, а также блок формирования давления жидкости в полости, причем входы блока вычисления кровяного давления связаны с преобразователем давления жидкости в электрический сигнал и с датчиком положения мембраны, а выход блока вычисления кровяного давления - с компьютером.
Выходы модуля вычисления кровяного давления связаны с первым входом модуля формирования прогноза и входом модуля вычисления АКФ, выход которого связан с модулем вычисления локального периода, выход которого связан со вторым входом модуля формирования прогноза параметров последующей пульсовой волны, выход которого соединен со входом блока формирования давления жидкости и компрессором.
Устройство может характеризоваться тем, что модуль вычисления АКФ содержит средства для формирования аналитических спектров фрагмента вычисленных значений артериального давления, длительность которого равна длительности удвоенного максимального периода сердечных сокращений, перемножения спектров, их взвешивания и выполнения обратного преобразования Фурье, с получением на выходе значений АКФ.
Устройство может характеризоваться и тем, что модуль вычисления локального периода выполнен с возможностью поиска по вычисленной АКФ положения ее первого бокового максимума, по значению которого определяют момент времени в предшествующий фрагмент времени, который принимают за начало прогноза последующего фрагмента пульсовой волны.
Устройство может характеризоваться также тем, что модуль формирования прогноза значений последующей пульсовой волны выполнен с возможностью выбора фрагмента вычисленных значений артериального давления, длительность которого равна величине длительности найденного локального периода.
Устройство может характеризоваться, кроме того, тем, что оптический датчик положения мембраны выполнен в виде оптронной пары, которая размещена на корпусе аппликатора с возможностью регистрации положения световой заслонки, скрепленной с мембраной и размещенной в заполненной жидкостью полости, а также тем, что компрессор и преобразователь давления сообщены с полостью аппликатора посредством трубчатых отведений.
Технический результат изобретения - повышение точности и достоверности определения кровяного давления за счет прогнозирования сигнала последующей пульсовой волны, формируемого с помощью величины локального периода, найденного по АКФ значений сигнала за предшествующий промежуток времени.
Существо изобретения поясняется на чертежах, где:
фиг. 1 - структурная схема устройства;
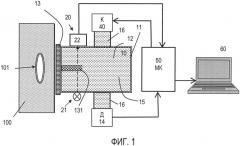
фиг. 2 - блок-схема микроконтроллера;
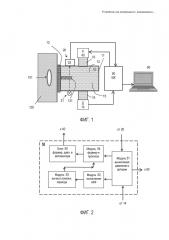
фиг. 3 - экспериментальная зависимость рассчитанного артериального давления;
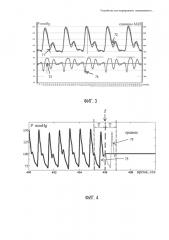
фиг. 4 - формирование прогноза значений на основе найденного локального периода.
В основе изобретения лежат следующие положения.
Как установлено заявителем, главным недостатком существующих неинвазивных методов измерения АД является то, что вне зависимости от способов "разгрузки стенок сосудов" контроль разгрузки осуществляется в них на основе интегральных параметров (кровенаполнение, полная сила, действующая на датчик, смещение датчика как целого и т.д.). Это позволяет отслеживать пульсовую волну АД в среднем за период, но не гарантирует передачи деталей формы импульса. Патентуемое устройство для измерения АД ориентировано на локальную разгрузку стенок артерий и на локальный же контроль разгрузки методом компенсации давления, который выбран в качестве принципиальной основы измерения меняющегося во времени АД. Если подобрать давление жидкости в полости аппликатора таким, что оно вернет мембрану в исходное плоское состояние, т.е. когда прогиб мембраны внутрь корпуса или наружу отсутствует, и если мембрана размещается непосредственно над лучевой артерией, то внешнее давление совпадает с артериальным, и тем самым имеется возможность его измерить.
Реализация устройства для измерения динамической величины АД стала возможной благодаря тому обстоятельству, что АД изменяется не столь быстро, его ритм составляет по порядку величины один удар в секунду, а спектр укладывается в несколько десятков Гц. Такие параметры сигнала позволяет использовать высокопроизводительные микроконтроллеры (ATMEL, MICROCHIP, STMicroelectronics и пр.), для которых отмеченная динамика АД представляет собой практически квазистатические изменения.
На фиг. 1, 2 представлена структурная схема устройства.
Устройство содержит аппликатор 10, включающий корпус 11 с заполненной жидкостью полостью 12 с гибкой мембраной 13 из эластичного резиноподобного материала для контакта с тканями 100 пациента и стенкой артерии 101, преобразователь 14 давления жидкости 15 в электрический сигнал. Средство для регулирования состояния мембраны 13 в процессе измерения включает связанные между собой оптический датчик 20 положения мембраны, блок 55 формирования давления жидкости, реализованный в блоке 50 управления, и компрессор 40, сообщенный с полостью аппликатора 10, установленные в корпусе 11. Оптический датчик 20 положения мембраны 13 выполнен в виде оптронной пары: светодиода 21 и фотоприемника 22, размещенных на корпусе 11 аппликатора с возможностью регистрации отклонения положения световой заслонки 131, скрепленной с мембраной 13 и являющейся, по существу, индикатором деформационных смещений. Датчик 20 определяет текущее положение световой заслонки 131 для поддержания неподвижного положения мембраны 13 в процессе измерения относительно ее исходного плоского состояния, соответствующего нулевой разности давлений снаружи и внутри полости 12. Сигнал калибровки, соответствующий плоскому, когда прогиб мембраны отсутствует, ненагруженному состоянию мембраны, фиксируется непосредственно перед началом измерений при отсутствии механического контакта с тканями пациента, окружающими артерию, т.е. когда мембрана снаружи аппликатора «нагружена» на воздух.
Устройство содержит блок 50 управления на основе микроконтроллера для вычисления параметров и регистрации полученных данных, связанный с компьютером 60. Преобразователь 14 давления и компрессор 40 сообщены с полостью 12 аппликатора 10 посредством трубчатых отведений 16 или встроены непосредственно в корпус 11.
Блок 50 управления включает средства прогнозирования периода сигнала последующей пульсовой волны, вычисленного на основе оценки локального периода по автокорреляционной функции значений сигнала за предшествующий промежуток времени. Блок 50 содержит модуль 51 вычисления кровяного давления, модуль 52 вычисления автокорреляционной функции, модуль 53 вычисления локального периода, модуль 54 формирования прогноза параметров последующей пульсовой волны, блок 55 формирования давления жидкости в полости 12.
Входы модуля 51 вычисления кровяного давления связаны с преобразователем 14 давления жидкости в электрический сигнал и с датчиком 20 положения мембраны, а вход-выход блока вычисления кровяного давления - с компьютером 60.
Выходы модуля 51 вычисления кровяного давления связаны с первым входом модуля 54 формирования прогноза и входом модуля 52 вычисления автокорреляционной функции. Выход модуля 52 связан с модулем 53 вычисления локального периода, выход которого связан со вторым входом модуля 54 формирования прогноза параметров последующей пульсовой волны. Выход модуля 54 соединен с входом блока 55 формирования давления жидкости и компрессором 40.
На фиг. 3 показана экспериментальная зависимость рассчитанного АД, спрогнозированного давления и их разность, соответствующая смещению мембраны 13. Для иллюстрации качества компенсации в верхней части фигуры приведены график (кривая 71) давления Р внутри полости 12 (данные с преобразователя 14 давления) и эти же данные (кривая 72), скорректированные на пересчитанную по смещениям мембраны 13 разность давлений, показанные в нижней части фигуры. Видно, что в сравнении с графиком Р (кривая 71), когда поправка невелика, давление Р в среднем совпадает с АД (кривая 72). В нижней части фигуры поз. 73 показан вид сигнала на выходе датчика 20 положения мембраны при наличии плоского, при отсутствии прогиба, ненагруженного состояния мембраны 13, поз. 74 - вид сигнала при проведении измерений.
На фиг. 4 показан пример формирования прогноза значений последующей за текущим моментом времени t пульсовой волны на основе выбора длительности фрагмента вычисленных значений артериального давления найденного локального периода Т. Если в текущий момент времени t известен интервал времени Т между импульсами пульсовой волны АД, то зная форму текущего импульса (поз. 75) и предполагая, что форма следующего импульса будет почти такой же, можно сформировать прогноз последующего сигнала (поз. 76). Для этого следует взять имеющийся фрагмент сигнала длительностью Т, непосредственно предшествующий текущему моменту времени t, и сместить его на интервал Т вправо по оси времени, при этом момент t принимают за начало прогноза последующего фрагмента пульсовой волны (поз. 76).
Блок 50 управления может быть реализован, например, на основе программируемого микроконтроллера марки STM32L152RBT, который имеет коммуникационный вход/выход (USB), связанный с компьютером 60, интерфейсы линий сигнала и управления. Линии сигнала связаны с преобразователем 14 и оптическим датчиком 20, линии управления - с компрессором 40. Компрессор 40 для жидкости может быть построен известным путем, например, в виде микронасоса с электроприводом и микросхемой его управления, и в данном описании не раскрывается как не характеризующий существо изобретения.
Устройство работает следующим образом.
После включения устройства автоматически запоминаются показатели исходного плоского состояния гибкой мембраны 13, соответствующие нулевой разности давлений снаружи и внутри полости 12 аппликатора при отсутствии механического контакта мембраны 13 с телом 100 пациента. Затем аппликатор приводится в механический контакт с телом 100 пациента таким образом, чтобы мембрана 13 из эластичного материала соприкасалась непосредственно со стенкой лучевой артерии 101, после этого подключается система поддержания исходного плоского положения мембраны 13. Датчик 20 определяет текущее положение световой заслонки 131, которая размещена в полости 12, реализуя тем самым индикатор деформационных смещений мембраны и производит наполнение полости 12 для поддержания ее исходного плоского состояния, соответствующего нулевой разности давлений снаружи и внутри полости 12. При величине давления жидкости в полости, при котором оно вернет мембрану 13 в плоское состояние, давление за мембраной оказывается скомпенсированным. Если аппликатор уставлен непосредственно над лучевой артерией, то внешнее давление в полости совпадает с артериальным, которое и регистрируется в модуле 51 вычисления давления в артерии и компьютере 60.
Значения регистрируемого давления в артерии буферизуются в памяти микроконтроллера. Размеры каждого буфера выбирают из расчета хранения отсчетов за время, превышающее два последовательных периода сердечного цикла максимально возможного размера. Программный модуль 52 вычисления АКФ вычисляет симметричный квадратичный функционал оценки автокорреляционной функции сигнала давления, анализ которой формирует в реальном времени достаточно точные оценки текущего квазипериода сердечных сокращений и выдает прогноз входящих сигналов на модуль формирования широтно-импульсной модуляции управления давлением.
Модуль 53 вычисления локального периода по вычисленной в модуле 52 АКФ осуществляет поиск положения первого бокового максимума АКФ, по значению которого определяют момент времени в предшествующий фрагмент времени, который принимают за начало прогноза последующего фрагмента пульсовой волны.
Модуль 54 формирования прогноза параметров последующей пульсовой волны, на основании данных, полученных из модуля 53 о величине длительности найденного локального периода и блока 51 и текущих значений выдает прогноз динамики изменений давления путем выбора фрагмента вычисленных значений артериального давления.
На основе прогноза, вычисленного в модуле 54, блоком 55 формируется сигнал управления для приведения к минимуму сигнала рассогласования, что достигается регулированием давления жидкости в полости 12. Величина давления Р жидкости в полости, при которой оно вернет мембрану 13 в плоское, когда прогиб мембраны отсутствует, первоначальное состояние, и соответствует искомому кровяному давлению.
Результаты экспериментов и проведенных оценок показывают, что за счет прогнозирования сигнала последующей пульсовой волны, вычисленного на основе значений локального периода, найденного по автокорреляционной функции за предшествующий промежуток времени, удается повысить точность и достоверность неинвазивного непрерывного определения кровяного давления.
1. Устройство для непрерывного неинвазивного измерения кровяного давления, содержащее установленный в корпусе аппликатор, выполненный в виде заполненной жидкостью полости с гибкой мембраной для обеспечения механического контакта с тканями пациента непосредственно над лучевой артерией, преобразователь давления жидкости в электрический сигнал, связанный с полостью,
средство для регулирования состояния мембраны в процессе измерения на основе контура управления, включающего связанные между собой оптический датчик положения мембраны, блок формирования давления жидкости и компрессор, сообщенный с полостью аппликатора,
блок управления на основе микроконтроллера для вычисления параметров и регистрации артериального давления, связанный с компьютером,
отличающееся тем, что
средство для регулирования состояния мембраны в процессе измерения выполнено с возможностью поддержания исходного плоского состояния мембраны, соответствующего нулевой разности давлений снаружи и внутри полости при отсутствии механического контакта мембраны с телом пациента;
блок управления выполнен с возможностью прогнозирования параметров сигнала последующей пульсовой волны на основе значения локального периода сигнала за предшествующий промежуток времени, рассчитываемого по автокорреляционной функции (АКФ), и содержит сформированные программными средствами модуль вычисления кровяного давления, модуль вычисления АКФ, модуль вычисления локального периода, модуль формирования прогноза параметров последующей пульсовой волны, а также блок формирования давления жидкости в полости, причем
входы модуля вычисления кровяного давления связаны с преобразователем давления жидкости в электрический сигнал и с датчиком положения мембраны, а выход модуля вычисления кровяного давления - с компьютером, при этом выходы модуля вычисления кровяного давления связаны с первым входом модуля формирования прогноза и входом модуля вычисления АКФ, выход которого связан с модулем вычисления локального периода, выход которого связан со вторым входом модуля формирования прогноза параметров последующей пульсовой волны, выход которого соединен со входом блока формирования давления жидкости и компрессором.
2. Устройство по п. 1, отличающееся тем, что модуль вычисления АКФ содержит средства для формирования аналитических спектров фрагмента вычисленных значений артериального давления, длительность которого равна длительности удвоенного максимального периода сердечных сокращений, перемножения спектров, их взвешивания и выполнения обратного преобразования Фурье, с получением на выходе значений АКФ.
3. Устройство по п. 1, отличающееся тем, что модуль вычисления локального периода выполнен с возможностью поиска по вычисленной АКФ положения ее первого бокового максимума, по значению которого определяют момент времени в предшествующий фрагмент времени, который принимают за начало прогноза последующего фрагмента пульсовой волны.
4. Устройство по п. 1, отличающееся тем, что модуль формирования прогноза значений последующей пульсовой волны выполнен с возможностью выбора фрагмента вычисленных значений артериального давления, длительность которого равна величине длительности найденного локального периода.
5. Устройство по п. 1, отличающееся тем, что оптический датчик положения мембраны выполнен в виде оптронной пары, которая размещена на корпусе аппликатора с возможностью регистрации положения световой заслонки, скрепленной с мембраной и размещенной в заполненной жидкостью полости.
6. Устройство по п. 1, отличающееся тем, что компрессор и преобразователь давления сообщены с полостью аппликатора посредством трубчатых отведений.