Фосфоркалийазотсодержащее npk-удобрение и способ получения гранулированного фосфоркалийазотсодержащего npk-удобрения
Иллюстрации
Показать всеИзобретения относятся к сельскому хозяйству. Сложное азотно-фосфорно-калийное удобрение (NPK) содержит нитрат аммония, моноаммонийфосфат, сульфат кальция безводный, нитрат калия, хлорид аммония, причем массовая доля общего азота от 13-15%, массовая доля общих фосфатов в пересчете на Р2О5 от 11-15%, массовая доля калия в пересчете на К2О от 7-8%. Способ получения сложного удобрения NPK из твердой фосфатной соли, представляющей собой смесь фторапатита Са5(PO4)3F и дикальций фосфата CaHPO4×nH2O, где n - от 0 до 2, а содержание фторапатита Са5(PO4)3F от 27 до 99% включает стадию разложения указанной твердой фосфатной соли серной кислотой полусухим методом, стадии добавления хлорида калия в качестве источника калия, нитрата аммония в качестве источника азота, стадию приготовления сларри NPK, а также стадию грануляции и сушки готового продукта. Изобретения позволяют улучшить свойства NPK-удобрения, повысить прочность гранул, решить проблему, связанную с пластичностью гранулированных сложных удобрений. 2 н. и 12 з.п. ф-лы, 1 ил., 3 табл., 3 пр.
Реферат
Изобретение относится к химической промышленности и находит применение в технологии производства сложных минеральных NPK-удобрений. NPK-удобрение (азофоска, нитроаммофоска) - это высокоэффективное экономическое комплексное удобрение, предназначенное для внесения под различные сельскохозяйственные культуры и практически в любые грунты. Тип NPK характеризуется массовыми долями азота, калия и фосфора в удобрении.
Современная агрохимическая наука предполагает применение удобрений с диапазоном соотношения питательных веществ N:P:K, а именно N:P2O5:K2O в разнообразных пределах, что требует создания технологических процессов, обеспечивающих возможность получения удобрений с регулируемым соотношением питательных веществ в соответствии с запросом потребителей.
Настоящее изобретение относится к получению гранулированных NPK-удобрений из фосфатной соли с содержанием фторапатита до 99%, в частности данная фосфатная соль представляет собой смесь СаНРО4×nН2О (дикальций фосфата) и Са5(РO4)3F (фторапатита), где n - от 0 до 2, содержание фторапатита Са5(РO4)3F в фосфатной соли 27% до 99%, при этом способ позволяет использовать различные соли калия и аммония в качестве источников питательных веществ в удобрении.
Также изобретение относится к непрерывному способу получения гранулированного NPK-удобрения из вышеуказанной фосфатной соли с содержанием фторапатита. В качестве источника калия применяют соли калия, как наиболее доступное на рынке сырье, в частности хлорид калия KCl. В качестве источника азота применяют аммиачную селитру (нитрат аммония) NH4NO3 и сульфат аммония (NH4)2SO4. Сульфат аммония применяется как стабилизирующий агент при использовании KCl, как источника калия, в заявленном NPK.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ:
Из RU 2216526 известен способ получения сложного NPK-удобрения с регулируемым соотношением N:P2О5:K2O, включающий кислотное разложение фосфатного сырья азотной кислотой, добавку азотсодержащего компонента, нейтрализацию аммиаком, смешение NP-пульпы с хлоридом и сульфатом кали
Из патентов RU 2439039 и RU 2223933 также известны способы разложения фосфатных руд азотной кислотой с нейтрализацией пульпы аммиаком и добавлением солей калия.
Недостатком способов является использование в качестве кислоты - азотной кислоты - дорогого и дефицитного компонента, неудовлетворительные потребительские свойства гранул из-за низкой прочности гранул и выделение соляной кислоты при хранении при использовании в качестве сырья хлорида калия. Стадия упаривания продукта до остаточной влажности ведет к дополнительным энергетическим затратам на процесс, а использование аммиака для нейтрализации остаточной кислоты приводит к снижению содержания растворимых солей фосфора в продукте.
Из патента RU 2107055 известен способ получения сложных удобрений с помощью разложения фосфатных руд смесью фосфорной и серной кислот с нейтрализацией смеси щелочной калийной солью, например карбонатом калия, а затем нейтрализацию аммиаком. Недостатком данного способа является применение экстракционной фосфорной кислоты, которая является дорогим продуктом, при производстве которого появляется большое количество отходов - фосфогипса, кроме того, с фосфорной кислотой в систему вводится большое количество воды, что приводит к необходимости проведения процесса выпарки для получения готового продукта.
Использование аммиака для нейтрализации смеси приводит к снижению водорастворимой части фосфора ниже 60%.
Для процесса получения сложных удобрений из растворимых фосфатных солей также существуют некоторые исследованные способы.
Приготовление удобрения с содержанием азота и фосфора описывает китайский патент CN 1113900 (1994), где удобрение приготовляется из фосфатной руды и азотной кислоты, а результатом является Са(Н2РO4)2, который кристаллизируется, смешиванием нитрата аммония с маточным раствором получают NH4H2PO4, барботированием полученного маточного раствора аммиаком получают СаНРO4. К недостаткам такого способа можно отнести - наличие стадии упаривания в процессе, фосфор в продукте находится не в водорастворимой форме дикальцийфосфата, не раскрыт способ введения калия в удобрение.
Патент GB 662079 раскрывает получение удобрений, содержащих растворимые соли фосфора на основе пульпы при разложении природных фосфатов, DCP (дикальцийфосфат) или TCP (трикальцийфосфат). Фосфаты разлагают действием серной кислоты, далее на смесь действуют азотной кислотой так, чтобы образовался MAP и нитрат кальция. Продукт стабилизируют добавлением сульфата аммония, в результате чего из нитрата кальция образуется гипс и нитрат аммония. Дополнительное количество добавленного сульфата аммония оказывает благоприятное влияние на удобрение, так как образуется двойная соль сульфата аммония с двумя молекулами нитрата аммония. В конце к смеси добавляют газообразный аммиак для того, чтобы достичь образования цитраторастворимого фосфата - DCP из остатков присутствующего МСР. К недостаткам можно отнести наличие в системе гигроскопичного нитрата калия из-за чего смесь трудно обрабатывать для получения гранулированного продукта, а также наличие дикальцийфосфата в продукте, что снижает содержание водорастворимой формы фосфора.
В патенте Великобритании GB 702860 описано получение гранулированных NPK удобрений на основе сырья, полученного разложением фосфата. В соответствии с описанным, (монокальций фосфат) МСР получают путем разложения фосфатной руды азотной кислотой. Разложение осуществляется в два этапа. Одним из недостатков гранулированных сложных NP удобрений, в соответствии с описанием, является их пластичность, эту проблему не смогли решить в процессе производства.
Патент CN 1220236 (1997) описывает процесс, который включает смешивание гашеной извести с одним или обоими веществами, порошкообразными Са3(РO4)2 и СаНРO4, добавлением фосфорной кислоты с концентрацией 62-85% при перемешивании при 80°С в течение 20-60 с с получением (монокальций фосфата) МСР, далее следует отверждение в течение 8-100 часов, естественная сушка и измельчение с получением продукта. Соотношения Н3РO4/Са3(РO4)2, или Н3РO4/СаНРO4 одинаковы (7-16) : 100. Порошкообразный Са(Н2РO4)2 реагирует с порошкообразным Са(ОН)2 с образованием СаНРO4 и соотношение Са(ОН)2/Са(Н2РO4)2 составляет (10-22) : 100. К недостаткам данного способа можно отнести использование гашеной извести, для производства которой необходимы дополнительные энергетические затраты, процесс является периодическим (существует стадия созревания продукта).
Другими способами получения МСР являются процессы разложения апатитов фосфорной кислотой. Реакция апатита с фосфорной кислотой
Ca5(PO4)3F+7Н3РО4→5Са(Н2РO4)2+HF
Процесс, способ и формы основных продуктов изменяются в зависимости от того, какие кислоты HCl, HNO3, H2SO4 и смеси кислот используют в качестве исходного материала.
Получение монокальций фосфата (МСР) из фосфорита описывает китайский патент CN 1305946. Этот способ включает реакцию фосфорита и серной кислоты при температурах от 70 до 95°С в течение 2-8 часов; фильтрование с получением от 10 до 30% фосфорной кислоты; добавление СаСO3 в фосфорной кислоты и удаления примесей; нейтрализацию с Са(ОН)2 и фильтрацию; добавление СаНРО4 и СаО; и распылительную сушку с получением Са(H2РО4)2 и продукта с высоким содержанием фосфора (ядра кальциевых солей фосфорной кислоты, 19-22% фосфора). Недостаток данного процесса заключается в том, что одной из стадий проведения процесса является производство водного раствора фосфорной кислоты, поэтому необходимость выпарки воды приводит к дополнительным затратам на проведение процесса.
Изменения монокальцийфосфата (МСР), содержащегося в суперфосфатах кальция, рассматривают авторы в патенте MX NL03000044 (2003). При получении используется 98% серная кислота, безводный аммиак, оксид кальция и МСР, DCP или TCP. В первой фазе монокальцийфосфат и фосфорная кислота выделяют с водой из исходного суперфосфата, а твердые нерастворимые компоненты (сульфат кальция, фосфат кальция, фосфат железа и фосфат алюминия, соединения фтора, непрореагировавшие фосфорные исходные материалы и другие нерастворимые вещества, такие как диоксид кремния и силикаты) отделяются декантацией в воде. Очищенный раствор вступает в реакцию с суспензией гидроксида кальция с образованием суспензии кристаллов DCP, которые отделяют декантированием. Полученные кристаллы затем подвергают взаимодействию с кислым сульфатом аммония с образованием раствора моноаммонийфосфата, нерастворимые кристаллы дигидрата сульфата кальция отделяют фильтрованием. При реакции на последней стадии к суспензии с DCP добавляют концентрированную соляную кислоту и аммиак. По фильтрации получают раствор с концентрацией больше 48% МСР. Недостатком является - технологическая сложность проведение процесса, использование большого количества реагентов, потери продукта с осадком при фильтрации и декантации, а также получение МСР в виде раствора, что затрудняет его дальнейшую переработку.
Мексиканский патент MX NL0500002 описывает способ получения монокальций фосфата МСР, фосфата натрия, калия и MAP, при котором в качестве исходных материалов используются фосфатная руда, серная кислота, оксид кальция, сульфат аммония или сульфат калия. Важным является способ получения фосфатных солей, которые получают по реакции (дикальций фосфата) DCP с соответствующими кислыми сульфатами соответствующих солей (магния, аммония, калия). Полученный MAP или другие соли после фильтрации гипса концентрируются в испарителе и кристаллизируются. Недостаток способа - наличие стадии получения раствора солей и фильтрации гипса, что приводит к дополнительным затратам для перевода продукта в твердую форму выпариванием. Использование для разложения природной фосфорной руды приводит к образованию большого количества отходов - фосфогипса.
МСР (монокальций фосфат) в промышленной практике получают, главным образом, реакцией солей кальция с фосфорной кислотой. Примером может служить реакция Н3РO4 с соединениями, содержащими кальций, такими как известковое молоко, при низкой температуре. Кроме того, существует возможность получения реакцией тонкоизмельченного известняка и фосфорной кислоты.
Другой метод состоит в приготовлении из ортофосфата кальция Са3(РO4)2, известный как фосфат кальция, путем обработки серной кислотой смеси сульфата кальция и фосфорной кислоты, или с помощью реакции серной кислоты со смесью сульфата кальция и монокальцийфосфата Са(Н2РО4)2.
Фактически приготовление NPK происходит преимущественно разложением природных фосфатов кислотами. Уровень техники описывает приготовление материала, которым является простой суперфосфат (SSP) или тройной суперфосфат (TSP), полученный в результате реакции фосфатов с серной или фосфорной кислотой. Растворимая часть состоит в основном из монофосфата кальция, а нерастворимой частью является гипс в случае SSP (и другие нерастворимые примеси, кроме тех, которые содержатся в гипсе).
Во время переработки в сложные удобрения исходное сырье гранулируют в барабанных грануляторах, с добавлением небольшого количества щелочи (напр. аммиака). Содержание свободной фосфорной кислоты, содержание которой в порошковом суперфосфате доходит до 5%, снижается нейтрализацией при грануляции на 1-2%. Но одновременно снижается и содержание водорастворимой части, которая при таких способах достигает уровня около 60%.
Вышеприведенный уровень техники позволяет выявить основные аспекты и недостатки поведения реакционных систем грануляции сложных минеральных удобрений.
К недостаткам известных способов можно отнести то, что на текущем этапе развития технологии остаются проблематичными или не решенными следующие проблемы технологии получения сложных удобрений NPK:
- Сложные удобрения на основе (монокальцийфосфата) МСР и нитрата аммония технологически проблематичны, актуальны проблемы со слеживаемостью. Гранулят получается эластичным, что затрудняет его производство по обычным технологическим процессам грануляции.
- МСР и KCl, в присутствии определенного количества влаги, реагируют с выделением газообразного HCl,
- МСР при нагревании может раствориться в "собственной" воде.
В настоящее время не известно производство в промышленных масштабах сложных удобрений, где фосфатная часть входит или присутствует в качестве монокальций фосфата МСР, то есть на базе суперфосфата или на базе тройного суперфосфата.
Таким образом целью настоящего изобретения явилась разработка нового типа сложного NPK-удобрения с высокой водорастворимостью Р2О5.
Поставленная задача решается за счет того, что NPK-удобрение производится с использованием хлористого калия KCl в качестве источника калия, и нитрата аммония в качестве источника азота, в присутствии (монокальций фосфата) МСР и гипса.
Поскольку одним из требований к получаемому удобрению является высокая водорастворимость Р2О5, важно, чтобы весь продукт, полученный в результате разложения сложной фосфатной соли по существу был в виде монокальций фосфата МСР, или другой соли фосфорной кислоты, которая обеспечит водорастворимость. При этом МСР должен остаться стабильным, чтобы предотвратить его конверсию в дикальций фосфат и фосфорную кислоту.
Необходимо также отметить, что в настоящее время сера рассматривается как один из важных питательных элементов в удобрениях заявленного типа. Согласно настоящему изобретению в целевом продукте присутствует безводный мелкодисперсный гипс (сульфат кальция), обеспечивающий доступность (для растений) такого элемента как сера, необходимого и присутствующего в целевом, вносимом в почву удобрении.
Таким образом, заявленное изобретение обеспечивает улучшение свойств NPK-удобрения, а способ его получения позволяет повысить прочность гранул, решить проблему, связанную с пластичностью гранулированных сложных удобрений и тем самым улучшить потребительские свойства NPK-удобрений.
Следствием решения поставленной задачи является, эффективность получаемого продукта, снижение себестоимости конечного продукта и значительное расширение сырьевой базы.
Согласно настоящему изобретению получают сложное азотно-фосфорно-калийное удобрение (NPK), содержащее нитрат аммония, моноаммонийфосфат, сульфат кальция безводный, нитрат калия, хлорид аммония, причем массовая доля общего азота от 13-15%, массовая доля общих фосфатов в пересчете на Р2О5 от 11-15%, массовая доля калия в пересчете на K2О от 7-8%.
Поставленная техническая задача получения такого удобрения решается тем, что способ получения сложного удобрения NPK из твердой фосфатной соли, представляющей собой смесь фторапатита и дикальций фосфата, включает разложение указанной твердой фосфатной соли серной кислотой полусухим методом, добавления хлористого калия в качестве источника калия, нитрата аммония в качестве источника азота, приготовление сларри (пульпы) NPK, а также грануляцию и сушку готового продукта.
При этом твердая фосфатная соль представляет собой смесь фторапатита Ca5(PO4)3F и дикальций фосфата СаНРО4×nН2O, где n - от 0 до 2, с содержанием фторапатита Ca5(PO4)3F от 27 до 99%.
Технический результат осуществления такого способа состоит в том, что водорастворимая форма Р2О5 достигает 98%, иными словами фосфор, содержащийся в удобрении растворим в воде на 98%. Важным моментом решения технической задачи являлся факт того, что в результате проводимого технологического процесса (монокальций фосфат) МСР, получаемый по реакции взаимодействия, был сформирован в виде моногидрата (т.е. оставался стабильным), с этой целью, температура при разложении дикальций фосфата не должна превышать 120°С. Именно при этой температуре начинает происходить обезвоживание.
Иными словами важным аспектом является то, что способ получения подразумевает использование МСР в виде моногидрата при температурном режиме, не превышающем 120°С, что в свою очередь позволяет избежать разложения МСР на дикальций фосфат и фосфорную кислоту.
Помимо этого при получении заявленного NPK добавление сульфатов, в частности сульфата аммония позволяет перевести МСР в моноаммоний фосфат с целью избежания содержания в конечном продукте остаточного реакционноспособного МСР, что решает проблему разложения компонентов NPK с выделением HCl при хранении, а также избежать проблемы с пластичностью при грануляции.
Также важным аспектом осуществления заявленного способа является добавление сульфатов к МСР, что позволяет получить безводный гипс в определенных условиях проведения процесса. А именно взаимодействие МСР с сульфатами при температурном режиме не ниже 120°С позволяет получить преимущественно безводный гипс.
Технологические условия получения безводного гипса в мелкодисперсной форме в дальнейшем обеспечивают доступность важного в удобрении элемента - серы, уже непосредственно при внесении в почву.
Резюмируя вышеизложенное следует подчеркнуть, что условия предложенной технологии, а именно после приготовления МСР и подачи в реактор приготовления сларри (пульпы) температура должна быть не ниже 120°С, что позволяет избежать образования полугидрата гипса (которое крайне нежелательно для получаемого удобрения).
Таким образом, в процессе заявленного производства решили проблему, связанную с пластичностью гранулированных сложных удобрений NPK.
СУЩНОСТЬ ЗАЯВЛЕННОГО ИЗОБРЕТЕНИЯ:
Процесс разложения дикальций фосфата (DCP):
При контакте концентрированной серной кислоты и дикальций фосфата образуется монокальций фосфат (МСР). Ингредиенты смешивают в эквимолярном соотношении по отношению к кальцию в DCP (эквимолярное количество серной кислоты рассчитывается в соответствии с составом DCP по химическим реакциям (1) и (4)).
Этот метод выбирается с учетом того, что DCP в качестве исходного материала не является чистым веществом, а смесью, в которой присутствует кроме DCP по крайней мере фторапатит.
Процессы, происходящие при смешивании, можно выразить следующей системой уравнений:
Более конкретно, значение энтальпии реакции относится к следующему суммарному уравнению:
2CaHPO4.2H2O+H2SO4=CaSO4+Ca(H2PO4)2.H2O+3H2O
С точки зрения минералогии DCP, как правило, называют «brushite», что и есть дигидрат дикальций фосфата. В соответствии с результатами RTG измерений, поставленного образца DCP, он присутствует в безводной форме «monetite», поэтому в уравнении (1) DCP показан в безводной форме. В соответствии с RTG записью после реакции приготовления МСР, возникающий гипс находится в виде ангидрида, реакция является экзотермической.
В итоге реакция 1, образование МСР протекает в два этапа:
Параллельно со стадией разложения фосфатной соли происходит взаимодействие серной кислоты и фторапатита.
Данная реакция сильно экзотермическая, в отличие от преобразования DCP. В соответствии с механизмом, реакция разложение фосфатов происходит в два этапа, второй этап на практике происходит медленнее и не совсем до конца:
Образовавшийся МСР подвергается «деградации» в присутствии воды с образованием DCP и фосфорной кислоты, из которых в свою очередь в результате обратной реакции образуется опять МСР. Эта обратная реакция протекает в присутствии воды, поэтому трудно достичь высокого уровня содержания водорастворимого фосфора (МСР) в реакционной смеси. На практике это решается способом проведения разложение при низком содержании воды в системе.
Необходимо, чтобы МСР был сформирован в виде моногидрата, из за этого, температура при разложении DCP не должна превышать 120°С, при этой температуре начинает происходить обезвоживание. В случае образования безводного МСР в условиях недостатка воды или высокой температуры реакционной смеси, гидратация протекает при приготовлении пульпы с отрицательным воздействием на баланс воды и вязкость реакционной среды, в условиях трудно контролируемых сопутствующих температурных изменений.
Осуществление получения NPK-удобрения с использованием хлорида калия в качестве источника калия:
Система, содержащая рядом с собой МСР, аммиачную селитру и хлорид калия является нестабильной из-за взаимодействия МСР и KCl и образования интермедиата аммиачной селитры и МСР. Чтобы избежать этих реакций и для стабилизации качества конечного продукта следует удалить из системы реактивный МСР, этого добиваемся взаимодействием с сульфатами, в конкретном случае применением сульфата аммония с последующим образованием гипса и моноаммонийфосфата. Сульфат аммония дозируется эквимолярно в отношении к полученному МСР в системе:
После добавления KCl к сларри (пульпе), содержащей нитрат аммония, происходят реакции конверсии в зависимости от времени контакта и места его дозировки:
С точки зрения условий процесса, эти химические перемены происходят при температуре 100-130°С. Тепло подается извне. Глубина и степень протекания реакции зависит как от температуры и содержания воды в системе, так и интенсивности перемешивания, времени пребывания, а также от тонкости частиц сырья, которая влияет на их растворимость. Учитывая относительную чистоту компонентов процесса, доля других реакций незначительна.
Продукт, NPK приготовленный с использованием DCP, серной кислоты, нитрата аммония и KCl в основном содержит следующие компоненты:
- Нитрат аммония
- Моноаммонийфосфат
- Сульфат кальция безводный
- Нитрат калия
- Хлорид аммония
В целом технологический процесс производства заявленного согласно изобретению NPK состоит из следующих стадий:
1. Мокрая часть - приготовление сларри
2. Сухая часть - грануляция
3. Переработка абгазов и сточных вод
Мокрая часть представляет из себя систему процессов, в итоге которых производится сларри NPK, пригодный для грануляции:
- разложение фосфатной соли (в частности смеси DCP с фторапатитом) с помощью серной кислоты в монокальцийфосфат (МСР), процесс проводится в смесителе с псевдоожиженном слое для достижения оптимального контакта частиц при проведении реакций. После проведения реакции в смесителе окончание реакции и выделение абгазов происходит в дозревателе;
Дальнейшее приготовление сларри происходит каскаде из трех реакторов, снабженных мешалками.
При использования хлористого калия, как источника калия для NPK дальнейшая схема проведения процесса следующая:
- в первом реакторе подается мелкозернистый сульфат аммония, происходит реакция МСР с сульфатом аммония с образованием гипса и моноаммонийфосфата.
- во второй реактор каскада подается аммиачная селитра. Дозирование аммиачной селитры производится в виде расплава или в виде гранул через дозатор;
- в третий реактор подается мелкокристаллический хлористый калий для окончания реакции.
Из мокрой части процесса сларри поступает на грануляцию, которая осуществляется в грануляторе подходящей конструкции путем агломерации и наслаивании в псевдоожиженном слое. Ретур вводится в переднюю часть гранулятора. Сушка осуществляется горячим воздухом. После проведения следующих операций - грохочение, дробление, охлаждения и поверхностной обработки антислеживающей добавкой получается готовый продукт, готовый к хранению и транспортировке.
Абгазы, содержащие пыль продуктов и сырья, используемого в производстве, а также газы, выделяющиеся в процессе производства улавливаются в мокрых скрубберах с добавлением нейтрализующих реагентов в абсорбент.
Основной целью данного изобретения является приготовление удобрения NPK с использованием KCl, в качестве источника калия, и нитрата аммония, в качестве источника азота в присутствии МСР и гипса. В связи с высокими требованиями к водорастворимости Р2О5, необходимо, чтобы, по существу, все фосфорное сырье было в виде МСР, или другой соли фосфорной кислоты, которая обеспечит водорастворимость. МСР должен остаться стабильным, чтобы предотвратить его конверсию в DCP и фосфорную кислоту.
В отличии от остальных макропитательных элементов, для фосфорных соединений, вносимых в почву, основной вопрос состоит в их полезности для питания растений. Исходя из этого, все удобрения, содержащие фосфор, редко оценивают по общему содержанию фосфора, но всегда приводят критерий относительной растворимости, установленный при определенных условиях - в воде (самая быстродействующая форма), в слабых кислотах (2%-ная лимонная кислота или муравьиная кислота) или в растворах, которые могут моделировать условия в почве (например в нейтральном или щелочном растворе цитрата аммония).
Таким образом весь предлагаемый процесс производства NPK можно разделить на 2 основных этапа - процесс получения водорастворимой фосфатной соли и процесс получения из этой соли сложных удобрений. Настоящее производство заявленного сложного удобрения NPK состоит из двух основных процессов - мокрого (производство сларри NPK) и сухого (гранулирование, помол, грохочение и охлаждение готового продукта).
1. Мокрая часть
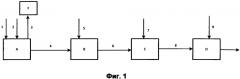
На Фиг. 1 представлена схема мокрого процесса для получения сларри NPK при использовании в качестве источника калия, хлористого калия KCl.
Фосфатная соль, представляющая собой смесь фосфатов кальция с фторапатитом (поток 1) совместно с серной кислотой (поток 2) поступают в проточный аппарат (блок А), представляющий собой смеситель с быстроходно вращающимися лопастями и дозреватель реакционной массы. Дозировка серной кислоты производится в эквимолярном соотношении к фосфатной соли. В результате проведения процесса в реакционной массе блока А происходят следующие химические процессы:
H2SO4+2СаНРO4+Н2O=Са(Н2РO4)2+CaSO4
7H2SO4+2Ca5(PO4)3F+3H2O=3Ca(H2PO4)2×H2O+7CaSO4+2HF
8 обоих случаях реакции происходят в 2 этапа - реакция фосфата с серной кислотой и выделение фосфорной кислоты, реакция фосфорной кислоты с фосфатной солью с образованием монокальцийфосфата (МСР). Реакция образования МСР может происходить не до конца, в том числе из-за разложения МСР в присутствии воды.
Реакции 1 и 2 являются экзотермическими, в особенности реакция 2. Техническое решение по отведению тепла реакции является комплексным - реактор оснащен водяной рубашкой, также часть тепла выводится из системы отходящими газами часть с парами воды. Для обеспечения отвода паров и газов смеситель блок А работает под вакуумом. Параметры системы отведения тепла должны быть подобраны таким образом, чтобы температура реакционной смеси не превышала 120°С.
После смесителя реакционная смесь подается в дозреватель, входящий в состав блока А, представляющий из себя аппарат с мешалкой. В дозревателе происходят следующие процессы:
- идет завершение реакционных процессов;
- происходит окончательное освобождение реакционной смеси от газов;
- происходит усреднение химических и физических свойств реакционной массы.
Дальнейшее приготовление сларри осуществляется в каскаде из трех реакторов (Блок В, С, D) с мешалкой и рубашкой для обогрева, оснащенных переливом.
Первый реактор сларри (блок В):
В первый реактор подается (моноаммонийфосфат) MAP (поток 6) и кристаллический сульфат аммония (поток 5).
Система, содержащая МСР, аммиачную селитру и хлористый калий является нестабильной из-за взаимодействия МСР и KCl и образования интермедиата аммиачной селитры и МСР. Чтобы избежать этих реакций и для стабилизации качества конечного продукта следует удалить из системы реактивный МСР взаимодействием с сульфатами, в конкретном случае применением сульфата аммония с последующим образованием гипса и моноаммонийфосфата. Сульфат аммония дозируется эквимолярно в отношении к полученному МСР в системе:
Са(Н2РO4)+(NH4)SO4=2NH4H2PO4+CaSO4
Реакционная масса (поток 6), содержащая моноаммонийфосфат и гипс перетоком поступает в следующий реактор
Второй реактор сларри (Блок С):
Основным агентом процесса в реакторе является аммиачная селитра. Она поставляется в гранулированном виде. Для ее внесения в систему можно применить два подхода:
1. Селитру до внесения в систему расплавить в отдельном реакторе, получить расплав, раствор в воде с содержанием селитры 93-97% при температуре примерно 158°С и это дозировать в сларри реактор.
2. Селитру вносить в систему в виде гранул, дозатором в сларри реактор.
В реактор блок С подается аммиачной селитра в виде гранул или расплава (поток 7), в зависимости от состава продукта. Смесь в реакторе поддерживается при температуре не выше 160°С. Тепло подается паром рубашкой и прямым паром. В реакторе не протекают химические процессы, в результате смешения образуется однородная сларри в насыщенном растворе аммиачной селитры.
Третий реактор сларри:
Сларри из второго реактора (поток 8) поступает переливом в третий реактор (блок D), в который дозатором подается кристаллический хлорид калия. При контакте с селитрой протекает реакция замещения в соответствии с следующим уравнением:
NH4NO3+KCl=KNO3+NH4Cl
Реакция протекает очень быстро и на выходе из реактора реакция практически завершена. В зависимости от состава, качества получаемого продукта, конкретных условий, можно часть хлорида калия дозировать помимо третьего сларри реактора прямо в ретур. Температура в реакторе поддерживается в пределах 125-145°С. После третьего реактора сларри поступает в сухой процесс (поток 9)
Улавливание фтористого водорода происходит в блоке F.
Поток пара и газов низкого давления из смесителя (поток 3) поступает в абсорбционную колону, где на улавливание фтороводорода применяется основной раствор (сларри карбоната кальция или гидроксид кальция). Конечный продукт, фторид кальция фильтруется, промывается и в зависимости от применения, или утилизируется, или сушится и упаковывается и поступает на склад.
Таким образом продукт NPK, приготовленный с использованием фосфатной соли, серной кислоты, нитрата аммония и сульфата аммония и хлорида калия в основном содержит следующие компоненты:
- Нитрат аммония
- Моноаммонийфосфат
- Сульфат кальция безводный
- Нитрат калия
- Хлорид аммония
При этом диапазон соотношений питательных веществ в получаемом типе NPK-удобрения иллюстрируется в нижеприведенных примерах.
2.Сухая часть
Сларри с температурой 125-145°С поступает самотеком из третьего реактора в гранулятор, типа лопастного смесителя. В его переднюю часть поступает ретур. Сларри распределяется по материалу в грануляторе распределителем. Грануляция осуществляется за счет агломерации и наслаивания в псевдоожиженном слое, который создается лопастями установленными на двух валах. В гранулятор может подаваться пар 0,3-0,4 МПа для подстройки оптимальных условий работы гранулятора (температура, влажность), который соответствует выпускаемому качеству комбинированного удобрения. Влажные гранулы, с температурой в пределах 90-110°С, в зависимости от состава удобрения и содержанием воды 1,5-3% масс., прямо из лотка гранулятора удобрение через желоб падает в сушильный барабан. При грануляции и суше могут протекать последние химические реакции.
Примеры
Пример 1
За основу проведения принят процесс, описанный выше, согласно схеме на Фиг. 1.
Получаемый ниже продукт, сложное азотно-фосфорно-калийное удобрение (NPK), приготовленный с использованием фосфатной соли, серной кислоты, нитрата аммония и сульфата аммония, а также хлорида калия по существу содержит следующие компоненты нитрат аммония, сульфат кальция безводный, нитрат калия, дигидрофосфат калия, причем массовая доля общего азота от 13-15%, массовая доля общих фосфатов в пересчете на Р2O5 от 11-15%, массовая доля калия в пересчете на K2O от 7-8%.
В более конкретном случае технологические условия осуществления процесса позволяют получить сложное NPK-удобрение типа 15:15:8, что подразумевает массовую долю общего азота, массовую долю общих фосфатов в пересчете на Р2О5 и массовую долю калия в пересчете на K2O.
Согласно варианту осуществления изобретения, производство указанного выше NPK на основе твердой фосфатной соли, представляющей собой смесь фторапатита Са5(РO4)3F и дикальций фосфата СаНРО4×nН2О, где n - от 0 до 2, а содержание фторапатита Ca5(PO4)3F от 27 до 99%, позволяет использовать хлорид калия и аммиачную селитру.
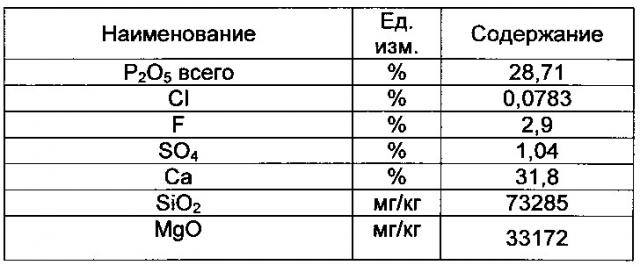
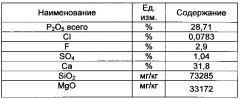
В качестве сырья используется фосфатная соль, полученная путем солянокислого разложения фосфорной руды, отделением нерастворимого осадка с последующим высаждением твердой фосфатной соли с помощью сларри карбоната кальция. Для производства фосфатной соли использовалась руда месторождения Кейсик состава
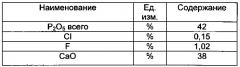
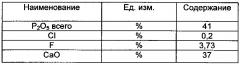
В результате процесса получена смесь фтораппатита Ca5(PO4)3F и дикальций фосфата СаНРO4×nН2О, где n - от 0 до 2, а содержание фторапатита Ca5(PO4)3F от 27 до 99%, используемая в дальнейшем для процесса производства NPK состава
Фтор, содержащийся в фосфатной соли, произведенной солянокислым разложением фосфатной руды, существует в смеси в качестве фторапатита, что подтверждено аналитическим контролем образцов. Фосфатная соль DCP с содержанием фторапатита 27% используется в дальнейшем для процесса производства NPK.
При температуре 110-120°С проводят стадию разложения указанной твердой фосфатной соли серной кислотой полусухим методом, где разложение осуществляется при низком содержании воды. Это необходимое условие обусловлено подбором эквимолярных соотношений в систем таким образом, чтобы МСР оставался в виде моногидрата стабильным.
Более конкретно, в фосфатную соль [557 кг/ч] в смесителе с псевдоожиженным слоем подается 98% серная кислота [272 кг/ч] в эквимолярном соотношении. Процесс проводится под вакуумом для лучшего удаления выделившихся газов, главным образом фтористого водорода. Реакционная масса через дозреватель подается в каскад реакторов с мешалкой. Газ, в основном фтористый водород, поступает на абсорбцию. Процесс проводится при температуре не более 120°С.
Далее в каскад реакторов в первый реактор подается сульфат аммония [224 кг/ч], в виде мелкого порошка, процесс проводится при температуре 130°С с целью обеспечения условий образования безводного гипса. Во второй реактор подается аммиачная селитра в виде расплава [726 кг/ч], процесс в реакторе проводится при 160°С. В третий реактор вводится мелкозернистый хлорид калия [320 кг/ч], реакция в третьем реакторе протекает быстро и до конца при температуре 120°С.
После завершения процесса в третьем реакторе смесь подается в сухую часть процесса, в результате грануляции и сушки произведено сложное удобрение NPK компонентного состава N:P2О:K2О = 15:15:8 с содержанием серы в виде безводного мелкодисперсного гипса.
Пример 2
За основу проведения принят процесс, описанный выше, согласно схеме на Фиг. 1.
Получаемое сложное азотно-фосфорно-калийное удобрение (NPK) содержит нитрат аммония, моноаммонийфосфат, сульфат кальция безводный, нитрат калия, хлорид аммония, причем массовая доля общего азота от 13-15%, массовая доля общих фосфатов в пересчете на Р2