Применение селективного иммуносорбента для удаления антител к десмоглеину 3 типа из сыворотки крови у больных пузырчаткой
Иллюстрации
Показать всеИзобретение относится к медицине и касается способа получения селективного иммуносорбента для удаления антител к десмоглеину 3 типа (Dsg3) из крови больных пузырчаткой, при котором приготавливают раствор Dsg3 в фосфатном буфере. В пустую центрифужную микроколонку добавляют сухую NHS-активированную агарозу, вносят раствор Dsg3 в микроколонку с агарозой и, перемешивая, инкубируют; по окончании инкубации микроколонку центрифугируют с охлаждением, затем получившийся фильтрат отбирают, после чего для отмывки от несвязавшегося Dsg3 в колонку добавляют фосфатный буфер, центрифугируют; повторяют процедуру отмывки, фильтраты после отмывок отбирают; далее для блокирования остаточных активных NHS-групп сорбента добавляют раствор буфера - этаноламина и, перемешивая, инкубируют; по окончании инкубации центрифугируют, фильтрат удаляют; повторяют процедуру отмывки, фильтраты после отмывок отбирают; готовый сорбент используют для выделения аутоантител к Dsg3. Изобретение обеспечивает получение селективного иммуносорбента для избирательного удаления антител к десмоглеину 3 типа из сыворотки крови у больных пузырчаткой. 4 ил., 1 табл., 3 пр.
Реферат
Область техники, к которой относится изобретение.
Изобретение относится к иммунохимии, а именно к способам получения материалов с нерастворимым носителем для иммобилизации иммунологических материалов, в том числе сорбирующих колонок.
Непосредственной целью изобретения является способ получения селективного иммуносорбента для удаления антител к десмоглеину 3 типа из сыворотки крови у больных пузырчаткой. Селективный сорбент относится к материалам для биологического связывания антител в десмоглеину 3 типа с помощью сорбирующих колонок.
Полученный иммуносорбент может быть использован при проведении экстракорпоральной терапии при кожных заболеваниях, в частности для лечения аутоиммунных буллезных дерматозов, а именно пузырчатки.
Уровень техники
Пузырчатка (пемфигус) - тяжелое аутоиммунное буллезное заболевание, характеризующееся образованием пузырей и эрозий на коже и/или слизистых оболочках [Дерматовенерология, 2010. (Клинические рекомендации / Российское общество дерматовенерологов) / [под ред. А.А. Кубановой]. - М.: ДЭКС-Пресс, 2010. - 428 с.; Grando S.A. Pemphigus autoimmunity: hypotheses and realities// Autoimmunity. - 2012. - Vol. 45. - №1. - P. 7-35].
Патогенетическую роль в формировании пузырей при пузырчатке играют циркулирующие аутоантитела, обладающие высокой тканевой специфичностью, преимущественно относящиеся к классу иммуноглобулинов G (IgG), и вызывающие разрушение десмосом, что приводит к акантолизу [Матушевская Е.В., Кубанова А.А., Самсонов В.А. и др. Аутоантитела и аутоантигены при пузырчатке и пемфигоиде // Вестник дерматологии и венерологии. - 1995. - №5. - С.28-33; Joly P., Bernard P., Bedane C. et al. Pemphigus. Guidelines for the diagnosis and treatment. Centres de reference des maladies bulleuses auto-immunes. Societe Francaise de Dermatologie // Ann Dermatol Venereol. - 2011. - Vol. 138. - P. 252-258]. У больных пузырчаткой выявлены все 4 субкласса IgG с преобладанием в стадию обострения IgG4, а в стадию ремиссии - IgG1 [Bhol K., Mohimen A., Ahmed A.R. Correlation of subclasses of IgG with disease activity in pemphigus vulgaris // Dermatology. -1994. - Vol. 189 Suppl 1. - P. 85-89].
Основными структурами, к которым вырабатываются аутоантитела при вульгарной пузырчатке, являются белки десмосомального аппарата - десмоглеины 3 типа (Dsg 3) [Stanley J.R., Yaar М., Hawley-Nelson P. et al. Pemphigus antibodies identify a cell surface glycoprotein synthesized by human and mouse keratinocytes // J. Clin. Invest. - 1982. - Vol. 70. - P. 281-288; Stanley J.R., Koulu L. and Thivolet C. Distinction between epidermal antigensbinding pemphigus vulgaris and pemphigus foliaceus autoantibodies // J. Clin. Invest. - 1984. - Vol. 74 - P. 313-320; Ohyama M., Ota Т., Aoki M. et al. Suppression of the immune response against exogenous desmoglein 3 in desmoglein 3 knockout mice: an implication for gene therapy // J Invest Dermatol. - 2003 Apr. - Vol. 120(4). - P. 610-615]. Десмосомы состоят из белков клеточной адгезии, относящихся к семейству кадгеринов и соединительных (адапторных) белков, которые соединяют их с промежуточными филаментами. Белки клеточной адгезии, формирующие десмосомы, - десмоглеины и десмоколлины. Эти кальцийзависимые гликозилированные протеины состоят из экстрацеллюлярного амино-терминального участка, трансмембранного домена и внутриклеточного карбокситерминального участка. Известны три формы десмоколлина (1-3 типы) и четыре десмоглеина (1-4 типы) [Махнева Н.В., Белецкая Л.В. Молекулярно-биологическая характеристика десмосом как системы межклеточного соединения // Вестник дерматологии и венерологии. - 2009. - №2. - С. 25-381; Garrod D.R., Merritt A.J., Nie Z. Desmosomal cadherins // Curr. Opin.Cell Biol. - 2002. - Vol. 14. - P. 537-545].
При вульгарной пузырчатке у 80-100% больных в сыворотке крови выявляются аутоантитела именно к Dsg3, т.е. этот белок является строго специфичным для данного заболевания [Свирщевская Е.В., Лысенко А.А., Матушевская Е.В. и др. Аутоиммунная пузырчатка: идентификация патогенных эпитопов десмоглеина 3 // Современные проблемы дерматовенерологии, иммунологии и медицинской косметологию. - 2009. - №3. - С. 5-13]. Установлена связь между уровнем IgG к Dsg3 и тяжестью поражения при пузырчатке [Cozzani Е, Di Zenzo G., Riva S. et al. Are clinical phenotype and autoantibody profile always concordant in pemphigus? A study in a cohort of pemphigus patients // Eur J Dermatol. - 2013 Jan-Feb. - Vol. 23(1). - Р. 40-48].
Терапия больных пузырчаткой должна проводиться с момента появления пузырей и/или эрозий даже при ограниченном характере высыпаний [Соколовский Е.В. Пузырные дерматозы. Псориаз. Современные методы лечения. Серия «Библиотека врача-дерматовенеролога». Выпуск 3. - СПб: СОТИС, 1999. - 134 с.].
Известен способ лечения пузырчатки, включающий назначение системных глюкокортикостероидных (ГКС) препаратов [Каламкарян А.А., Трофимова Л.Я., Хапилова В.И. Иммунодепрессанты в комплексной терапии пузырчатки // Вестник дерматологии. - 1979. - №12. - С. 28-32; Самцов В.И., Клибсон С.К., Подвысоцкая И.И. и соавт. Дифференциальная диагностика и лечение больных буллезными дерматозами. Вестник дерматологии и венерологии // 1988. - №5. - С. 46-49]. Наиболее часто применяют преднизолон, другие ГКС (триамцинолон, метипред, гидрокортизон, дексаметазон) назначают в соответствии с преднизолоновым эквивалентом [Самцов А.В., Белоусова И.Э. Буллезные дерматозы: Монография. - СПб.: ООО «Издательско-полиграфическая компания «Коста», 2012. - 144 с.]. Введение в схему лечения пузырчатки системных ГКС препаратов увеличило продолжительность жизни больных пузырчаткой.
Однако длительное применение системных ГКС препаратов сопряжено с трудностями, обусловленными развитием тяжелых осложнений, что отягощает состояние больных и ухудшает прогноз пузырчатки [Ruocco Е., Wolf R., Ruocco V. et al. Pemphigus: Associations and management guidelines: Facts and controversies // Clin Dermatol. - 2013. - Vol. 31(4). - P. 382-390].
Побочные действия ГКС многообразны: синдром Иценко-Кушинга, стероидный диабет, нарушения водного и минерального обмена, остеопороз, осложнения со стороны желудочно-кишечного тракта (эзофагит, гастрит, язвенная болезнь желудка и 12-перстной кишки), тромбоэмболия, острая сердечная или сосудистая недостаточность, гипопротеинемия. Тяжелым осложнением ГКС терапии является иммуносупрессивное состояние, ДВС-синдром, сетицемия [Решетникова Т.Б. Лыкова С.Г., Спицына А.В., Макарова Я.Ю. Влияние гормональной терапии на состояние иммунной системы, частоту и характер осложнений у больных истинной акантолитической пузырчаткой в зависимости от исходного состояния Т-хелперов // Сибирский медицинский журнал. - 2004. - №4. - С. 13-17; 22. Brenner S., Goldberg I. Drug-induced pemphigus // Clin. Dermatol. - 2011. - Vol. 29. - №4. - P. 455-457; D, Harman M, F, Akpolat V. The frequency of osteoporosis in patients with pemphigus vulgaris on treatment // Indian J Dermatol Venereol Leprol. - 2013. - Vol. 79, №2. - P. 211-215].
Серьезные осложнения ГКС терапии, а также необходимость длительного приема больших доз иммуносупрессивных препаратов требуют совершенствования методов терапии пузырчатки.
Для снижения дозы ГКС, а также при их недостаточной эффективности рекомендуется присоединение к ГКС цитостатиков: азатиоприна, микофенолата мофетила, метотрексата и циклофосфамида (заместительная терапия). Цитостатики обладают стероид-сберегающим действием, уменьшают частоту развития побочных эффектов ГКС и способны увеличить длительность ремиссии [Машкиллейсон А.Л., Антонова Т.Н., Глебова Л.И. и др. Комбинированная терапия пемфигуса кортикостероидами и метотрексатом // Вестник дерматологии. - 1977. - №3. - С. 60-63; Кубанова А.А., Самсонов В.А., Хапилова В.И., Матушевская Е.В. Сандиммун в терапии больных истинной пузырчаткой // Вестник дерматологии. - 1994. - №6. - С. 42-44; Bystryn J.C. Adjuvant therapy of pemphigus // 1984. Jul. - Vol. 120(7). - P. 941-951; Sharma V.K., Khandpur S. Evaluation of cyclophosphamide pulse therapy as an adjuvant to oral corticosteroid in the management of pemphigus vulgaris // Clin Exp Dermatol. - 2013 Aug. - Vol. 38(6). - P. 659-664].
Однако при комбинации ГКС и цитостатиков количество осложнений продолжает оставаться высоким [Schmidt Е., Zillikens D. The Diagnosis and Treatment of Autoimmune Blistering Skin Diseases // Dtsch Arztebl Int. - 2011. June. - Vol. 108(23). - P. 399-405.]. К тому же, данные группы препаратов усугубляют уже имеющееся иммунодефицитное состояние больных, что часто приводит к развитию инфекционных осложнений [Теплюк Н.П., Потекаев Н.Н., Кузьмина Т.С. и др. Летальный исход при кортикостероидной терапии акантолитической пузырчатки в результате инфекционных осложнений // Клин, дерматол. и венерол. - 2005. - №2. - С. 16-19].
В последние десятилетия для лечения пузырчатки используются эфферентные методы терапии: гемосорбция, плазмаферез, энтеросорбция, иммуносорбция. Для иммуносорбции используется 3 вида сорбентов: неселективные, с низкой селективностью и с высокой степенью селективности. Неселективные сорбенты (декстрансульфат, триптофан, фенилаланинсодержащие и другие) способны сорбировать такие компоненты плазмы крови, как фибриноген, альбумин, липиды, иммуноглобулины. Сорбенты с низкой селективностью (с иммобилизованным стафилококковым протеином А, антителами к Ig человека и другими) имеют сродство к определенной фракции протеинов плазмы. Сорбенты с высокой степенью селективности извлекают только определенные протеины без изменения концентрации других компонентов плазмы пациента.
Одним из наиболее эффективных и безопасных методов лечения аутоиммунных заболеваний является экстракорпоральный метод терапии с использованием специфических иммуносорбентов [Keller F., Wagner K., Faber U. et al. Elimination kinetics of plasma exchange // Klin. Wochen schr. - 1983. - Vol. 61, N22. - P. 1115-1122].
Известными на сегодняшний день способами-аналогами изобретения являются документы, представленные ниже.
Известен способ получения углеродного гемосорбента в сорбционных колонках для использования при лечении аутоиммунных заболеваний, в частности, пузырчатки [Грандо С.А., Глухенький Б.Т., Романенко А.Б. и соавт. Механизмы терапевтического действия экстракорпоральной детоксикации при аутоиммунных буллезных дерматозах // Вестник дерматологии и венерологии. - 1988. - №7. - С. 6-11; Eming R., Hertl М. Immunoadsorption in pemphigus // Autoimmunity. - 2006. - Vol. 39(7). - P. 609-616]. Гемоперфузия проводится по вено-венозному контуру через углеродный гемосорбент в сорбционных колонках, предназначенных для очистки и фильтрации крови вне организма со скоростью кровотока 80-120 мл/мин в объеме 1,5 объема циркулирующей плазмы. Положительный эффект иммуносорбции связывают с удалением из крови больных пузырчаткой циркулирующих аутоантител и иммунных комплексов.
Однако при использовании данных сорбентов, вследствие элиминации из сыворотки больных аутоантител и циркулирующих иммунных комплексов и других жизненно важных компонентов крови, без дифференциации к удалению определенных комплексов с IgG, обуславливающей более быстрое наступление клинического эффекта, наблюдался феномен рикошета (экзацербация патологического кожного процесса, сопровождающаяся резким повышением титра иммуноглобулинов в сыворотке крови больных), что является недостатком данного метода [Гребенников В.А., Белявский А.Д., Каминский М.Ю. Изучение иммунокорригирующего и детоксицирующего воздействия гемосорбции, плазмафереза и энтеросорбции при пузырчатке // Вестник дерматологии. - 1990. - №5. - С. 33-38].
Известен способ получения триптофансодержащих сорбентов для применения с целью удаления аутоантител при пузырчатке посредством иммуноадсорбции [ М., Stauber A., Mainka A., Klingel R., Schuler G., Hertl M. Successful removal of pathogenic autoantibodies in pemphigus by immunoadsorption with a tryptophan-linked polyvinylalcohol adsorber // Br J Dermatol. - 2003, Sep. - Vol. 149(3). - P. 598-605]. Триптофановые столбы состояли из поливиниловых шариков, сшитых алкоголь-гелем, которые иммобилизировали гидрофобной аминокислотой и триптофаном в качестве лиганда. В исследованиях in vitro было продемонстрировано, что триптофановые столбы более эффективно удаляют все классы аутоантител при пузырчатке, чем декстрановые, преимущество которых в избирательном удалении аффинных белков. К тому же, триптофановые столбы более дешевые. Недостаток данного метода: триптофановые столбы сорбируют необходимые для жизнедеятельности компоненты плазмы крови (фибриноген, альбумин, липиды, все классы иммуноглобулинов), к тому же, синтез триптофановых столбов является довольно сложным процессом.
Ближайшим аналогом-прототипом в лечении больных пузырчаткой является иммуноадсорбент с использованием стафилококкового протеина А (protein A affinity resin), представляющий собой рекомбинантный белок А Staphylococcus aureus, иммобилизованный на CNBr-активированной сефарозе FF (GEHealthcare). Преимущества данного иммуносорбента по сравнению с триптофановыми колоннами в том, что метод не требует замены компонентов плазмы [Samuelsson G. Extracorporeal immunoadsorption with protein A: technical aspects and clinical results // J Clin Apher. - 2001. - Vol. 16. - Р. 49-52].
Однако при проведении иммуносорбции с использованием данного иммуносорбента снижается количество иммуноглобулинов всех подклассов, уменьшается концентрация антител к ДНК, человеческому лейкоцитарному антигену [Samuelsson G. Extracorporeal immunoadsorption with protein A: technical aspects and clinical results // J Clin Apher. - 2001. - Vol. 16. - Р. 49-52].
Кроме того, после проведения иммуноадсорбции с использованием стафилококкового протеина А у больных пузырчаткой риск развития инфекционных заболеваний остается высоким, так как наряду с патогенетически значимыми аутоантителам IgG при пузырчатке во время процедуры выводятся иммуноглобулины всех подклассов (IgA, IgM, IgE), циркулирующие иммунные комплексы, иммунные комплексы другой специфичности. К тому же, стоимость данного сорбента значительно выше других [Schmidt Е., Klinker Е., Opitz A. et al. Protein A immunoadsorption: a novel and effective adjuvant treatment of severe pemphigus // Br J Dermatol. - 2003. - Vol. 148. - P. 1222-1229].
Заявляемый способ отличается от прототипа тем, что вместо иммунносорбентов, неспецифически связывающих белки и низкомолекулярные продукты, в качестве сорбента использована крупнозернистая агарозная матрица с ковалентно иммобилизованным рекомбинантным десмоглеином 3 типа человека, специфически связывающая антитела к десмоглеину 3 типа, в результате чего выводятся только пемфигусные, патогенетически значимые, аутоатитела к десмоглеинам 3 типа, а антитела другой специфичности, отвечающие за иммунный ответ на вирусные и бактериальные агенты, сохраняются, уменьшая частоту развития инфекционных осложнений. Сорбенты с высокой степенью селективности для удаления антител - IgG, строго специфичных именно к Dsg3, из доступных источников научной и научно-технической информации не известны.
Непосредственной целью изобретения является способ получения селективного иммуносорбента для удаления антител к десмоглеину 3 типа из сыворотки крови у больных пузырчаткой. Селективный сорбент относится к материалам для биологического связывания антител в десмоглеину 3 типа с помощью сорбирующих колонок.
Применение данного иммуносорбента у больных пузырчаткой не имеет противопоказаний и должно позволить в короткие сроки получить выраженный и стойкий терапевтический эффект, в том числе при стероидорезистентной форме.
Таким образом, изобретение не известно из уровня техники, т.е. является новым.
Сущность изобретения
Технический результат, на достижение которого направлено изобретение, заключается в способе получения селективного иммуносорбента для избирательного удаления антител к десмоглеину 3 типа из сыворотки крови у больных пузырчаткой.
Применение данного иммуносорбента позволяет селективно связывать аутоантитела к компоненту десмосом - десмоглеину 3 типа, играющих ключевую роль в патогенезе пузырчатки, циркулирующих в сыворотке крови больных пузырчаткой и вырабатываемых строго иммунноспецифично к такому заболеванию.
В связи с этим, применение данного иммуносорбента является высокоэффективным, позволяет более быстро снижать дозы ГКС препаратов, достигать клинической ремиссии в 87% случаев. Полученный терапевтический эффект при применении такого избирательного иммуносорбента является стойким. При его использовании в схеме лечения больных пузырчаткой противопоказаний не выявлено.
Предложенный иммуносорбент позволяет проводить терапию стероидорезистентных форм пузырчатки, лечение во время беременности и грудного вскармливания, так как избирательная очистка крови от антител к десмоглеину 3 типа у больных пузырчаткой обеспечивает высокую эффективность и безопасность проводимой терапии.
Технический результат также достигается за счет того, что авторами впервые установлена избирательная (селективная) степень очистки крови именно от антител к десмоглеину 3 типа у больных пузырчаткой при применении разработанного иммуносорбента при сохранении иммуноглобулинов другой специфичности. Целевой иммуносорбент, получаемый в результате реализации способа, представляет собой агарозу с N-гидроксисукцинимидными группами (NHS-активированную сефарозу), на которой иммобилизирован рекомбинантный человеческий десмоглеин 3 типа (Dsg3).
Указанный технический результат обеспечивается определенной последовательностью действий и условий их выполнения.
Способ получения иммуносорбента реализуется следующим образом:
1.1 Материалы и реактивы:
- рекомбинантный человеческий десмоглеин 3 типа;
- центрифужная микроколонка с NHS-активированной агарозой;
- азид натрия;
- этанол амин;
- тест-системы EUROIMMUN Anti-Desmoglein 3 (IgG) (Canada).
1.2 Используемые растворы:
- буфер для связывания/промывки - 0,1М фосфатный буфер, рН 7,2;
- блокирующий раствор - 1М этаноламин рН 8;
- раствор для хранения - 0,1М фосфатный с 0,05% азида натрия.
1.3 Оборудование
- центрифуга с охлаждением;
- лабораторный шейкер.
1.4 Методика иммобилизации рекомбинантного десмоглеина 3 типа на NHS-активированной агарозе
Для получения селективного иммуносорбента рекомбинантый человеческий десмоглеин 3 типа (Dsg3) путем ковалентного связывания иммобилизируется на твердофазном аффинном носителе - NHS-активированной агарозе следующим образом.
1. Приготовление раствора белка Dsg3 в фосфатном буфере (рН 7,2), который обеспечивает оптимальное для эффективного ковалентного связывания с NHS-активированной агарозой расположение активных групп белка:
- в микропробирку с 33 мкг сухого рекомбинантного белка добавляют 400 мкл охлажденного до 4°С фосфатного буфера;
- микропробирку осторожно встряхивают, не допуская вспенивания, до полного растворения белка.
2. В пустую центрифужную микроколонку помещают 33 мг сухой NHS-активированной агарозы и вносят раствор Dsg3 в фосфатном буфере.
Микроколонку закрывают крышкой и инкубируют 16-18 ч, перемешивая на лабораторном шейкере при 4°С. На данном этапе обеспечивается необходимое для наиболее оптимального взаимодействия соотношение агарозной матрицы и белка-лиганда.
3. По окончании инкубации микроколонку центрифугируют (4°С, 1000 g, 1 мин), снимают верхнюю крышку, убирают надосадок и трижды промывают фосфатным буфером. Этап необходим для освобождения системы от несвязавшегося белка.
4. Для блокирования непрореагировавших групп активированной агарозы добавляют 100 мкл 1М этаноламина. Длительность блокирования - 1 ч при 4°С и перемешивании. Блокирование оставшихся свободными групп NHS-активированной агарозы исключит возможность неспецифического связывания с готовым сорбентом иммуноглобулинов класса G, отличных от антидесмоглеиновых антител.
5. Гель в колонке трижды отмывают буфером связывания/промывки, центрифугируя (1 мин 1000 g 4°С) и заменяя буфер на свежий. На данном этапе обеспечивается удаление этаноламина и заполнение системы рабочим буфером. Теперь колонка с иммуносорбентом готова к работе.
Готовый сорбент используют для выделения аутоантител к Dsg3 или, если эксперимент по выделению аутоантител будет проводиться позже, добавляют консервирующий раствор (0,1М фосфатный буфер содержащий 0,05% азида натрия, рН 7,2) и помещают на хранение при 4°С.
Осуществление изобретения
Практическая применимость способа подтверждается, но не исчерпывается следующими примерами.
Пример 1. Сорбция антител к десмоглеину 3 типа из сывороток крови больных пузырчаткой in vitro с использованием селективного иммуносорбента.
Для проведения исследований по определению условий эффективного применения селективного иммуносорбента для удаления антител к десмоглеину 3 типа из сывороток крови больных пузырчаткой были получены два препарата IgG: препарат из сыворотки крови больных пузырчаткой и препарат из сыворотки крови здоровых добровольцев. Количественная характеристика активности иммуноглобулинов класса G в отношении десмоглеина 3 типа (Ds3) определена в ест-системе EUROIMMUN Anti-Desmoglein 3 (IgG). В системе установлена единица измерения иммунологической активности антител класса IgG, обозначенная как relative units в миллилитре (RU/мл). Активность препарата IgG, полученного из сыворотки крови больных пузырчаткой, составила 15000 RU/мл. Препарат IgG из сыворотки здоровых добровольцев не обладал активностью в отношении Dsg3. Концентрацию растворов иммуноглобулинов определяли на спектрофотометре при длине волны 280 нм, умножая значение оптической плотности на коэффициент экстинкции 1,4, принятый для IgG. Концентрация IgG в обоих препаратах была 70 мг/мл.
0,5 мл препарата из сыворотки крови больных пузырчаткой, содержащий IgG с суммарной активностью 7500 RU был нанесен на колонку с 0,5 мл селективного иммуносорбента NHS-активированная агароза - Dsg3 для удаления антител к Dsg3. В сравнительной серии экспериментов такое же количество препарата IgG было пропущено через 0,5 мл NHS-активированной агарозы (неселективная матрица). После 30 мин инкубации при комнатной температуре и осаждения сорбента центрифугированием (1 мин, 4°С, 1000 об/мин) в супернатантах определяли концентрацию и активность IgG. Характеристики препарата IgG до и после сорбции на селективном и неселективном сорбентах представлены в таблице 1.
Таким образом, после взаимодействия с 0,5 мл селективного иммуносорбента NHS-активированная агароза - Dsg3 активность препарата IgG из сыворотки крови больных пузырчаткой снизилась на 2300 RU (30%), а после взаимодействия с неселективным сорбентом только на 300 RU (4%).
Представленные результаты доказывают селективность полученного сорбента по сравнению с неселективной матрицей. В условиях эксперимента in vitro количество иммунологически-активных антител в сыворотке уменьшилось на 30%. Применение данного иммуносорбента у больных пузырчаткой позволит снизить тяжесть заболевания и добиться ремиссии.
Пример 2. Эффективность селективного иммуносорбента для удаления антител-IgG к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vivo на экспериментальной модели.
Проводились экспериментальные исследования по определению эффективности селективного иммуносорбента для удаления IgG - антител к десмоглеину 3 типа из сыворотки крови больных пузырчаткой in vivo с использованием 15 лабораторных животных (новорожденных мышей линии BALB/c).
Мыши были разделены на 3 группы по 5 животных в каждой. Первой группе животных (основная группа) вводили по 30 мг препарата IgG, выделенного из сыворотки крови больных пузырчаткой (не очищенного на иммуносорбенте); Второй (контрольной) группе - по 30 мг препарата IgG, выделенного из сыворотки крови здоровых лиц; Третьей группе вводили по 30 мг препарата IgG, полученного из сыворотки крови больных пузырчаткой и очищенных на селективном иммуносорбенте от антител к Dsg3. Все препараты вводили в объеме 150 мкл в стерильном фосфатно-солевом буфере (рН 7,2) инсулиновым шприцом на 1 мл с иглой 27G (один шприц на животное). Через 48 ч животные подвергались эвтаназии. Производили осмотр кожных покровов и забор биопсийного материала для гистологического изучения и исследования в реакции непрямой иммунофлюоресценции.
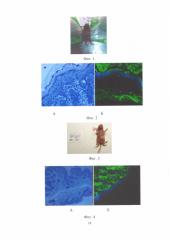
После введения IgG от больных пузырчаткой у мышей наблюдались эрозии в абдоминальной области, по 3-бальной шкале оцениваемые как 1+ (т.е. три или менее поражений кожи) (Фиг. 1. Экспериментальная модель; препараты IgG от больных пузырчаткой; эрозии на коже мыши, положительный симптом Никольского).
При патоморфологическом исследовании аутопсийного материала выявлены признаки акантолиза (Фиг. 2А. Гистологическая картина (субкорнеальная полость, содержащая акантолитические клетки), х50. Окр. гем. эоз.); при исследовании фиксированных IgG методом нРИФ определялась фиксация IgG в межклеточных промежутках эпидермиса (Фиг. 2Б. Реакция иммунофлюоресценции; конфокальная лазерная сканирующая микроскопия, х20; фиксация IgG в межклеточных промежутках эпидермиса).
При введении препарата IgG от здоровых добровольцев не зафиксировано патологических изменений при клиническом осмотре (Фиг. 3. Экспериментальная модель; препарат IgG от здоровых добровольцев), патоморфологическом исследовании и проведении нРИФ препаратов кожи мышей (Фиг. 4А. Гистологическая картина, х50. Окр. гем. эоз., Фиг. 4Б. Реакция иммунофлюоресценции; конфокальная лазерная сканирующая микроскопия, КЛСМ х20).
При введении препарата IgG, полученного от больных пузырчаткой и очищенных на предложенном иммуносорбенте от антител к десмоглеину 3 типа, не выявлены клинические, патоморфологические и иммунологические признаки пузырчатки у мышей.
Данный пример свидетельствует об эффективности удаления антител из сыворотки крови больных пузырчаткой твердофазным агарозным сорбентом, несущим на своей поверхности N-гидроксисукцинимидные группы: NHS-активированную агароз, ковалентно связанным с рекомбинантым человеческим десмоглеином 3 типа.
Пример 3. Оценка эффективности удаления антител к десмоглеину 3 типа из сыворотки крови больного вульгарной пузырчаткой при прохождении через селективный иммуносорбент.
У больного В., 34 лет, с диагнозом «Вульгарная пузырчатка с поражением кожи и слизистых оболочек рта» (диагноз устанавливался на основании данных клинического осмотра, цитологического, гистологического и иммунофлюоресцентного исследований), находящегося на стационарном лечении, определяли содержание антител в крови методом иммуноферментного анализа. Анализ проводили с использованием тест-системы EUROIMMUN Anti-Desmoglein 3. При исследовании у больного пузырчаткой В., 34 г. уровень антител к десмоглеину 3 типа в сыворотке крови составлял 86,8 RU/мл, у здорового добровольца С., 28 лет - 3,9 RU/мл.
Сыворотку крови больного пузырчаткой пропустили через предложенный иммуносорбент, после чего повторно измерили уровень антител в сыворотке крови. Уровень антител к десмоглеину 3 типа после прохождения через иммуносорбент приблизился к диагностическому порогу и составил 22,2 RU/мл, что позволяет предположить положительный эффект данного экстракорпорального метода терапии.
Таким образом, приведенные выше примеры подтвердили практическую применимость селективного иммуносорбента для удаления антител к десмоглеину 3 типа из сыворотки крови больных пузырчаткой, позволяющего избирательно удалять специфические антитела, являющиеся ключевым звеном в иммунопатогенезе пузырчатки. Применение такого вида иммуносорбента у больных пузырчаткой позволит повысить качество проводимой терапии, уменьшить дозы и длительность системных глюкокортикостероидных препаратов, а также снизить частоту развития побочных эффектов вследствие иммуносупрессивной терапии.
Способ получения селективного иммуносорбента для удаления антител к десмоглеину 3 типа (Dsg3) из крови больных пузырчаткой, при котором приготавливают раствор Dsg3 в фосфатном буфере, в пустую центрифужную микроколонку добавляют сухую NHS-активированную агарозу, вносят раствор Dsg3 в микроколонку с агарозой и, перемешивая, инкубируют; по окончании инкубации микроколонку центрифугируют с охлаждением, затем получившийся фильтрат отбирают, после чего для отмывки от несвязавшегося Dsg3 в колонку добавляют фосфатный буфер, центрифугируют при 4°С при 1000 g в течение 1 мин; повторяют процедуру отмывки, фильтраты после отмывок отбирают; далее для блокирования остаточных активных NHS-групп сорбента добавляют раствор буфера - этаноламина и, перемешивая, инкубируют; по окончании инкубации центрифугируют при 4°С при 1000 g в течение 1 мин, фильтрат удаляют; повторяют процедуру отмывки, фильтраты после отмывок отбирают; готовый сорбент используют для выделения аутоантител к Dsg3.