Катетер лечения трепетания предсердий с механизмом двойного отклонения однократного действия
Иллюстрации
Показать всеГруппа изобретений относится к медицинской технике, а именно к вариантам выполнения отклоняющегося катетера. Отклоняющийся катетер содержит продолговатый корпус, имеющий внешнюю стенку, проксимальный и дистальный концы и проходящий через них просвет. Катетер содержит секцию дистального конца, содержащую трубку, имеющую проксимальный конец и дистальный конец, и множество просветов, проходящих через них. Причем проксимальный конец секции дистального конца прикреплен к дистальному концу корпуса катетера. Секция дистального конца содержит нитиноловую трубку, имеющую прорези Секция содержит первую и вторую вытягивающие проволоки, проходящие через продолговатый корпус катетера и секцию дистального конца. Нитиноловая трубка и первая и вторая вытягивающие проволоки выполнены таким образом, что одно продольное перемещение любой из них приводит к проксимальному отклонению продолговатого корпуса катетера и дистальному отклонению секции дистального конца. Раскрыты альтернативные варианты отклоняющегося катетера, в которых катетер содержит шарнирно-сочлененную трубку с гребнем и прорезью. Также в этих вариантах катетер содержит промежуточную отклоняющуюся секцию, концевой электрод, рукоятку управления. В этих вариантах секция дистального конца имеет большую жесткость, чем промежуточная отклоняющаяся секция, варианты отличаются направлением отклонения промежуточной отклоняющейся части и секции дистального конца. Заявленная группа изобретений расширяет арсенал известных средств известного назначения. 3 н. и 17 з.п. 10 ил.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
Эта заявка испрашивает приоритет и привилегии Предварительной заявки на патент США сер. № 61/605886, поданной 2 марта 2012 г., содержание которой во всей своей полноте включено в настоящее описание путем ссылки.
ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к катетеру и к способу использования абляции для лечения нарушений сердечного ритма, в частности трепетания предсердий. В частности, катетер, и способ использует механизм двойного отклонения однократного действия, чтобы предоставить электрофизиологу катетер, который можно применять в лечении аритмий сердца и, в частности, трепетания предсердий.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Аритмии сердца, такие как трепетание предсердий и мерцательная аритмия предсердий, являются наиболее распространенными и опасными заболеваниями, особенно среди людей старшего возраста. У пациентов с нормальным синусовым ритмом сердце, состоящее из тканей предсердий, желудочков и проводящей системы и возбуждаемое электрическими импульсами, бьется синхронно и ритмично. У пациентов с аритмией сердца патологические участки сердечной ткани выпадают из синхронного ритма биения, характерного для нормально проводящей ткани, как у пациентов с нормальным синусовым ритмом. Вместо этого патологические участки сердечной ткани искажают электрический импульс, передаваемый прилегающей ткани, тем самым сбивая сердечный цикл на асинхронный ритм. Нарушения проводимости, как известно, могут возникать в различных участках сердца, например в области синусно-предсердного (СП) узла, вдоль проводящих путей атриовентрикулярного (АВ) узла и пучка Гиса, или в сердечной мышечной ткани, из которой состоят стенки нижних и верхних камер сердца.
Сердечные аритмии, в том числе предсердные аритмии, могут быть мелковолнового возвратного типа, который характеризуется множеством асинхронных петель электрических импульсов, рассредоточенных вокруг предсердия и зачастую являющихся спонтанно распространяющимися. Помимо аритмий мелковолнового возвратного типа различают фокальные сердечные аритмии, при которых изолированный участок ткани в предсердии периодически быстро приходит в возбуждение. Желудочковая тахикардия (ЖТ) - тахикардия или учащенный сердечный ритм, возникающий в одном из желудочков сердца. Такая аритмия потенциально опасна для жизни, так как может привести к фибрилляции желудочков и мгновенной смерти.
Другим типом аритмии является трепетание предсердий (ТП). Трепетание предсердий представляет собой патологию сердечного ритма, которая встречается в предсердиях сердца. В первый раз это, как правило, связано с тахикардией и относится к категории суправентрикулярной тахикардии (СВТ). В то время как такой ритм возникает чаще всего у пациентов с сердечнососудистыми заболеваниями или сахарным диабетом, он может также возникнуть спонтанно у людей с ранее здоровым сердцем. Как правило, этот ритм не является стабильным и часто вырождается в мерцательную аритмию предсердий (МАП). Таким образом, лечение ТП является желательным. Из-за того, что трепетание предсердий носит реципрокный характер, часто имеется возможность подвергнуть абляции цепь, которая вызывает трепетание предсердий. Это делается в электрофизиологической лаборатории путем создания гребня рубцовой ткани, которая пересекает путь цепи, вызывающей трепетание предсердий. Абляция перешейка, как говорилось выше, является распространенным методом лечения типичного трепетания предсердий. В настоящее время врачи используют кончики электродов, размещая их перпендикулярно ткани во время трепетания и перетаскивая кончики над тканью для выполнения линейной абляции. Настоящее изобретение позволит врачу располагать кончик электрода параллельно ткани над ней одним вытягивающим движением.
Трепетание предсердий возникает, когда нормальные электрические импульсы, генерируемые синусно-предсердным узлом, заглушаются дезорганизованными электрическими импульсами, возникающими в предсердных и легочных венах, в результате чего беспорядочные импульсы проводятся к желудочкам. Возникает беспорядочное сердцебиение, которое может продолжаться от нескольких минут до нескольких недель или даже лет. Мерцательная аритмия предсердий (МАП) часто представляет собой хроническое заболевание, приводящее к небольшому увеличению риска летального исхода, часто в результате инфаркта. Риск увеличивается с возрастом. МАП в той или иной степени встречается приблизительно у 8% людей в возрасте более 80 лет. Мерцательная аритмия предсердий часто проходит бессимптомно и сама по себе в целом не представляет угрозы для жизни, однако может вызывать учащенное сердцебиение, слабость, головокружение, боли в груди и застойную сердечную недостаточность. Риск инфаркта при МАП возрастает, поскольку кровь может накапливаться и образовывать сгустки в плохо сокращающихся предсердиях и в ушке левого предсердия. Первым подходом к лечению МАП является медикаментозная терапия, которая либо замедляет частоту сердечных сокращений, либо возвращает сердечный ритм к нормальным показателям. Кроме того, пациентам с МАП часто даются антикоагулянты для защиты от инфаркта. Применение антикоагулянтов создает опасность внутренних кровотечений. Для некоторых пациентов медикаментозная терапия оказывается недостаточной, и предсердная аритмия является устойчивой к лекарствам, т.е. неизлечимой обычными фармакологическими средствами. Для прекращения МАП и возврата к нормальному сердечному ритму может применяться электроимпульсная терапия синхронизированными электрическими разрядами. Как вариант, у пациентов с МАП может применяться катетерная абляция. Однако такая абляция не всегда оказывается успешной. Следовательно, существует потребность в альтернативном способе лечения таких пациентов. Одним из вариантов является хирургическая абляция, однако этот вариант связан с традиционными рисками хирургического вмешательства.
Диагностика и лечение аритмий сердца включает картирование электрических свойств ткани сердца, в особенности эндокарда и объема сердца, и селективную абляцию ткани сердца путем воздействия энергией. Абляция может остановить или изменить распространение нежелательных электрических сигналов из одной части сердца в другую. В процессе абляции происходит разрушение нежелательных путей прохождения электрического сигнала с образованием непроводящих разрушенных участков. Известны различные способы подачи энергии для создания разрушенных участков, они включают использование микроволновой, лазерной и чаще всего радиочастотной энергии для создания блоков проводимости ткани стенки сердца. В ходе процедуры, проводимой в два этапа (с последующей абляцией), как правило, регистрируется и измеряется электрическая активность в точках внутри сердца путем введения в полости сердца катетера, содержащего один или более электрических датчиков (или электродов), и получения данных во множестве точек. Полученные данные затем используются для определения целевых областей эндокарда, в которых затем выполняется абляция.
Электродные катетеры широко применяются в медицинской практике в течение многих лет. Они используются для стимуляции и картирования электрической активности сердца, а также для абляции участков с нарушенной электрической активностью. На практике электродный катетер вводят в главную вену или артерию, например в бедренную артерию, а затем направляют в соответствующую камеру сердца. Стандартная процедура абляции включает введение в камеру сердца катетера с точечным электродом на дистальном конце. Также предусмотрен контрольный электрод, который, как правило, фиксируется на коже пациента или при помощи второго катетера, размещаемого в полости сердца или рядом с ним. Радиочастотный (РЧ) ток подается к точечному электроду абляционного катетера и проходит через окружающую среду, а именно через кровь и ткань, по направлению к контрольному электроду. Распределение тока зависит от величины поверхности электрода, входящей в контакт с тканью по сравнению с кровью, которая обладает более высокой электропроводностью, чем ткань. Нагревание ткани обусловлено ее удельным электрическим сопротивлением. Ткань нагревается в достаточной степени, чтобы вызвать разрушение клеток ткани сердца, в результате чего в ней формируется поврежденный участок, который не проводит электрический ток. В ходе этого процесса нагревание электрода также происходит в результате проведения возбуждения от нагретой ткани к электроду. Если температура электрода повышается значительно, предположительно выше 60°C, на поверхности электрода может образовываться тонкое прозрачное покрытие из дегидратированного белка крови. В случае, если температура продолжает повышаться, этот дегидратированный слой крови постепенно утолщается, что приводит к коагуляции крови на поверхности электрода. В силу того, что дегидратированный биологический материал обладает более высоким электрическим сопротивлением, чем ткань, сопротивление проникновению электрической энергии в ткань тоже возрастает. Если сопротивление значительно возрастает, происходит повышение сопротивления, в этом случае необходимо извлечь катетер из полости организма и очистить точечный электрод.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к катетеру и к способу лечения пациентов, в частности при лечении сердечных аритмий, таких как трепетание предсердий и мерцательная аритмия предсердий, с использованием абляционного катетера.
Изобретение, показанное в этом документе, относится к механизму двойного отклонения однократного действия, который стало возможным реализовать благодаря вытягивающему движению одной проволоки. Во время выполнения этого вытягивающего движения достигается одно проксимальное и одно дистальное отклонение. Катетер сконструирован с дистальной трубкой из нитинола, которая под воздействием сжимающей силы занимает желаемую ориентацию, что позволяет участку дистального кончика катетера отклоняться в дистальном направлении с помощью той же вытягивающей проволоки, которая отклоняет катетер в проксимальном направлении. В зависимости от активации единственной вытягивающей проволоки проксимальное отклонение избирательно находится либо в том же направлении, что и дистальное отклонение, либо отклоняется в противоположном направлении. Внутри гибкой конструкции наконечника вытягивающая проволока крепится к купольному электроду, проходит в проксимальном направлении через трубку из нитинола и выходит через противоположный конец трубки. В одном предпочтительном варианте осуществления каждая вытягивающая проволока входит в просвет гибкого наконечника в поперечной ориентации, под углом 180° к якорю тяги (сторона гибкого наконечника, на которой будет формироваться проксимальная кривая). Вытягивающая проволока затем проходит вдоль длину катетера к фиксированной точке крепления, например, к поршню рукоятки. Таким образом, дистальный конец и проксимальный конец каждой вытягивающей проволоки закреплены в диаметрально противоположных положениях относительно друг друга. Конструкция катетера обеспечивает большую жесткость проксимальному участку и меньшую жесткость дистальному участку. Таким образом, сжимающее усилие, необходимое для свертывания нитиноловой трубки в то время, когда проволока вытягивается, может быть меньше сжимающего усилия, требуемого для отклонения гибкого наконечника, когда нужно, чтобы дистальная кривая отклонялась первой. При приложении большей вытягивающей силы врач будет использовать проксимальную кривую для доступа к стенкам правого предсердия, имея возможность управлять положением купольного электрода и перемещать его в процессе абляции. Абляционный катетер, используемый при данном способе, может содержать датчик местоположения, например магнитный датчик местоположения, способный дать информацию о местонахождении кончика абляционного катетера.
Использование одного механизма для выполнения двойного отклонения. Настоящее изобретение сводит к минимуму количество компонентов, необходимых для достижения результата. Катетер имеет уникально простую конструкцию, позволяющую быстро выполнять двойное отклонение. Еще одной особенностью катетера является его универсальность во время проведения процедур абляции.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Эти и другие особенности и преимущества настоящего изобретения будут более понятными на примере следующего подробного описания в сочетании с сопроводительными чертежами.
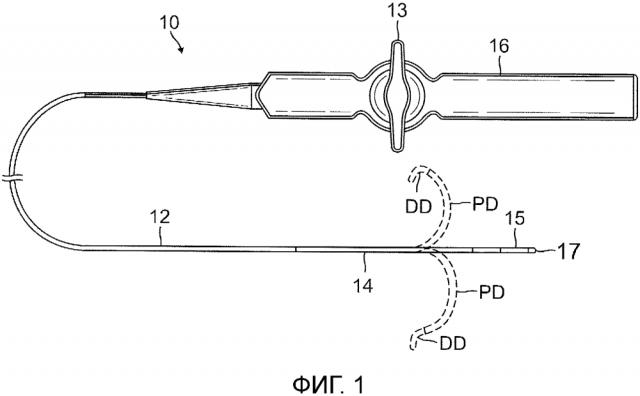
ФИГ. 1 показывает вид сверху катетера в соответствии с вариантом осуществления настоящего изобретения.
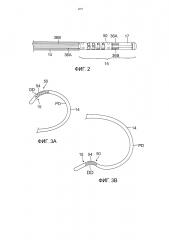
ФИГ. 2 показывает прозрачный вид участка дистального кончика катетера, показанного на ФИГ. 1, на котором видны вытягивающие проволоки и шарнирно-сочлененная трубка.
ФИГ. 3A показывает вид сверху катетера, показанного на ФИГ. 1, на котором изображено отклонение двойного действия, при котором промежуточная секция отклонена проксимально, а секция дистального кончика отклонена дистально в том же направлении.
ФИГ. 3B показывает вид сбоку катетера, показанного на ФИГ. 1, на котором изображено отклонение двойного действия, при котором промежуточная секция отклонена проксимально, а секция дистального кончика отклонена дистально в противоположном направлении.
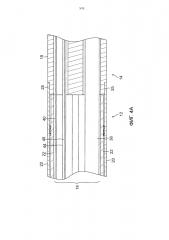
ФИГ. 4A представляет вид сбоку катетера, показанного на ФИГ. 1, показанного в поперечном сечении вдоль первого диаметра, включая соединение между корпусом катетера и промежуточной секцией.
ФИГ. 4B представляет вид сбоку в сечении катетера, изображенного на ФИГ. 1, включая соединение между корпусом катетера и промежуточной секцией, вдоль второго диаметра, по существу перпендикулярного первому диаметру.
ФИГ. 5A представляет вид сбоку катетера, показанного на ФИГ. 1, показанного в поперечном сечении вдоль первого диаметра, включая соединение между промежуточной секцией и секцией дистального кончика.
ФИГ. 5B представляет вид сбоку в сечении катетера, изображенного на ФИГ. 1, включая соединение между промежуточной секцией и секцией дистального кончика, вдоль второго диаметра, по существу перпендикулярного первому диаметру.
ФИГ. 6A представляет поперечный срез катетера, показанного на ФИГ. 5А и 5В в плоскости А-А.
ФИГ. 6B представляет поперечный срез катетера, показанного на ФИГ. 5А и 5В в плоскости B-B.
ФИГ. 6C представляет поперечный срез катетера, показанного на ФИГ. 5А и 5В в плоскости C-C.
ФИГ. 6D представляет поперечный срез катетера, показанного на ФИГ. 5А и 5В в плоскости D-D.
ФИГ. 7A представляет вид в перспективе шарнирно-сочлененной трубки в соответствии с вариантом осуществления настоящего изобретения.
ФИГ. 7B представляет еще один вид в перспективе шарнирно-сочлененной трубки, показанной на ФИГ. 7A.
ФИГ. 7C представляет вид сбоку шарнирно-сочлененной трубки, показанной на ФИГ. 7А, в вертикальном разрезе.
ФИГ. 7D представляет вид с торца шарнирно-сочлененной трубки, показанной на ФИГ. 7A.
ФИГ. 7E представляет вид сверху шарнирно-сочлененной трубки, показанной на ФИГ. 7А.
ФИГ. 7F представляет вид снизу шарнирно-сочлененной трубки, показанной на ФИГ. 7A.
ФИГ. 8 является схематической картинкой, иллюстрирующей медицинскую систему реализации данного изобретения, основанную на катетере.
ФИГ. 9 иллюстрирует секции катетера, показанного на ФИГ. 8, во время его использования в правом предсердии.
ФИГ. 10A является видом сверху катетера в соответствии с вариантом осуществления настоящего изобретения во время дистального отклонения.
ФИГ. 10B представляет вид в плане катетера в соответствии с вариантом осуществления настоящего изобретения, во время однонаправленного дистального отклонения (в положении полного отклонения) и во время двунаправленного проксимального отклонения (в положении частичного отклонения).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как показано на ФИГ. 1 и 2, изобретение, показанное и описанное в настоящем документе, относится к катетеру 10, имеющему удлиненный корпус катетера 12, промежуточную секцию 14 с двунаправленным отклонением, секцию гибкого дистального кончика 15 с однонаправленным отклонением и пару вытягивающих проволок 36A и 36B, причем катетер 10 предоставляет механизм двойного отклонения однократного действия, работа которого возможна благодаря вытягивающей силе одной проволоки. При выполнении этого действия достигается как отклонение промежуточной секции 14, так и отклонение секции дистального кончика 15 с помощью вытягивающего действия одной проволоки, приводимой в действие посредством отклоняющей ручки 13, при этом направление отклонения промежуточной секции 14 (или проксимальное отклонение PD) и направление отклонения дистальной секции 15 (или дистальное отклонение DD) могут совпадать (см. ФИГ. 3A) или быть противоположными (см. ФИГ. 3B), в зависимости от того, какую из вытягивающих проволок задействует пользователь. Конструкция секции гибкого дистального кончика 15 катетера имеет шарнирно-сочлененную трубку 50, адаптированную для сворачивания под воздействием сжимающего усилия в требуемую ориентацию, позволяя, таким образом, выполнять предопределенное однонаправленное дистальное отклонение DD и выборочное двунаправленное проксимальное отклонение PD.
Как изображено на ФИГ. 4A и 4B, корпус катетера 12 представляет собой продолговатую полую конструкцию с одним осевым или центральным просветом 18. Корпус катетера может быть гибким, т.е. сгибаемым, но практически не поддающимся сжатию по всей длине. Корпус катетера может иметь любую допустимую конструкцию и быть изготовленным из любого пригодного материала. Настоящая предпочтительная конструкция содержит наружную стенку 20, изготовленную из полиуретана или материала PEBAX. Наружная стенка включает в себя встроенную плетеную сетку из нержавеющей стали или подобного материала для повышения жесткости на скручивание корпуса катетера, так чтобы при вращении рукоятки управления 16 промежуточная секция 14 катетера поворачивалась соответствующим образом.
Внешний диаметр корпуса катетера не очень важен, но предпочтительно не превышает приблизительно 8 пунктов французского калибра, а более предпочтительно - 7 пунктов французского калибра. Аналогичным образом толщина наружной стенки не критична, однако она достаточно тонкая, чтобы центральный просвет мог вместить вытягивающие проволоки, токопроводящие проводники и любые другие желательные провода, кабели или трубки, такие как орошающие трубки. При желании внутренняя поверхность наружной стенки 20 покрыта упрочняющей трубкой 22 для обеспечения улучшенной устойчивости к скручиванию.
Компоненты, которые проходят между рукояткой управления 16 и отклоняемым участком 14, проходят через центральный просвет 18 корпуса катетера 12. Такими компонентами являются токопроводящие проводники 40 для концевого купольного электрода 17 (и любых кольцевых электродов 21), расположенных проксимально по отношению к концевому купольному электроду в дистальной секции 15, орошающий трубопровод 38 для доставки жидкости в дистальную секцию, вытягивающие проволоки 36А и 36В для выполнения проксимального и дистального отклонения и пара проводов термопар 44 и 45 для контроля температуры секции дистального участка 15.
На ФИГ. 4A и 4B проиллюстрирован вариант осуществления промежуточной секции 14, которая содержит короткую секцию трубки 19. Трубка также снабжена плетеной сеткой с множеством внеосевых просветов, например просветы 26, 27, 28 и 29. Первый просвет 26 вмещает токопроводящие проводники 40 концевого и кольцевого электродов 17 и 21. Второй просвет 27 вмещает орошающую трубку 38. Каждый из диаметрально противоположных - третий и четвертый просвет 28 и 29 вмещает вытягивающие проволоки 36A и 36B. Трубка 19 промежуточного участка 14 изготовлена из подходящего нетоксичного материала, более гибкого, чем корпус катетера 12. Подходящим материалом для трубки 19 является оплетенный полиуретан, т.е. полиуретан со встроенной сеткой из оплетенной нержавеющей стали или т.п. Размер каждого просвета не критичен, но он достаточен для того, чтобы вместить соответствующие компоненты, проходящие через него.
Средство для прикрепления корпуса катетера 12 к промежуточной секции 14 представлено на ФИГ. 4A и 4B. Проксимальный конец промежуточной секции 14 содержит внешнюю круговую прорезь 25, которая принимает внутреннюю поверхность наружной стенки 20 корпуса катетера 12. Промежуточный участок 14 и корпус катетера 12 прикреплены с помощью клея или т.п. При желании в корпусе катетера между дистальным концом упрочняющей трубки (при наличии) и проксимальным концом промежуточного участка может быть размещен разделитель (не показан). Разделитель обеспечивает гибкий переход в месте соединения корпуса катетера и промежуточного участка, что позволяет этому соединению плавно изгибаться без образования складок или перекручивания. Катетер, имеющий такой разделитель, описан в патенте США № 5964757, содержание которого включено в настоящий документ путем ссылки.
Каждая вытягивающая проволока 36A и 36B предпочтительно покрыта материалом Teflon.RTM. Они могут быть изготовлены из любого подходящего металла, такого как нержавеющая сталь или нитинол, а тефлоновое покрытие придает вытягивающей проволоке смазывающие свойства. Предпочтительный диаметр каждой вытягивающей проволоки находится в диапазоне от приблизительно 0,15 мм до приблизительно 0,25 мм (от приблизительно 0,006 дюйма до приблизительно 0,010 дюйма).
Как показано на ФИГ. 4B, часть каждой вытягивающей проволоки в корпусе катетера 12 проходит сквозь соответствующую компрессионную обмотку 35А и 35В, причем компрессионные обмотки окружают проволоки. Каждая компрессионная обмотка 35 проходит от проксимального конца корпуса катетера 12 до проксимального конца промежуточной секции 14 или рядом с ним. Компрессионные обмотки изготовлены из любого подходящего металла, предпочтительно из нержавеющей стали, и плотно намотаны для обеспечения гибкости, т.е. способности к изгибу, но с сопротивлением сжатию. Внутренний диаметр компрессионной обмотки предпочтительно незначительно превышает диаметр вытяжной проволоки. В корпусе катетера 12 внешняя поверхность каждой компрессионной обмотки также покрыта гибкой непроводящей оболочкой 39A и 39B, например, выполненной из полиимидной трубки. Часть каждой вытягивающей проволоки, расположенная дистально относительно компрессионной обмотки, может проходить через защитную пластиковую оболочку (не показана на фигурах), выполненную, например, из материала TEFLON.RTM, для предотвращения врезания вытягивающей проволоки в трубку 19 промежуточной секции 14 в процессе отклонения. Проксимальные концы каждой вытяжной проволоки зафиксированы в рукоятке управления 16. Дистальные концы прикреплены к концевому купольному электроду 17, как детальнее описано ниже. Как показано на ФИГ. 5A и 5B, дистальный концевой участок 15 проходит от дистального конца трубки 19 промежуточного отклоняемого участка 14. Секция дистального кончика 15 включает в себя шарнирно-сочлененную трубку 50, имеющую полый цилиндрический корпус 51 с просветом 56, дистальный конец 51D, проксимальный конец 51P, длину L и диаметр D, как показано на ФИГ. 7A-7F. В соответствии с особенностью настоящего изобретения корпус имеет N поперечных прорезей 52, число которых определяет (N-1) множество шарниров 53 между ними, которые, как правило, перпендикулярны гребню 54, проходящему по всей длине корпуса. Каждый паз 52 (или шарнир 53) имеет аналогичную глубину d и ширину w. В показанном на ФИГ. 7С варианте осуществления ширина w каждой прорези возрастает с увеличением глубины d (иными словами ширина w каждого шарнира уменьшается с увеличением глубины d). Прорези 52 вырезаны или сформированы с помощью электроэрозионной обработки (ЭЭО) или лазерной обработки. Подходящим материалом для изготовления трубки является металл и металлические сплавы, например, нитинол.
В показанном варианте осуществления трубка 50 имеет длину в пределах между приблизительно 5,08 и 25,4 мм (между приблизительно 0,2 и 1,0 дюймами) с четырьмя прорезями (или тремя шарнирами). Преимущественно, конфигурация или «шаг» прорезей 52 и шарниров 53 (в том числе количество, угловой поворот, ширина и глубина) позволяют трубке 50 отклоняться предопределенным образом в направлении от гребня 54 под воздействием сжимающего усилия, независимо от любого другого направления отклонения вдоль катетера. При сжатии шарнирно-сочлененная трубка 50 позволяет дистальному концу 51D отклоняться в направлении от гребня на 0-90 градусов по отношению к проксимальному концу 51P (см. ФИГ. 3A и 3B).
На ФИГ. 5А и 5В трубка 50 покрыта непроводящей трубкой 55, которая простирается между дистальным концом трубки 19 и проксимальным концом концевого купольного электрода 17. Трубка 55 может быть изготовлена из термопластичного материала, который может быть нагрет и расплавлен для соединения с трубкой 50. В этой связи, в проксимальном и дистальном концах 51P и 51D трубки предусмотрены полые отверстия 57 для формирования узлов 59, которые крепят трубку 55 к трубке 50. В качестве альтернативы может применяться клей или другие клеящие вещества между трубкой 55 и трубкой 50 с образованием узлов, которые крепят трубку 55 к трубке 50.
От полостей промежуточной отклоняющейся секции и через просвет 56 полого корпуса 51 трубки 50 проходят подводящие провода 40 концевого электрода 17, провода термопары 44 и 45, орошающая трубка 38 и вытягивающие проволоки 36А и 36B. Эти компоненты проходят далее в концевой купольный электрод 17.
Проксимальный конец концевого купольного электрода 17 подрезан так, чтобы в него вмещался дистальный конец трубки 50. Дистальный конец трубки 55 плотно прилегает к подрезанному проксимальному концу концевого купольного электрода 17, чтобы обеспечить плавный профиль, как показано на ФИГ. 5А и 5В. Проксимальная поверхность концевого купольного электрода 17 имеет центральный проход 58, в который входит дистальный конец орошающей трубки 38. Проход 58 проходит в осевом направлении через концевой купольный электрод 17 и связывается с поперечными ветвями 60, которые связаны с отверстиями орошения 62, ведущими за пределы конечного купольного электрода 17. Жидкость, транспортируемая через орошающую трубку 38, поступает к концевому купольному электроду 17 с наружной его стороны, через проход 58, поперечные ветви 60 и отверстия 62.
Катетер может также иметь улучшенный поток орошения через концевой абляционный электрод для использования в способе по настоящему изобретению. Более подробно данный катетер описывается в заявке на патент США № 12/770582, поданной 29 апреля 2010 года, которая включена в настоящий документ путем ссылки. Точечный электрод выполнен с возможностью продвижения жидкости к точечному электроду и ее дисперсии в этой зоне для более полного охвата зоны и растекания во всех направлениях по внешней поверхности точечного электрода. Катетер, следовательно, работает при более низких скоростях потока с низкой нагрузкой жидкости на пациента, обеспечивая улучшенное охлаждение концевого электрода, чем использовалось для электродов предыдущего уровня техники. Кроме того, высокая скорость жидкости на выходе из точечного электрода обеспечивает «выброс струей», благодаря чему формируется пограничный слой жидкости вокруг точечного электрода, что снижает частоту образования нагара и (или) тромбов в процессе абляции. Жидкость, например физиологический раствор или гепаринизированный физиологический раствор, доставляют к месту абляции через точечный электрод для охлаждения ткани, снижения коагуляции и (или) упрощения формирования более глубоких поврежденных участков. Необходимо понимать, что таким же образом могут доставляться любые другие жидкости, в том числе диагностические или лекарственные жидкости, такие как нейроингибиторы и нейростимуляторы.
Проксимальная поверхность концевого купольного электрода 17 также имеет множество глухих отверстий, в том числе глухое отверстие 64 для приема дистального конца провода концевого электрода 40 и глухое отверстие 66 для дистальных концов проводов термопары 44 и 45. Есть также глухие отверстия 68 и 70, в которых закреплены дистальные концы вытягивающих проволок 36А и 36B.
Закрепленные таким образом вытягивающие проволоки 36A и 36B могут по отдельности приводиться в действие пользователем посредством манипулирования отклоняющей ручки 13 (см. ФИГ. 1) на рукоятке управления 16, чтобы приложить осевое усилие к вытягивающей проволоке для изначального отклонения секции дистального конца 15 в дистальное отклонение DD в направлении от гребня 54 под воздействием меньшей силы приведения в действие и последующего отклонения промежуточной секции 14 в проксимальное отклонение PD под воздействием большей силы приведения в действие либо в том же направлении (см. ФИГ. 3A), либо в противоположном направлении (см. ФИГ. 3B). Следует отметить, что для того, чтобы секция дистального конца 15 отклонялась раньше промежуточной секции 14 при вытягивании вытягивающей проволоки в проксимальном направлении, дистальная секция 15 (с трубкой 50) имеет меньшую жесткость, а промежуточная секция 14 имеет большую жесткость, таким образом, сила сжатия, требуемая для сворачивания нитиноловой трубки 50, меньше, чем сила, требуемая для отклонения промежуточной секции 14. Проксимальное отклонение PD облегчает доступ к правому предсердию сердца для оператора катетера, а также предоставляет оператору улучшенный контроль движения концевого купольного электрода в процессе абляции.
Глухие отверстия 68 и 70 для закрепления дистальных концов вытягивающих проводов в концевом купольном электроде 17 диаметрально противоположны и лежат, как правило, в той же плоскости, определяемой диаметрально противоположными третьим и четвертым просветами 28 и 29 промежуточной секции 14, через которые проходят вытягивающие проволоки 36А и 36B. Несмотря на то, что вытягивающие проволоки 36А и 36B могут оставаться на их соответствующей стороне катетера так, чтобы быть соосными с их соответствующими просветами в трубке 19 при прохождении через трубку 50 в концевой купольный электрод, особенность настоящего изобретения обеспечивает поперечное расположение под углом 180 градусов вытягивающих проволок с одной стороны трубки 50 к другой стороне трубки 50 таким образом, что дистальный конец каждой вытягивающей проволоки закреплен диаметрально противоположно от проксимального конца этой вытягивающей проволоки. Это перекрестное расположение предпочтительно поддерживает отклонение секции дистального конца 15 «в плоскости» за счет уменьшения тенденции к скручиванию секции дистального конца во время отклонения.
Эта нитиноловая трубка и связанный с нею механизм позволит секции кончика быть ориентированной параллельно ткани одним действием, отклоняющим кончик.
Секция дистального кончика 15 катетера 10 обеспечивает много привилегий и преимуществ, в том числе контролируемое угловое отклонение, в том числе проксимальное отклонение и дистальное отклонение, одним действием при приложении очень малого усилия, необходимого для отклонения дистального конца, связанного с выполнением двух отклонений в рамках единого механизма.
Другие варианты осуществления включают в себя использование секционного плоского лезвия в том же самом положении, в котором трубка 50 расположена в рамках этой концепции.
Эта концепция может быть использована с орошаемым или неорошаемым концевым купольным электродом.
Эта концепция может быть также использована в сочетании с датчиком навигации (магнитный датчик), который будет размещен ниже нитиноловой трубки, чтобы избежать экранирования.
ФИГ. 8 представляет собой схематичную наглядную иллюстрацию традиционной системы 120, предназначенной для проведения катетеризации сердца, известную в данной области техники. Система 120 может быть основана, например, на системе CARTO.TM., которую производит Biosense Webster Inc. (Diamond Bar, Calif.). Данная система содержит инвазивный зонд, имеющий форму катетера 128, и панель управления 134. В варианте осуществления, описанном ниже в настоящем документе, предполагается, что катетер 128 используется для разрушения ткани эндокарда способом, известным специалисту в данной области. В альтернативном варианте соответственно измененный катетер может быть использован для других лечебных или диагностических целей в сердце или другом органе тела. Как изображено на ФИГ. 7, катетер 28 состоит из удлиненного корпуса катетера 11, отклоняемого промежуточного сегмента 12, дистального сегмента 13, несущего как минимум концевой электрод 15 на своем периферическом конце 30, а также рычага управления 16.
Оператор 126, такой как интервенционный кардиолог или электрофизиолог, вводит катетер 128 по настоящему изобретению через сосудистую систему пациента таким образом, что дистальный конец катетера попадает в камеру сердца пациента, как показано на ФИГ. 9. Оператор продвигает катетер вперед настолько, чтобы дистальный кончик катетера вошел в зацепление с эндокардиальной тканью в желательном местонахождении, включая правое предсердие, как показано на ФИГ. 130. Катетер, как правило, подсоединяют с помощью подходящего соединителя на его проксимальном конце к консоли. Консоль 134 может включать в себя радиочастотный (РЧ) генератор, который подает высокочастотную электрическую энергию через катетер для абляции ткани сердца в местах контакта с дистальной секцией 15. Как вариант, катетер и система могут быть выполнены с возможностью проведения абляции иными способами, известными в данной области, например криоабляции, ультразвуковой абляции или абляции при помощи микроволновой энергии.
Консоль 134 может также использовать магнитное обнаружение положения для определения координат положения дистального конца внутри сердца пациента. Для этой цели возбуждающий контур 138 консоли 134 приводит в действие генераторы поля F1, F2 и F3, которые создают магнитные поля внутри тела пациента. Как правило, генераторы поля представляют собой катушки, размещенные ниже туловища пациента в строго определенных местах, находящихся вне тела пациента. Эти катушки генерируют магнитные поля заданной величины, распространяющиеся на сердце. Датчик магнитного поля, вмонтированный в дистальный конец катетера под действием магнитного поля, генерирует электрические сигналы. Процессор обрабатывает эти сигналы и определяет координаты положения (как правило, места и ориентации) дистального конца 15. Данный способ определения положения реализован в упомянутой выше системе CARTO и детально описан в патентах США №№ 5391199, 6690963, 6484118, 6239724, 6618612 и 6332089, в патентной публикации PCT WO 96/05768 и в опубликованных заявках на патент США №№ 2002/0065455 A1, 2003/0120150 A1 и 2004/0068178 A1, описания которых полностью включены в настоящий документ путем ссылки.
Процессор системы, как правило, содержит компьютер общего назначения 136 со средствами предварительной обработки и интерфейсами, подходящими для приема сигналов с катетера и контроля других компонентов консоли. Для осуществления описанных в настоящем документе функций процессор может быть снабжен специальным программным обеспечением. Программу можно загрузить в панель управления в электронной форме по сети или с носителей, например оптических, магнитных или электронных устройств памяти. В другом варианте осуществления изобретения некоторые или все функции процессора 136 осуществляются специализированными или программируемыми компонентами цифровых аппаратных средств. С учетом сигналов, получаемых от катетера и других компонентов системы, процессор управляет дисплеем, позволяя оператору визуально контролировать положение дистального конца катетера в теле пациента, а также получать информацию о состоянии и инструкции, относящиеся к производимой процедуре.
Как показано на ФИГ. 8, концевой купольный электрод 17 находится в контакте с тканью в правом предсердии 130 путем манипуляций с катетером, проводимых с помощью поворотной ручки 13 рукоятки управления 16 (см. ФИГ. 1), с помощью которого оператор 126 вытягивает выбранную вытягивающую проволоку, прилагая начальную силу, чтобы отклонить сначала секцию дистального конца 15 в дистальное отклонение DD в направлении от гребня 54 нитиноловой трубки 50