Новые аналоги сс-1065 и их конъюгаты
Иллюстрации
Показать всеИзобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, где DB является ДНК-связывающей группой и представляет собой группу DB6; R1 представляет собой хлор; R2, R2', R3, R3', R4, R4', R12 и R19 представляют собой Н; X2 выбран из С(R14)(R14'), где R14 имеет то же значение, которое определено для R7 и выбрано независимо, и R14' и R7' отсутствуют, что дает двойную связь между атомами, несущими R7' и R14'; R5, R6 и R7 независимо выбраны из Н, Re, где Re выбран из C1алкила, и R5'+R6' отсутствуют, что дает двойную связь между атомами, несущими R5' и R6'; X1 выбран из О; X3 выбран из S, N и NR15; X4 выбран из N и CR16; X5 выбран из О; X6* выбран из CR11; X7 выбран из CR8, N; X8 выбран из CR9, N; X9* выбран из CR10; X10* выбран из CR20; X11* выбран из С; X7* и X8* имеют те же значения, которые определены для X7 и X8 соответственно и выбраны независимо; X34 выбран из С; кольцевой атом В в X11* в DB6 соединен с кольцевым атомом кольца А таким образом, что кольцо А и кольцо В в DB6 непосредственно связаны через прямую связь; подразумевает, что указанная связь может быть прямой связью или некумулированной, необязательно делокализованной двойной связью; R8, R9, R10, R11, R15, R16, R20 каждый, независимо, выбраны из Н, N(Rh)C(O)Ri, где Rh, Ri независимо выбраны из Н и необязательно замещенного С6арила, один необязательный заместитель в Ri представляет собой -ОН или -NH2; а представляет собой 0 и b представляет собой 1. Изобретение относится к фармацевтической композиции для лечения или профилактики опухоли у млекопитающего, содержащей терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель. Технический результат – аналоги ДНК-алкилирующего средства СС-1065. 2 н. и 4 з.п. ф-лы, 13 ил., 1 табл., 23 пр.
,
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым аналогам ДНК-алкилирующего средства CC-1065 и их конъюгатам. Кроме того, настоящее изобретение относится к промежуточным соединениям для получения указанных средств и конъюгатов. Конъюгаты предназначены для высвобождения своей (множественной) эффективной части после одной или нескольких стадий активации и/или со скоростью и в интервале времени, контролируемом конъюгатом, для селективной доставки и/или контролируемого высвобождения одного или нескольких указанных ДНК-алкилирующих средств. Средства, конъюгаты и промежуточные соединения можно использовать для лечения заболеваний, отличающихся нежелаемой (клеточной) пролиферацией. Например, средства и конъюгаты по настоящему изобретению можно использовать для лечения опухолей.
УРОВЕНЬ ТЕХНИКИ
Дуокармицины, которые впервые были выделены из культурального бульона вида Streptomyces, являются представителями семейства противоопухолевых антибиотиков, к которому также относится CC-1065. Эти чрезвычайно эффективные вещества, по-видимому, проявляют свою биологическую активность благодаря способности селективно алкилировать последовательность ДНК на N3 аденина малой борозды, что запускает каскад событий, приводящих к запуску механизма апоптической гибели клеток.1
Хотя CC-1065 показал очень сильную цитотоксичность, он не мог быть использован в клинике вследствие значительной замедленной гепатотоксичности.2 Это наблюдение привело к разработке синтетических аналогов CC-1065 (см. производные CC-1065, например, Aristoff et al., J. Org. Chem. 1992, 57, 6234; Boger et al., Bioorg. Med. Chem. Lett. 1996, 6, 2207; Boger et al., Chem. Rev. 1997, 97, 787; Milbank et al., J. Med. Chem. 1999, 42, 649; Atwell et al., J. Med. Chem. 1999, 42, 3400; Wang et al., J. Med. Chem. 2000, 43, 1541; Boger et al., Bioorg. Med. Chem. Lett 2001, 11, 2021; Parrish et al., Bioorg. Med. Chem. 2003, 11, 3815; Daniell et al., Bioorg. Med. Chem. Lett. 2005, 15, 177; Tichenor et al., J. Am. Chem. Soc. 2006, 128, 15683; Purnell et al., Bioorg. Med. Chem. 2006, 16, 5677; Bando and Sugiyama, Acc. Chem. Res. 2006, 39, 935; Tichenor et al., Nat. Prod. Rep. 2008, 25, 220; MacMillan et al., J. Am. Chem. Soc. 2009, 131, 1187; Tietze et al., Anti-Cancer Agents Med. Chem. 2009, 9, 304; Gauss et al., Tetrahedron 2009, 65, 6591; EP 0154445; WO 88/04659; WO 90/02746; WO 97/12862; WO 97/32850; WO 97/45411; WO 98/52925; WO 99/19298; WO 01/83482; WO 02/067937; WO 02/067930; WO 02/068412; WO 03/022806; WO 2004/101767; WO 2006/043839, и WO 2007/051081), которые обычно показывают аналогичную цитотоксичность, но пониженную гепатотоксичность. Тем не менее, эти производные все еще не обладают достаточной селективностью в отношении опухолевых клеток, поскольку селективность этих средств - и цитотоксических средств вообще - некоторым образом базируется на различии в скорости пролиферации опухолевых и нормальных клеток, и, соответственно, они также оказывают воздействие на здоровые клетки, которые демонстрируют относительно высокую скорость пролиферации. Это обычно приводит к тяжелым побочным эффектам. Концентрации лекарственного средства, которые полностью ликвидировали бы опухоль, не могут быть достигнуты из-за ограничивающих дозу побочных эффектов, таких как токсичность в отношении желудочно-кишечная тракта и костного мозга. Кроме того, опухоли могут развить резистентность к средствам против злокачественных опухолей после длительного лечения. Таким образом, при разработке современных лекарственных средств, нацеливание цитотоксических препаратов на участок опухоли можно рассматривать в качестве одной из основных задач.
В одном из перспективных подходов получения повышенной селективности в отношении опухолевых клеток или опухолевых тканей должно использоваться существование связанных с опухолью антигенов, рецепторов и других рецептивных элементов, которые могут служить в качестве цели. Такая цель может повысить контролируемость или до некоторой степени конкретно присутствовать в ткани опухоли или в близлежащей ткани, такой как неоваскулярная ткань, относительно других тканей для достижения эффективного нацеливания. Было идентифицировано и оценено большое количество целей, и было разработано несколько методов для идентификации и оценки целей.3 Путем связывания лиганда, например, антитела или фрагмента антитела, для такого связанного с опухолью антигена, рецептора или другого рецептивного элемента с терапевтическим средством, это средство может быть селективно нацелено на ткань опухоли.
Другой перспективный подход для достижения селективности в отношении опухолевых клеток или опухолевых тканей состоит в использовании наличия связанных с опухолью ферментов. Фермент, который локализован главным образом на участке опухоли, может преобразовать фармакологически неактивное пролекарство, которое состоит из ферментного субстрата, прямо или косвенно связанного с токсичным препаратом, в соответствующее лекарственное средство в области или в пределах опухоли. В этом методе высокая концентрация токсичного средства против злокачественной опухоли может быть селективно достигнута на участке опухоли. Если доза достаточно высока, все опухолевые клетки могут быть убиты, что может уменьшить распространение резистентных к лекарственным средствам опухолевых клеток.
Ферменты могут также быть транспортированы в окружающую область или в целевые клетки или ткани-мишени посредством, например, антитело-направленной ферментной пролекарственной терапии (ADEPT)4, полимер-направленной ферментной пролекарственной терапии (PDEPT) или макромолекула-направленной ферментной пролекарственной терапии (MDEPT)5, вирус-направленной ферментной пролекарственной терапии (VDEPT)6 или ген-направленной ферментной пролекарственной терапии (GDEPT)7. С помощью ADEPT, например, нетоксичное пролекарство селективно преобразуется в цитоксичное соединение на поверхности целевых клеток конъюгатом антитело-фермент, который был предварительно нацелен на поверхность этих клеток.
В еще одном перспективном подходе получения селективности в отношении опухолевых клеток или ткани опухоли используется эффект расширенной проницаемости и задержки (EPR). Посредством этого эффекта EPR макромолекулы пассивно накапливаются в твердых опухолях как следствие неорганизованной патологии ангиогенной сосудистой сети опухоли с ее прерывистым эндотелием, приводя к гиперпроницаемости для больших макромолекул и нехватке эффективного лимфатического дренажа опухоли.8 При связывании терапевтического средства напрямую или косвенно с макромолекулой, указанное средство может быть селективно нацелено на ткань опухоли.
Помимо эффективного нацеливания, другими важными критериями для успешного применения нацеленных конъюгатов цитотоксических средств в терапии опухоли являются такие, чтобы одно или несколько средств эффективно высвобождались из конъюгата на участке опухоли, и чтобы конъюгат являлся нецитотоксическим или только очень слабо цитотоксическим, тогда как само цитотоксическое средство демонстрирует очень сильную цитотоксичность. В идеальном случае это приводит к образованию цитотоксических молекул только на участке опухоли, что дает значительно увеличенный терапевтический индекс относительно ненацеленного цитотоксического средства. Другим важным критерием успешного нацеленного конъюгата является такой, чтобы у конъюгата были подходящие фармакологические свойства, такие как достаточная стабильность в кровотоке, тенденция к низкой агрегации и хорошая водорастворимость. Подходящая водорастворимость и гидрофильность лекарственного средства и/или линкера могут способствовать улучшению фармакологических свойств.
Некоторые конъюгаты CC-1065 и производные были описаны (см. конъюгаты производных CC-1065, например, Suzawa et al., Bioorg. Med. Chem. 2000, 8, 2175; Jeffrey et al., J. Med. Chem. 2005, 48, 1344; Wang et al., Bioorg. Med. Chem. 2006, 14, 7854; Tietze et al., Chem. Eur. J. 2007, 13, 4396; Tietze et al., Chem. Eur. J. 2008, 14, 2811; Tietze et al., ChemMedChem 2008, 3, 1946; Li et al., Tetrahedron Lett. 2009, 50, 2932; WO 91/16324; WO 94/04535; WO 95/31971; US 5475092; US 5585499; US 5646298; WO 97/07097; WO 97/44000; US 5739350; WO 98/11101; WO 98/25898; US 5843937; US 5846545; WO 02/059122; WO 02/30894; WO 03/086318; WO 2005/103040; WO 2005/112919; WO 2006/002895; WO 2006/110476; WO 2007/038658; WO 2007/059404; WO 2008/083312; WO 2008/103693; WO 2009/026274, и WO 2009/064908). В этих конъюгатах одно или несколько рассмотренных выше благоприятных свойств могут быть неоптимальными.
Соответственно все еще существует очевидная потребность в конъюгатах производных CC-1065, которые демонстрировали бы высокие показатели цитотоксичности (то есть IC50, конъюгат/IC50, исходное лекарственное средство), содержали производные CC-1065, обладающие сильной цитотоксичностью и благоприятными фармакологическими свойствами, и эффективно высвобождали производные CC-1065.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
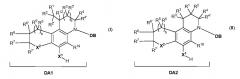
Настоящее изобретение удовлетворяет вышеуказанную потребность и относится к соединению формулы (I) или (II):
,
или к его фармацевтически приемлемой соли, гидрату или сольвату, где
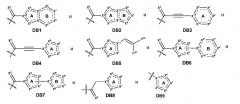
DB представляет собой ДНК-связывающую группу и выбран из группы, состоящей из
;
R1 представляет собой удаляемую группу;
R2, R2', R3, R3', R4, R4', R12 и R19 независимо выбраны из H, OH, SH, NH2, N3, NO2, NO, CF3, CN, C(O)NH2, C(O)H, C(O)OH, галогена, Ra, SRa, S(O)Ra, S(O)2Ra, S(O)ORa, S(O)2ORa, OS(O)Ra, OS(O)2Ra, OS(O)ORa, OS(O)2ORa, ORa, NHRa, N(Ra)Rb, +N(Ra)(Rb)Rc, P(O)(ORa)(ORb), OP(O)(ORa)(ORb), SiRaRbRc, C(O)Ra, C(O)ORa, C(O)N(Ra)Rb, OC(O)Ra, OC(O)ORa, OC(O)N(Ra)Rb, N(Ra)C(O)Rb, N(Ra)C(O)ORb и N(Ra)C(O)N(Rb)Rc, где
Ra, Rb и Rc независимо выбраны из H и необязательно замещенного C1-3алкила или C1-3гетероалкила,
или R3+R3' и/или R4+R4' независимо выбраны из =O, =S, =NOR18, =C(R18)R18' и =NR18, R18 и R18' независимо выбраны из H и необязательно замещенного C1-3алкила, два или более R2, R2', R3, R3', R4, R4' и R12 необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов;
X2 выбран из O, C(R14)(R14') и NR14', где R14 и R14' имеют такое же значение, как определено для R7, и выбраны независимо, или R14' и R7' отсутствуют, что дает двойную связь между атомами, которые, как предусмотрено, несут R7' и R14';
R5, R5', R6, R6', R7 и R7' независимо выбраны из H, OH, SH, NH2, N3, NO2, NO, CF3, CN, C(O)NH2, C(O)H, C(O)OH, галогена, Re, SRe, S(O)Re, S(O)2Re, S(O)ORe, S(O)2ORe, OS(O)Re, OS(O)2Re, OS(O)ORe, OS(O)2ORe, ORe, NHRe, N(Re)Rf, +N(Re)(Rf)Rg, P(O)(ORe)(ORf), OP(O)(ORe)(ORf), SiReRfRg, C(O)Re, C(O)ORe, C(O)N(Re)Rf, OC(O)Re, OC(O)ORe, OC(O)N(Re)Rf, N(Re)C(O)Rf, N(Re)C(O)ORf, N(Re)C(O)N(Rf)Rg и водорастворимой группы, где
Re, Rf и Rg независимо выбраны из H и необязательно замещенного (CH2CH2O)eeCH2CH2X13Re1, C1-15алкила, C1-15гетероалкила, C3-15циклоалкила, C1-15гетероциклоалкила, C5-15арила или C1-15гетероарила, где ee равен 1-1000, X13 выбран из O, S и NRf1, и Rf1 и Re1 независимо выбраны из H и C1-3алкила, один или несколько необязательных заместителей Re, Rf и/или Rg необязательно являются водорастворимой группой, два или более Re, Rf и Rg необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов,
или R5+R5' и/или R6+R6' и/или R7+R7' независимо выбраны из =O, =S, =NORe3, =C(Re3)Re4 и =NRe3, Re3 и Re4 независимо выбраны из H и необязательно замещенного C1-3алкила, или R5'+R6' и/или R6'+R7' и/или R7'+R14' отсутствуют, что дает двойную связь между атомами, которые определены как несущие R5' и R6' и/или R6' и R7' и/или R7' и R14', соответственно, два или более из R5, R5', R6, R6', R7, R7', R14 и R14' необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов;
X1 выбран из O, S, и NR13, где R13 выбран из H и необязательно замещенного C1-8алкила или C1-8гетероалкила и не соединены с другими заместителями;
X3 выбран из O, S, C(R15)R15', -C(R15)(R15')-C(R15'')(R15''')-, -N(R15)-N(R15')-, -C(R15)(R15')-N(R15'')-, -N(R15'')-C(R15)(R15')-, -C(R15)(R15')-O-, -O-C(R15)(R15')-, -C(R15)(R15')-S-, -S-C(R15)(R15')-, -C(R15)=C(R15')-, =C(R15)-C(R15')=, -N=C(R15')-, =N-C(R15')=, -C(R15)=N-, =C(R15)-N=, -N=N-, =N-N=, CR15, N и NR15, или в DB1 и DB2 -X3- представляет собой -X3a и X3b-, где X3a соединен с X34, двойная связь присутствует между X34 и X4, и X3b соединен с X11, где X3a независимо выбран из H и необязательно замещенного (CH2CH2O)eeCH2CH2X13Re1, C1-8алкила или C1-8гетероалкила и не соединен с другими заместителями;
X4 выбран из O, S, C(R16)R16', NR16, N и CR16;
X5 выбран из O, S, C(R17)R17', NOR17 и NR17, где R17 и R17' независимо выбраны из H и необязательно замещенного C1-8алкила или C1-8гетероалкила и не соединены с другими заместителями;
X6 выбран из CR11, CR11(R11'), N, NR11, O и S;
X7 выбран из CR8, CR8(R8'), N, NR8, O и S;
X8 выбран из CR9, CR9(R9'), N, NR9, O и S;
X9 выбран из CR10, CR10(R10'), N, NR10, O и S;
X10 выбран из CR20, CR20(R20'), N, NR20, O и S;
X11 выбран из C, CR21 и N, или X11-X3b выбран из CR21, CR21(R21'), N, NR21, O и S;
X12 выбран из C, CR22 и N;
X6*, X7*, X8*, X9*, X10* и X11* имеют те же значения, которые определены для X6, X7, X8, X9, X10 и X11, соответственно, и выбраны независимо;
X34 выбран из C, CR23 и N;
атом X11* кольца B в DB6 и DB7 соединен с кольцевым атомом кольца A так, что кольцо A и кольцо B в DB6 и DB7 напрямую соединены через прямую связь;
означает, что указанная связь может быть одинарной связью или неаккумулированной, необязательно делокализованной, двойной связью;
каждый R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22 и R23 независимо выбран из H, OH, SH, NH2, N3, NO2, NO, CF3, CN, C(O)NH2, C(O)H, C(O)OH, галогена, Rh, SRh, S(O)Rh, S(O)2Rh, S(O)ORh, S(O)2ORh, OS(O)Rh, OS(O)2Rh, OS(O)ORh, OS(O)2ORh, ORh, NHRh, N(Rh)Ri, +N(Rh)(Ri)Rj, P(O)(ORh)(ORi), OP(O)(ORh)(ORi), SiRhRiRj, C(O)Rh, C(O)ORh, C(O)N(Rh)Ri, OC(O)Rh, OC(O)ORh, OC(O)N(Rh)Ri, N(Rh)C(O)Ri, N(Rh)C(O)ORi, N(Rh)C(O)N(Ri)Rj и водорастворимой группы, где
Rh, Ri и Rj независимо выбраны из H и необязательно замещенного (CH2CH2O)eeCH2CH2X13Re1, C1-15алкила, C1-15гетероалкила, C3-15циклоалкила, C1-15гетероциклоалкила, C5-15арила или C1-15гетероарила, один или несколько необязательных заместителей в Rh, Ri и/или Rj необязательно являются водорастворимой группой, два или более из Rh, Ri и Rj необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов,
или R8+R8' и/или R9+R9' и/или R10+R10' и/или R11+R11' и/или R15+R15' и/или R15''+R15''' и/или R16+R16' и/или R20+R20' и/или R21+R21' независимо выбраны из =O, =S, =NORh1, =C(Rh1)Rh2 и =NRh1, Rh1 и Rh2 независимо выбраны из H и необязательно замещенного C1-3алкила, два или более из R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22 и R23 необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов;
R8b и R9b выбраны независимо и имеют те же значения, которые определены для R8, кроме того, что они не могут быть связаны с другими заместителями;
один из R4 и R4' и один из R16 и R16' могут быть необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов;
один из R2, R2', R3, и R3' и один из R5 и R5' могут быть необязательно соединены одной или несколькими связями с образованием одного или нескольких необязательно замещенных карбоциклов и/или гетероциклов; и
a и b независимо равны 0 и 1.
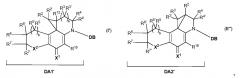
В другом аспекте настоящее изобретение относится к соединению формулы (I') или (II'):
которое образуется путем перегруппировки и одновременного удаления H-R1 из соответствующих соединений формулы (I) и (II), которые являются seco соединениями (фиг. 1). Указанные аналоги, содержащие циклопропильное кольцо, вероятно, являются активными видами, которые, по-видимому, образуются in vivo из соединений формул (I) и (II) путем указанной перегруппировки.
В более конкретном варианте осуществления настоящее изобретение относится к соединению формулы (I) или (II), как описано выше в настоящем документе, где
a) группа DB не содержит группу DA1, DA2, DA1' или DA2'; и
b) кольцо B в DB1 является гетероциклом; и
c) если X3 в DB1 представляет собой -X3a и X3b-, а кольцо B является ароматическим, то два соседних заместителя на указанном кольце B объединены с образованием необязательно замещенного карбоцикла или гетероцикла, конденсированного с указанным кольцом B; и
d) если X3 в DB2 представляет собой -X3a и X3b-, а кольцо B является ароматическим, то два соседних заместителя на указанном кольце B объединены с образованием необязательно замещенного гетероцикла, конденсированного с указанным кольцом B, необязательно замещенного неароматического карбоцикла, конденсированного с указанным кольцом B, или замещенного ароматического карбоцикла, который конденсирован с указанным кольцом B и к которому присоединен, по меньшей мере, один заместитель, содержащий гидроксигруппу, первичную аминогруппу или вторичную аминогруппу, где первичный или вторичный амин ни является атомом кольца в ароматической кольцевой системе, ни является частью амида; и
e) если кольцо A в DB2 является 6-членным ароматическим кольцом, то заместители на кольце B не объединены с образованием кольца, конденсированного с кольцом B; и
f) два соседних заместителя на кольце A в DB8 объединены с образованием необязательно замещенного карбоцикла или гетероцикла, конденсированного с указанным кольцом A с образованием бициклической группы, с которой не конденсированы другие кольца; и
g) кольцо A в DB9 вместе с любым другим кольцом, конденсированным с указанным кольцом A, содержат, по меньшей мере, два кольцевых гетероатома.
В другом варианте осуществления настоящее изобретение относится к соединению формулы (I) или (II), как описано выше в настоящем документе, где, по меньшей мере, один из заместителей R1, R5, R5', R6, R6', R7, R7', R14, R14', R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22 и R23 содержит группу X14(CH2CH2O)ffCH2CH2X14, где ff равно 1-1000, а каждый из X14 независимо выбран из
который присоединен к месту присоединения указанного заместителя либо непосредственно с помощью связи, либо через группу, которая является частью того же заместителя, которая не содержит дисульфид, гидразон, гидразид, сложный эфир, природную аминокислоту или пептид, содержащий, по меньшей мере, одну природную аминокислоту, и где, если кольцо B в DB1 представляет собой полностью углеродное кольцо, X3 представляет собой O или NR15, X4 представляет собой CH, X34 представляет собой C, то в указанном соединении формулы (I) или (II) присутствует только одна группа X14(CH2CH2O)ffCH2CH2X14 и указанная группа является частью R6, R7, R8, R10 или R15, когда b=1 и ff ≥5.
Соединение формулы (I) или (II) или их конъюгат, в котором ff больше 1000, также входит в объем настоящего изобретения.
В другом варианте осуществления настоящее изобретение относится к соединению формулы (I) или (II), как описано выше в настоящем документе, где, по меньшей мере, один из заместителей R1, R5, R5', R6, R6', R7, R7', R14, R14', R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22 и R23 содержит триазольную группу.
Следует учесть, что, если -X3- представляет собой -X3a и X3b- в группах DB1 и DB2, то эти группы фактически представлены следующими структурными формулами:
В другом аспекте настоящее изобретение относится к конъюгатам соединения формулы (I), (II), (I') или (II').
В еще одном аспекте настоящее изобретение относится к соединению формулы (III):
,
или к его фармацевтически приемлемой соли, гидрату или сольвату, где
V2 либо отсутствует, либо является функциональной группой;
каждый L2, независимо, отсутствует или является связывающей группой, связывающей V2 и L;
каждый L, независимо, отсутствует или является связывающей группой, связывающей L2 и один или несколько V1 и/или Y;
каждый V1, независимо, отсутствует или является группой, отщепляющейся или трансформирующейся в определенных условиях, которая может отщепляться или трансформироваться в течение химического, фотохимического, физического, биологического или ферментативного процесса;
каждый Y, независимо, отсутствует или является самоудаляемой промежуточной системой, которая состоит из 1 или нескольких самоудаляемых промежуточных групп и связана с V1, необязательно L, и одним или несколькими Z;
каждый p и q равен числу, соответствующему степени разветвления, и, каждый, независимо, равен положительному целому числу;
z равно положительному целому числу, равному или меньшему общему количеству мест присоединения Z;
каждый Z, независимо, представляет собой соединение формулы (I), (II), (I') или (II'), как определено в настоящем документе выше, где один или несколько из X1, R5, R5', R6, R6', R7, R7', R14, R14', R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22 и R23 могут быть, необязательно, кроме того, замещены или могут представлять собой заместитель формулы (V):
где каждый V2', L2', L', V1', Y', Z', p', q' и z' имеют то же значение, которое определено для V2, L2, L, V1, Y, Z, p, q и z, соответственно, и выбраны независимо, один или несколько заместителей формулы (V) независимо соединены через Y' с одним или несколькими X1, R5, R5', R6, R6', R7, R7', R14, R14', R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22, R23 и/или с одним или несколькими атомами, несущими эти заместители R;
каждый Z независимо соединен с Y либо через X1, либо через атом в R5, R5', R6, R6', R7, R7', R14, R14', R8, R8', R9, R9', R10, R10', R11, R11', R15, R15', R15'', R15''', R16, R16', R20, R20', R21, R21', R22, R23, либо через атом, несущий любой из этих заместителей R; и
по меньшей мере, присутствует V2 или V1.
Следует отметить, что в соединении формулы (III) должны присутствовать V2 или V1. Однако в одной или нескольких группах формулы (V), которые необязательно присутствуют в Z, каждый V2' и V1' может независимо отсутствовать или присутствовать.
В другом аспекте настоящее изобретение относится к соединению формулы (III), где
V2 присутствует и выбран как нацеливающий фрагмент, и присутствует, по меньшей мере, одна группа формулы (V), которая содержит группу V1' и содержит либо группу V2', либо L2', либо группу L', которая содержит группу X14(CH2CH2O)ggCH2CH2X14, где gg равен 3-1000 и каждый из X14 независимо выбран из
или та же указанная группа формулы (V) содержит, по меньшей мере, 2 группы X14CH2CH2OCH2CH2X14, в которых каждый из X14 выбран независимо.
Следует отметить, что индивидуальные группы X14 в группах -CH2CH2X14, которые могут присутствовать в соединении формулы (III), выбраны независимо.
Также следует отметить, что z не представляет собой степень полимеризации; поэтому z не указывает на количество групп Z, связанных друг с другом.
Также следует отметить, что если Y или Y' связаны с атомом, несущим конкретный заместитель R вместо самого этого заместителя R, то это обозначает, что этот заместитель R отсутствует, если это необходимо для соблюдения правил валентности.
Также следует отметить, что если X14, например, в -CH2CH2X14, представляет собой , то -CH2CH2X14 следует читать как -CH2CHX14.
Настоящее изобретение также относится к соединению формулы (IV):
,
или его фармацевтически приемлемой соли, гидрату или сольвату, где
RM представляет собой реакционноспособную группу, и L, V1, Y, Z, p и z такие, как определено в настоящем документе выше, кроме того, что L теперь связан с RM с помощью одной или нескольких V1 и/или Y, и V1, Y и Z могут содержать защитные группы, и одна или несколько групп V2'-L2', необязательно присутствующие в Z, как определено в настоящем документе выше, могут необязательно и независимо быть вместо RM', который представляет собой реакционноспособную группу, и где, если присутствует больше, чем 1 реакционноспособная группа в (IV), некоторые или все реакционноспособные группы являются одинаковыми или различными. Эти конъюгаты линкер-агент формулы (IV) могут рассматриваться или не могут рассматриваться в качестве промежуточных соединений для соединений формулы (III).
В дополнительном аспекте настоящее изобретение относится к соединению формулы (IV), где RM представляет собой реакционноспособную группу, выбранную из карбамоилгалогенида, ацилгалогенида, активированного сложного эфира, ангидрида, α-галогенацетила, α-галогенацетамида, малеимида, изоцианата, изотиоцианата, дисульфида, тиола, гидразина, гидразида, сульфонилхлорида, альдегида, метилкетона, винилсульфона, галогенметила и метилсульфоната, и где, по меньшей мере, одна группа формулы (V), представляющая собой часть Z, содержит группу V1' и либо содержит группу V2', L2' или L', которая содержит группу X14(CH2CH2O)ggCH2CH2X14, где gg равен 3-1000 и каждый из X14 независимо выбран из
либо та же указанная группа формулы (V) содержит, по меньшей мере, 2 группы X14CH2CH2OCH2CH2X14, в которой каждый из X14 независимо выбран. Эти конъюгаты линкер-агент формулы (IV) могут рассматриваться или не могут рассматриваться в качестве промежуточных соединений для соединений формулы (III).
Настоящее изобретение относится к энантиомерно чистым и/или диастереомерно чистым соединениям формул (I)-(IV), а также к энантиомерным и/или диастереоизомерным смесям соединений формулы (I)-(IV). Настоящее изобретение относится к чистым соединениям формулы (I)-(IV), а также к смесям изомеров соединений формулы (I)-(IV).
Соединения формул (I) и (II) и их конъюгаты представляют новые дуокармициновые производные, которые предпочтительно имеют новые ДНК-связывающие фрагменты и/или предпочтительно гетероатомы в выбранных положениях в ДНК-связывающем фрагменте или в заместителях в ДНК-связывающего или ДНК-алкилирующего фрагмента, или в одном или нескольких расщепляемых линкерах, присоединенных к соединению формулы (I) или (II). Эти модификации получены для улучшения фармакологических свойств и цитотоксической активности по сравнению с производными дуокармицина, известными из предшествующего уровня техники.
В одном из вариантов осуществления соединение формулы (I) или (II) содержит новый ДНК-связывающий фрагмент. Не будучи связанными с какой-либо теорией, предполагается, что эти новые ДНК-связывающие фрагменты могут способствовать цитотоксической активности соединений формулы (I) и (II), связываясь с ДНК аналогично ДНК-связывающим фрагментам в CC-1065 аналогах, известных из предшествующего уровня техники. Новые ДНК-связывающие агенты могут быть более водорастворимы, могут иметь повышенную аффинность связывания и/или могут быть более легко метаболизированы, например, в печени, с образованием соединений формул (I) и (II), обладающих улучшенными фармакологическими свойствами, например, повышенным терапевтическим индексом, относительно аналогичных соединений, известных из предшествующего уровня техники.
В другом варианте осуществления соединение формулы (I) или (II) содержит триазольную группу. Не будучи связанными с какой-либо теорией, предполагается, что эта гетероароматическая группа может быть введена в молекулу таким образом, чтобы она способствовала связыванию соединения формулы (I) или (II) с ДНК клетки-мишени, тем самым улучшая активность указанного соединения. Хотя аналогичный эффект может быть достигнут с помощью другой (гетеро)ароматической группы, например, фенильного кольца, триазольная группа имеет дополнительное преимущество, заключающееся в том, что она является относительно полярной группой (относительно других (гетеро)ароматических групп), что может привести к улучшению фармакологических свойств (например, водорастворимости, гидрофильности, параметров агрегации) соединений формул (I) и (II) и их конъюгатов.
В другом варианте осуществления соединение формулы (I) или (II) содержит группу олигоэтиленгликоля или полиэтиленгликоля или их производное. Указанная группа олигоэтиленгликоля или полиэтиленгликоля может быть или разветвленной, или линейной. Не будучи связанной с какой-либо теорией, предположено, что эта группа может быть введена в соединение формулы (I) или (II) для улучшения, например, физико-химических, биофизических, фармакодинамических и/или фармакокинетических свойств соединения, например, водорастворимости и параметров агрегации. Кроме того, благодаря гидрофильности группы олигоэтиленгликоля или полиэтиленгликоля, соединение формулы (I) или (II), например, может быть более цитотоксичным в отношении опухолевых клеток, резистентных ко многим лекарственным средствам, поскольку соединение представляет собой плохой субстрат для эффлюксных насосов. Если соединение формулы (I) или (II) входит в конъюгат, то возможно, что группа олигоэтиленгликоля или полиэтиленгликоля расположена между прогруппой, т.е. группой, присоединенной к соединению формулы (I) или (II) для изменения его свойств и которая (частично) удаляется in vivo из указанного соединения формулы (I) или (II), и остатком соединения формулы (I) или (II) или тем, что расположено в положении несколько противоположном к месту присоединения прогруппы, таким образом размещая остаток соединения формулы (I) или (II) между прогруппой и группой олигоэтиленгликоля или полиэтиленгликоля. Последнее условие может иметь преимущество в том смысле, что гидрофобная (ароматическая) структура ядра соединения формулы (I) или (II) более защищена от неблагоприятных взаимодействий со своей окружающей средой, например, водной окружающей средой, таким образом, например, уменьшая количество агрегатной формации.
В другом варианте осуществления настоящее изобретение относится к конъюгату соединения формулы (I) или (II) в соответствии с одним из вышеуказанных вариантов осуществления и его производным. Эти конъюгаты содержат одну или несколько прогрупп.
В другом варианте осуществления конъюгат соединения формулы (I) или (II) содержит, по меньшей мере, две группы, из которых первая группа является расщепляемой in vivo прогруппой, которая содержит олигоэтиленгликолевую или полиэтиленгликолевую группу или ее производное, а вторая группа содержит, по меньшей мере, нацеливающую группу. Такой конъюгат имеет относительно гидрофобную структуру ядра соединения формулы (I) или (II) или его производного, размещенного между направляющей группой и группой, содержащей олигоэтиленгликоль или полиэтиленгликоль, защищая таким образом структуру ядра от возможных неблагоприятных взаимодействий со своей окружающей средой.
Соединения формулы (I) и (II) являются подходящими для применения в целях доставки лекарственного средства, включая нацеливание лекарственного средства и контролируемого высвобождения, используя соединения формул (III) и (IV).
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
На фиг. 1 представлена перегруппировка seco соединения для циклопропил-содержащего соединения.
На фиг. 2 изображен синтез алкилирующих групп 4a-4k.
На фиг. 3 представлен синтез алкилирующих групп 8a-8d.
На фиг. 4 изображен синтез алкилирующих групп 12 и 16.
На фиг. 5 изображен синтез дуокармицинов, содержащих 7-замещенный индолизин.
На фиг. 6 изображен синтез дуокармицинов, содержащих 6-замещенный индолизин.
На фиг. 7 представлен синтез соединения 110.
На фиг. 8 представлен синтез дуокармицинов, содержащих 7-азабензофуран.
На фиг. 9 изображен синтез соединения 112.
На фиг. 10 изображен синтез конъюгата линкер-агент 114.
На фиг. 11 представлен синтез конъюгата линкер-агент 115.
На фиг. 12 изображен синтез конъюгата линкер-агент 116.
На фиг. 13 изображены конъюгаты линкер-агент 117, 118, 119 и 120.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Следующее подробное описание приведено для более полного понимания изобретения.
Определения
Если не определено иначе, все технические и научные термины, используемые в настоящем документе, имеют те же значения, которые определены для обычного понимания специалиста в данной области.
Используемый в настоящем документе термин "антитело" относится к молекуле иммуноглобулина с полной длиной, иммунологически активной части молекулы иммуноглобулина с полной длиной или производному молекулы иммуноглобулина с полной длиной или его активной части, т.е. молекуле, которая содержит антигенсвязывающий сайт, который иммуноспецифически связывает антиген представляющей интерес цели или его часть, такие цели включают, но ими не ограничиваются, опухолевые клетки. Иммуноглобулин может быть любого типа (например, IgG, IgE, IgM, IgD, IgA или IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 или IgA2) или подкласса. Иммуноглобулин или его производное или активная часть могут быть выделены от особей любого биологического вида, например, человека, грызунов (например, мыши, крысы или хомяков), осла, овцы, кролика, козы, морской свинки, верблюда, лошади, коровы или курицы, но предпочтительно человека, мыши или кролика, или выделены от более чем одного биологического вида. Антитела, используемые в