Хинуклидиновые эфиры 1-азагетероциклилуксусной кислоты в качестве антимускариновых средств, способ их получения и их лекарственные композиции
Иллюстрации
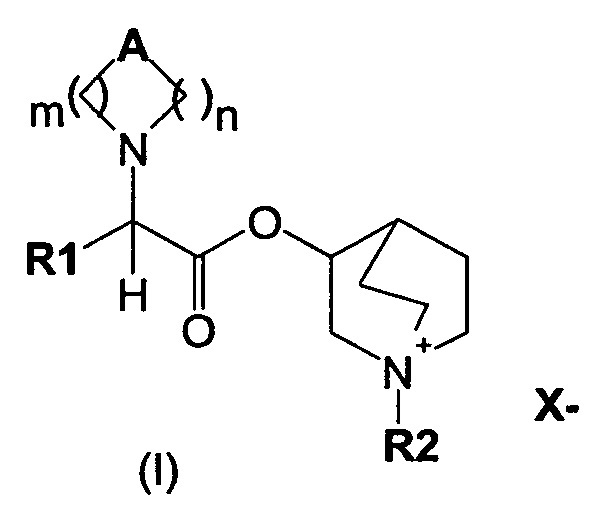
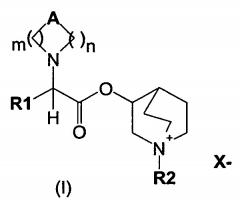
Показать всеИзобретение относится к соединениям формулы (I),
где А может представлять собой простую связь, двойную связь, О, S, NR3, C(R3)R4, СО, C(O)N(R3), N(R3)C(O) и C(R3)-(CH2)-C(R4); m представляет собой целое число от 1 до 4; n равно 0 или представляет собой целое число от 1 до 4; R1 выбран из группы, состоящей из фенила и 5-членного гетероарила, содержащего один гетероатом S, возможно замещенных одним или более чем одним заместителем, выбранным из группы, состоящей из атомов галогена, (С1-С6)алкила и (С1-С6)алкоксила; X- представляет собой физиологически приемлемый анион; R2 представляет собой группу формулы (Y)
где р равно 0 или представляет собой целое число от 1 до 4; q равно 0 или представляет собой целое число от 1 до 4; Р отсутствует или выбран из группы, состоящей из СО, N(R3)C(O) и C(O)N(R3); W выбран из группы, состоящей из Н, (С1-С10)алкоксила, фенила, гетероарила, возможно замещенных одним или более чем одним заместителем, выбранным из группы, состоящей из атомов галогена, ОН, оксо (=O), CO2R3, (С1-С6)алкила, (С1-С6)алкоксила и фенила; где гетероарил представляет собой моно- или бициклическую кольцевую систему, имеющую от 5 до 9 кольцевых атомов и от 1 до 3 гетероатомов, выбранных из N, О и S; R3 и R4 независимо выбраны из группы, состоящей из Н, атомов галогена, CONH2, (С1-С6)алкила, (С1-С6)алканоила и (С3-С8)циклоалкила, в качестве селективных антагонистов рецептора М3, к способу их получения, к содержащей их композиции и к их терапевтическому применению при лечении респираторного заболевания, такого как астма и хроническая обструктивная болезнь легких (ХОБЛ). 5 н. и 9 з.п. ф-лы., 2 табл., 34 пр.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к аналогам хинуклидинового эфира 1-азагетероциклилуксусной кислоты, действующим в качестве антагонистов мускаринового рецептора, к способу их получения, к содержащей их композиции и к их терапевтическому применению.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Соли четвертичного аммония, действующие в качестве лекарственных средств-антагонистов мускаринового (М) рецептора, применяют в настоящее время в терапии для индукции бронходилатации для лечения респираторных заболеваний. Примеры хорошо известных антагонистов М рецептора представлены ипратропия бромидом и тиотропия бромидом.
Несколько химических классов, действующих в качестве лекарственных средств, являющихся селективными антагонистами мускаринового рецептора М3, разработано для лечения воспалительных или обструктивных заболеваний дыхательных путей, таких как астма и хроническая обструктивная болезнь легких (ХОБЛ).
Производные хинуклидинкарбамата и их применение в качестве антагонистов М3 раскрыты, например, в WO 02/051841, WO 03/053966 и WO 2008/012290.
В WO 2010/015324 раскрыты карбонатные производные и их применение в качестве антагонистов М3.
Спазмолитическая активность 1-этил-3-пиперидинилового эфира возможно замещенной альфа-фенил-1-пиперидин-/1-пирролидин-/4-морфолин-уксусной кислоты по отношению к ацетилхолину раскрыта в US 2952685 и в Bull Soc Chim France 355-359, 1958.
1-Метил-3-пиперидиниловый эфир альфа-фенил-1-пиперидинуксусной кислоты и его аналоги получены и протестированы в качестве потенциальных психотропных лекарственных средств в связи с их психодислептическими свойствами в статье Chim Ther 7, 408-414, 1966.
Соли четвертичного аммония хинуклидиновых эфиров альфа-фенил-альфа-метил-1-пиперидинуксусной кислоты и их аналогов раскрыты в следующих документах: WO 2008/075005, WO 2009/153536 и Bioorg Med Chem Lett (2011), doi:10.1016/j.bmcl.2011.10.002. Данные соединения, имеющие метильную группу вместо гидроксильной группы хорошо известных антагонистов М3 предшествующего уровня техники (тиотропия, гликопирролата, аклидиния бромида), должны обладать более высокой вероятностью связывания с белками плазмы.
Тем не менее, в высокой степени желательно разработать антагонисты рецептора М3 для введения путем ингаляции, способные действовать локально, при этом обладающие высокой эффективностью и большой продолжительностью действия. Данные лекарственные средства сразу после всасывания должны разлагаться до неактивных соединений, лишенных каких-либо системных побочных эффектов, характерных для мускариновых антагонистов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены аналоги хинуклидинового эфира 1-азагетероциклилуксусной кислоты общей формулы (I) в качестве селективных антагонистов рецептора М3, способных к введению путем ингаляции и действовать локально.
Соединение согласно изобретению способно производить устойчивый бронходилатирующий эффект в легком, но стабильно и быстро преобразовываться в легком в неактивные метаболиты после прохождения в плазму человека. Такие свойства дают значительные преимущества в отношении безопасности.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В частности, изобретение направлено на хинуклидиновый эфир 1-азагетероциклилуксусной кислоты общей формулы (I)
где А может представлять собой простую связь, двойную связь, О, S, SO, SO2, NR3, C(R3)R4, CO, С(O)N(R3), N(R3)С(O)O, SO2N(R3), N(R3)С(O), ОС(O)N(R3), N(R3)SO2, С(R3)=С(R4) и С(R3)-(СН2)-С(R4);
m представляет собой целое число от 1 до 4;
n равно 0 или представляет собой целое число от 1 до 4;
R1 выбран из группы, состоящей из (С1-С10)алкила, арила, (С3-C8)-циклоалкила, гетероарила, арил(С1-С6)алкила и гетероарил(С1-С6)алкила, возможно замещенных одним или более чем одним заместителем, выбранным из группы, состоящей из атомов галогена, ОН, оксо (=O), SH, NO2, CN, CON(R3)2, СООН, CO2R3, CF3, (С1-С10)алкоксикарбонила, (C1-С10)алкилсульфанила, (С1-С10)алкилсульфинила, (С1-С10)алкилсульфонила, (С1-С10)алкила, (С1-С10)алкоксила, арилокси и гетероарила;
где X- представляет собой физиологически приемлемый анион;
R2 представляет собой группу формулы (Y)
где p равно 0 или представляет собой целое число от 1 до 4;
q равно 0 или представляет собой целое число от 1 до 4;
P отсутствует или выбран из группы, состоящей из О, S, SO, SO2, СО, NR3, СН=СН, N(R3)SO2, N(R3)СОО, N(R3)С(O), SO2N(R3), СО(O)N(R3) и C(O)N(R3);
W выбран из группы, состоящей из Н, (С1-С10)алкила, (С1-С10)алкоксила, (С3-С8)-циклоалкила, арила, гетероарила, (С5-С10)гетероциклоалкила, возможно замещенных одним или более чем одним заместителем выбранным из группы, состоящей из атомов галогена, ОН, оксо (=O), SH, NO2, CN, CON(R3)2, СООН, NH2, NHCOR3, CO2R3, (С1-С10)алкоксикарбонила, (С1-С10)алкилсульфанила, (C1-С10)алкилсульфинила, (С1-С10)алкилсульфонила, (С1-С10)алкила, (C1-С10)алкоксила, (С1-С10)алканоила и арила;
R3 и R4 независимо выбраны из группы, состоящей из Н, атомов галогена, CONH2, (С1-С10)алкила, (С2-С6)алкинила, (С2-С6)алкенила, (С1-С10)алканоила, (С3-С8)циклоалкила, гетероарила и арила, возможно замещенных одним или более чем одним заместителем, выбранный из группы, состоящей из атомов галогена, ОН, оксо (=O), SH, NO2, CN, CONH2, СООН, (C1-С10)алкоксикарбонила, (С1-С10)алкилсульфанила, (С1-С10)алкилсульфинила, (С1-С10)алкилсульфонила, (С1-С10)алкила, (С1-С10)алкоксила и (С3-С7)циклоалкила.
Настоящее изобретение также направлено на соединение общей формулы (II):
где A, R1, m и n являются такими, как описано выше, и их фармацевтически приемлемую соль.
Изобретение также относится к способу получения соединения формулы (I), как описано на схеме 1, следующим путем:
(а) сочетание соединения формулы (IX), в котором K может представлять собой алкоксигруппу, гидроксигруппу или атом галогена, такой как атом хлора, а А, R1 являются такими, как определено выше, с соединением формулы (X), в котором J представляет собой Н, Na, Li или К, с получением соединений формулы (II),
(b) алкилирование соединения формулы (II) алкилирующими агентами общей формулы (XI)
в которых R2 является таким, как определено выше, а Х представляет собой подходящую уходящую группу, выбранную из группы, состоящей из атомов галогена и сложных эфиров сульфокислоты, включающих тозилат, трифлаты или мезилат, с получением соединений общей формулы (I).
В изобретении также предложены фармацевтические композиции соединений общей формулы (I) или общей формулы (II), отдельно, либо в комбинации или в смеси с одним или более чем одним фармацевтически приемлемым носителем и/или эксципиентом.
В изобретении также предложены соединения общей формулы (I) или (II), применяемые в качестве лекарственного средства.
В следующем аспекте в изобретении предложено применение соединений формулы (I) или общей формулы (II) для получения лекарственного средства для предупреждения и/или лечения бронхообструктивных или воспалительных заболеваний, предпочтительно астмы, либо хронического бронхита, либо хронической обструктивной болезни легких (ХОБЛ).
В изобретении также предложен способ предупреждения и/или лечения бронхообструктивных или воспалительных заболеваний, предпочтительно астмы, либо хронического бронхита, либо хронической обструктивной болезни легких (ХОБЛ), включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения общей формулы (I) или (II).
В изобретении также предложены фармацевтические препараты соединений общей формулы (I) или общей формулы (II), подходящие для введения путем ингаляции, такие как ингаляционные порошки, управляемые пропеллентом ингаляторы отмеренных доз с распылением сжатым воздухом или ингаляционные препараты без пропеллента.
Изобретение также относится к устройству, которое может представлять собой ингалятор сухого порошка однократной или многократной дозы, ингалятор отмеренной дозы и небулайзер с мягким распылением, содержащее соединения общей формулы (I) или (II).
Изобретение также относится к набору, содержащему фармацевтические композиции соединений общей формулы (I) или (II) отдельно, либо в комбинации или в смеси с одним или более чем одним фармацевтически приемлемым носителем и/или эксципиентом, и устройство, которое может представлять собой ингалятор сухого порошка однократной или многократной дозы, ингалятор отмеренной дозы и небулайзер с мягким распылением, содержащее соединение общей формулы (I) или (II).
В настоящем описании, если не указано иное, термин "атом галогена" включает атомы фтора, хлора, брома и йода.
Выражение "(С1-С10)алкил" относится к прямоцепочечным или разветвленным алкильным группам, где число атомов углерода составляет от 1 до 10. Примерами этих групп являются следующие группы: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, нонил, децил и тому подобное.
Выражение "(С2-С6)алкенил" относится к прямоцепочечным или разветвленным углеродным цепям с одной или более чем одной двойной связью. Примерами этих групп являются следующие группы: этенил, пропенил, бутенил, пентенил, гексенил и тому подобное.
Выражение "(С1-С10)алкоксил" относится к вышеупомянутым алкилокси (например, алкокси) группам. Примерами этих групп являются следующие группы: метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, гексокси и тому подобное.
Выражение "(С1-С10)алканоил" относится к карбонильному остатку, замещенному атомом водорода или прямоцепочечной или разветвленной алкильной группой из атомов углерода в количестве от 1 до 9. Примерами этих групп являются формил, ацетил, пропаноил, бутаноил, изобутаноил и пивалоил.
Выражения "(С1-С10)алкилсульфанил", "(С1-С10)алкилсульфинил" или "(С1-С10)алкилсульфонил" также относятся, соответственно, к следующим группам: алкил-S-, алкил-SO- или алкил-SO2-.
Выражение "(С3-С8)циклоалкил" относится к циклическим неароматическим углеводородным группам, имеющим от 3 до 8 атомов углерода. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и тому подобное.
Выражение "(С5-С10)гетероциклоалкил" относится к циклическим неароматическим системам, имеющим от 5 до 10 кольцевых атомов, в которых по меньшей мере один кольцевой атом представляет собой гетероатом (например, N, NH, S или О).
Выражение "арил" относится к моно-, либо би-, либо трициклическим кольцевым системам, имеющим от 6 до 20 кольцевых атомов, предпочтительно от 6 до 15, и где по меньшей мере одно кольцо является ароматическим.
Выражения "арил(С1-С6)алкил", "гетероарил(С1-С6)алкил" относятся к (C1-С6)алкильным группам, дополнительно замещенным арильными или гетероарильными кольцами.
Выражение "арилокси" относится к вышеописанной арилокси-группе. Пример может представлять собой фенилокси.
Выражение "гетероарил" относится к моно-, би- или трициклическим кольцевым системам, имеющим от 5 до 20 кольцевых атомов, предпочтительно от 5 до 15, в которых по меньшей мере одно кольцо является ароматическим, и в которых по меньшей мере один кольцевой атом представляет собой гетероатом или гетероароматическую группу (например, N, NH, S или О).
Примеры подходящих арильных или гетероарильных моноциклических систем включают, например, тиенильные, фенильные, пирролильные, пиразолильные, имидазолильные, изоксазолильные, оксазолильные, оксадиазолильные, изотиазолильные, тиазолильные, пиридинильные, имидазолидинильные и фуранильные остатки и тому подобное.
Примеры подходящих арильных или гетероарильных бициклических систем включают бензодиоксольные, нафталиновые, дифениленовые, пуриновые, птеридиновые, бензотриазольные, хинолиновые, изохинолиновые, индольные, изоиндольные, бензотиофеновые, дигидробензодиоксиновые, дигидробензодиоксепиновые и бензооксазиновые остатки и тому подобное.
Предпочтительно физиологически приемлемые анионы X- включают анионы, выбранные из хлора, брома, йода, трифторацетата, формиата, сульфата, фосфата, метансульфоната, нитрата, малеата, ацетата, цитрата, фумарата, тартрата, оксалата, сукцината, бензоата и пара-толуолсульфоната.
Помимо присутствия аниона X-, в том случае, когда дополнительные основные аминогруппы присутствуют в соединениях формулы (I) или (II), могут присутствовать дополнительные физиологически и/или фармацевтически приемлемые анионы, среди указанных ранее, с образованием соли присоединения кислоты с неорганической или органической кислотой. Также в присутствии кислотных групп, таких как СООН группы, могут также присутствовать соответствующие физиологические катионные соли, например, включающие ион щелочного или щелочноземельного металла или ион аммония.
Подходящая неорганическая кислота для образования соли присоединения кислоты соединения формулы (I) или (II) выбрана из галогеноводородных кислот, таких как фтористоводородная кислота, соляная кислота, бромисто-водородная кислота и йодистоводородная кислота, но также из азотной кислоты, серной кислоты и фосфорной кислоты. Подходящие органические кислоты для образования соли присоединения кислоты соединения формулы (I) или (II) выбраны из следующих кислот: алифатических монокарбоновых кислот, таких как муравьиная кислота, уксусная кислота, трифторуксусная кислота и пропионовая кислота; алифатических гидроксикислот, таких как молочная, лимонная, винная и яблочная кислоты; дикарбоновых кислот, таких как малеиновая или янтарная кислота; ароматических карбоновых кислот, таких как бензойная кислота; ароматических гидроксикислот и сульфоновых кислот.
Первая предпочтительная группа соединений общей формулы (I) или (II) представляет собой группу, где А выбран из О, S, N(R3) или C(R3)R4, R1 выбран из группы, состоящей из арила, арил(С1-С6)алкила и гетероарила, возможно замещенных одним или более чем одним заместителем, выбранным из атомов галогена, (С1-С10)алкила, (С1-С10)алкоксила, арилокси и гетероарила; и R3 является таким, как определено выше.
В пределах этого класса еще более предпочтительны соединения общей формулы (I) или (II), где А представляет собой С(R3)R4, R1 выбран из группы, состоящей из арила и гетероарила, возможно замещенных одним или более чем одним заместителем, выбранным из атомов галогена, (С1-С10)алкила, (C1-С10)алкоксила, арилокси и гетероарила; m и n оба равны 2, и R3 представляет собой группу формулы (Y), где р равно 0, 1 и 3, Р представляет собой СО, q равно 0, W выбран из группы, состоящей из (С1-С10)алкила, арила, гетероарила, возможно замещенных одним или более чем одним заместителем, выбранным из группы, состоящей из атомов галогена, (С1-С10)алкила, (С1-С10)алкоксила, ОН и (С1-С10)алканоила.
В пределах этого класса еще более предпочтительны соединения общей формулы (I), где W выбран из группы, состоящей из фенила, бензотиоксола, тиофенила и тиазолила, возможно замещенных одним или более чем одним атомом галогена, ОН, метилом и ацетилом.
Специалистам в данной области техники очевидно, что соединения общей формулы (I) и (II) содержат асимметрические центры. Следовательно, изобретение также включает оптические стереоизомеры и их смеси.
Активные соединения общей формулы (I) и (II) проявляют по меньшей мере два хиральных центра, которые, соответственно, представлены хинуклидиновым атомом углерода, несущим кислород сложноэфирной группы, и атомом углерода, несущим группу R1. Эти соединения общей формулы (I) и (II) могут быть получены в чистых S-R, R-R, R-S, S-S конфигурациях или в виде смесей диастереоизомеров.
Кроме того, в зависимости от значений R1, R2, R3 и А ясно, что в соединениях формулы (I) и (II) могут присутствовать дополнительные асимметрические центры. Следовательно, изобретение также включает любой из оптических стереоизомеров, диастереоизомеров и их смесей в любом соотношении.
Согласно конкретным воплощениям в настоящем изобретении предложены соединения, приведенные ниже:
Соединения общей формулы (I) и (II) могут быть получены в соответствии с известными способами. Некоторые из способов, которые можно использовать, описаны ниже и представлены на схеме 1.
Метод получения соединений Формулы (I) и (II)
Соединения общей формулы (IX) могут быть получены в соответствии со стандартными методами, широко представленными в литературе (например, следуя методу, представленному авторами Kiskinen et al. в статье Tetrahedron, 1983, 39/9, 1627; Haurena et al. в J.O.C., 2010, 75/8, 264; Najer, Bulletin de la Societe Chimique de France, 1958, 1189; Duan et al. Bioorganic and Medicinal Chemistry Letters, 2009, 19/6, 1610). Наиболее предпочтительно соединения общей формулы (IX) могут быть получены в соответствии с тремя различными путями: А, Б и В.
Путь А - Соединения общей формулы (IX) могут быть получены посредством алкилирования реагента общей формулы (III) соединением общей формулы (IV), в котором LG представляет собой подходящую уходящую группу (галогенид, такой как бромид, или сульфоновую сложноэфирную группу, такую как мезилат), и K представляет собой карбоксильную группу, в возможно защищенной форме (в характерном случае включающую карбоксиалкильную сложноэфирную группу (например, K=O(С1-С6)алкил), такую как карбоксиметил (K=ОМе). Данное алкилирование может быть выполнено, следуя одному из стандартных методов, широко представленными в литературе (например, Melloni et al., European Journal of Medicinal Chemistry, 1984, 19/3, 235; Duran et al., Journal of Medicinal Chemistry, 1965, 8, 598; Venkatesan, A.M. et al., Journal of Medicinal Chemistry, 2004, 47/25, 6255; Wlasislaw, В. et al. Synthesis, 1997, 4, 420).
При типовом методе реакцию алкилирования активируют присутствием основания, например амина, выбранного из группы, состоящей из триэтиламина, диизопропилэтиламина, пиридина и 4-диметиламинопиридина, или неорганического основания, такого как карбонат калия или гидрид натрия. Эту реакцию, как правило, проводят в подходящем растворителе (например, в ацетонитриле, тетрагидрофуране (THF), N,N-диметилформамиде (DMF)) в диапазоне температуры от примерно 0°С до примерно 130°С в течение периода времени от примерно 1 часа до примерно 74 часов. Реакцию можно проводить при традиционном нагревании (используя масляную баню) или при микроволновом нагревании. Реакцию можно проводить в открытом сосуде или в запаянной трубке.
Реагенты общей формулы (IV) имеются в продаже или могут быть традиционно получены в соответствии со стандартными методами, широко представленными в литературе. Например, соединения общей формулы (IV), в которых уходящая группа (LG; от англ. leaving group) представляет собой атом галогена, такой как атом брома, могут быть получены путем галогенирования соответствующим образом замещенного сложного эфира фенилуксусной кислоты (например, следуя методу, описанному Epstein, J.W. в статье J. Med. Chem., 1981, 24/5, 481). Альтернативно соединения общей формулы (IV) могут быть получены, начиная с соответствующим образом замещенного производного (IV) миндальной кислоты, используя известные методы (обзор подходящих реакций приведен в книге Larock, L.C., Comprehensive Organic Transformation, Second edition (1999), John Wiley & Son Inc, pg 689-700). Производное миндальной кислоты общей формулы (IV) можно подвергать прямому сочетанию с реагентом общей формулы (III) посредством реакции Мицунобу (Kumara Swamy, K.C. et al. Chem. Rev. 2009, 109, 2551; Powell, N.A. et al. Bioorganic and Medicinal Chemistry 2007, 15/17, 5912). Эту реакцию в характерном случае проводили в присутствии фосфина (например, трифенилфосфина) и азодикарбоксилата (например, диизопропилазодикарбоксилата или диэтилазодикарбоксилата) в подходящем растворителе (таком как дихлорметан (DCM) и THF) и в диапазоне температуры от -10°С до 110°С в течение периода от 1 часа вплоть до 74 часов.
Согласно пути Б соединения общей формулы (IX) могут быть получены посредством реакции Петасиса-Манниха, следуя любому из различных методов, описанных в литературе (например: Petasis N.A., Akritopoulou I., Tetrahedron Lett. 1993, 34, 583; Follmann, M., Synlett, 2005, 6, 1009; Kausik K.N., Tetrahedron Letters, 2005, 46, 2025). При характерном методе эквимолярную смесь амина (III), глиоксиловой кислоты (V) и бороновой кислоты (VI) растворяли в подходящем растворителе (например, в дихлорметане, ацетонитриле) и перемешивали. Обычно данную реакцию проводят в диапазоне температуры от примерно 0°С до примерно 110°С в течение периода времени от примерно 1 часа до примерно 74 часов. Реакцию можно проводить при традиционном нагревании (используя масляную баню) или при микроволновом нагревании. Реакцию можно проводить в открытом сосуде или в запаянной трубке.
Путь В - Соединения общей формулы (IX) могут быть получены, начиная с подходящих производных аминокислот общей формулы (VIII). Эти реагенты могут быть преобразованы в соединения общей формулы (IX), используя известные протоколы (например, Benasutti et al., Tetrahedron Asymmetry, 2006, 17/5, 842; Benson et al., J.O.C., 1988, 53/22, 5335; Cuevas et al., Synlett, 2007, 1, 119; Juarez et al., Tetrahedron Asymmetry, 1997, 8/2, 203). Эти протоколы включают, но не ограничены ими, восстановительное аминирование, образование амида или алкилирование производных аминокислот формулы (VIII) реагентами общей формулы (VII), в которой R1, А, K, m и n являются такими, как определено выше, и Y может представлять собой альдегидную группу (СНО), карбоновую кислоту (СООН), ацильную группу (например, Y=COCl) или подходящую уходящую группу (галогенид, такой как бромид, или сложноэфирную группу сульфоновой кислоты, такую как мезилат).
Затем соединения формулы (IX) могут быть преобразованы в соединения общей формулы (II) путем сочетания с соединениями общей формулы (X). Данное сочетание можно проводить несколькими путями, при которых К может представлять собой алкоксигруппу, гидроксильную группу или атом галогена, такой как атом хлора (обзор подходящих реакций приведен в книге Carey, F.A. and Sundeberg, R.J. Advanced Organic Chemistry, Third Edition (1990), Plenum Press, New York and London, pg 145).
В частности, в случае, когда К представляет собой защищенную гидроксильную группу, такую как алкоксигруппа (например, K=ОМе, OEt или OtBu), сложный эфир (IX) можно либо подвергать взаимодействию с подходящими солями хинуклидин-3-ола, либо подвергать гидролизу с получением соответствующего производного кислоты (IX; K=ОН).
В первом случае соединения формулы (II) получают, подвергая взаимодействию соединения общей формулы (IX), в которых К представляет собой алкоксигруппу (например, K=ОМе), с солями хинуклидин-3-ола (X), в которых J представляет собой Na, Li или К. При характерном методе раствор сложных эфиров (IX) и подходящих солей хинуклидин-3-ола (полученных ранее или образованных in situ) в подходящем растворителе (например, в толуоле, DMF или N-метилпирролидоне (NMP)) нагревают при температуре, находящейся в диапазоне от примерно 80°С до примерно 200°С в течение периода от примерно 1 часа до примерно 74 часов.
Во втором случае гидролиз сложноэфирной группировки в (IX) (например, K=OMe) можно проводить, обрабатывая эти соединения подходящим водным раствором основания, выбранного из группы, состоящей из гидроксида натрия, лития и калия, в подходящих растворителях (например, в тетрагидрофуране, диоксане, воде и т.д.). Реакция протекает при комнатной температуре (KT) в течение периода от 1 часа вплоть до 36 часов. Полученную в результате карбоновую кислоту можно подвергать сочетанию с хинуклидин-3-олом в соответствии с несколькими протоколами.
Первая альтернатива. При типичном методе соединения (II) могут быть получены путем конденсации между спиртом (X) (J=H) и кислотой (IX) (K=ОН) в стандартных условиях амидирования и пептидного сочетания. Например, обработка кислоты (IX) одним или более чем одним эквивалентом имеющегося в продаже агента конденсации, такого как карбодиимид (например, гидрохлорид 1-(3-диметиламино)пропил)-3-этилкарбодиимида (EDC) и тому подобное), например, в присутствии N-гидроксибензотриазола (HOBt), с последующим взаимодействием активированного промежуточного соединения со спиртом (X) приводит в результате к образованию соединений (II). В реакционной смеси может также присутствовать органическое основание, такое как триэтиламин. Активированное промежуточное соединение можно либо выделить, либо образовать предварительно, либо образовать in situ. Подходящие растворители для сочетания включают, но не ограничены ими, галогенуглеродные растворители (например, дихлорметан), тетрагидрофуран, диоксан и ацетонитрил. Реакция протекает в диапазоне температуры от 0°С вплоть до 170°С в течение периода времени в диапазоне от примерно 1 часа вплоть до 72 часов. Эту реакцию можно проводить при традиционном нагревании (используя масляную баню) или при микроволновом нагревании. Реакцию можно проводить в открытом сосуде или в запаянной трубке.
Вторая альтернатива. В случае, где К представляет собой атом галогена, такой как атом хлора, спирт (X) (J=H) подвергают взаимодействию с подходящим ацилгалогенидом (IX), используя известные способы. Эта реакция может быть активирована основанием, таким как триэтиламин, пиридин и 4-диметиламинопиридин, в подходящем растворителе (например, в дихлорметане). Эту реакцию проводят в диапазоне температуры от 0°С до 130°С в течение периода от 1 часа вплоть до 74 часов. Эту реакцию можно проводить при традиционном нагревании (используя масляную баню) или при микроволновом нагревании. Реакцию можно проводить в открытом сосуде или в запаянной трубке.
В некоторых воплощениях настоящего изобретения необходимый ацилгалогенид (IX) может быть легко получен из соответствующей кислоты (IX) (K=ОН). Данную активацию можно осуществлять в соответствии с любым из стандартных методов, представленных в литературе. Например, в результате обработки кислоты (IX) (K=ОН) одним или более чем одним эквивалентом оксалилхлорида в присутствии каталитического количества диметилформамида (DMF) в галогенуглеродном растворителе, таком как дихлорметан, при температуре в диапазоне от 0°С до 35°С получают требуемый ацилхлорид (IX) (K=Cl).
Третья альтернатива. Альтернативно ацилирование спирта (X) (J=H) с получением соединений общей формулы (IX) может быть выполнено, используя методы, преобразующие in situ кислоту (IX) (K=ОН) в соответствующие ацилгалогениды. Например, спирты (X) подвергают взаимодействию с кислотами (IX) (K=ОН) в присутствии трифенилфосфина и галогенуглеродного растворителя, такого как тетрахлорид углерода или дихлорметан, примерно при KT в течение максимального периода времени 16 часов (Lee, J.B. J. Am. Chem. Soc., 1966, 88, 3440).
Четвертая альтернатива. При другом способе для получения соединений по настоящему изобретению кислоту (IX) (K=ОН) можно активировать другими имеющимися в продаже активирующими агентами, такими как гексафторфосфат бромтрипирролидинофосфония (PyBrOP) или карбонилимидазол, в подходящем апротонном растворителе (например, в дихлорметане, тетрагидрофуране), примерно при KT. В результате последующего взаимодействия активированного промежуточного соединения со спиртом (X) получают желаемое соединение формулы (II). Для взаимодействия может также требоваться использование органического основания, такого как диизопропилэтиламин, и обычно протекает примерно при KT.
Пятая альтернатива. При другом способе для получения соединений по настоящему изобретению соединения (II) могут быть эффективно получены путем конденсации между кислотами (IX) (K=ОН) и спиртом (X) (J=H) в характерных условиях Мицунобу (Kumara Swamy, K.C., Chem. Rev. 2009, 109, 2551-2651). Например, кислоты (IX) и спирт (X) подвергают взаимодействию в присутствии фосфина (например, трифенилфосфина) и сложного эфира азодикарбоксилата (например, диэтилазодикарбоксилата или диизопропилазодикарбоксилата) в апротонном растворителе, таком как тетрагидрофуран. В характерном случае эта реакция протекает в диапазоне температуры от 0°С вплоть до 100°С в течение периода времени, находящегося в диапазоне от примерно 30 минут вплоть до 72 часов.
Соединение общей формулы (II), в котором R1, A, m и n являются такими, как определено в данном описании выше, может быть получено либо в виде отдельного диастереоизомера, либо в виде смеси диастереоизомеров. Хинуклидин-3-ол может характеризоваться либо R, либо S конфигурацией. При использовании R-энантиомера соединение (II) может быть получено в S-R конфигурации, в R-R конфигурации или в виде смеси диастереоизомеров (R-R и S-R конфигурации).
При получении смеси диастереоизомеров она может быть преобразована в соединения формулы (I) Схемы 1 или чаще всего могут быть разделены с получением двух отдельных диастереоизомеров, которые, в свою очередь, могут быть преобразованы в соединения формулы (I) Схемы 1. Это разделение может быть выполнено, используя известные методы. Эти методы включают, но не ограничены ими, хроматографическую очистку, очистку препаративной ВЭЖХ (высокоэффективная жидкостная хроматография) и кристаллизацию. Например, два диастереоизомера можно разделить с помощью флэш-хроматографии на силикагеле, элюируя подходящими растворителями или смесью растворителей, например, DCM и метанолом и тому подобным. При другом способе по настоящему изобретению разделение диастереоизомеров может быть получено, используя колонку, наполненную хиральной стационарной фазой, например, колонку Chiralpack AY, либо Chiralcel OD или Chiralcel OZ, и элюируя, например, ацетонитрилом и/или смесями ацетонитрила и спирта. Альтернативно разделение диастереоизомеров может быть легко достигнуто путем кристаллизации из подходящего растворителя (например, этилового эфира) в виде свободного основания или после образования подходящей соли (например, соли (+)-винной кислоты)).
В результате алкилирования соединений общей формулы (II)
алкилирующими агентами общей формулы (XI)
в которых Х представляет собой подходящую уходящую группу, выбранную из группы, состоящей из галогенида (например, атома брома, йода, хлора) и сложного эфира сульфоната (например, тозилата, трифлатов, мезилата) получают соединения общей формулы (I).
Данный вид реакции широко описан в литературе в нескольких различных условиях, например, реакцию можно проводить в чистом виде или в подходящем растворителе, выбранном из группы, состоящей из ацетонитрила, DMF, DMSO и тетрагидрофурана. Эта реакция в характерном случае протекает в диапазоне температур от 0°С вплоть до 170°С в течение периода времени, находящегося в диапазоне от нескольких минут вплоть до 72 часов. Эту реакцию можно проводить при традиционном нагревании (используя масляную баню) или при микроволновом нагревании. Реакцию можно проводить в открытом сосуде или в запаянной трубке.
Соединение общей формулы (I) и (II) на Схеме 1 можно рассматривать либо в качестве конечного продукта, либо в качестве промежуточного соединения для получения других соединений общей формулы (I) и (II). Таким образом, часть группы R1, R2 или А в общей формуле (I) и (II) может претерпевать реакции окисления, восстановления или расщепления (например, для удаления защитной группы) с получением других конечных соединений общей формулы (I) и (II).
В настоящем изобретении также предложена фармацевтическая композиция соединения общей формулы (I) или (II) в смеси с одним или более чем одним фармацевтически приемлемым носителем или эксципиентом, например, описанным в руководстве Remington's Pharmaceutical Sciences Handbook, XVII Ed., Mack Pub., N.Y., U.S.A.
Введение соединений по настоящему изобретению можно осуществлять в соответствии с потребностями пациента, например, перорально, назально, парентерально (подкожно, внутривенно, внутримышечно, внутригрудинно и путем инфузии), путем ингаляции, ректально, вагинально, местно, локально, трансдермально и путем глазного введения.
Для введения соединений по изобретению можно применять различные твердые пероральные дозируемые формы, включая такие твердые формы, как таблетки, желатиновые капсулы, капсулы, каплетки, гранулы, лепешки и нерасфасованные порошки. Соединения по настоящему изобретению можно вводить отдельно или объединять с различными фармацевтически приемлемыми носителями, разбавителями (такими как сахароза, маннит, лактоза, крахмалы) и эксципиентами, известными в данной области техники, включающими, но не ограниченными ими, суспендирующие агенты, солюбилизаторы, буферные агенты, связующие агенты, разрыхлители, консерванты, красители, ароматизаторы, смазывающие агенты и тому подобное. Капсулы, таблетки и гели с замедленным высвобождением также обладают преимуществом при введении соединений по настоящему изобретению.
Для введения соединений по изобретению можно также применять различные жидкие пероральные дозируемые формы, включая водные и неводные растворы, эмульсии, суспензии, сиропы и эликсиры. Такие дозируемые формы могут также содержать подходящие инертные разбавители, известные в данной области техники, такие как вода, и подходящие эксципиенты, известные в данной области техники, такие как консерванты, увлажняющие агенты, подсластители, ароматизаторы, а также агенты для эмульгирования и/или суспендирования соединений по изобретению. Соединения по настоящему изобретению можно инъецировать, например, внутривенно, в форме изотонического стерильного раствора. Возможны также другие препараты.
Суппозитории для ректального введения соединений по настоящему изобретению могут быть получены путем смешивания соединения с подходящим эксципиентом, таким как масло какао, салицилаты и полиэтиленгликоли.
Препараты для вагинального введения могут находиться в форме препарата в виде крема, геля, пасты, пенки или спрея, содержащего в дополнение к активному ингредиенту такие подходящие носители, которые известны в данной области техники.
Для местного введения фармацевтическая композиция может находиться в форме кремов, мазей, жидких мазей, лосьонов, эмульсий, суспензий, гелей, растворов, паст, порошков, спреев и капель, подходящих для введения на кожу, в глаз, ухо или нос. Местное введение может также включать трансдермальное введение с помощью таких средств, как трансдермальные пластыри.
Для лечения заболеваний дыхательных путей соединения согласно изобретению предпочтительно вводят путем ингаляции.
Ингаляционные препараты включают порошки для ингаляции, аэрозольных ингаляторов отмеренных доз с распылением сжатым воздухом, активируемым пропеллентом, или небулизированных препаратов без пропеллента.
Для введения сухого порошка можно использовать ингаляторы однократной или многократной дозы, известные из предшествующего уровня техники. В этом случае соединение по изобретению в форме порошка можно заполнять в желатиновые, полимерные или другие капсулы, картриджи или блистерные упаковки, либо в резервуар.
К порошкообразному соединению по изобретению можно добавлять разбавитель или носитель, как правило, нетоксичный и химически инертный по отношению к соединению по изобретению, например, лактозу или любую другую добавку, подходящую для улучшения вдыхаемой фракции.
Аэрозольные ингаляторы отмеренных доз с распылением сжатым воздухом, активируемым пропеллентом, содержат соединение по изобретению либо в растворе, либо в диспергируемой форме по меньшей мере в пропеллентном газе, таком как гидрофторалкан. Препараты, активируемые пропеллентом, могут также содержать другие ингредиенты, такие как сорастворители, стабилизаторы и возможно другие эксципиенты.
Ингаляционные