Пиридин-n-оксиды и способы их получения
Иллюстрации
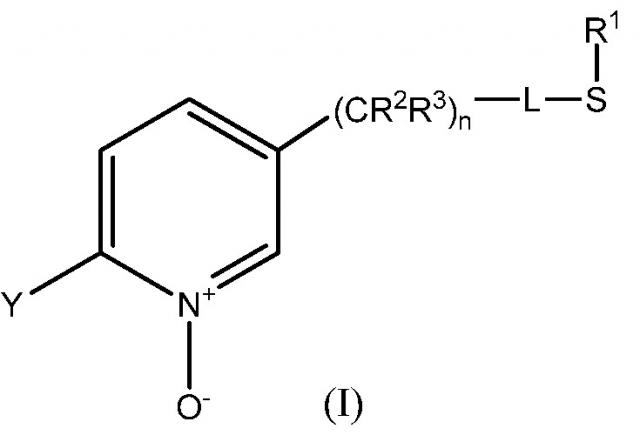
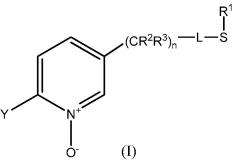
Показать всеИзобретение относится к сельскому хозяйству. Для получения 2-замещенного-5-(1-алкилтио)алкил-пиридин-N-оксида, соответствующего формуле (I):
,
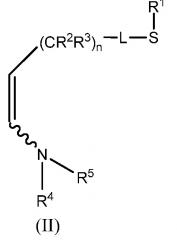
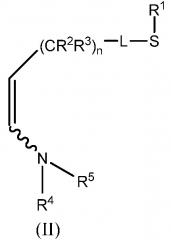
где L представляет собой одинарную связь или R1, S и L, взятые вместе, представляют собой 4-, 5- или 6-членное кольцо; R1 представляет собой (С1-С4)-алкил; R2 и R3 по отдельности представляют собой водород, метил, этил, фтор, хлор или бром; n представляет собой целое число от 0 до 3; и Y представляет собой (С1-С4)-галогеналкил; в котором: (i) енамин, соответствующий формуле (II):
,
где R1, R2, R3, L и n имеют значения, определенные выше; и R4 и R5 независимо представляют собой С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил или R4 и R5, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо; конденсируют с α,β-ненасыщенным кетоном, соответствующим формуле (III):
,
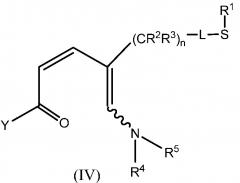
где Y имеет значения, определенные выше; и Х1 представляет собой галоген, OR6, OSO2R6, SR6, SOR6, SO2R6 или NR7R8, где R6 представляет собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, и R7 и R8 независимо представляют собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, или R7 и R8, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо; с получением промежуточного соединения, соответствующего формуле (IV):
,
где R1, R2, R3, R4, R5, L и n имеют значения, определенные выше; и (ii) промежуточное соединение, соответствующее формуле (IV), подвергают циклизации с использованием аминного нуклеофила, соответствующего формуле (V): H2N-X2 , где Х2 представляет собой гидроксил, алкокси, циано, амино или меркаптан. Изобретение позволяет реализовать указанное назначение. 3 н. и 18 з.п. ф-лы, 2 табл., 7 пр.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка заявляет приоритет предварительной патентной заявки США №61/666811, направленной на рассмотрение 30 июня 2012 г., содержание которой полностью включено в описание посредством ссылки.
Область техники
Изобретение, раскрытое в данном документе, относится к области некоторых функционализированных пиридин-N-оксидов, включая, например, 2-замещенные-5-(1-алкилтио)алкилпиридин-N-оксиды, и к методикам их получения и применения.
Уровень техники
Контроль популяций насекомых является существенным для современного сельского хозяйства, хранения пищевых продуктов и гигиены. Существует более десяти тысяч видов насекомых, которые вызывают потери в сельском хозяйстве. Каждый год мировые сельскохозяйственные потери достигают миллиардов долларов США. Насекомые, такие как термиты, также, как известно, вызывают повреждение всех видов частных и общественных строений, приводя каждый год к потерям в миллиарды долларов США. Насекомые также поедают и загрязняют хранящиеся на складе пищевые продукты, приводя каждый год к потерям в миллиарды долларов США, а также к поражению пищи, необходимой людям.
Некоторые насекомые имеют или развивают устойчивость к пестицидам при современном применении. Сотни видов насекомых являются устойчивыми к одному или нескольким пестицидам. Соответственно, существует постоянная потребность в новых пестицидах и в способах получения таких пестицидов.
В патентах США №№7678920 и 7687634 описаны некоторые пестицидные сульфоксиминные соединения, а в патенте США №8188292 описаны некоторые пестицидные сульфилиминные соединения. Некоторые из таких сульфоксиминных и сульфилиминных соединений содержат пиридиновую функциональную группу. Неожиданно было установлено, что вариации одного или нескольких таких соединений, где пиридиновая функциональная группа была N-окислена, проявляют пестицидные свойства. Пиридин-N-оксиды обычно получают прямым окислением перкислотами, такими как м-хлорпероксибензойная кислота (mCPBA)). В случае некоторых функционализированных пиридинов, таких как 2-замещенные-5-(1-алкилтио)алкилпиридины, однако, сульфидная функциональность чувствительна к окислению, так что прямое окисление с помощью mCPBA неприемлемо. Таким образом, существует потребность в способах получения таких N-окисленных соединений.
Сущность изобретения
Один из вариантов осуществления, раскрытый в изобретении, относится к способу получения некоторых функционализированных пиридин-N-оксидов, включая, например, 2-замещенные-5-(1-алкилтио)алкилпиридин-N-оксиды. В одном более конкретном, но неограничивающем варианте предложен способ получения 2-замещенного-5-(1-алкилтио)алкилпиридин-N-оксида, соответствующего формуле (I):
где
L представляет собой одинарную связь или R1, S и L, взятые вместе, представляют собой 4-, 5- или 6-членное кольцо;
R1 представляет собой (С1-С4)-алкил;
R2 и R3 по отдельности представляют собой водород, метил, этил, фтор, хлор или бром;
n представляет собой целое число от 0 до 3; и
Y представляет собой (С1-С4)-галогеналкил.
В одном из вариантов такой способ включает конденсацию енамина, соответствующего формуле (II):
где
R1, R2, R3, L и n имеют значения, определенные выше; и
R4 и R5 независимо представляют собой С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил или R4 и R5, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо;
с α,β-ненасыщенным кетоном, соответствующим формуле (III):
где
Y имеет значения, определенные выше; и
Х1 представляет собой галоген, OR6, OSO2R6, SR6, SOR6, SO2R6 или NR7R8, где R6 представляет собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, и R7 и R8 независимо представляют собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, или R7 и R8, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо;
с получением промежуточного соединения, соответствующего формуле (IV):
где R1, R2, R3, R4, R5, L и n имеют значения, определенные выше.
Этот вариант способа дополнительно включает циклизацию промежуточного соединения, соответствующего формуле (IV), с использованием аминного нуклеофила, соответствующего формуле (V):
H2N-X2
(V),
где Х2 представляет собой гидроксил, алкокси, циано, амино или меркаптан, в условиях кипячения с обратным холодильником с получением соединения, соответствующего формуле (I).
В другом варианте этот способ включает взаимодействие ацетилхлоридного соединения, соответствующего формуле (VI):
где Y представляет собой С1-С4-галогеналкил, с алкилвиниловым эфиром, соответствующим формуле (VII):
где R10 представляет собой С1-С4-алкил, с получением промежуточного соединения, соответствующего формуле (VIII):
Этот вариант способа также включает конденсацию промежуточного соединения, соответствующего формуле (VIII), с енамином, соответствующим формуле (II):
где
R1, R2, R3, L и n имеют значения, определенные выше; и
R4 и R5 независимо представляют собой С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил или R4 и R5, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо, с получением промежуточного соединения, соответствующего формуле (IV):
где R1, R2, R3, R4, R5, L и n имеют значения, определенные выше.
Промежуточное соединение, соответствующее формуле (IV), затем подвергают циклизации с использованием аминного нуклеофила, соответствующего формуле (V):
H2N-X2
(V),
где Х2 представляет собой гидроксил, алкокси, циано, амино или меркаптан, в условиях кипячения с обратным холодильником с получением соединения, соответствующего формуле (I).
Более конкретные, но неограничивающие вариации соединений формулы (I) включают следующие классы:
(1) Соединения формулы (I), где Y представляет собой CF3.
(2) Соединения формулы (I), где R2 и R3 независимо представляют собой водород, метил или этил.
(3) Соединения формулы (I), где R1 представляет собой СН3 и L представляет собой одинарную связь, т.е. имеющие структуру:
где n=1-3.
(4) Соединения формулы (I), где R1, S и L, взятые вместе, образуют насыщенное 5-членное кольцо, и n равно 0, т.е. имеющие структуру:
Специалисту в данной области техники будет понятно, что возможны одна или несколько комбинаций описанных выше классов соединения формулы (I).
В другом варианте осуществления предложено новое соединение, соответствующее формуле (I):
где
L представляет собой одинарную связь или R1, S и L, взятые вместе, представляют собой 4-, 5- или 6-членное кольцо;
R1 представляет собой (С1-С4)-алкил;
R2 и R3 по отдельности представляют собой водород, метил, этил, фтор, хлор или бром;
n представляет собой целое число от 0 до 3; и
Y представляет собой (С1-С4)-галогеналкил.
Более конкретные, но неограничивающие вариации соединений формулы (I) в этом варианте осуществления включают следующие классы:
(1) Соединения формулы (I), где Y представляет собой CF3.
(2) Соединения формулы (I), где R2 и R3 независимо представляют собой водород, метил или этил.
(3) Соединения формулы (I), где R1 представляет собой СН3 и L представляет собой одинарную связь, т.е. имеющие структуру:
где n=1-3.
(4) Соединения формулы (I), где R1, S и L, взятые вместе, образуют насыщенное 5-членное кольцо, и n равно 0, т.е. имеющие структуру:
Специалисту в данной области техники будет понятно, что возможны одна или несколько комбинаций описанных выше классов соединения формулы (I).
Другие аспекты, варианты осуществления, формы, признаки, положительные эффекты, объекты и преимущества станут очевидны из подробного описания, представленного в описании.
Подробное описание изобретения
Для облегчения понимания принципов изобретения будут сделаны ссылки на приведенные ниже варианты осуществления, и конкретный язык будет использован для их описания. Тем не менее будет понятно, что в связи с этим никакого ограничения объема изобретения не подразумевается, такие изменения и дополнительные модификации в проиллюстрированном способе и такие дополнительные варианты применения принципов изобретения, которые проиллюстрированы в данном случае, специалистом в области техники, к которой относится изобретение, подразумеваются как обычно встречающиеся.
Если специально не ограничено иное, нижеперечисленные определения, которые используют в описании, будут означать следующее:
«алкенил», как используется в описании, означает ациклический, ненасыщенный (по меньшей мере одна двойная углерод-углеродная связь), разветвленный или неразветвленный заместитель, состоящий из углерода и водорода, например винил, аллил, бутенил, пентенил, гексенил, гептенил, октенил, ноненил и деценил;
«алкокси», как используется в описании, означает алкил, также содержащий углерод-кислородную одинарную связь, например, метокси, этокси, пропокси, изопропокси, 1-бутокси, 2-бутокси, изобутокси, трет-бутокси, пентокси, 2-метилбутокси, 1,1-диметилпропокси, гексокси, гептокси, октокси, нонокси и децокси;
«алкил», как используется в описании, означает ациклический, насыщенный, разветвленный или неразветвленный заместитель, состоящий из углерода и водорода, например метил, этил, пропил, изопропил, 1-бутил, 2-бутил, изобутил, трет-бутил, пентил, 2-метилбутил, 1,1-диметилпропил, гексил, гептил, октил, нонил и децил;
«арил», как используется в описании, означает циклический, ароматический заместитель, состоящий из водорода и углерода, например фенил, нафтил и бифенилил;
«галоген», как используется в описании, означает фтор, хлор, бром и йод;
«галогеналкил», как используется в описании, означает алкил, также содержащий от одного до максимально возможного числа одинаковых или разных атомов галогена, например фторметил, дифторметил, трифторметил, 1-фторметил, 2-фторэтил, 2,2,2-трифторэтил, хлорметил, трихлорметил и 1,1,2,2-тетрафторэтил; и
«гетероарил», как используется в описании, относится к 5- или 6-членному ароматическому кольцу, содержащему один или несколько гетероатомов, например, N, O или S; такие гетероароматические кольца могут быть конденсированы с другими ароматическими системами.
Соединения, раскрытые в описании, могут существовать в виде одного или нескольких стереоизомеров. Различные стереоизомеры включают геометрические изомеры, диастереомеры и энантиомеры. Таким образом, соединения, раскрытые в данном документе, могут включать рацемические смеси, индивидуальные стереоизомеры и оптически активные смеси. Специалисту в данной области техники будет понятно, что один стереоизомер может быть более активным, чем другой. Индивидуальные стереоизомеры и оптически активные смеси могут быть получены с помощью селективных синтетических методик, путем обычных синтетических методик с использованием оптически разрешенных исходных веществ или с помощью обычных методик оптического разрешения.
В одном из вариантов осуществления предложен способ получения 2-замещенного-5-(1-алкилтио)алкилпиридин-N-оксида, соответствующего формуле (I):
где
L представляет собой одинарную связь или R1, S и L, взятые вместе, представляют собой 4-, 5- или 6-членное кольцо;
R1 представляет собой (С1-С6)-алкил;
R2 и R3 по отдельности представляют собой водород, метил, этил, фтор, хлор или бром;
n представляет собой целое число от 0 до 3; и
Y представляет собой (С1-С4)-галогеналкил.
В одном из вариантов в способе используют методику, проиллюстрированную на схеме А:
Схема А
На схеме А енамин, соответствующий формуле (II):
где
R1, R2, R3, L и n имеют значения, определенные выше; и
R4 и R5 независимо представляют собой С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил или R4 и R5, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо;
конденсируют с α,β-ненасыщенным кетоном, соответствующим формуле (III):
где
Y имеет значения, определенные выше; и
Х1 представляет собой галоген, OR6, OSO2R6, SR6, SOR6, SO2R6 или NR7R8, где R6 представляет собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, или R7 и R8 независимо представляют собой водород, С1-С8-алкил, С2-С8-алкенил, С1-С8-арилалкил, С1-С8-галогеналкил, С1-С8-алкоксиалкил, С1-С8-алкиламиноалкил, арил или гетероарил, или R7 и R8, взятые вместе с N, представляют собой 5- или 6-членное насыщенное или ненасыщенное кольцо;
с получением промежуточного соединения, соответствующего формуле (IV):
где R1, R2, R3, R4, R5, L и n имеют значения, определенные выше.
Как также показано на схеме А, промежуточное соединение, соответствующее формуле (IV), подвергают циклизации с использованием аминного нуклеофила, соответствующего формуле (V):
H2N-X2
(V),
где Х2 представляет собой гидроксил, алкокси, циано, амино или меркаптан, в условиях кипячения с обратным холодильником с получением соединения, соответствующего формуле (I).
Енамины, соответствующие формуле (II), обычно могут быть получены путем добавления соответствующим образом замещенного амина к подходящим образом замещенному альдегиду в присутствии поглощающего воду средства с подходящим растворителем или без растворителя. Как правило, подходящим образом замещенный альдегид подвергают взаимодействию с безводным дизамещенным амином при температуре приблизительно от -20°C до 20°C в присутствии осушителя, такого как безводный карбонат калия, и продукт выделяют с помощью рутинных способов и обычно используют без дополнительной очистки. В одном из неограничивающих вариантов, например, где енамин, соответствующий формуле (II), имеет следующую структуру:
подходящим образом замещенный альдегид подвергают взаимодействию с пирролидином при температуре приблизительно от -20°C до 20°C в присутствии осушителя, такого как безводный карбонат калия, и полученный продукт выделяют с помощью рутинных способов и обычно используют без дополнительной очистки. Другие детали, связанные с получением енаминов, соответствующих формуле (II), можно найти, например, в патентной публикации США №2008/0033180, содержание которой полностью включено в описание посредством ссылки.
α,β-Ненасыщенные кетоны, соответствующие формуле (III), являются коммерчески доступными или могут быть получены из соответствующих подобных винилу субстратов и ацилирующих агентов. В одном из вариантов, например, алкилвиниловые эфиры можно ацилировать галогеналкилуксусным ангидридом с получением соединений, соответствующих формуле (III).
Приблизительно эквимолярные количества енамина, соответствующего формуле (II), и α,β-ненасыщенного кетона, соответствующего формуле (III), требуются в процессе конденсации.
В одном из вариантов конденсацию проводят при температуре приблизительно от -20°C до 35°C. В другом более конкретном варианте используют температуру от приблизительно -5°C до приблизительно 20°C.
Конденсация енамина, соответствующего формуле (II), с α,β-ненасыщенным кетоном, соответствующим формуле (III), может быть проведена в полярном или неполярном растворителе, хотя также подразумеваются варианты, в которых конденсацию проводят в условиях без растворителя. Неограничивающие примеры полярных растворителей включают дихлорметан, тетрагидрофуран, этилацетат, ацетон, диметилформамид, ацетонитрил и диметилсульфоксид, тогда как неограничивающие примеры неполярных растворителей включают углеводородные и ароматические углеводородные растворители, такие как толуол. В одном из конкретных, но неограничивающих вариантов такую конденсацию проводят в толуоле.
В одном из аспектов α,β-ненасыщенный кетон, соответствующий формуле (III), добавляют к предварительно приготовленной смеси енамина, соответствующего формуле (II).
В типичной реакции конденсации енамин, соответствующий формуле (II), растворяют в желаемом растворителе при температуре от приблизительно -5°C до приблизительно 20°C и α,β-ненасыщенный кетон, соответствующий формуле (III), непрерывно добавляют к этому раствору с помощью капельной воронки. Смесь перемешивают до тех пор, пока не израсходуются енамин, соответствующий формуле (II), и α,β-ненасыщенный кетон, соответствующий формуле (III). При использовании неполярного растворителя, такого как толуол, промежуточное соединение, соответствующее формуле (IV), может быть использовано без последующего выделения или очистки.
Циклизацию промежуточного соединения, соответствующего формуле (IV), аминным нуклеофилом, соответствующим формуле (V), проводят в условиях кипячения с обратным холодильником; т.е. при температуре в интервале от 50°C до 90°C. Как указано выше, Х2 может представлять собой гидроксил, алкокси, циано, амино или меркаптан. Также допустимо, чтобы аминный нуклеофил, используемый в реакционной схеме А, присутствовал в форме кислой соли. Если используют форму кислой соли аминного нуклеофила, то ненуклеофильное основание также используют для нейтрализации аналога кислой соли. Неограничивающие примеры ненуклеофильных оснований включают карбонатные соли, триэтиламин, N,N-диизопропилэтиламин и 1,8-диазабициклоундец-7-ен. В одном из неограничивающих вариантов, где Х2 представляет собой гидроксил и соединение, соответствующее формуле (V), представляет собой гидроксиламин, в реакционной схеме А используют гидрохлорид гидроксиламина вместе с триэтиламином. Также следует отметить, что другие вариации аминного нуклеофила, соответствующего формуле (V), и ненуклеофильного основания, когда оно присутствует, допустимы и подразумеваются.
Циклизация промежуточного соединения, соответствующего формуле (IV), может быть проведена в том же самом растворителе, что и конденсация енамина, соответствующего формуле (II), и α,β-ненасыщенного кетона, соответствующего формуле (III).
В другом варианте в способе по такому варианту осуществления используют методику, проиллюстрированную на схеме В:
Схема В
На схеме В ацетилхлоридное соединение, соответствующее формуле (VI), где Y представляет собой С1-С4-галогеналкил, подвергают взаимодействию с алкилвиниловым эфиром, соответствующим формуле (VII), где R10 представляет собой С1-С4-алкил. Приблизительно эквимолярные количества соединений, соответствующих формулам (VI) и (VII), обычно используют в данном способе, хотя могут быть использованы избытки одного или другого. В конкретном варианте используют 10-50%-ный стехиометрический избыток алкилвинилового эфира, соответствующего формуле (VII).
Эту реакцию проводят или в отсутствие растворителя, например с избытком алкилвинилового эфира, соответствующего формуле (VII), или в присутствии безводного органического растворителя. Неограничивающими примерами подходящих растворителей являются углеводородные растворители, включающие ароматические углеводороды, такие как толуол. Реакция может быть проведена при температуре от приблизительно -10°C до приблизительно 35°C. В одном из конкретных вариантов используют температуры от приблизительно 0°C до приблизительно 20°C. В типичной реакции ацетилхлоридное соединение, соответствующее формуле (VI), барботируют ниже поверхности алкилвинилового эфира, соответствующего формуле (VII), или в чистом виде, или в присутствии углеводородного растворителя, при температуре 0-5°C. Реакционной смеси дают нагреться при перемешивании в течение приблизительно 1 часа, поддерживая температуру не выше комнатной температуры. Неочищенная реакционная смесь, содержащая промежуточное соединение, соответствующее формуле (VIII), может быть использована как она есть без дополнительного выделения или без очистки реакционной смеси.
Промежуточное соединение, соответствующее формуле (VIII), затем конденсируют с енамином, соответствующим формуле (II), в присутствии третичного аминного основания с получением промежуточного соединения, соответствующего формуле (IV), где Y представляет собой С1-С4-галогеналкил. Приблизительно эквимолярные количества промежуточного соединения, соответствующего формуле (VIII), и енамина, соответствующего формуле (III), требуются в процессе конденсации; по меньшей мере один эквивалент третичного аминного основания требуется приблизительно с 1-2 эквивалентами, используемыми в некоторых вариантах.
Такая конденсация может быть проведена при температуре от приблизительно -20°C до приблизительно 35°C. В одном из конкретных вариантов используют температуры от приблизительно –5°C до приблизительно 20°C. Такая конденсация может быть проведена в неполярном или полярном апротонном растворителе. Примеры неполярных растворителей включают углеводородные растворители и ароматические углеводороды. Полярные апротонные растворители также являются хорошим выбором для такой химии. В конкретных, но не ограничивающих вариантах способа используют или ацетонитрил, или толуол. В одном из вариантов промежуточное соединение, соответствующее формуле (VIII), добавляют к предварительно приготовленной смеси енамина, соответствующего формуле (II), и третичного аминного основания. В типичной реакции конденсации енамин, соответствующий формуле (II), и по меньшей мере стехиометрическое количество третичного аминного основания растворяют в желаемом растворителе при температуре от приблизительно -50°C до приблизительно 200°C, а промежуточное соединение, соответствующее формуле (VIII), непрерывно добавляют к этому раствору через капельную воронку. Смесь перемешивают до тех пор, пока промежуточное соединение, соответствующее формуле (VIII), и енамин, соответствующий формуле (II), не израсходуются. Промежуточное соединение, соответствующее формуле (IV), может быть использовано, как оно есть, без дополнительного выделения или без очистки. Другие детали, относящиеся к рассмотренным выше стадиям методики схемы В, приведены в международной патентной публикации №WO 2010/002577, содержание которой полностью включено в описание посредством ссылки.
Как дополнительно проиллюстрировано на схеме В, промежуточное соединение, соответствующее формуле (IV), полученное по этой методике, затем подвергают циклизации с использованием аминного нуклеофила, соответствующего формуле (V), как обсуждалось выше.
Более конкретные, но неограничивающие вариации соединений формулы (I) включают следующие классы:
(1) Соединения формулы (I), где Y представляет собой СF3.
(2) Соединения формулы (I), где R2 и R3 независимо представляют собой водород, метил или этил.
(3) Соединения формулы (I), где R1 представляет собой СН3 и L представляет собой одинарную связь, т.е. имеющие структуру:
где n=1-3.
(4) Соединения формулы (I), где R1, S и L, взятые вместе, образуют насыщенное 5-членное кольцо и n равно 0, т.е. имеющие структуру:
Специалисту в данной области технике будет понятно, что возможны одна или несколько комбинаций описанных выше классов соединения формулы (I).
2-Замещенные-5-(1-алкилтио)алкилпиридин-N-оксиды, описанные в изобретении, могут быть использованы, например, вместо соответствующих 2-замещенных-5-(1-алкилтио)алкилпиридиновых промежуточных соединений при получении различных N-замещенных сульфилиминных и сульфоксиминных пиридиновых соединений, описанных, например, в патентах США №№7678920, 7687634 и 8188292, с целью получения N-замещенных сульфилиминных или сульфоксиминных пиридин-N-оксидных соединений. Содержание патентов США №№7678920, 7687634 и 8188292 полностью включено в описание посредством ссылки.
Таким образом, в дополнительном варианте осуществления способ получения некоторых N-замещенных сульфилиминных или сульфоксиминных пиридин-N-оксидных соединений, соответствующих формуле (IX):
где
R1, R2, R3, L, n и Y имеют ранее определенные значения;
Х3 является необязательным и представляет собой О, когда он присутствует;
Х4 представляет собой NNO2, NCN, NCOOR9 или NCONH2; и
R9 представляет собой (С1-С3)-алкил;
с использованием 2-замещенных-5-(1-алкилтио)алкилпиридин-N-оксидов, описанных в изобретении, проиллюстрирован на реакционной схеме С:
Схема С
В зависимости от желаемой конечной формы соединения, соответствующего формуле (IX), схема С является примером добавления Х4 к соединению, соответствующему формуле (I), с получением N-замещенного сульфилиминного пиридин-N-оксидного соединения, или добавления как Х3, так и Х4 к соединению, соответствующему формуле (I), с получением N-замещенного сульфоксиминного пиридин-N-оксидного соединения.
В одном из вариантов получение N-замещенного сульфилиминного пиридин-N-оксидного соединения, где Х4 представляет собой NNO2, включает реакцию соединения, соответствующего формуле (I), с нитрамидом в присутствии уксусного ангидрида по схеме С. В другом варианте получение N-замещенного сульфилиминного пиридин-N-оксидного соединения, где Х4 представляет собой NСN, включает окисление соединения, соответствующего формуле (I), диацетатом йодбензола в присутствии цианамида по схеме С.Такое окисление может быть проведено в полярном апротонном растворителе, таком как СН2Сl2. Другие детали, относящиеся к способам получения N-замещенных сульфилиминных пиридинов такой природы и в которых 2-замещенные-5-(1-алкилтио)алкил-пиридин-N-оксиды, раскрытые в изобретении, могут быть использованы для получения соответствующих N-замещенных сульфилиминных пиридин-N-оксидов, раскрыты в патенте США №8188292.
Получение N-замещенного сульфоксиминного пиридин-N-оксидного соединения, соответствующего формуле (IX), т.е. где X3 присутствует и представляет собой О, может быть выполнено путем дополнительного окисления N-замещенных сульфилиминных пиридин-N-оксидных соединений, описанных выше. Например, в одном из неограничивающих вариантов N-замещенное сульфилиминное пиридин-N-оксидное соединение, которое включает фрагмент NCN, добавленный путем окисления соединения, соответствующего формуле (I), диацетатом йодбензола в присутствии цианамида, может быть дополнительно окислено м-хлорпероксибензойной кислотой (mCPBA) в присутствии основания, такого как карбонат калия, с получением соответствующего N-замещенного сульфоксиминного пиридин-N-оксидного соединения. Эта реакция может быть проведена в протонных полярных растворителях, таких как этанол и вода.
Получение N-замещенных сульфоксиминных пиридин-N-оксидных соединений, соответствующих формуле (IX), т.е. где Х3 присутствует и представляет собой О, также может быть осуществлено путем ступенчатого присоединения Х3 и Х4 к соединению, соответствующему формуле (I). Например, соединение, соответствующее формуле (I), может быть окислено с помощью mCPBA в полярном растворителе, таком как дихлорметан, при температуре ниже 0°C с получением сульфоксида. Сульфоксид затем иминируют азидом натрия в присутствии концентрированной серной кислоты в апротонном растворителе, таком как хлороформ, при нагревании, с получением сульфоксимина. Для вариантов, где Х3 присутствует и Х4 представляет собой NNO2, NCN, NCOOR4, такой сульфоксимин может быть или подвергнут нитрованию с помощью азотной кислоты в присутствии уксусного ангидрида при умеренно повышенной температуре, или цианирован с помощью бромциана в присутствии основания, или карбоксилирован алкил(R9)хлорформиатом в присутствии основания, такого как 4-диметиламинопиридин (DMAP), с получением N-замещенного сульфоксимина. Основание необходимо для эффективного цианирования и карбоксилирования, и предпочтительным основанием является DMAP, тогда как серную кислоту используют в качестве катализатора для эффективной реакции нитрования. Другие детали, относящиеся к способам получения N-замещенных сульфоксимин-пиридинов такой природы и в которых 2-замещенные-5-(1-алкилтио)алкилпиридин-N-оксиды, раскрытые в изобретении, могут быть использованы с получением соответствующих N-замещенных сульфоксиминных пиридин-N-оксидов, раскрыты в патентах США №№7678920 и 7687634.
Получение N-замещенных сульфоксиминных пиридин-N-оксидных соединений, соответствующих формуле (IX), где Х4 представляет собой NCONH2, может быть проведено с помощью кислоты, которая гидролизует сульфоксиминное соединение, соответствующее формуле (IX), где была присоединена группа NCN, т.е. имеющее следующую структуру:
Неограничивающие примеры кислот, которые могут быть использованы в этой реакции, включают серную кислоту, хлористоводородную кислоту, фосфорную кислоту, трифторуксусную кислоту и азотную кислоту.
В одном из вариантов кислотный гидролиз проводят при температуре от приблизительно 50°C до приблизительно 90°C и при нормальном давлении, но подразумевается использование более высоких или более низких температур и давления, если желательно.
Неограничивающие примеры растворителей, которые могут быть использованы в реакции кислотного гидролиза, включают полярные растворители, такие как дихлорметан, тетрагидрофуран, этилацетат, ацетон, диметилформамид, ацетонитрил и диметилсульфоксид.
ПРИМЕРЫ
Примеры представлены с целью иллюстрации, и их не следует рассматривать в качестве ограничивающих изобретение, раскрытое в этом документе, только вариантами осуществления, описанными в этих примерах.
Исходные вещества, реагенты и растворители, которые получают из коммерческих источников, используют без дополнительной очистки. Молекулам даны их известные названия, предложенные в соответствии с программами наименования в пределах ISIS Draw, ChemDraw или ACD Name Pro. Если такие программы не способны давать название молекуле, то молекулу называют с использованием обычных правил. Спектры 1Н и 13С ЯМР получают с использованием прибора Bruker 300 МГц. Газовую хроматографию проводят с использованием системы Agilent 6850 Network GC или Agilent 6890 со способностью охлаждения на колонках впрыскивания с капиллярной колонкой. ВЭЖХ проводят с использованием системы Agilent 1200, включающей автоматический пробоотборник, вакуумный дегазатор, колоночный нагреватель и УФ детектирование.
Пример 1: Малообъемное получение 5-(1-(метилтио)этил)-2-(трифторметил)пиридин-N-оксида (1):
Реакция конденсации 1-(3-метилтиобут-1-енил)пирролидона (2):
с 4-этокси-1,1,1-трифторбут-3-ен-2-оном (3):
в толуоле дает 27 мас.% 1,1,1-трифтор-6-(метилтио)-5-(пирролидин-1-илметилен)гепт-3-ен-2-она (4) в толуоле.
В трехгорлую круглодонную колбу объемом 25 мл, оборудованную обратным холодильником и продуваемую в отбеливающий скруббер, добавляют 403 мг (0,37 ммоль) 27 мас.% 1,1,1-трифтор-6-(метилтио)-5-(пирролидин-1-илметилен)гепт-3-ен-2-она (4) в толуоле. К этой смеси одной порцией добавляют 34 мг (0,34 ммоль) триэтиламина. Реакционную смесь охлаждают приблизительно до 12,8°C и затем одной порцией добавляют 24 мг (0,34 ммоль) гидрохлорида гидроксиламина. Реакционную смесь медленно нагревают до 85°C и перемешивают 1 час и сорок пять минут. Затем реакционную смесь охлаждают до комнатной температуры. Эту смесь делят на много фракций для инструментального анализа и очистки. Часть реакционной смеси распределяют между толуолом и водой. Как органический, так и водный слои анализируют с помощью ЖХ/МС. Оба слоя, как подтверждено, имеют пик с молекулярным соответствием для 5-(1-(метилтио)этил)-2-(трифторметил)пиридин-N-оксида (C9H10F3NOS). Вычислено: m/z=237,04. Найдено: m/z=237,04.
Небольшую порцию реакционной смеси очищают с использованием препаративной тонкослойной хроматографии путем загрузки 2 мл реакционной смеси на пластину размером 20×20 см (1000 микрон) и элюируют ее с помощью смеси, имеющей соотношение 4:1 между гексанами и 2-пропанолом (Rf составляет приблизительно от 0,5 до 0,6). Соответствующую полосу вырезают из пластины и экстрагируют с силикагеля с помощью 20 мл этилацетата. Спектр 1Н ЯМР получают для наилучших фракций такого разделения. Продукт содержит небольшую часть этилацетата, а химические сдвиги для целевого соединения имеют значения: 1H ЯМР (300 МГц, CDC13) δ 8,30 (с, 1H), 7,64 (д, J=8,3 Гц, 1H), 7,35 (д, J=8,3 Гц, 1H), 3,78 (кв, J=7,1 Гц, 1H), 1,98 (с, 3H), 1,58 (д, J=7,1 Гц, 3H).
Пример 2: Объемное получение 5-(1-(метилтио)этил)-2-(трифторметил)пиридин-N-оксида (1)
Добавляют 5,0 г (0,03 моль) 1-(3-метилтиобут-1-енил)пирролидона (2) и 100 мл ацетонитрила (ACN) в сухую круглодонную колбу объемом 250 мл, оборудованную магнитной мешалкой, вводом азота, капельной воронкой и обратным холодильником. Затем по каплям в течение 2-3 минут добавляют 4-этокси-1,1,1-трифторбут-3-ен-2-он (3) (ETFBO) (4,9 г, 0,03 моль) и полученный темный раствор перемешивают при комнатной температуре 1 час. Затем к этому раствору добавляют 2,1 г (0,03 моль) гидрохлорида гидроксиламина, после чего добавляют 4,2 мл (0,03 моль) триэтиламина. Реакционную смесь затем кипятят с обратным холодильником при 85°C в течение 2 часов, охлаждают и аликвоту анализируют с помощью ТСХ и ГХ/МС, которые показывают, что реакция по существу закончилась, исходный продукт отсутствует и присутствуют два новых продукта. Основной продукт, идентифицированный при анализе с помощью ГХ/МС, соответствует структуре, приписываемой 5-(1-(метилтио)эти