Рекомбинантный ген l1hpv16, рекомбинантная плазмида pqe-l1/16, белок l1hpv16 и их применение
Иллюстрации
Показать всеГруппа изобретений относится к области биотехнологии. Представлен рекомбинантный ген, кодирующий белок L1 вируса папилломы человека 16 типа, с кодонами, оптимизированными для гетерологичной экспрессии в штаммах Е. coli. Представлен экспрессионный плазмидный вектор pQE-L1/16, несущий указанный рекомбинантный ген. Представлен способ получения рекомбинантного белка L1HPV16 с использованием указанного вектора, которым трансформируют штаммы Е. coli. Представлены иммуногенная композиция и вакцина для индукции специфического клеточного и гуморального иммунитета против HPV16, содержащие рекомбинантный белок L1HPV16. Группа изобретений позволяет получать устойчивый очищенный иммуногенный белок L1HPV16, а также позволяет снизить стоимость процесса его получения для применения в составе эффективных иммуногенных композиций и вакцин против вируса папилломы человека 16 типа. 6 н.п. ф-лы, 3 ил., 1 табл., 5 пр.
Реферат
Изобретение относится к генной инженерии, биохимии, биотехнологии и иммунологии. Получают синтетический ген белка L1 вируса папилломы человека 16 типа (L1HPV16), оптимизированный для гетерологичной экспрессии в непатогенных лабораторных штаммах Escherichia coli. На его основе получают рекомбинантную плазмиду pQE-L1/16, состоящую из синтетического гена белка L1HPV16, включающего промоторную область раннего промотора бактериофага Т5, ген белка L1HPV16 и терминатор транскрипции Т1; гена бета-лактамазы и бактериального участка инициации репликации типа ColE1. Изобретение также включает способ рефолдинга белка в корректную пространственную структуру и его очистки методом гель-фильтрации. Изобретение относится к самому рекомбинантному белку L1HPV16, экспрессионному вектору pQE-L1/16 и иммуногенной вакцинной композиции, содержащей рекомбинантный белок L1HPV16, направленной на индукцию иммунитета против вируса папилломы человека (HPV). Изобретение позволяет получать устойчивый очищенный иммуногенный белок L1HPV16, а также получать эффективные иммуногенные вакцинные композиции против HPV.
На сегодняшний день доказано, что эффективным методом предотвращения инфекции HPV является профилактическая вакцинация. В настоящее время на рынке присутствуют три профилактические вакцины - двухвалентный церварикс от компании GSK, четырехвалентный гардасил и девятивалентный гардасил-9 от компании Merck&Co. Целевым контингентом этих вакцин являются дети и молодые люди, не инфицированные HPV. Во всех этих вакцинах иммуногеном является белок капсида вируса L1, способный самопроизвольно формировать псевдовирусные частицы, не обладающие инфекционной активностью. Псевдовирусные частицы являются эффективной формой презентации вирусного антигена иммунной системе и обеспечивает развитие стойкого гуморального и клеточного иммунного ответа (DraperE. et al. A randomized, observer-blinded immunogenicity trial of Cervarix® and Gardasil® human papillomavirus vaccines in 12-15 year old girls. // PloS one - 2013. - Vol. 8. - №.5. - P. e61825; Toft L. et al. Comparison of the immunogenicity of Cervarix® and Gardasil® human papillomavirus vaccines for oncogenic non-vaccine serotypes HPV-31, HPV-33, and HPV-45 in HIV-infected adults. // Human vaccines & immunotherapeutics - 2014. - Vol. 10. - №.5. - P. 1147-1154; Godi A. et al. Relationship between Humoral Immune Responses against HPV16, HPV18, HPV31 and HPV45 in 12-15 Year Old Girls Receiving Cervarix® or Gardasil® Vaccine. // PloSone - 2015. - Vol. 10. - №.10. - P. e0140926; Giuliano A.R. et al. Immunogenicity and safety of Gardasil among mid-adult aged men (27-45 years) - The MAM Study. // Vaccine. - 2015. - Vol. 33. - №.42. - P. 5640-5646; Gizzo S., Noventa M., Nardelli G.B. Gardasil administration to hr-HPV-positive women and their partners. // Trends Pharmacol Sci. - 2013. - Vol. 34. - №.9. - P. 479-480; Luna J. et al. Long-term follow-up observation of the safety, immunogenicity, and effectiveness of Gardasil™ in adult women. // PloS one. - 2013. - Vol. 8. - №.12. - P. e83431; Petrosky E. et al. Use of 9-valent human papillomavirus (HPV) vaccine: updated HPV vaccination recommendations of the advisory committee on immunization practices. // MMWR Morb Mortal Wkly Rep. - 2015. - Vol. 64. - №.11. - P. 300-304).
Церварикс содержит L1 белки ПВЧ двух наиболее онкогенных типов - 16 и 18, которые обуславливают развитие около 70% случаев рака шейки матки (РШМ). Доказано, что церварикс существенно снижает риск инфекции HPV 16 и 18 типов и предотвращает развитие РШМ. Церварикс показан женщинам в возрасте от 9 до 26 лет (Monie A. et al. Cervarix™: a vaccine for the prevention of HPV 16, 18-associated cervical cancer. // Biologies: targets & therapy. - 2008. - Vol. 2. - №.1. - P. 107-113; WO 2010012780 A1).
Гардасил в своем составе содержит L1 белки четырех онкогенных типов HPV - 6, 11, 16 и 18. Показано, что эта вакцина предотвращает не только развитие РШМ, но и рака вульвы и влагалища, а также папилломатоз и формирование аногенитальных бородавок. В связи с этим Гардасил рекомендован женщинам и мужчинам в возрасте от 9 до 26 лет (McLemore M.R. Gardasil®: introducing the new human papillomavirus vaccine. // Clinical journal of oncology nursing - 2006. - Vol. 10. - №. 5. - P. 559).
Гардасил-9 содержит LI белки девяти типов HPV. Гардасил-9 предотвращает развитие дополнительных (по сравнению с Гардасилом) 20% HPV-опосредованных видов аногенитального рака и доброкачественных новообразований. Гардасил-9 показан и для мужчин, и для женщин в возрасте от 9 до 26 лет (Printz C. FDA approves Gardasil 9 for more types of HPV. // Cancer. - 2015. - Vol. 121. - №.8. - P. 1156-1157).
Кроме самого белка L1, вакцины содержат адъюванты - аморфный гидроксифосфат-сульфат алюминия, который является стимулятором гуморального иммунного ответа (используется в вакцинах гардасил и гардасил-9), а также гидрат окиси алюминия с монофосфорил липидом А1 из Salmonella enterica, который является эффективным стимулятором клеточного иммунного ответа (используются в вакцине церварикс) (Mata-HaroV. etal. The vaccine adjuvant monophosphoryl lipid A as a TRIF-biased agonist of TLR4. // Science. - 2007. - Vol. 316. - №.5831. - P. 1628-1632; Casella C.R., Mitchell Т.C. Putting endotoxin to work for us: monophosphoryl lipid A as a safe and effective vaccine adjuvant. // Cellular and molecular life sciences. - 2008. - Vol. 65. - №.20. - P. 3231-3240; Lindblad E.B. Aluminium compounds for use in vaccines. // Immunology and cell biology - 2004. - Vol. 82. - №.5. - P. 497-505; Marrack P., McKee A.S., Munks M.W. Towards an understanding of the adjuvant action of aluminium // Nature Reviews Immunology. - 2009. - Vol. 9. - №.4. - P. 287-293). Кроме того, в состав этих вакцин входят стабилизаторы суспензии полисорбат-80 и L-гистидин, поддерживающие свойства суспензии и повышающие стабильность комплекса между аморфным алюминием и антигеном (патент US 20050158334 А1).
Описанные выше вакцины позволяют значительно снизить распространенность инфекции HPV и снизить риск связанных с HPV заболеваний. В то же время данные вакцины имеют существенный недостаток: их стоимость достаточно высока по причине использования для получения белка L1 и сборки псевдовирусных частиц дорогостоящих бакуловирусных (церварикс) и дрожжевых (гардасил и гардасил-9) экспрессионных систем. Отсюда следует высокая актуальность разработки новых решений для удешевления процесса получения иммуногена белка L1 и формируемых им псевдовирусных частиц для применения в составе иммуногенных композиций.
Технический результат выражается в получении отдельных высокоочищенных и стабильных белковых компонентов, которые характеризуются высоким уровнем экспрессии и стабильности в бактериальных экспрессионных системах, на основе которых могут быть получены вакцины.
Получен иммуногенный белок L1 папилломавируса человека 16 типа (L1HPV16) в экспрессионной системе непатогенных лабораторных штаммов Escherichia coli с последующим рефолдингом L1HPV16 и его очисткой методом гель-фильтрации.
Была получена синтетическая последовательность ДНК, кодирующая белок L1HPV16. Для обеспечения высокого уровня продукции рекомбинантного белка L1HPV16 в гетерологичной системе проводили оптимизацию кодонов. Спланированная кодирующая последовательность ДНК отличалась от нативной последовательности ДНК вируса папилломы человека 16 типа нуклеотидным составом. Этот прием позволил получить высокоэффективную продукцию рекомбинантного белка L1HPV16 в нерастворимой фракции в количествах около 20% от суммарного белка клетки.
Заявляемая группа изобретений позволяет получить оптимальную для гетерологичной экспрессии синтетическую последовательность ДНК, кодирующую рекомбинантный белок L1HPV16, обеспечивающую высокий уровень продукции белка L1HPV16 в непатогенных лабораторных экспрессионных штаммах Е. coli; проводить простую и эффективную очистку белка L1HPV16, способного собираться в псевдовирусные частицы, и в этой форме эффективно и специфически индуцировать гуморальный и клеточный иммунный ответ к папилломавирусу человека 16 типа; создавать иммуногенные композиции на основе рекомбинантного белка с использованием геля гидрата окиси алюминия (Al) и монофосфорил липида А1 из Salmonella enterica (MPLA) в качестве адъювантов.
Указанный результат достигается за счет синтеза рекомбинатного белка L1HPV16 в клетках лабораторных штаммов Е. coli, несущих рекомбинантную плазмиду pQE-L1/16, а также за счет создания комплексного препарата L1HPV16 (5 или 0,5 мкг) с адъювантами Al (200 мкг) и MPLA (1 мкг).
Сущность изобретения состоит в том, что плазмида pQE-L1/16 содержит следующие существенные для ее функционирования структурные элементы:
а) искусственный ген L1HPV16, состоящий из:
- промоторной области раннего промотора бактериофага Т5 (10-54 п.н.), обеспечивающей эффективную транскрипцию мРНК;
- рекомбинантного гена, кодирующего белок L1 папилломавируса человека 16 типа (117-1524 п.н.);
- нетранслируемой области терминации транскрипции бактериального оперона, обеспечивающей эффективное окончание транскрипции гена L1HPV16 (2150-2236 п.н.);
в) бактериального гена bla, находящегося под контролем промотора AmpR (3477-4442 п.н.), кодирующего белок бета-лактамазу - селективный маркер для трансформации штамма Е. coli;
г) бактериального участка инициации репликации типа ColE1, обеспечивающего репликацию плазмиды в штамме Е. coli: L1HPV16 (2718-3306 п.н.).
Таким образом, создана рекомбинантная плазмида pQE-L1/16 (4542 п.н.), кодирующая рекомбинантный белок L1HPV16, обладающий способностью самопроизвольно формировать псевдовирусные частицы. Плазмида содержит следующие структурные элементы: искусственный ген полноразмерного белка L1 вируса папилломы человека 16 типа, включающий промоторную область раннего промотора бактериофага Т5 (45 п.н.), ген химерного белка L1HPV16 (1524 п.н.) и терминатор транскрипции Т1 (87 п.н.); ген бета-лактамазы (966 п.н.) и бактериальный участок инициации репликации типа ColE1 (589 п.н.).
По формулированию препарата рекомбинантного белка L1HPV16 в виде псевдовирусных частиц в комплексе с адъювантами (гелем гидрата оксида алюминия и монофосфорил липидом А1 из S. enterica) технический результат достигается за счет создания рекомбинантного белка L1HPV16, а также за счет получения иммунологической вакцинной композиции, в которой рекомбинантный белок L1HPV16 содержится в виде комплекса с MPLA и частицами Al.
Была исследована иммуногенность комплексного вакцинного препарата L1HPV16-Al-MPLA на мышах. Мышей иммунизировали вакцинной композицией подкожно три раза с интервалом в две недели и через неделю сравнивали гуморальный и клеточный иммунный ответ с ответом мышей, иммунизированных равными количествами белка L1HPV16. Был выявлен выраженный специфический гуморальный и клеточный иммунный ответ на композицию, содержащую L1HPV16 с добавлением Al и MPLA.
Техническим результатом, достигаемым при осуществлении изобретения, является получение высокого уровня продукции белка L1HPV16, который после рефолдинга и очистки формирует стабильные псевдовирусные частицы, обладающие способностью индуцировать гуморальный и клеточный иммунный ответ. Кроме этого, техническим результатом является эффективная иммуногенная вакцинная композиция, эффективно и специфически индуцирующая гуморальный и клеточный иммунный ответ к папилломавирусу человека 16 типа.
Изобретение проиллюстрировано следующими примерами, приведенными ниже. Генно-инженерные и микробиологические манипуляции, амплификацию и секвенирование ДНК проводили по стандартным методикам (Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование, М.: Мир, 1984; Клонирование ДНК. Методы. Под ред. Д. Гловера, Пер. с англ., М.: Мир, 1988; Saiki R.K., Gelfand D.H., StoffelS. etal. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science, 1988, Vol. 239, No. 4839, pp. 487-491; Sanger F., Nicklen S., Coulson A.R. DNA sequencing with chain-terminating inhibitors (DNA polymerase/nucleotide sequences/bacteriophage 4X174). Proc. Nat. Acad. Sci. USA, 1977, Vol. 74, No. 12, pp. 5463-5467).
Пример 1
Получение плазмиды pQE-L1/16
Синтетическая последовательность ДНК, кодирующая ген белка L1HPV16, была спланирована таким образом, чтобы нуклеотидный состав кодонов был оптимизирован для гетерологичной экспрессии в непатогенном лабораторном штамме Е. coli, а аминокислотный состав синтезируемого рекомбинатного белка при этом не изменялся (последовательность №1). Для клонирования фрагмента ДНК последовательность гена была фланкирована сайтами эндонуклеаз рестрикции BamHI и KpnI. Для инициации и остановки трансляции были предусмотрены стартовый и терминирующий кодоны.
Фрагмент ДНК, кодирующий белок L1HPV16, был синтезирован твердофазным амидофосфитным методом (ЗАО «Евроген», РФ) на синтезаторе AppliedBiosystemsABI 3900 с последующим клонированием ДНК дуплекса в pAL-TA вектор. Первичную структуру полученной конструкции подтверждали секвенированием.
Для получения конструкции, кодирующей последовательность гена L1HPV16, плазмиды pALTA-L1HPV16 и pQE6 гидролизовали эндонуклеазами рестрикции BamHI и KpnI при 37°C в буфере, содержащем 50 мМ Трис-HCl (pH 7,5), 10 мМ хлорида магния, 100 мМ хлорида натрия и 0,1 мг/мл BSA, в течение 1 часа. В 1,2% агарозном геле проводили разделение продуктов рестрикции. Выделенный из агарозного геля фрагмент плазмиды pALTA-L1HPV16 (1521 п.н.) лигировали с выделенным из агарозного геля фрагментом плазмиды pQE6 (3028 п.н.) с помощью ДНК-лигазы бактериофага Т4. Методом электропорации полученной лигазной смесью трансформировали компетентные клетки Е. coli M15 [pREP4]. После трансформации клоны отбирали на агаризованнной среде LB, содержащей антибиотики ампициллин и канамицин. Плазмидную ДНК выделяли методом щелочного лизиса и анализировали методом рестрикционного картирования. Отбирали клоны плазмидной ДНК pQE-L1/16 (4542 п.н., последовательность №2), содержащей в своем составе последовательность ДНК, кодирующую полноразмерный белок L1HPV16. Первичную структуру полученной конструкции подтверждали секвенированием. Схема плазмиды pQE-L1/16 приведена на фиг. 1.
Пример 2
Получение, рефолдинг и очистка рекомбинантного белка L1HPV16
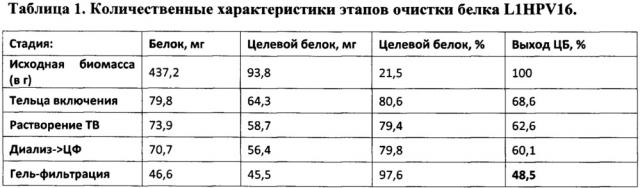
Культуру клеток E.coli осаждали, взвешивали, отмывали 10-кратным объемом буфера для отмывки А: 20 мМ Трис-HCl, pH 7.5, 50 мМ натрия хлорида, 0.5 мМ ЭДТА, 1 мМ PMSF. После отмывки клетки Е. coli снова ресуспендировали в 10-кратном объеме того же буфера и добавляли лизоцим из расчета 25 мкг/мл суспензии клеток. Инкубировали 30 мин при комнатной температуре, периодически перемешивая. Проводили озвучивание суспензии в течение 5 мин с помощью ультразвукового дезинтегратора BandelinSonopuls (20% амплитуды, 5 сек - импульс, 3 сек - пауза). Центрифугировали 30 мин при 10000 g и температуре 5°C. Целевой белок находится в телах включения (ТВ) в осадочной фракции. Супернатант декантировали, осадочную фракцию взвешивали и отмывали повторно 10-кратным объемом буфера для отмывки А. Отмытые ТВ растворяли в 10-кратном объеме буфера для отмывки А+5-20 мМ DTT+1-5% натрия лаурилсаркозината. Содержание целевого белка в отмытых ТВ составляло порядка 80%. После солюбилизации целевого белка из ТВ раствор осветляли центрифугированием при 10000 g. Для снижения содержания детергента раствор диализовали против буфера для отмывки А+10 мМ DTT+0.06% натрия лаурилсаркозината, 0.02% Твин-20. Дальнейшую очистку белка проводили методом гель-фильтрации на сорбенте ToyopearlHW-65, уравновешенном буфером для отмывки А+0-10 мМ DTT+0-1% натрия лаурилсаркозината, 0-1% Твин-20. Количественные характеристики этапов очистки приведены в таблице:
Пример 3
Проверка сборки белка L1HPV16, формирования пентамеров и псевдовирусных частиц.
Медные сеточки (200 меш) покрывали коллодием (4%-ный раствор нитроцеллюлозы в амиалацетате) и напыляли углем. Далее сеточки ионизировали в тлеющем разряде для гидрофилизации поверхности. Образцы белка L1HPV16, растворенного в фосфатно-солевом буфере в концентрации 50 мкг/мл, наносили на поверхность сеточек в объеме 15 мкл и контрастировали 2%-ным водным раствором уранил ацетата или 1,5%-ым водным раствором фосфовольфрамовой кислоты. Анализ проводили на просвечивающем электронном микроскопе JEM-1400 ТЕМ (JEOL, Япония) при ускоряющем напряжении 80 кВ. Электронные изображения получали с помощью цифровой камеры OlympusQuemesa (Olympus-SIS, Германия) и программного обеспечения iTEM (Olympus Soft Imaging Solutions GmbH, Германия). С помощью электронной микроскопии в образце белка L1HPV16 обнаруживали псевдовирусные частицы диаметром 40-50 нм (фиг. 2).
Пример 4
Проверка взаимодействия белка L1HPV16 с моно- и поликлональными специфическими антителами
Проверку взаимодействия L1HPV16 со специфическими поликлональными антителами проводили с помощью иммуноферментного анализа. В лунки планшетов для иммуноферментного анализа вносили 50 мкг раствора очищенного рефолдированного белка L1HPV16 в PBS c концентрацией 1 мкг/мл и инкубировали 2 ч при 25°C, после чего отмывали три раза PBS с добавлением 0,02% Tween-20. Блокировку свободных мест связывания проводили 5% раствором фетальной бычьей сыворотки в PBS (2 ч при 25°C) с последующей отмывкой PBS с добавлением 0,02% Tween-20. В качестве первичных антител к L1HPV16 использовали сывороточные антитела кролика, иммунизированного вакциной «Гардасил». Связывание с первичными антителами проводили в течение 2 ч при 25°C с последующей трехкратной отмывкой PBS, 0,02% Tween-20. Связывание с вторичными антителами козла к иммуноглобулинам кролика, конъюгированными с пероксидазой хрена (Имтек, Россия), проводили в течение 2 ч при 25°C с последующей трехкратной отмывкой PBS, 0,02% Tween-20. Детекцию вторичных антител проводили с помощью хромогенного субстрата 3,3',5,5'-тетраметибензидина в течение 10 минут при температуре 25°C. Реакцию останавливали 0.16 М водным раствором серной кислоты. Измерение интенсивности свечения хромогенного субстрата проводили на длине волны 450 нм с использованием плашечного спектрофотометра Multiskan™ FC MicroplatePhotometer (ThermoFisher, США). Коррекцию фонового сигнала проводили при длине волны 620 нм. С помощью иммуноферментного анализа было показано, что очищенный рефолдированный L1HPV16 эффективно распознается поликлональными антителами, полученными к компонентам вакцины «Гардасил» (фиг. 3 А).
Способность коммерчески доступных моноклональных антител CamVir-1 (клон 289-16981, MeridianLifeScience, США) эффективно распознавать белок L1HPV16, полученный и очищенный предлагаемыми в данной заявке способами, была продемонстрирована с помощью метода «Вестерн-блот» (фиг. 3 Б).
Пример 5
Проверка иммуногенности вакцинной композиции на основе белкового препарата L1HPV16 на мышах.
Самкам мышей линии balb/c вводили подкожно трехкратно с двухнедельным интервалом следующие препараты:
1) 5 мкг очищенного рекомбинантного белка L1HPV16;
2) 0,5 мкг очищенного рекомбинантного белка L1HPV16;
3) 5 мкг очищенного рекомбинантного белка L1HPV16 с добавлением 200 мкг Al и 1 мкг MPLA;
4) 0,5 мкг очищенного рекомбинантного белка L1HPV16 с добавлением 200 мкг Al и 1 мкг MPLA.
Все инъекционные препараты были растворены в 100 мкл стерильного фосфатно-солевого буфера. Через неделю после последней иммунизации у животных отбирали кровь и проводили резекцию селезенки с выделением спленоцитов для определения клеточного иммунного ответа (оценивали количество интерферона-гамма, синтезируемого спленоцитами мышей после стимуляции антигеном). Иммуногенная композиция, содержащая 0,5 мкг или 0,5 мкг L1HPV16+200 мкг Al+1 мкг MPLA, является оптимальной как для индукции клеточного иммунного ответа (от 300 до 1630 пг/мл интерферона-гамма в зависимости от животного), так и для индукции формирования специфических антител (определение методом иммуноферментного анализа: титр около 1/60000).
Таким образом, результаты свидетельствуют, что полученная вакцинная композиция приводит к специфической индукции гуморального и клеточного иммунного ответа.
1. Рекомбинантный ген с последовательностью №1, кодирующий белок L1 вируса папилломы человека 16 типа, с кодонами, оптимизированными для гетерологичной экспрессии в штаммах Е. coli.
2. Экспрессионный плазмидный вектор pQE-L1/16 с последовательностью №2, физической картой, представленной на фиг.1, несущий рекомбинантный ген по п.1.
3. Способ получения рекомбинантного белка L1HPV16, включающий:
- получение белка L1HPV16 в виде телец включения в экспрессионных штаммах Е. coli, трансформированных экспрессионным плазмидным вектором по п.2;
- отмывку телец включения, солюбилизацию L1HPV16 и его рефолдинг;
- очистку белка методом гель-фильтрации.
4. Иммуногенная композиция для индукции специфического клеточного и гуморального иммунитета против HPV16, содержащая рекомбинантный белок L1HPV16 с молекулярной массой 56.47 кДа, pI 8.64, полученный способом по п.3, гель гидрата оксида алюминия и монофосфорил липид А из S. enterica.
5. Вакцина, вызывающая специфический клеточный и гуморальный иммунитет против HPV16, содержащая рекомбинантный белок LlHPV16 c молекулярной массой 56.47 кДа, pI 8.64, полученный способом по п.3, в количестве 0,5-5 мкг, гель гидрата оксида алюминия 200 мкг и монофосфорил липид А из S. enterica, 1 мкг.
6. Способ индукции специфического клеточного и гуморального иммунитета против HPV16, включающий вакцинацию мышей линии balb/c трижды, подкожно, с интервалом 2 недели вакциной по п.5.