Лекарственное средство иммуномодулирующего действия
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к лекарственному средству, обладающему иммуномодулирующим и противовирусным действием. Лекарственное средство, обладающее иммуномодулирующим и противовирусным действием, представляющее собой экстракт травы солянки лиственничнолистной [Salsola laricifolia], полученный экстракцией сухой травы солянки лиственничнолистной [Salsola laricifolia] 30-80% водным раствором многоатомного спирта при 60-90°С; при этом используют соотношение экстрагент:сухая трава равное 1:(0,003-0,6) соответственно. Предлагаемое средство обладает выраженным иммуномодулирующим и противовирусным действием, эффективно повышает неспецифическую резистентность организма млекопитающих. 9 з.п. ф-лы, 9 ил., 67 табл., 55 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к медицине и ветеринарии, в частности к области разработки новых эффективных фитопрепаратов-иммуномодуляторов.
Уровень техники
Известно, что значение иммуномодуляторов в настоящее время в клинической медицине и ветеринарии возрастает. Иммуномодуляторы, позволяющие реализовать адекватный иммунный ответ на болезнетворный агент, обеспечив лечение без применения токсичных химиотерапевтических средств, воспринимаются как наиболее перспективный путь развития фармацевтики. Восстановление и стимуляция иммунного ответа имеет большое значение не только при инфекционных заболеваниях, но и в онкологии, т.к. купирование иммунодепрессии, вызванной химиотерапией и самой опухолью, существенно повышает шансы больных на выздоровление. По этим причинам за последние годы в клинику введено большое количество препаратов-иммуномодуляторов, характеризующихся либо иммунопротективным действием, либо в определенной степени стимулирующих некоторые иммунные функции (фагоцитоз, активность Т-киллеров, натуральных киллеров и т.п.). Большую часть препаратов составляют ксенобиотики, из которых можно упомянуть циклоферон (меглюмина акридонацетат), тилорон (амиксин), глутоксим, левамизол, полиоксидоний [РЛС Энциклопедия лекарств, 8-е изд., под ред. Ю.Ф. Крылова, М., 2001], леакадин [РЛС Энциклопедия лекарств, М., 2004], галавит, кагоцел, иммунофан [РЛС Энциклопедия лекарств, М., 2007], диуцифон [RU 2292892, опубл. 10.02.2007], сульпифон [RU 2136668, опубл. 10.09.1999], ингавирин [Справочник Видаль, 17-е изд., М., 2011], тимоген [М.Д. Машковский, Лекарственные средства, 16-е изд., М., 2012] и др. Общим недостатком веществ данной категории является несбалансированное воздействие на сложную иммунную систему, что нередко вызывает тяжелые побочные эффекты (агранулоцитоз, аутоиммунные заболевания и т.п.). С другой стороны, препараты-ксенобиотики часто обладают гепатотоксичностью. Более безопасными представляются препараты природного происхождения - настойки левзеи, элеутерококка, родиолы розовой, женьшеня, эхинацеи (Иммунал), стандартизованный экстракт проростков картофеля (Панавир) и др. Наиболее широко в качестве иммуномодуляторов используются экстракты и настойки эхинацеи, которые собственно и относятся к иммуномодуляторам (настойки левзеи, элеутерококка, родиолы розовой, женьшеня и др. относят к адаптогенам). В 1996 г., к примеру, в США препараты эхинацеи были самыми популярными среди фитопрепаратов [Бертрам Г. Катцунг, Базисная и клиническая фармакология, 2-е изд., Т. 2, 2008]. Не остаются без внимания терапевтов препараты эхинацеи и в России [РЛС Энциклопедия лекарств, М., 2007; В.Ю. Мартов, А.Н. Окороков, Лекарственные средства в практике врача, 2-е изд., М., 2010; Справочник Видаль, 17-е изд., М., 2011; М.Д. Машковский, Лекарственные средства, 16-е изд., М., 2012], с каждым годом их номенклатура расширяется на рынке [РЛС России, 8-е изд., под ред. Ю.Ф. Крылова, М., 2001; РЛС России, М., 2007]. В эксперименте in vitro сок Е. purpurea повышал выработку фагоцитами человека интерлейкинов-1, -6, -10 и фактора некроза опухоли-α, увеличивал активность натуральных киллеров и уровень антителозависимой цитотоксичности. Также экстракты эхинацеи обнаруживают и противовоспалительные эффекты, связанные с ингибированием циклооксигеназы [Бертрам Г. Катцунг, Базисная и клиническая фармакология, 2-ое изд., Т. 2, 2008]. В клинике их применение существенно уменьшает выраженность симптомов ОРЗ и сроки выздоровления. Учитывая очень низкую токсичность и сравнительно редко встречающиеся побочные эффекты, интерес к разработке иммуномодуляторов на основе сока или экстрактов растений рода эхинацея очень велик. Только за последнее время было создано большое число препаратов и БАД для применения в медицине (RU 2468810 опубл. 10.12.2012, RU 2137490 опубл. 20.09.1999, RU 2182011 опубл. 10.05.2002, ЕР 0464298 опубл. 08.01.1992 и др.) и ветеринарии (CN 102716164 опубл. 10.10.2012, RU 2525426 опубл. 10.08.2014, RU 2356557 опубл. 27.05.2009 и др.). Однако лекарственные средства из растений рода эхинацея далеко не решают задачу безопасного воздействия на иммунную систему. Во-первых, эффект этих препаратов несбалансированный, они способны усугублять аутоиммунные заболевания [Бертрам Г. Катцунг, Базисная и клиническая фармакология, 2-е изд., Т. 2, 2008], и их применение противопоказано при иммунодефицитных состояниях (СПИД, онкозаболевания), аутоиммунных заболеваниях любой этиологии, туберкулезе и других нозологиях, при которых больные как раз и нуждаются в безопасных иммуномодуляторах. Во-вторых, не обнаружено достоверное повышение резистентности к заболеваниям при профилактическом применении [Бертрам Г. Катцунг, Базисная и клиническая фармакология, 2-е изд., Т. 2, 2008; М.Д. Машковский, Лекарственные средства, 16-е изд., М., 2012]. В-третьих, большинство препаратов на основе эхинацеи содержит большое количество этанола, что ограничивает их использование в педиатрии и опасно при одновременном приеме с лекарственными средствами, обладающими ингибирующим эффектом на алкогольдегидрогеназу. В-четвертых, эхинацея - растение семейства сложноцветных, а к этим растениям относительно часто развиваются аллергические реакции [Бертрам Г. Катцунг, Базисная и клиническая фармакология, 2-е изд., Т. 2, 2008], в т.ч. и достаточно тяжелые - анафилаксия, приступы бронхиальной астмы.
Разработан ряд препаратов с высокой иммуномодулирующей и противовирусной активностью на основе пептидогликанов и кислых гликанов, выделенных из растущих побегов различных растений [RU 2195308 опубл. 27.12.2002, RU 2151600 опубл. 27.06.2000, RU 2028303 опубл. 09.02.1995, RU 2003110010 опубл. 20.10.2004]. В медицинскую практику было введено лекарственное средство «Панавир», которое зарекомендовало себя как безопасный и эффективный иммуномодулятор [М.Д. Машковский, Лекарственные средства, 16-е изд., М., 2012]. Недостатком указанных препаратов является узкое и ограниченное воздействие на иммунную систему и необходимость использования инъекционного введения в условиях стационара.
Предложено много комплексных фитопрепаратов с иммуномодулирующим эффектом на основе компонентов, для которых известно определенное влияние на иммунную систему - растения рода эхинацея, облепиха крушиновидная, солодка, алоэ, чага, левзея, аралия маньчжурская, женьшень, лимонник, кошачий коготь, родиола розовая, элеутерококк [RU 2516932 опубл. 20.05.2014, RU 2510277 опубл. 27.03.2014, CN 103933097 опубл. 23.07.2014, UA 49851 опубл. 11.05.2010, RU 2401121 опубл. 10.10.2010, RU 2236244 опубл. 20.09.2004, RU 2438694 опубл. 10.01.2012, RU 2525426 опубл. 10.08.2014, CN 103877437 опубл. 25.06.2014, KR 20140003866 опубл. 10.01.2014, CN 101828703 опубл. 15.09.2010, RU 2516886 опубл. 20.05.2014, RU 2129433 опубл. 27.04.1999, CN 101361774 опубл. 11.02.2009, US 2012039918 опубл. 16.02.2012, RU 2496510 опубл. 27.10.2013, RU 2393871. опубл. 10.07.2010, CN 103860906 опубл. 18.06.2014, RU 2283657 опубл. 20.09.2006 и др.]. Недостатком этих препаратов является вариабельный клинический эффект и чрезвычайная сложность стандартизации многокомпонентных фитопрепаратов.
Наиболее близким к предлагаемому нами лекарственному средству является разработка монгольских ученых [MN2031, выдан 27.09.2002] - препарат «Салимон», представляющий водно-этанольный экстракт травы солянки лиственничнолистной (Salsola laricifolia). Салимон показал неплохую эффективность при лечении онкобольных (в комплексе с другими препаратами и процедурами) [MN2031, выдан 27.09.2002; Монголын анагаах ухаан, 2001, 1(114), Шинэсэрхуу бударганы дархлал сэргээх уйлдлийн судалгаа; Монголын анагаах ухаан, 2002, 1(118), «Салимон эмийн эмнэл зуйн судалгааны дун»; Эруул Мэндийн Шинжлэх Ухаан, 2013, 9(3)(25), Шинэсэрхуу бударгана "Salsola laricifolia Turcz. ex Litv" ургамлын хавдрын эсрэг уйлдлийн судалгаа], а также было выявлено достоверное повышение неспецифической резистентности к вирусным заболеваниям [Эруул Мэндийн Шинжлэх Ухаан, 2013, 9(6)(28), Зарим ургамлын нийлмэл найрлагын дархлаа зугшруулэх уйлдлийн судалаа; Монголын анагаах ухаан, 1995, 4(93), Эмийн бодисын иммун заслын уйлдлийн эрчимжилт, мембраны телвеес хамаарахуй]. Недостатком данного лекарственного средства является неудовлетворительная эффективность экстракции сильнополярных полисахаридов и гликозидов водно-этанольными смесями. К тому же использование этанола в производстве лекарственных препаратов влечет определенные экономические затраты и организационные сложности, в результате чего продукт становится нерентабельным, либо недоступным по цене для потребителя. Хранение, перевозка и продажа ГЛФ также связана с большими трудностями из-за пожароопасности таких продуктов и жесткой регламентации оборота спиртосодержащих продуктов в России. В частности, не допускается использование спиртовых экстрактов для изготовления биологически активных добавок и препаратов для детей младших возрастов. В ветеринарии использование фитопрепаратов на основе спиртовых экстрактов также затруднительно из-за негативной реакции животных на сильный и резкий запах этанола.
Предпринимались попытки использования в эксперименте чисто водных экстрактов (отваров, настоев) солянки лиственничнолистной [Монголын анагаах ухаан, 1995, 4(93), Эмийн бодисын иммун заслын уйлдлийн эрчимжилт, мембраны телвеес хамаарахуй; П. Болормаа «Шинэсэрхуу бударгана, хуурмаг булчирхайт ортуузын иммунотроп уйлдлийн фармакологи», дисс. на соиск. уч.ст.докт.вет. наук], однако в этом случае препараты оказались менее эффективными и не стабильны при хранении и применения в практике не нашли.
Раскрытие изобретения
Целью разработки было создание высокоэффективного и безопасного фитопрепарата-иммуномодулятора из растения, не относящегося к семейству сложноцветных, повышающего неспецифическую резистентность млекопитающих и птиц к заболеваниям различной этиологии, не содержащего в своем составе этилового спирта.
Изобретение реализовано тем, что предложено лекарственное средство с иммуномодулирующим и противовирусным действием, повышающее неспецифическую резистентность организма теплокровных животных к бактериальным и вирусным инфекциям, представляющее собой экстракт травы солянки лиственничнолистной (Salsola laricifolia), полученный экстракцией сухой травы солянки лиственничнолистной (Salsola laricifolia) 30-80% водным раствором многоатомного спирта при 60-90°С; при этом используют соотношение экстрагент: сухая трава равное 1:(0,003-0,6) соответственно.
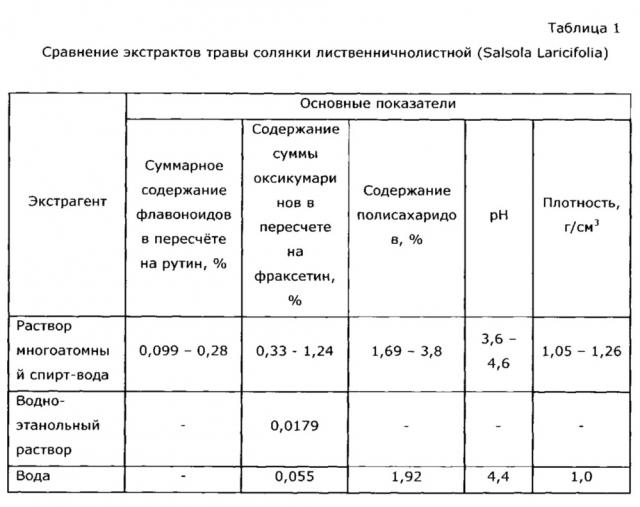
Неожиданным оказалось, что экстракция сухой травы солянки лиственничнолистной (Salsola laricifolia) водными растворами таких многоатомных спиртов как 1,2-пропиленгликоль и/или глицерин, и/или эритритол, и/или ксилит, и/или сорбит, и/или маннит, и/или дульцит, и/или инозит, или их смесей проходит более эффективно, чем экстракция водно-этанольным раствором или водой (см. таблицу 1).
Поскольку водные растворы многоатомных спиртов обладают повышенной вязкостью, целесообразно проводить экстракцию при умеренно повышенных температурах (60-90)°С; при температуре ниже 60°С раствор излишне вязкий и удерживается шротом, что резко снижает выход продукта, при температуре выше 90°С возможна деструкция биологически активных компонентов экстракта (пример 4). Изучение кинетики экстракции показало, что в этих условиях равновесные концентрации индикаторных компонентов (флавоноидов, оксикумаринов, полисахаридов) устанавливаются через 4-10 часов в зависимости от температуры и экстрагента, в то время как при использовании в качестве экстрагента 30-50% этанола при комнатной температуре равновесные концентрации устанавливаются через 3-5 суток (примеры 14, 31).
В качестве экстрагента для сухой травы используют 30-80% водный раствор многоатомного спирта. При концентрации многоатомного спирта меньше 30% резко снижается эффективность экстракции полифенольных соединений, при большей концентрации, нежели 80%, возрастает вязкость, что препятствует отделению полученного экстракта от шрота фильтрацией и снижает выход готового продукта (пример 1).
Количество экстрагент: сухая трава солянки лиственничнолистной оптимально в весовом соотношении 1:(0,2-0,6). Увеличение количества сухой травы более 0,6 весовых частей технически не выполнимо из-за свойств травы; пористость и влагоемкость даже спрессованной сухой травы такова, что количество экстрагента не заполняет объем до верхнего уровня "пакета" травы, и следовательно, часть загруженной травы не подвергается экстракции. На экстракцию можно брать меньше 0,2 весовых частей травы, вплоть до 0,003 как при получении ветеринарного препарата, однако при этом резко снижается экономичность процесса, возрастают энергозатраты, возникают проблемы со стандартизацией экстракта (см. пример 30).
Экстракцию при заданном соотношении экстрагент - сухая трава можно проводить как одной процедурой, так и многократной экстракцией небольшими порциями экстрагента, до достижения заданного соотношения. Оба способа имеют свои преимущества, но получаемые в результате экстракты не отличаются существенно ни по составу (содержанию сигнальных компонентов), ни по биологической активности, и относятся к общеизвестным способам получения фитоэкстрактов [Минина С.А., Каухова И.Е. / Химия и технология фитопрепаратов: учебное пособие. М.: ГЭОТАР-Медиа. 2009. 560С. ISBN 978-5-9704-0878-0], по этой причине мы не сочли необходимым вводить в формулу изобретения указанные технологические нюансы. Однократная процедура реализуется быстро, но требует при промышленной реализации использования оборудования неприемлемо большой емкости; многократная экстракция длительна, но позволяет использовать оборудование приемлемых размеров (примеры 12, 14, 26, 36-38); в этом случае необходимую производительность аппаратурной схемы достигают последовательным использованием «батареи» экстракторов приемлемых размеров [Минина С.А., Каухова И.Е. / Химия и технология фитопрепаратов: учебное пособие. М.: ГЭОТАР-Медиа. 2009. 560С. ISBN 978-5-9704-0878-0]. При использовании для приготовления экстрагента многоатомных спиртов с низкой растворимостью в холодной воде, но достаточной растворимостью в условиях экстракции (60-90°С), неожиданным оказалось, что при охлаждении экстракта некоторые многоатомные спирты выкристаллизовываются, при этом они практически не содержат компонентов фитоэкстракта (см. пример 20, 23, 24). Высокочистый многоатомный спирт легко отделяется фильтрацией и может быть использован для последующих экстракций. Концентрированный таким образом экстракт с уменьшенным содержанием многоатомного спирта и высокой концентрацией активных компонентов, стабилен при хранении, имеет приятный, не приторно-сладкий вкус, характерный для многоатомных спиртов.
В предлагаемых условиях экстракции в шроте практически не остается экстрактивных веществ, предложенный способ получения лекарственного препарата позволяет максимально извлечь биологически активные вещества при минимальной потере ценных компонентов. Данный способ получения высококонцентрированных экстрактов травы солянки лиственничнолистной не был обнаружен в доступной литературе. При этом экстракт, полученный при использовании в качестве экстрагента водного раствора многоатомного спирта, проявил значимо более высокую иммуномодулирующую активность по используемым тестам, нежели спиртовые экстракты (см. примеры 14. 43. 44), в то же время оказались приемлемы для разных видов животных (пример 7-9, 14, 37, 38), не огнеопасны, применимы в педиатрии и в других случаях, где ограничивается применение спиртовых экстрактов
Результаты получения экстрактов солянки лиственничнолистной (Salsola laricifolia) в различных условиях при разном соотношении сухая трава: экстрагент приведены в таблице 2.
Разработанные на основе экстрактов солянки лиственничной (Salsola laricifolia) лекарственные препараты для медицинского и ветеринарного применения проверены на токсические свойства. Результаты изучения острой токсичности и токсикометрии лекарственного препарата, полученного по примеру 28, позволяют отнести его к V классу практически нетоксичных лекарственных веществ [Н. Hodge et al. Clinical Toxicology of Commercial Products. Acute Poisoning. Ed. IV, Baltimore, 1975, 427 p.] и малоопасным веществам (IV класс опасности по ГОСТ 12.1.007-76) (см. пример 41). Идентичные результаты токсикометрии получены и для ветеринарного препарата, приготовленного по примеру 29 (см. пример 42).
Фармакологическая активность медицинского препарата по изобретению изучена на модели лечения острой гриппозной пневмонии у мышей (см. пример 39, 43). В качестве препаратов сравнения использовали широко известный препарат из эхинацеи пурпурной «Иммунал», а также препарат, изготовленный по примеру 31 - прототип. Все исследуемые препараты мало повлияли на интенсивность размножения вируса гриппа в легочной ткани, препарат по прототипу вообще не оказал эффекта, а в случае «Иммунала» и экспериментального средства титр вируса был ниже, на уровне 83,8% от контроля; хотя это различие нельзя отнести к достоверным, тем не менее просматривается тенденция, позволяющая считать, что имеется слабовыраженное прямое ингибирование размножения вируса гриппа. Значительно более выраженными оказались клинические эффекты. Так, степень поражения легких при применении препарата по примеру 28, оказалась, более чем в 2 раза ниже, чем у контрольной группы, и значительно ниже, чем в группе, использующей прототип. Морфологический анализ паренхимы легких также подтвердил двукратное снижение поражения структур легких. При этом антиоксидантная активность легочной ткани возросла в 2,5 раза, а также снизился по сравнению с контролем уровень продуктов перекисного окисления, что свидетельствует об активации защитных и репаративных процессов под воздействием экспериментального препарата. Лечебный эффект проявился как в бронхиальных структурах, так и в альвеолах, гиперплазия эпителия в обоих случаях была ниже практически в 3 раза по сравнению с контролем, воспалительная инфильтрация снизилась в 2 раза, по этим параметрам препарат по изобретению существенно превосходил прототип и препарат сравнения. Результат исследования коры надпочечников показал, что все три изучаемых лекарственных средства примерно в равной степени ингибировали стрессиндуцированные изменения клеток коры надпочечников; клетки по размерам в 2 раза превосходили клетки контрольных животных.
Была изучена профилактическая активность препарата, полученного по примеру 28, при гриппозной инфекции (см. пример 44). Эффект оказался существенно выше, нежели в случае препарата-прототипа, полученного по примеру 31, и сравним с эффектом препарата «Иммунал».
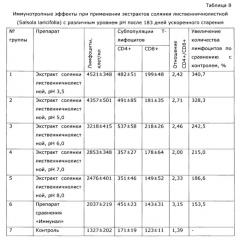
Оптимальный иммунный ответ достигается только при взаимодействии гуморального и клеточного звеньев иммунитета. В-клетки отвечают за гуморальное звено приобретенного иммунитета, то есть вырабатывают антитела, в то время как Т-клетки представляют собой основу клеточного звена специфического иммунного ответа. Под действием разработанного препарата наблюдалось усиление В-клеточного звена иммунитета животных; увеличение количества антителообразующих клеток в селезенке опытных животных в ответ на введение тимусзависимого антигена достоверно приводило к повышению индекса стимуляции в 2,5 раза по сравнению с контролем, аналогично возросли титры агглютининов в сыворотке крови почти в 4 раза (см. примеры 12, 45-47). Усиление Т-клеточного звена иммунитета произошло за счет увеличения количества аутологичных розеткообразующих клеток (ауто-РОК) как в абсолютном, так и относительном выражении и составило соответственно 2 и 10 раз. Результаты проведенных тестов свидетельствуют о значительной активизации Т- и В-клеточных звеньев иммунитета под воздействием экспериментального лекарственного средства, что говорит об иммуномодулирующем действии препарата.
Было изучено профилактическое и лечебное применение разработанного препарата при бактериальных респираторных заболеваниях щенков. В контрольных группах, несмотря на использование антибиотиков, летальность составляла 15%. При профилактическом применении экспериментального препарата летальность отсутствовала, в случае наступления болезни собаки быстро выздоравливали. В комплексной терапии лечения препаратом летальность хотя и имелась, но была снижена. Период реконвалесценции по сравнению с контролем был в 2 раза короче (см. пример 48).
При герпесной инфекции кошек, сопровождающейся в тяжелых случаях летальностью приблизительно 30% и реабилитационным периодом у выживших животных более 1,5 месяцев, применение препарата позволило исключить гибель животных и сократить сроки выздоровления. Применение препарата в начальной стадии заболевания уменьшило время реконвалесценции до 7-9 суток (см. пример 49).
Препарат оказал высокую эффективность после хирургических вмешательств у собак и кошек, исключив возникновение осложнений и сократив сроки выздоровления (см. пример 50, 51).
Известно, что применение антибиотиков и химиотерапии всегда сопровождается выраженной иммунодепрессией, это удлиняет период выздоровления и способствует возникновению осложнений. Применение препарата по изобретению позволило быстро нормализовать гематологические и биохимические показатели крови животных, что существенно сократило сроки реконвалесценции (см. пример 52).
Большой проблемой в ветеринарии мелких домашних животных является вирусный энтерит кошек, высоко контагиозное заболевание, сопровождающееся массовой гибелью котят и молодых животных. Специфические препараты для лечения вирусных энтеритов кошек отсутствуют. Применение разработанного препарата с профилактической и лечебной целью позволило избежать летальности и уменьшить период выздоровления животных (см. пример 53).
У собак часто наблюдаются тяжелые заболевания желудочно-кишечного тракта с выраженным дисбактериозом, сопровождающиеся патологическими изменениями иммунной системы. Эти состояния, хотя и имеют бактериальную природу, очень трудно поддаются терапии. Введение в комплекс лечебных мероприятий разработанного препарата позволило уменьшить в 2 раза период реконвалесценции и быстро нормализовать иммунологический статус животных. Так, при отсутствии клинических проявлений заболевания после проведенного лечения у контрольной группы животных наблюдались низкий иммуннорегуляторный индекс (CD4+/CD8+) 1,38, снижение функции фагоцитов и т.д.; у животных, получавших экспериментальное средство, в этот же период времени все исследованные показатели находились в пределах нормы, что подтверждает иммуномодулирующее действие предложенного препарата. Препарат эффективно повышал неспецифическую резистентность у продуктивных животных (пример 37); оказывал значимый иммуномодулирующий эффект при выращивании бройлеров (пример 38). Сравнение нативных экстрактов, полученных с использованием различных многоатомных спиртов (пример 40) выявило, что биологический эффект во всех случаях различался очень незначительно, при некоторой корреляции между полярностью экстрагента и проявлением иммуномодулирующего эффекта. То же самое обнаружено в эксперименте по примеру 2.
Разработанное лекарственное средство позволяет осуществлять эффективное лечение иммунодепрессивных состояний, при этом восстанавливается адекватный иммунный ответ и сокращаются сроки выздоровления (см. пример 52, 54 и др.). Предложенный способ лечения иммунодепрессивных состояний заключается в длительном, до нормализации иммунных функций, перроральном введении разработанного препарата, может быть использован как в виде монотерапии, так и сопровождаться применением других терапевтических агентов - антибиотиков, витаминов, спазмолитиков и т.д. (см. пример 48, 49, 53, 54).
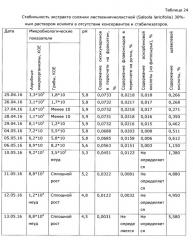
Экстракт солянки лиственничнолистной (Salsola laricifolia), полученный путем экстракции травы водными растворами многоатомных спиртов, может быть использован, в соответствии с ОФС.1.4.1.0018.15 в течение суток после получения, либо в течение несколько более продолжительного времени при хранении при низкой температуре, в целом эти фито-экстракты потенциально могут поддерживать рост микроорганизмов, поэтому длительное хранение при нормальных условиях невозможно; хотя некоторые многоатомные спирты (пропиленгликоль, ксилит) проявляют собственное бактериостатическое действие и экстракты с их использованием сохраняются относительно долго (примеры 37, 38). Тем не менее, все же основной фактор риска нестабильности безспиртовых фитоэкстрактов - возможный рост микроорганизмов (бактерий и грибов), что недопустимо само по себе, т.к. микроорганизмы продуцируют токсины, и к тому же вегетатирующие микроорганизмы быстро разрушают биологически активные вещества фитоэкстрактов. Для предотвращения роста микроорганизмов в фитоэкстракты вводят фармацевтически приемлемые консерванты - сорбаты, бензоаты, бензиловый спирт, парабены, сульфиты и т.п., большинство из перечисленных консервантов существенно более эффективны в слабокислой среде. Следует подчеркнуть, что, как было обнаружено в процессе разработки, экстракты солянки лиственничнолистной водными растворами многоатомных спиртов для длительного хранения (что обеспечивает удобство использования препарата в практике) требуют стабилизации - а именно, поддержания рН в области максимальной стабильности биологически активных веществ (экспериментально выявлен интервал значений рН 3,5-5,0), блокирующих нежелательные процессы окисления флавоноидов, лигнанов и др. компонентов фенольной структуры, и бактериостатиков-консервантов. В качестве слабых нетоксичных кислот, удобных для стабилизации рН, без изменения биологических свойств лекарственного средства, может быть взята пищевая нетоксичная кислота: янтарная, яблочная, уксусная, молочная, фосфорная, пропионовая, глюконовая и т.п., однако нами выбрана для реализации изобретения предпочтительна аскорбиновая кислота, т.к. она обладает также и антиоксидантными свойствами, стабилизируя биофенолы (что упрощает состав и технологию производства), обладает приятным вкусом, недорога и доступна на рынке. В качестве антиоксиданта, также без изменения биологических свойств лекарственного препарата, может быть использован любой из известных пищевых стабилизаторов-антиоксидантов: эфиры аскорбиновой кислоты и ее соли, пропилгаллат, ионол, трет-бутилгидрокси анизол, сульфиты и другие. Однако по сравнению с аскорбиновой кислотой они обладают некоторыми недостатками, а именно, требуют дополнительно использования кислоты для регулирования рН, часто придают неприятный вкус, плохо и медленно растворяются в водных растворах многоатомных спиртов. При длительном применении некоторые из них обладают нежелательными токсическими эффектами. К примеру, ионол и трет-бутилгидрокси анизол могут проявлять гепатотоксичность, а сульфиты относительно аллергенны и опасны для больных с бронхиальной астмой [особые указания для растворов в/в и в/м введения препаратов Метадоксил и Но-шпа на www.webvidal.ru] [Е226, Е227, Е228 www.procook.ru/articles.php?do=68], [Hugot D., Causeret J., Leclerc J. Effets d I'ingest on de sulfites sur l'excretion du calcium chez Ie rat. Ann. Biol. Anim. Biochim. Biophys., 5, 53-59 (1965)], [Вредные вещества в промышленности. Неорганические и элементорганические соединения: Справочник. / Под ред. проф. Н.В. Лазарева, Изд. 7-е перер. и доп. - Л.: Химия, 1977, стр. 65], [Rehm H.J., Wittmann Н. Beitrag zur Kenntnis der antimikrobiellen Wirkung der schwefligen Saure. II. Mitteilung. Die Wirkung der dissoziierten und undissoziierten Saure auf verschiedene Mikroorganismen. Z. Lebensin. Unters. Forsch., 120 (6), 465-478 (1963)].
Аналогично в качестве консерванта-бактериостатика может быть использован любой известный достаточно эффективный пищевой консервант: сорбиновая и бензойная кислоты, их соли, бензиловый спирт, бензилбензоат, низин, натамицин, парабены, феноксиэтанол и другие. Сорбиновая и бензойная кислота, и отчасти бензиловый спирт, оцениваются как одни из самых безопасных консервантов, в эффективных дозах не влияют на вкус, и вместе с тем доступны на рынке и недороги. Минимальные значения приемлемых концентраций консервантов (0,01% масс. сорбаты и бензоаты, 0,014% - бензиловый спирт) приняты из условия эффективности бактериостатического эффекта по отношению к обнаруживаемым резистентным микроорганизмам - контаминантам (примеры 6, 10, 25); верхние допустимые уровни ограничиваются влиянием на органолептические свойства лекарственного средства, а также в соответствии с нормами ТР/ТС.
Для получения стабильного лекарственного средства не существенно какой конкретно стабилизатор и консервант используется. Как мы считаем, оптимальным стабилизатором является аскорбиновая кислота, обладающая приятным вкусом, витаминной активностью, являющаяся антиоксидантом, но это не исключает использование других карбоновых кислот в качестве стабилизаторов. С ее помощью легко поддерживают значение рН в области максимальной химической стабильности компонентов фитоэкстракта - от 3,5 до 5,0. В этой же области рН наиболее эффективны пищевые консерванты (см. пример 10). При рН больше 5,0 наблюдается быстрая деструкция оксикумаринов и флавоноидов (гидролиз, окисление), что снижает биологический эффект при хранении лекарственного средства. При рН менее 3,5 лекарственное средство становится неприемлемым по ррганолептическим свойствам (кислый вкус). Оптимальное значение рН достигается обычно при концентрации аскорбиновой кислоты в интервале от 0,1 до 3,05 масс. % и зависит от параметров фитосырья.
В качестве бактериостатиков-консервантов могут быть использованы признанные безопасными бензойная кислота или ее фармацевтически приемлемые соли в концентрации (0,01-0,5) масс. % и/или сорбиновая кислота или ее фармацевтически приемлемые соли в концентрации (0,01-0,6) масс. %, и/или бензиловый спирт в концентрации (0,014-0,6) масс. %. При концентрации консервантов менее 0,01% лекарственное средство не выдерживает заявленного срока годности (2 года) по микробиологической чистоте (см. примеры 10, 25). Использование консервантов в количествах, чем предложено, нецелесообразно по экономическим причинам и, как обнаружено, сказывается отрицательно на органолептических свойствах экстракта (сильно раздражает слизистую поверхность гортани). Известные в качестве бактериостатиков-стабилизаторов для «фитоэкстрактов» эфиры п-оксибензойной кислоты («парабены») также могут быть использованы, но они менее приемлемы ввиду известных побочных эффектов и неприятного вкуса. Определение эффективных концентраций консервантов приведено в примере 6.
Целевые добавки - консерванты и стабилизаторы, технически просто добавлять в готовый экстракт, с получением продукта, обладающего должной для промышленного производства лекарственного средства, стабильностью - 2 и более лет при естественном хранении (примеры 8, 9). Однако в этом случае при вынужденных остановках процесса экстракции (см. пример 13) возможно возникновение аварийной ситуации - бурный рост микрофлоры в экстракторе, что ведет к экономическим потерям. Для исключения этого явления целевые добавки лучше добавлять в экстрагент (пример 14-26) или в процессе экстракции (пример 5-7), последнее удобно в случае, если экстрактор снабжен перемешивающим устройством и средством контроля уровня рН.
Следует заметит, что целевые добавки закономерно влияют на стабильность лекарственного средства, но не влияют на биологические эффекты (см. пример 7). При этом наиболее благоприятно влияют на органолептические свойства продукта, что имеет значение при коммерческом применении, в первую очередь аскорбиновая кислота и отчасти лимонная, в то время как другие стабилизаторы (к примеру, уксусная кислота) ухудшают органолептические свойства (вкус, запах) (см. примеры 7, 8).
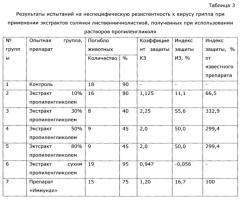
Как следует из проведенных исследований, уже очень небольшие количества экстрактивных веществ из солянки лиственничнолистной (Salsola laricifolia) оказывают выраженный иммуномодулирующий эффект (примеры 3). При этом эффект в области эффективных доз экстрактивных веществ практически не увеличивается (примеры 3, 39); хотя даже в очень больших дозах экстракты солянки лиственничнолистной не проявляют токсических (пример 3) и сенсибилизирующих (пример 55) эффектов, по экономическим причинам, учитывая что солянка лиственничнолистная (Salsola laricifolia) - эндемичное растение Монгольской Гоби и относительно дорогостоящее сырье, целесообразно минимизировать используемые количества фитосырья. Технически можно получить сразу экстракты с минимально эффективной концентрацией экстрактивных веществ (пример 14), но с точки зрения организации экономически рентабельного производства фитопрепарата и для ветеринарного, и для медицинского применения, целесообразно получать концентрированный экстракт, затем стандартизировать разбавлением до определенных концентраций сигнальных компонентов (пример 27) и далее использовать для изготовления конкретных препаратов, БАД и кормовых добавок, вводя необходимое количество фармацевтически приемлемого разбавителя. В качестве последнего можно использовать как очищенную воду (пример 39), так и растворы многоатомных спиртов (примеры 27-29), что обеспечивает необходимые органолептические свойства (примеры 39) препаратов, кроме того, в качестве фармацевтически приемлемого разбавителя можно использовать физиологический раствор, растворы Рингера и др. При этом необходимо обеспечивать эффективные концентрации консервантов, препятствующих росту микроорганизмов (см. пример 6) и стабилизаторов, обеспечивающих рН препаратов в области стабильности и приемлемых органолептических свойств - от 3,5 до 5,0 (примеры 7, 8).
Таким образом, разработан высокоэффективный и безопасный фитопрепарат-иммуномодулятор из растения, не относящегося к семейству сложноцветных, повышающий неспецифическую резистентность организма млекопитающих и птиц к заболеваниям различной этиологии, пригодный для использования в онкологии, не содержащий в своем составе этиловый спирт, что дает возможность применения его в ветеринарии и для лечения детей младших возрастов, а также исключает известные сложности обращения с препаратами, содержащими высокие концентрации этанола, обладающего токсичностью, наркотическими свойствами и пожароопасностью.
Краткое описание чертежей.
На Фиг. 1 показана динамика высвобождения флавоноидов при экстракции солянки лиственничнолистной (Salsola laricifolia) растворами пропиленгликоля. Флавоноиды определяли СФ-методом по окрашиванию алюминиевого комплекса в пересчете на рутин, где: 1 - экстракция с использованием 80% раствора пропиленгликоля; 2 - экстракция с использованием 50% раствора пропиленгликоля; 3 - экстракция с использованием 30% раствора пропиленгликоля; 4 - экстракция с использованием 10% раствора пропиленгликоля; 5 - экстракция с использованием чистого пропиленгликоля (100%).
На Фиг. 2 показана динамика высвобождения оксикумаринов при экстракции солянки лиственничнолистной (Salsola laricifolia) растворами пропиленгликоля. Оксикумарины определяли СФ-методом в пересчете на фраксетин, где: 1 - экстракция с использованием 80% раствора пропиленгликоля; 2 - экстракция с использованием 50% раствора пропиленгликоля; 3 - экстракция с использованием 30% раствора пропиленгликоля; 4 - экстракция с использованием 10% раствора пропиленгликоля; 5 - экстракция с использованием чистого пропиленгликоля (100%).
На Фиг. 3 показана Динамика высвобождения полисахаридов при экстракции солянки лиственничнолистной (Salsola laricifolia) растворами пропиленгликоля. Полисахариды определяли СФ-методом, где: 1 - экстракция с использованием 80% раствора пропиленгликоля; 2 - экстракция с использованием 50% раствора пропиленгликоля; 3 - экстракция с использованием 30% раствора пропиленгликоля; 4 - экстракция с использованием 10% раствора пропиленгликоля; 5 - экстракция с использованием чистого пропиленгликоля (100%).
На Фиг. 4 показана динамика высвобождения оксикумаринов при экстракции солянки лиственничнолистной (Salsola laricifolia) растворами многоатомных спиртов. Оксикумарины определяли СФ-методом в пересчете на фраксетин, где: 1 - экстракция 30% раствором ксилита; 2 - экстракция 30% раствором сорбита; 3 - экстракция 30% раствором эритритола; 4 - экстракция 30% раствором пропиленгликоля; 5 -экстракция 30% раствором глицерина.
На Фиг. 5 показана динамика высвобождения оксикумаринов при экстракции солянки лиственничнолистной (Salsola laricifolia) в зависимости от температуры экстрагирования. Оксикумарины определяли СФ-методом в пересчете на фраксетин, где: 1 - экстракция при 105°С; 2 - э